Чем лечат папиллому в матке
Что такое папилломавирусная инфекция (ВПЧ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Борисова Э. В., гинеколога со стажем в 34 года.
Определение болезни. Причины заболевания
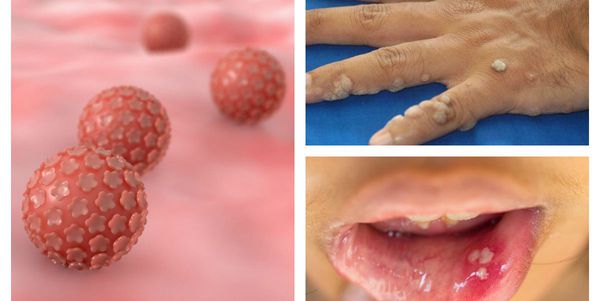
Папилломавирусная инфекция — это состояние, развивающееся при заражении какой-либо разновидностью вируса папилломы человека (ВПЧ). Возбудители данной группы могут существовать только в человеческом организме, поражая кожу и слизистые оболочки, приводя к появлению папиллом, бородавок, плоских и остроконечных кондилом. [1] [2] [4]
ВПЧ довольно широко распространён в человеческой популяции, особенно среди сексуально активных людей, а это свыше 80% всего населения. До недавнего времени вирусы этой группы считались относительно безобидными, вызывающими лишь косметические дефекты, но последние научные исследования показывают, что проблема гораздо серьёзнее. [9]
Чаще всего заражение происходит в молодом возрасте, как правило, с началом половой жизни, при этом возможно неоднократное инфицирование. Наиболее уязвимой группой в плане вероятности заражения ВПЧ и развития неблагоприятных последствий являются молодые женщины в возрасте 15-30 лет.
Помимо этого ВПЧ может перейти от инфицированной матери к ребёнку, например, при родах. Не исключается и контактно-бытовой способ передачи возбудителя, например, при соприкосновениях и даже при совместном использовании предметов личной гигиены.
К факторам риска, способствующим заражению ВПЧ, развитию хронической папилломавирусной инфекции и её переходу в предраковые состояния с потенциальным перерождением в злокачественную опухоль, относятся:
Симптомы папилломавирусной инфекции
Далеко не всегда человек догадывается о наличии в своём организме папилломавирусной инфекции, оставаясь при этом источником заражения для потенциальных партнёров. [1] [2] Дело в том, что заболевание может долгое время протекать бессимптомно: вирус скрыто существует в организме от нескольких месяцев до нескольких лет, никак себя не проявляя. Кроме того, уже имеющиеся проявления инфекции не всегда доступны для наружного обзора. Например, если папилломы, бородавки и кондиломы на открытых участках тела и поверхности гениталий ещё можно заметить самостоятельно, то патологические изменения, локализующиеся на шейке матки, сможет обнаружить только специалист в ходе осмотра с применением соответствующих инструментов.
И всё же существует несколько симптомов, которые прямо или косвенно могут указывать на наличие папилломавирусной инфекции и её неблагоприятных последствий. [3] К ним относятся:
Наиболее тревожными признаками заболевания являются:
Патогенез папилломавирусной инфекции
Заражение папилломавирусной инфекцией происходит при попадании вирусных частиц на кожу или слизистую оболочку. [1] [2] Излюбленная локализация инфекции на теле женщины — промежность, большие и малые половые губы, вульва, влагалище и шейка матки, у мужчин — половой член. Может также произойти поражение слизистой полости рта, пищевода, мочевого пузыря, трахеи, конъюнктивы и других органов и тканей.
Заражению способствуют микротравмы и потёртости. Особенно благоприятные для инфицирования условия создаются при половом акте. В 60–80% случаев достаточно однократного сексуального контакта с больным папилломавирусной инфекцией или бессимптомным носителем ВПЧ. К развитию заболевания может привести попадание в организм буквально единичных вирусных частиц.
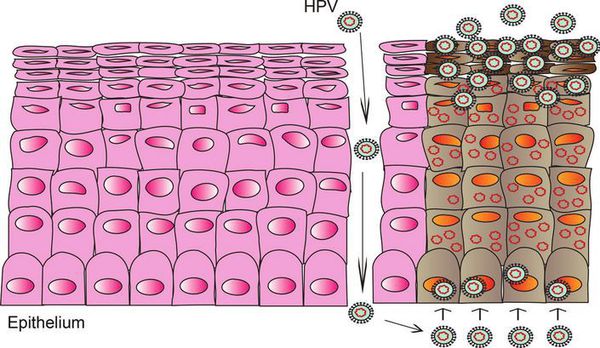
При наличии предрасполагающих факторов (микроповреждения, слабого иммунитета и других) возбудитель проникает в эпителиальную ткань до её базального слоя. Там он прикрепляется к оболочке незрелой клетки и внедряется сначала в её цитоплазму, а затем и в ядро, где повреждает генетический аппарат. После этого начинается деление клеток с изменённым геномом, что приводит к появлению в месте внедрения вируса генитальных кондилом (образований, которые постепенно разрастаются), а, например, на шейке матки — к развитию диспластических процессов различной степени тяжести (дисплазия шейки матки).
В случае ВПЧ высокого онкогенного риска определённые гены в вирусной ДНК кодируют синтез специфических белков-онкопротеинов (Е6 и Е7), которые подавляют противораковую защиту клеток. Под действием онкопротеинов нарушается стабильность генома клеток, стимулируется их размножение и снижается способность к дифференцировке — всё это со временем может привести к онкопатологии. [12]
Формирование новых полноценных вирусных частиц, способных инфицировать другого человека, происходит уже не в базальном, а в самых поверхностных слоях поражённого эпителия. Возбудитель может содержаться в слущивающихся отмирающих клетках, которые отделаются слизистой оболочкой. Таким образом они переходят к новому хозяину при тесном (сексуальном или бытовом) контакте.
Классификация и стадии развития папилломавирусной инфекции
По способности индуцировать развитие злокачественных новообразований ВПЧ подразделяют на четыре группы: [8]
Максимально опасными считаются 16-й и 18-й типы: на их долю приходится до 70% случаев рака шейки матки. [7] [8]
Клинические формы папилломавирусной инфекции: [5]
Латентная инфекция может переходить в субклиническую и манифестную форму в случае возникновения предрасполагающих условий (факторов риска), но чаще всего она протекает бессимптомно, не манифестируя.
Клинические проявления папилломавирусной инфекции:
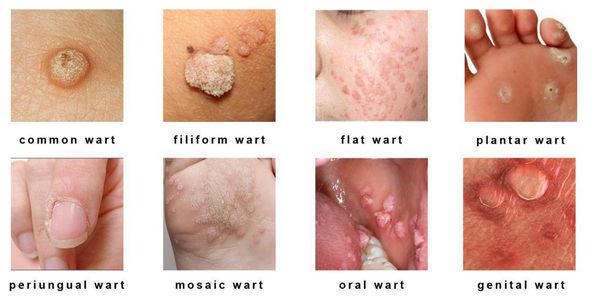
Разновидности поражений:
Осложнения папилломавирусной инфекции
Основными наиболее опасными осложнениями папилломавирусной инфекции являются злокачественные новообразования. Но возможны и другие серьёзные последствия:
Диагностика папилломавирусной инфекции
Основные цели диагностических мероприятий: [3]
Для выявления папилломавирусной инфекции на сегодняшний день существует целый комплекс диагностических процедур:
Целесообразно дополнительное обследование пациента на наличие других инфекций, передающихся половым путём, так как папилломавирус в 90% случаев с ними сочетается, и это может осложнять течение заболевания.
Лечение папилломавирусной инфекции
Лечение папилломавирусной инфекции должно быть комплексным и включать следующие составляющие: [3] [5]
Деструктивные методы делятся на две основные группы:
Лечение сопутствующих половых инфекций проводят до начала деструктивной терапии на фоне адекватной иммунокоррекции.
Удаление видимых проявлений папилломавирусной инфекции должно сочетаться с противовирусной терапией — как с общей, так и с применением препаратов местного действия после удаления кондилом.
Следует помнить, что успешно проведённое лечение не исключает развитие рецидивов в дальнейшем, особенно у пациентов с нарушениями иммунитета. Поэтому за ними устанавливается динамическое наблюдение в течение как минимум 1-2 лет.
Прогноз. Профилактика
В 90% случаев здоровая иммунная система человека справляется с папилломавирусной инфекцией самостоятельно за период от полугода до двух лет с момента инфицирования, после чего происходит полное выздоровление с исчезновением вируса из организма. При этом не формируется напряжённого пожизненного иммунитета, то есть человек может заразиться повторно.
В других случаях, при наличии предрасполагающих факторов, заболевание приобретает хроническую форму, склонную к длительному скрытому течению с периодическими рецидивами и возможным развитием тяжёлых осложнений.
От момента попадания вируса в организм до развития предраковых состояний и тем более возникновения рака может пройти достаточно много времени, иногда десятки лет. Поэтому регулярные профилактические обследования, своевременное выявление и лечение предраковых состояний — вполне реальный и эффективный способ избежать самого неблагоприятного варианта развития событий. [13] С этой целью Всемирная организация здравоохранения рекомендует всем женщинам старше 30 лет при первичном скрининге проходить не только “рутинное” цитологическое исследование, но и делать тест на наличие ВПЧ. [10]
Регулярное посещение гинеколога (при отсутствии каких-либо жалоб — раз в год) с проведением теста Папаниколау позволяет своевременно обнаружить начальные признаки дисплазии и предпринять все необходимые меры для предотвращения прогрессирования процесса и его перехода в онкологическое заболевание.
Использование методов барьерной контрацепции хоть и не полностью защищает от инфицирования, но несколько снижает его вероятность.
Главным методом первичной профилактики папилломавирусной инфекции считается вакцинация. [11] Современные вакцины разработаны с целью защиты от наиболее опасных, высокоонкогенных штаммов ВПЧ, ответственных за 70-80% случаев развития рака шейки матки. Стандартный курс, состоящий из трёх прививок, даёт вполне надёжную защиту.
Целесообразно вакцинировать детей (девочек, а для сдерживания распространения инфекции и мальчиков) с 9-10 до 17 лет, а также молодых женщин (18-25 лет) до вступления в половую жизнь, так как вакцина предотвращает заражение, но не является средством лечения уже развившейся инфекции. Если пациентка уже живёт половой жизнью, то перед вакцинацией ей необходимо пройти исследование на наличие папилломавирусной инфекции. Однако даже при выявлении одного из штаммов, входящих в состав вакцины, проводить вакцинирование всё равно можно, так как это не является противопоказанием.
Папилломатоз шейки матки
На сегодняшний день ВПЧ является наиболее распространенным из всех заболеваний, передающихся половым путем. Вирусом папилломы человека заражены около 50% всего населения земли. В настоящее время насчитывается около 180 типов ВПЧ, из них 29 типов обладают онкогенным потенциалом. По степени онкогенного риска выделяют следующие группы ВПЧ:
Инкубационный период заболевания составляет от 1-го до 12-ти месяцев.
Что такое папиллома?
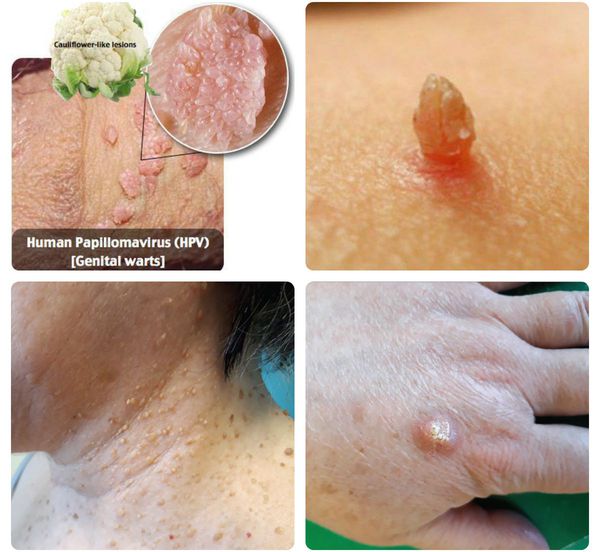
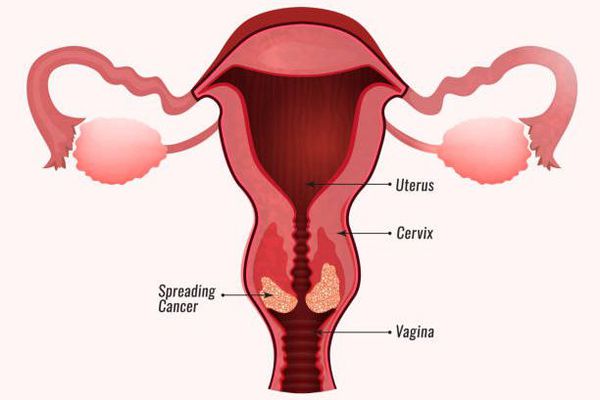
Папиллома выглядит как небольшой нарост (бородавка) телесного, розоватого или коричневатого цвета, на тонкой ножке. Она может достигать в размере 1-2 см. При обильном разрастании папилломы внешне напоминают структуру цветной капусты и, чаще всего, располагаются на половых органах, но могут появиться и в любом другом месте. У женщин они располагаются в области больших и малых половых губ, реже возникают папилломы шейки матки и влагалища.
Остроконечные кондиломы, вагинальные папилломы локализуются, в основном, в местах трения и травматизации при половом контакте. У женщин поражаются уздечка половых губ, большие и малые половые губы, клитор, уретра, лобок, промежность, перианальная область, преддверие и вход во влагалище, а также девственная плева, непосредственно влагалище и шейка матки. В уретре кондиломы располагаются кольцеобразно, главным образом в области наружного отверстия.
Чем опасен вирус папилломы человека
Знакомые многим папилломы, или бородавки, возникают в результате активности вируса, которым инфицирована значительная часть мирового населения. Вирус папилломы человека (ВПЧ) становится причиной появления специфических выростов не только на поверхности кожи, но также на слизистых оболочках (например, папиллома шейки матки) и в так называемых «пограничных» областях между слизистыми и эпителием кожи (например, кондиломы в области ануса и входа во влагалище).
Чем опасен вирус папилломы человека
Выросты на коже и слизистых оболочках, в зависимости от размера и расположения, часто бывают причиной ощутимого дискомфорта:
Но они представляют собой не только эстетическую проблему, но и потенциальную угрозу жизни и здоровью. Папиллома шейки матки основная причина рака шейки матки.
Когда возникает онкология?
Количество разных типов вируса папилломы человека достигает 180, и только 29 из них имеют доказанную способность провоцировать появление злокачественно изменённых клеток. Такие типы вируса называют «онкогенными». Наличие папилломы шейки матки, бородавок в области ануса и гениталий в любом случае должно стать поводом для начала лечения у хорошего специалиста, обязательных диагностических и лечебных процедур (лабораторное выявление типа вируса, удаление папиллом, коррекция иммунитета и др.).
Причины развития папиллом шейки матки
Заражение вирусом, которое впоследствии приводит к развитию папилломы шейки матки, как правило, происходит половым путем. Инфицирование может происходить также в бассейнах, банях, спортзалах и других общественных местах и в результате самозаражения при бритье, эпиляции, обкусывании ногтей, расчесах кожи.
Наблюдается также перенос вируса при папилломе шейки матке от родителей к детям. Новорожденные могут быть инфицированы в родах при прохождении через родовые пути матери, которая не прошла лечение папиллом влагалища, половых губ или шейки матки.
К группе риска заражения папилломой шейки матки относятся все женщины, живущие половой жизнью. Факторами риска развития инфекции являются:
Симптомы папилломатоза
Сложность диагностики и лечения папиллом шейки матки заключается в том, что данное заболевание может протекать практически бессимптомно! Тем не менее, некоторые пациенты отмечают косвенные признаки ВПЧ, к которым относятся:
Диагностика папилломатоза
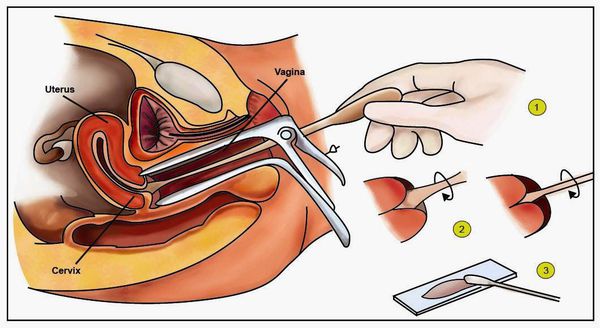
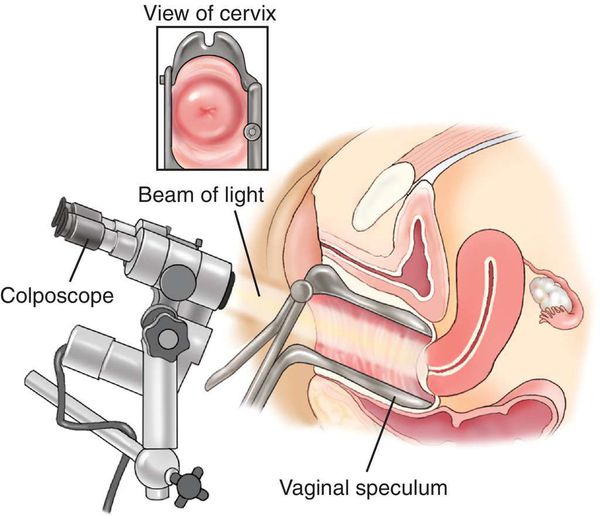
Диагноз «папилломатоз шейки матки» ставится на основании клинического осмотра, расширенной кольпоскопии, цитологического и гистологического исследования. Обязательным является обследование пациентов на наличие сопутствующих ИППП.
Обнаруженные при осмотре шейки матки в зеркалах и при расширенной кольпоскопии эктопия и лейкоплакия, являются обязательным показанием для обследования на ВПЧ. Наибольшее диагностическое значение в настоящее время придается методу полимеразной цепной реакции (ПЦР), позволяющий идентифицировать отдельные типы ВПЧ. Этот метод имеет большую прогностическую значимость, особенно если на фоне папилломавирусной инфекции уже имеется картина дисплазии эпителия шейки матки. Новым способом диагностики ВПЧ-инфекции является определение онкобелка Е7 в цервикальном материале методом иммунофлюоресцентного анализа.
Лечение папилломатоза
Лечение заболеваний, вызванных ВПЧ, включает в себя не только уничтожение образований, но и коррекцию общего и местного иммунодефицита, а также устранение факторов, способствующих развитию болезни. Адекватное лечение сопутствующих ИППП следует проводить перед деструкцией кондилом и обязательно на фоне приема иммунокорригирующих препаратов.
В клинике Гинеко для удаления папиллом применяется высокоэффективный и безболезненный метод высокочастотной радиоволновой деструкции.
Возможно ли удаление папиллом влагалища и шейки матки лазером?
В мировой медицинской практике папилломы в гинекологии удаляются хирургическим путем, химическим прижиганием, лазером, однако лучшим и наиболее эффективным методом считается малоинвазивная техника удаления папиллом радиоволновым аппаратом Сургитрон: цена на такую услугу невысока, а сама процедура практически безболезненна и не требует долгого восстановительного периода.
Разумеется, чтобы избежать рецидива, за подобной услугой стоит обращаться только в проверенные клиники, опытный специалист в обязательном порядке проводит диагностику, собирает анализы, чтобы точно установить причины папилломы шейки матки и назначить адекватную схему лечения.
Применение такого оперативного вмешательства в сочетании с индивидуально подобранной иммуномодулирующей и противовирусной терапией позволяет добиться полного выздоровления в короткие сроки.
Мы индивидуально подходим к решению проблем каждой пациентки, учитывая при выборе метода лечения ее возраст, иммунный статус, характер и локализацию заболевания, сопутствующие урогенитальные инфекции. Именно такой подход гарантирует нашим пациенткам высокую эффективность лечения и низкий риск возникновения рецидивов болезни.
В настоящее время, самым многообещающим и перспективным направлением борьбы с ВПЧ является, бесспорно, применение профилактической вакцинации против ВПЧ тех типов, которые являются самыми частыми виновниками рака шейки матки, рака вульвы, рака влагалища.
Лечение и профилактика прогрессирования заболеваний шейки матки, ассоциированных с вирусом папилломы человека
Приведены основные профилактические мероприятия, направленные на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки. Применение препарата инозин пранобекс повышает эффективность терапии заболеваний шейки матки, ассоц
Main preventive measures directed to early diagnostics and liquidation of development of HPV-associated cervical pathology. Use of inozin pranobex medication increases efficiency of therapy of cervical diseases associated with HPV infection.
Основными проблемами в тактике ведения женщин с заболеваниями шейки матки, ассоциированными с вирусом папилломы человека (ВПЧ), являются несвоевременная и некачественная диагностика, отсутствие четких алгоритмов при принятии решения, а также недостаточная приверженность пациенток к лечению, в основном связанная с полным или частичным невыполнением рекомендаций врача.
По оценкам Центров по контролю заболеваемости (англ. Centers for Disease Control and Prevention, CDC) в США ВПЧ инфицируются до 5,5 млн человек в год [1]. В Европе в год регистрируется 554 000 случаев заболеваний, вызванных этими вирусами, в том числе: цервикальных внутриэпителиальных (интраэпителиалъных) неоплазий (cervical intraepithelial neoplasia — CIN) легкой степени (CIN I), генитальных бородавок, CIN средней и тяжелой степени (CIN II и III), рака шейки матки (РШМ). Несмотря на современные методы диагностики и лечения предраковых заболеваний шейки матки, ежегодно в мире фиксируют 470 тыс. новых случаев РШМ, из которых 233 тыс. заканчиваются смертельным исходом [2]. По данным российских ученых папилломавирусная инфекция (ПВИ) гениталий встречается у 44,3% женщин, обращающихся в гинекологические клиники [3], а заболевания шейки матки, ассоциированные с ВПЧ, встречаются у 50–80% населения и 99,7% случаев подтвержденного РШМ.
Течение ВПЧ-инфекции зависит от состояния иммунной системы и может быть транзиторным, латентным и персистирующим [4–8]. Возможно самоизлечение латентных и начальных субклинических форм ПВИ, для чего важен врожденный компонент иммунной системы. Главное значение имеют клеточные, рецепторные и молекулярные механизмы защиты. Наиболее неблагоприятное течение — персистирующее. При этом ВПЧ «обманывает» иммунную систему макроорганизма, что позволяет ему длительно персистировать ввиду своих эволюционно приобретенных особенностей — репликационный цикл ограничен эпителием, нет виремии и цитолиза, имеется локальная иммуносупрессия за счет вирусных белков [9–11]. Длительная персистенция высокоонкогенных типов ВПЧ более двух лет является наиболее опасным фактором прогрессии предрака шейки матки [12]. При персистенции ВПЧ 16-го типа риск развития CIN составляет 40–50%, 26-го типа — 30–40%, 31-го, 58-го, 82-го типов — по 20–30%, 18-го, 33-го, 35-го, 51-го, 52-го типов — по 10–20% [12]. При обследовании молодых женщин с ПВИ персистенция ВПЧ через 1 год выявлялась у 30%, через 2 года — у 9%, в то время как у женщин старшего возраста — у 50% [13].
В мировой практике используются различные классификации ПВИ и ассоциированных с ней заболеваний. Ориентировочная классификация ПВИ представлена J. Handley и соавт. [14]:
Аногенитальная ВПЧ-инфекция и ассоциированные с ВПЧ заболевания
ВПЧ-инфекция
1. Клинические формы (видимые невооруженным глазом или невидимые, но при наличии соответствующей симптоматики):
2. Субклинические формы (невидимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом или гистологическом исследовании):
3. Латентные формы (отсутствие морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
Заболевания, ассоциированные с ВПЧ
Клинические и субклинические формы:
Кроме этого, в литературе при описании поражений шейки матки, ассоциированных с ВПЧ, применяют классификацию по Папаниколау — в зависимости от степени изменений в мазках выделяют 5 классов. ВОЗ рекомендует использовать терминологическую систему Бетесда (The Bethesda System — TBS) — норма, ASCUS (Atypical squamous cells of undertermined significance (атипичные клетки плоского эпителия неясного значения)), LSIL (Low grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение низкой степени тяжести)), HSIL (High grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение высокой степени тяжести)), карцинома. Однако TBS не исключает использование терминов CIN и «дисплазия».
Согласно существующим принципам по ведению больных с клиническими проявлениями, связанными с ВПЧ, лечение аногенитальных ВПЧ-поражений направлено на разрушение тем или иным методом папилломатозных очагов, возникающих на месте внедрения вируса. Именно такой подход приведен во всех основных рекомендациях по ведению больных с ВПЧ-инфекцией (CDC, Европейских рекомендациях, рекомендациях ВОЗ). Такой подход представлен и в рекомендациях Российского общества дерматовенерологов и косметологов.
Как для лечения клинических проявлений ВПЧ-инфекции, так и ассоциированных с ней заболеваний (в первую очередь это касается CIN II и CIN III), применяют деструктивные методы — хирургические, физические (крио-, электро- или лазеротерапия, радиоволновая хирургия) и химические.
При CIN I тактика может различаться в зависимости от величины поражения шейки матки, наличия другой патологии и возможностей самой пациентки [15]. Также в этом вопросе нет единогласия и ввиду возможности регресса данного заболевания. Общеизвестно, что хирургическое лечение может повлечь за собой до 40% осложнений (шеечное кровотечение, стриктуры цервикального канала, экстравазаты и субэпителиальные гематомы, истмико-цервикальную недостаточность, эндометриоз и др.), поэтому однозначность такого подхода при CIN I у женщин, зачастую еще не реализовавших репродуктивный потенциал, подлежит сомнению [16]. Установили, что прогностическими критериями течения CIN I могут служить анамнестические данные (возраст пациенток, возраст начала половой жизни, интервал между возрастом менархе и возрастом начала половой жизни) и данные клинико-лабораторных методов исследования — уровни вирусной нагрузки ВПЧ 16/18, клинико-кольпоскопического и иммуногистохимического индекса p16ink4a [16].
Одним из главных методов, позволяющих снизить заболеваемость РШМ, являются профилактические осмотры с проведением активного скрининга, направленного на выявление патологии шейки матки.
В ходе профилактического осмотра основными диагностическими методиками являются цитологическое исследование, кольпоскопия и определение ВПЧ.
С введения государственных программ ранней диагностики РШМ накоплен большой опыт по цитологическому скринингу, изложенный во множестве публикаций [17]. Одним из критериев оценки эффективности скрининга является изменение структуры патологии шейки матки за счет увеличения количества ранних предраковых состояний эпителия. Анализ литературы показывает, что при хорошо организованном цитологическом скрининге с широким охватом населения эффективность его очень высока и популяция женщин, прошедших обследование, имеет низкий риск развития РШМ. У них в 5 раз снижена вероятность обнаружения рака и в 10 раз — смертность по сравнению с группой необследованных женщин [18]. При этом вероятность пропуска заболевания на его начальном этапе составляет 1–2%, что связывают с недостаточной чувствительностью цитологических исследований [18]. Неправильный забор материала или недостаточная квалификация врача-цитолога могут приводить к большому количеству ложноотрицательных ответов, требующих дополнительных уточняющих методик. Накопленный опыт в нашей стране показал наилучшие результаты обследований в системах ведомственных лечебных учреждений, где охват прикрепленного контингента женщин достигает 100%, что в результате приводит к отсутствию случаев инвазивного РШМ в течение 2–5 лет [17].
Следующим после цитологического исследования важным диагностическим методом профилактического осмотра женщин является кольпоскопия. Среди задач, поставленных Министерством здравоохранения РФ на ближайшие годы, по внедрению стандартов диагностики и лечения в повседневную клиническую практику кольпоскопическое исследование является обязательным для первичных пациенток женских консультаций с ненормальными цитологическими мазками, женщин с патологией шейки матки и любыми заболеваниями влагалища, вульвы, шейки (код кольпоскопии А03.20.001) [17]. Таким образом, кольпоскопия является одним из ведущих методов обследования женщин, дополняющих цитологическое исследование.
Поскольку основная роль в генезе заболеваний шейки матки принадлежит ВПЧ, то тестирование на этот вирус является также важнейшим инструментом профилактических мероприятий. Особую озабоченность представляют пациентки с длительной персистенцией высокоонкогенных типов ВПЧ в сочетании с ASCUS. Женщинам, инфицированным ВПЧ, особенно типами высокого онкологического риска, требуется более активная диагностическая и терапевтическая тактика, соблюдение курсов терапии, строгий комплаенс.
При активном выявлении заболеваний шейки матки в ходе профилактических осмотров, а также при их ранней диагностике у женщин, самостоятельно обратившихся к гинекологу, чрезвычайно важным является выделение группы пациенток с минимальными субклиническими формами болезни для своевременного лечения и диспансерного наблюдения в женских консультациях [17]. В этой связи важное значение приобретает необходимость длительного контроля и фармакотерапии, направленной на подавление вируса, а также готовность пациентки следовать рекомендованному лечению.
Ранняя диагностика и принципы лечения начальных проявлений CIN остаются одной из дискутабельных проблем в акушерско-гинекологической практике. При небольшом поражении чаще рекомендуют оставить женщину под наблюдением и периодически выполнять обследования — тесты на ВПЧ, кольпоскопию, цитологию. Очень важно при этом диагностировать и лечить воспалительные, дисгормональные и другие заболевания урогенитального тракта. Большую роль в определении тактики ведения больных в этих случаях имеет желание пациентки и ее возможность регулярного посещения врача для проведения обследования и желание следовать рекомендациям врача в выборе медикаментозной терапии. Выжидательная тактика при ПВИ часто связана с тем, что носительство и персистенция свидетельствуют не о предраковом процессе как таковом, а о многократно повышенном риске возникновения последнего, усугубляющегося при дополнительных факторах риска у ряда пациенток [25]. Так, G. Но и соавт. [10] показали, что персистенция ВПЧ более 6 мес встречалась с увеличением возраста женщины и обусловлена типом ВПЧ.
Появление патологических изменений в цитологических мазках возрастает по мере персистенции ВПЧ высокого канцерогенного риска у большинства женщин. Согласно данным литературы после инфицирования ВПЧ CIN II–III развивается уже через 3 года у 27% женщин. При анализе исходов CIN, ассоциированных с ВПЧ, было показано, что при CIN I регрессия наблюдается в 57%, персистенция — в 32%, прогрессия — 11%, а развитие инвазивного рака — только в 1% случаев. При CIN II регрессия наблюдается в 43%, персистенция — в 35%, прогрессия — в 22%, а развитие инвазивного рака — в 5% случаев. В то же время при CIN III малигнизация происходит более чем в 12% случаев, а регрессия — лишь в 32% [26, 27].
В связи с вышесказанным, другим подходом в тактике ведения пациенток с начальными проявлениями CIN может быть назначение противовирусной терапии и контроль со стороны врача за четким выполнением рекомендаций и схем медикаментозной терапии.
Этиопатогенез минимальных изменений эпителия (легкая дисплазия или атипические изменения неясной причины) связан с ВПЧ, который на этой стадии заболевания еще находится в клетке в эписомальном состоянии и не повреждает ее геном. Следовательно, именно на этом этапе развития системный и местный иммунитет будет играть ведущую роль в прогнозе развития болезни. По данным биопсий шейки матки латентные формы инфекции выявляются у 8,1% женщин, а субклинические у 40–60% [25, 28]. Именно поэтому медикаментозная терапия при начальных формах поражения эпителия должна быть направлена на подавление вируса при соблюдении комплаенса, понимании пациенткой необходимости завершения курса для повышения эффективности лечения.
В своем исследовании R. Richard и B. Barron [29] показали, что среднее время для развития карциномы in situ составляет примерно 5 лет для больных со слабой дисплазией, 3 года — с умеренной и 1 год — с выраженной дисплазией. Это позволило предположить, что 66% всех дисплазий будет прогрессировать до карциномы, но достаточно длительное время, которое необходимо использовать для раннего выявления и лечения. В клинической ситуации, несмотря на то, что имеется достаточный период безопасного времени для динамического наблюдения, многие врачи и пациентки после информирования о диагнозе не хотят длительно наблюдаться даже с начальной патологией эпителия. Женщины хотят быть излеченными сразу, что часто предопределяет активную тактику ведения больных, включая деструкцию активной зоны трансформации и иммуно/противовирусную терапию [29–33].
Таким образом, у пациенток с «минимальным» повреждением эпителия шейки матки, например ASCUS, с наличием цитоплазматического эффекта ВПЧ (койлоцитоз при цитологическом исследовании) и положительном ВПЧ-тесте и его высоком титре, может оказаться актуальным применение препарата с двойным противовирусным действием — инозин пранобекс (Изопринозин).
Это один из немногих иммунотропных и противовирусных препаратов, в инструкции по применению которого указана терапия заболеваний, вызванных ВПЧ. Он также входит в Европейскую классификацию методов лечения аногенитальных бородавок [34]. В настоящее время накоплен огромный опыт применения Изопринозина, так как используется он с 1970-х гг. и зарегистрирован в большинстве стран Европы.
Изопринозин — иммуномодулятор, стимулирующий противовирусную защиту организма. Помимо иммунотропного, Изопринозин обладает прямым противовирусным действием, угнетая синтез вирусов путем встраивания инозин-оротовой кислоты в полирибосомы пораженной вирусом клетки и нарушая присоединение адениловой кислоты к вирусной РНК.
Таким образом, обладая противовирусным действием и оказывая влияние на противовирусный иммунитет, Изопринозин прямо и косвенно способен подавлять репликацию ВПЧ и образование вирусных белков. Эти эффекты могут изменять механизм взаимодействия ВПЧ и макроорганизма, препятствуя переходу вируса из транзиторной в персистирующую форму, а также влияя на клиническую манифестацию инфекции.
Одним из показаний применения препарата являются инфекции, вызванные вирусом папилломы человека: остроконечные кондиломы, ПВИ вульвы, вагины и шейки матки (в составе комплексной терапии).
При инфекциях, вызванных ВПЧ, Изопринозин назначают по 3 г/сут (2 таблетки 3 раза в сутки) как дополнение к местной терапии или хирургическому вмешательству в течение 14–28 дней или 5 дней в неделю последовательно в течение 1–2 недель в месяц в течение 3 месяцев. При дисплазии шейки матки, ассоциированной с ВПЧ: по 2 таблетки (1000 мг) 3 раза в сутки в течение 10 дней, далее 2–3 курса с интервалом 10–14 дней.
Улучшение морфологической картины эпителия вульвы показано в исследовании Sun Kuie Tay [32]. Инозин пранобекс назначали по 1 г 3 раза в сутки в течение 6 недель. Положительный эффект был достигнут у 63,5% больных, а в группе, принимавшей плацебо, — у 16,7%.
В другом исследовании при монотерапии Изопринозином по 3 г в сутки у 44 женщин с CIN I (длительность лечения 10 дней) и CIN II (длительность лечения 21 день) установлено, что выраженный клинический эффект наблюдался у 88,6% пациенток — полностью исчезало поражение эпителия экзоцервикса, что подтверждалось кольпоскопически и гистологически [35].
В работе Т. В. Клинышковой и соавт. [36] показана высокая частота регресса CIN I (70%) и прекращения выделения ВПЧ (83,3%) при использовании Изопринозина в режиме монотерапии и комбинированного лечения в сочетании с деструкцией у пациенток с ВПЧ-ассоциированными поражениями шейки матки. Изопринозин назначали по 3 г в сутки двумя 10-дневными курсами — за 1 месяц до деструкции и с 1-го дня деструкции при четком контроле за выполнением курса лечения.
В. Н. Прилепская сообщает о прекращении выделения ВПЧ у 65,6% больных после комбинированной терапии (Изопринозин + деструкция очагов) CIN низкой степени [3]. При использовании только деструкции очагов этот результат был достигнут у 46,9% больных. Изопринозин назначали по 1 г 3 раза в сутки в течение 5 дней за 7–10 дней до проведения деструкции.
Похожие результаты — прекращение выделения ВПЧ у 77% больных — показаны в исследовании И. В. Шевниной (2009 г.) при комбинированной терапии женщин с CIN и аногенитальными бородавками. Изопринозин назначали по 1 г 3 раза в сутки в течение 10 дней, затем по 0,5 грамма 3 раза в сутки в течение 20 дней.
В другом исследовании Изопринозин назначали женщинам с патологией шейки матки, ассоциированной с ВПЧ [37]. Препарат назначали после проведения обследования и противовоспалительной терапии по 3 г в сутки в течение 10 дней. Элиминация ВПЧ достигнута у 95,3% пациенток.
Есть и другие исследования, в которых показано прекращение выделения ВПЧ из очагов поражения у 69,6–97,8% женщин, принимавших Изопринозин [30, 38, 39].
Представленные данные свидетельствуют о возможной эффективности монотерапии Изопринозином при бессимптомном вирусовыделении, когда применение деструктивных методик не показано.
Сравнительная оценка лечения с применением Изопринозина и без него показала преимущество дополнительной лекарственной терапии вне зависимости от степени онкологического риска. Так, в группе женщин с начальными изменениями эпителия самостоятельное улучшение после санации влагалища достигнуто в 64,9% наблюдений, а при применении Изопринозина в 80,4% случаев [17]. У пациенток с изменениями легкой степени тяжести, выявленными при кольпоскопическом или цитологическом исследованиях, даже в случаях отсутствия самостоятельных улучшений более 3 мес Изопринозин был эффективен почти в 85% наблюдений [17].
Результаты исследования, проведенного в ФГБУ НЦАГиП им. акад. В. И. Кулакова [40, 41], показали, что инозин пранобекс подавляет репликацию высокоонкогенных типов ВПЧ и способствует исчезновению койлоцитарной атипии у 94% пациенток с поражением эпителия шейки матки.
При использовании Изопринозина в режиме монотерапии и в комбинации с деструкцией у пациенток с ВПЧ-ассоцированными поражениями низкой степени получена высокая частота регресса CIN I, прекращение выделения ВПЧ, снижение вирусной нагрузки, активация интерферонового ответа в сравнении с традиционными подходами [16]. Через 4 мес у пациенток, принимавших Изопринозин, в 2 раза снизилась частота экспрессии онкобелка Е7 по сравнению с контрольной группой. Кроме этого были отмечены и другие значимые позитивные изменения в отличие от контрольной группы, где имелась лишь тенденция к этому. Выявленные различия позволяют расценивать их как патогенетические предпосылки неполного клинического эффекта и отдаленного рецидивирования заболевания у пациенток контрольной группы. Эффективность лечения в группе пациенток, принимавших Изопринозин, по окончании лечения была в 1,4 раза выше, чем при традиционном лечении.
Заключение
Таким образом, основными профилактическими мероприятиями, направленными на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки, могут быть:
Многочисленные исследования, проведенные во многих странах мира, в том числе и в России, показали, что при применении Изопринозина (в комбинации с деструкцией или в виде монотерапии), благодаря его двойному противовирусному и иммуномодулирующему действию, подавляющему репликацию ВПЧ, повышается эффективность терапии заболеваний шейки матки, ассоциированных с ПВИ.
Для достижения этих результатов важным является соблюдение дозировок и продолжительности лечения. Как было указано выше, наиболее опасной с точки зрения прогрессирования дисплазии является персистенция ВПЧ, при которой вирус встраивается в геном эпителиальной клетки. Противовирусное действие при этом должно продолжаться несколько месяцев, чтобы захватить несколько циклов полного обновления эпителия. Именно поэтому для консервативной терапии дисплазий предлагается длительное многокурсовое лечение — два-три 10-дневных курса с интервалом 10–14 дней. Такие курсы, как показали результаты многочисленных исследований, приведенные в данной работе, позволяют достичь высокой эффективности лечения. Чем ниже уровень выполнения пациентками предписаний врача, тем ниже уровень эффективности лечения и выше риск рецидивирования и прогрессирования патологии.
Литература
А. М. Соловьев*, кандидат медицинских наук
Д. В. Логвинова**
*ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
**НПЦДК ДЗМ, Москва
Папиллома шейки матки
Довольно распространенной ситуацией при прохождении гинекологического осмотра является обнаружение такого образования, как папиллома шейки матки.
Иначе цервикальная папиллома.
Причиной возникновения данного образования служит вирус папилломы человека (ВПЧ).
Его специфической особенностью является способность поражать эпителиальные клетки слизистых и кожных покровов.
Огромное число известных на настоящий момент представителей ВПЧ принято выделять в три группы:
Какие ВПЧ вызывают поражения шейки матки?
Видимые папилломы на шейке матки, иначе называемые аногенитальными бородавками, провоцируются именно представителями 2й группы.
То есть имеют риск развития онкологии очень незначительный.
Примерно 90% эпизодов аногенитальных бородавок обусловлено вирусами 6 и 11 типов.
В то же время рак шейки матки вызывается в 93% случаев папилломавирусом высокой онкогенности, среди которых 70% приходится на долю вирусов 16 и 18 типа.
Особенностью именно папиллом шейки матки оказывается то, что их вызывают вирусы низкого онкогенного риска.
Они более склонны к озлокачествлению, нежели кондиломы иных локализаций.
Каковы особенности течения папилломавирусной инфекции и чем опасно заражение?
Инфицированность папилломавирусами среди взрослых, согласно данным ВОЗ, достигает 80%.
При этом какие-либо проявления болезни отмечаются не более чем у 10% инфицированных.
После заражения в ряде случаев в течение пары лет происходит самоизлечение.
Вот почему зачастую рекомендуют некоторое время не проводить активного лечения, придерживаясь выжидательной тактики.
Папилломавирусы проникают в эпителий, особенно затрагивая область перехода плоского эпителия в цилиндрический.
При этом вирус может находиться просто в клетке, а может встраиваться в геном, провоцируя мутации.
Если мутантные клетки размножаются, то появляется опухоль.
Вирусная инфекция может протекать в следующих формах:
Каковы пути инфицирования и заразность?
Передается ВПЧ преимущественно половым путем.
Дети могут заражаться от матерей в процессе родов.
Допускается вероятность контактно-бытового пути заражения, однако пока нет достаточного количества подтверждающих этот факт данных.
Какие бывают папилломы шейки матки и как они проявляются?
Кондиломы (папилломы) шейки матки представляют собой характерные образования, выявляемые при осмотре.
Они обычно сочетаются с аногенитальными бородавками (остроконечными кондиломами).
Более часто диагностируются такие образования у беременных.
Существует два типа кондилом маточной шейки:
Признаки экзофитных кондилом:
Осложнения остроконечных кондилом включают травмирование, появление болезненных трещин и кровоточивости.
Плоская папиллома шейки размещается в толще эпителиального слоя, не видна невооруженным взглядом.
Примерно в 4 – 10% случаев такие образования озлокачествляются в течение двух лет после появления.
На начальных стадиях симптомы у эндофитных папиллом отсутствуют.
Но при осмотре врач может обнаружить гипертрофические изменения и уплотнение шейки матки.
Обычно кондиломы на маточной шейке сливаются в светло-желтые либо белые бляшки, занимая практически всю поверхность маточного отверстия.
При переходе папиллом в рак на поздних стадиях могут проявляться (но не всегда):
Зачастую при обнаружении папилломы на шейке матки выявляется и сопутствующая эрозия – смещение от нормального положения границы между цилиндрическим и плоским эпителием.
Примерно каждая четвертая женщина имеет врожденную эрозию (иначе эктопию), не требующую терапии.
Истинная же эрозия, для которой характерно заметное повреждение плоского эпителия, вызывается травмой либо воспалением.
В подобной ситуации помимо папилломы шейки могут наблюдаться и выделения: розоватые, гнойные, кровянистые и т.п.
При наличии таких признаков обязательно следует показаться доктору, провести соответствующие диагностические исследования и лечение.
Довольно часто, а у женщин репродуктивного возраста почти в половине всех случаев заболевания, плоская кондилома маточной шейки сочетается с дисплазией легкой степени, реже – тяжелой.
В 5% эпизодов диагностируется и преинвазивная карцинома.
Женщины, у которых в шейке матки выявляется ВПЧ, имеют риск развития рака в 65 раз больший, чем те, у которых нет этого вируса.
А у женщин от 30-ти лет с инфицированием ВПЧ высокой онкогенности риск увеличивается в 130 раз.
Папилломатоз шейки матки
На сегодняшний день ВПЧ является наиболее распространенным из всех заболеваний, передающихся половым путем. Вирусом папилломы человека заражены около 50% всего населения земли. В настоящее время насчитывается около 180 типов ВПЧ, из них 29 типов обладают онкогенным потенциалом. По степени онкогенного риска выделяют следующие группы ВПЧ:
Инкубационный период заболевания составляет от 1-го до 12-ти месяцев.
Что такое папиллома?
Папиллома выглядит как небольшой нарост (бородавка) телесного, розоватого или коричневатого цвета, на тонкой ножке. Она может достигать в размере 1-2 см. При обильном разрастании папилломы внешне напоминают структуру цветной капусты и, чаще всего, располагаются на половых органах, но могут появиться и в любом другом месте. У женщин они располагаются в области больших и малых половых губ, реже возникают папилломы шейки матки и влагалища.
Остроконечные кондиломы, вагинальные папилломы локализуются, в основном, в местах трения и травматизации при половом контакте. У женщин поражаются уздечка половых губ, большие и малые половые губы, клитор, уретра, лобок, промежность, перианальная область, преддверие и вход во влагалище, а также девственная плева, непосредственно влагалище и шейка матки. В уретре кондиломы располагаются кольцеобразно, главным образом в области наружного отверстия.
Чем опасен вирус папилломы человека
Знакомые многим папилломы, или бородавки, возникают в результате активности вируса, которым инфицирована значительная часть мирового населения. Вирус папилломы человека (ВПЧ) становится причиной появления специфических выростов не только на поверхности кожи, но также на слизистых оболочках (например, папиллома шейки матки) и в так называемых «пограничных» областях между слизистыми и эпителием кожи (например, кондиломы в области ануса и входа во влагалище).
Чем опасен вирус папилломы человека
Выросты на коже и слизистых оболочках, в зависимости от размера и расположения, часто бывают причиной ощутимого дискомфорта:
Но они представляют собой не только эстетическую проблему, но и потенциальную угрозу жизни и здоровью. Папиллома шейки матки основная причина рака шейки матки.
Когда возникает онкология?
Количество разных типов вируса папилломы человека достигает 180, и только 29 из них имеют доказанную способность провоцировать появление злокачественно изменённых клеток. Такие типы вируса называют «онкогенными». Наличие папилломы шейки матки, бородавок в области ануса и гениталий в любом случае должно стать поводом для начала лечения у хорошего специалиста, обязательных диагностических и лечебных процедур (лабораторное выявление типа вируса, удаление папиллом, коррекция иммунитета и др.).
Причины развития папиллом шейки матки
Заражение вирусом, которое впоследствии приводит к развитию папилломы шейки матки, как правило, происходит половым путем. Инфицирование может происходить также в бассейнах, банях, спортзалах и других общественных местах и в результате самозаражения при бритье, эпиляции, обкусывании ногтей, расчесах кожи.
Наблюдается также перенос вируса при папилломе шейки матке от родителей к детям. Новорожденные могут быть инфицированы в родах при прохождении через родовые пути матери, которая не прошла лечение папиллом влагалища, половых губ или шейки матки.
К группе риска заражения папилломой шейки матки относятся все женщины, живущие половой жизнью. Факторами риска развития инфекции являются:
Симптомы папилломатоза
Сложность диагностики и лечения папиллом шейки матки заключается в том, что данное заболевание может протекать практически бессимптомно! Тем не менее, некоторые пациенты отмечают косвенные признаки ВПЧ, к которым относятся:
Диагностика папилломатоза
Диагноз «папилломатоз шейки матки» ставится на основании клинического осмотра, расширенной кольпоскопии, цитологического и гистологического исследования. Обязательным является обследование пациентов на наличие сопутствующих ИППП.
Обнаруженные при осмотре шейки матки в зеркалах и при расширенной кольпоскопии эктопия и лейкоплакия, являются обязательным показанием для обследования на ВПЧ. Наибольшее диагностическое значение в настоящее время придается методу полимеразной цепной реакции (ПЦР), позволяющий идентифицировать отдельные типы ВПЧ. Этот метод имеет большую прогностическую значимость, особенно если на фоне папилломавирусной инфекции уже имеется картина дисплазии эпителия шейки матки. Новым способом диагностики ВПЧ-инфекции является определение онкобелка Е7 в цервикальном материале методом иммунофлюоресцентного анализа.
Лечение папилломатоза
Лечение заболеваний, вызванных ВПЧ, включает в себя не только уничтожение образований, но и коррекцию общего и местного иммунодефицита, а также устранение факторов, способствующих развитию болезни. Адекватное лечение сопутствующих ИППП следует проводить перед деструкцией кондилом и обязательно на фоне приема иммунокорригирующих препаратов.
В клинике Гинеко для удаления папиллом применяется высокоэффективный и безболезненный метод высокочастотной радиоволновой деструкции.
Возможно ли удаление папиллом влагалища и шейки матки лазером?
В мировой медицинской практике папилломы в гинекологии удаляются хирургическим путем, химическим прижиганием, лазером, однако лучшим и наиболее эффективным методом считается малоинвазивная техника удаления папиллом радиоволновым аппаратом Сургитрон: цена на такую услугу невысока, а сама процедура практически безболезненна и не требует долгого восстановительного периода.
Разумеется, чтобы избежать рецидива, за подобной услугой стоит обращаться только в проверенные клиники, опытный специалист в обязательном порядке проводит диагностику, собирает анализы, чтобы точно установить причины папилломы шейки матки и назначить адекватную схему лечения.
Применение такого оперативного вмешательства в сочетании с индивидуально подобранной иммуномодулирующей и противовирусной терапией позволяет добиться полного выздоровления в короткие сроки.
Мы индивидуально подходим к решению проблем каждой пациентки, учитывая при выборе метода лечения ее возраст, иммунный статус, характер и локализацию заболевания, сопутствующие урогенитальные инфекции. Именно такой подход гарантирует нашим пациенткам высокую эффективность лечения и низкий риск возникновения рецидивов болезни.
В настоящее время, самым многообещающим и перспективным направлением борьбы с ВПЧ является, бесспорно, применение профилактической вакцинации против ВПЧ тех типов, которые являются самыми частыми виновниками рака шейки матки, рака вульвы, рака влагалища.
Папилломы на шейке матки: причины и лечение
Папилломы на шейке матки: причины и лечение
Говоря о причине появления папиллом, мы вступаем в одну из самых загадочных областей медицинских знаний – природы вирусов. Эти микроскопические образования имеют неклеточное строение в отличие от большинства живущих на Земле организмов. Существуют они, исключительно паразитируя на живых клетках.
Интересующий нас папилломавирус (ВПЧ или HPV) проникает в клетки кожи, встраивается в хромосомы и меняет программу роста тканей. Клетки начинают усиленное деление, разрастаясь с образованием папиллом. Уже выявлено более ста штаммов ВПЧ, но далеко не все из них хорошо изучены.
Отчего появляются папилломы
Причина папиллом на шейке матки одна – попадание в организм вируса. А вот путей, с помощью которых он может проникнуть, несколько. Перечислим их в порядке роста вероятности заражения:
Иммунитет здорового человека настолько силен, что способен побороть вирус папилломы. Если иммунные клетки контролируют вирус, внешние формы болезни развиваются не сразу после заражения. Однако при ослаблении защитных сил (сильном стрессе, утомлении, чрезмерном употреблении алкоголя, курении) вирус может активизироваться и вызвать образование папиллом, а также связанных с ними патологий.
Дисплазия и папилломы
При отсутствии лечения вирус папилломы повышенной онкогенности (в основном типы 16 и 18) может приводить к дисплазии. Это предраковое состояние, при котором выявляется нарушение строения шеечного эпителия и замещение нормальных клеток атипичными. Этот процесс еще не является злокачественным, но со временем может привести к раку. Время этого перехода индивидуально для каждой женщины и зависит от многих факторов: крепости иммунитета, наследственности и других.
По наблюдениям практикующих врачей время перерождения дисплазии в онкологический процесс варьируется от 10 до 20 лет. Если как можно раньше избавиться от причины дисплазии шейки матки – вируса папилломы, то это устранит неблагоприятный прогноз течения болезни.
Лучшее средство профилактики рака – регулярные осмотры у гинеколога и взятие контрольного мазка на онкоцитологию. Посещать гинеколога следует каждые шесть месяцев. Особенно четко соблюдать эти рекомендации должны женщины-носительницы ВПЧ.
Лечение папилломатоза шейки матки
Современные схемы избавления от этого заболевания базируются на трех основных моментах:
Оптимальный способ удаления папиллом определяется с учетом размера, вида, наличия осложнений после консультации с врачом-гинекологом. На сегодняшний момент успешно применяется множество методик:
Вопрос о том, возможно ли окончательное излечение от вируса папилломы, остается открытым. Большинство врачей сходится во мнении, что вне обострения ВПЧ не регистрируется современными диагностическими средствами. Альтернативная точка зрения заключается в том, что комплексное лечение позволяет навсегда забыть о данном заболевании при условии исключения повторного инфицирования.
Вакцинация
Революционным открытием стало изобретение вакцины, которая способна защитить от высокоонкогенных типов вируса. Наибольшей эффективности удается добиться, применяя вакцину до начала половой жизни у девочек 12-13 летнего возраста. Вакцинация от HPV официально одобрена более чем в 120 странах, включая Россию.
Лечение и профилактика прогрессирования заболеваний шейки матки, ассоциированных с вирусом папилломы человека
Приведены основные профилактические мероприятия, направленные на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки. Применение препарата инозин пранобекс повышает эффективность терапии заболеваний шейки матки, ассоц
Main preventive measures directed to early diagnostics and liquidation of development of HPV-associated cervical pathology. Use of inozin pranobex medication increases efficiency of therapy of cervical diseases associated with HPV infection.
Основными проблемами в тактике ведения женщин с заболеваниями шейки матки, ассоциированными с вирусом папилломы человека (ВПЧ), являются несвоевременная и некачественная диагностика, отсутствие четких алгоритмов при принятии решения, а также недостаточная приверженность пациенток к лечению, в основном связанная с полным или частичным невыполнением рекомендаций врача.
По оценкам Центров по контролю заболеваемости (англ. Centers for Disease Control and Prevention, CDC) в США ВПЧ инфицируются до 5,5 млн человек в год [1]. В Европе в год регистрируется 554 000 случаев заболеваний, вызванных этими вирусами, в том числе: цервикальных внутриэпителиальных (интраэпителиалъных) неоплазий (cervical intraepithelial neoplasia — CIN) легкой степени (CIN I), генитальных бородавок, CIN средней и тяжелой степени (CIN II и III), рака шейки матки (РШМ). Несмотря на современные методы диагностики и лечения предраковых заболеваний шейки матки, ежегодно в мире фиксируют 470 тыс. новых случаев РШМ, из которых 233 тыс. заканчиваются смертельным исходом [2]. По данным российских ученых папилломавирусная инфекция (ПВИ) гениталий встречается у 44,3% женщин, обращающихся в гинекологические клиники [3], а заболевания шейки матки, ассоциированные с ВПЧ, встречаются у 50–80% населения и 99,7% случаев подтвержденного РШМ.
Течение ВПЧ-инфекции зависит от состояния иммунной системы и может быть транзиторным, латентным и персистирующим [4–8]. Возможно самоизлечение латентных и начальных субклинических форм ПВИ, для чего важен врожденный компонент иммунной системы. Главное значение имеют клеточные, рецепторные и молекулярные механизмы защиты. Наиболее неблагоприятное течение — персистирующее. При этом ВПЧ «обманывает» иммунную систему макроорганизма, что позволяет ему длительно персистировать ввиду своих эволюционно приобретенных особенностей — репликационный цикл ограничен эпителием, нет виремии и цитолиза, имеется локальная иммуносупрессия за счет вирусных белков [9–11]. Длительная персистенция высокоонкогенных типов ВПЧ более двух лет является наиболее опасным фактором прогрессии предрака шейки матки [12]. При персистенции ВПЧ 16-го типа риск развития CIN составляет 40–50%, 26-го типа — 30–40%, 31-го, 58-го, 82-го типов — по 20–30%, 18-го, 33-го, 35-го, 51-го, 52-го типов — по 10–20% [12]. При обследовании молодых женщин с ПВИ персистенция ВПЧ через 1 год выявлялась у 30%, через 2 года — у 9%, в то время как у женщин старшего возраста — у 50% [13].
В мировой практике используются различные классификации ПВИ и ассоциированных с ней заболеваний. Ориентировочная классификация ПВИ представлена J. Handley и соавт. [14]:
Аногенитальная ВПЧ-инфекция и ассоциированные с ВПЧ заболевания
ВПЧ-инфекция
1. Клинические формы (видимые невооруженным глазом или невидимые, но при наличии соответствующей симптоматики):
2. Субклинические формы (невидимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом или гистологическом исследовании):
3. Латентные формы (отсутствие морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
Заболевания, ассоциированные с ВПЧ
Клинические и субклинические формы:
Кроме этого, в литературе при описании поражений шейки матки, ассоциированных с ВПЧ, применяют классификацию по Папаниколау — в зависимости от степени изменений в мазках выделяют 5 классов. ВОЗ рекомендует использовать терминологическую систему Бетесда (The Bethesda System — TBS) — норма, ASCUS (Atypical squamous cells of undertermined significance (атипичные клетки плоского эпителия неясного значения)), LSIL (Low grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение низкой степени тяжести)), HSIL (High grade squamous intraepithelial lesion (интраэпителиальное плоскоклеточное поражение высокой степени тяжести)), карцинома. Однако TBS не исключает использование терминов CIN и «дисплазия».
Согласно существующим принципам по ведению больных с клиническими проявлениями, связанными с ВПЧ, лечение аногенитальных ВПЧ-поражений направлено на разрушение тем или иным методом папилломатозных очагов, возникающих на месте внедрения вируса. Именно такой подход приведен во всех основных рекомендациях по ведению больных с ВПЧ-инфекцией (CDC, Европейских рекомендациях, рекомендациях ВОЗ). Такой подход представлен и в рекомендациях Российского общества дерматовенерологов и косметологов.
Как для лечения клинических проявлений ВПЧ-инфекции, так и ассоциированных с ней заболеваний (в первую очередь это касается CIN II и CIN III), применяют деструктивные методы — хирургические, физические (крио-, электро- или лазеротерапия, радиоволновая хирургия) и химические.
При CIN I тактика может различаться в зависимости от величины поражения шейки матки, наличия другой патологии и возможностей самой пациентки [15]. Также в этом вопросе нет единогласия и ввиду возможности регресса данного заболевания. Общеизвестно, что хирургическое лечение может повлечь за собой до 40% осложнений (шеечное кровотечение, стриктуры цервикального канала, экстравазаты и субэпителиальные гематомы, истмико-цервикальную недостаточность, эндометриоз и др.), поэтому однозначность такого подхода при CIN I у женщин, зачастую еще не реализовавших репродуктивный потенциал, подлежит сомнению [16]. Установили, что прогностическими критериями течения CIN I могут служить анамнестические данные (возраст пациенток, возраст начала половой жизни, интервал между возрастом менархе и возрастом начала половой жизни) и данные клинико-лабораторных методов исследования — уровни вирусной нагрузки ВПЧ 16/18, клинико-кольпоскопического и иммуногистохимического индекса p16ink4a [16].
Одним из главных методов, позволяющих снизить заболеваемость РШМ, являются профилактические осмотры с проведением активного скрининга, направленного на выявление патологии шейки матки.
В ходе профилактического осмотра основными диагностическими методиками являются цитологическое исследование, кольпоскопия и определение ВПЧ.
С введения государственных программ ранней диагностики РШМ накоплен большой опыт по цитологическому скринингу, изложенный во множестве публикаций [17]. Одним из критериев оценки эффективности скрининга является изменение структуры патологии шейки матки за счет увеличения количества ранних предраковых состояний эпителия. Анализ литературы показывает, что при хорошо организованном цитологическом скрининге с широким охватом населения эффективность его очень высока и популяция женщин, прошедших обследование, имеет низкий риск развития РШМ. У них в 5 раз снижена вероятность обнаружения рака и в 10 раз — смертность по сравнению с группой необследованных женщин [18]. При этом вероятность пропуска заболевания на его начальном этапе составляет 1–2%, что связывают с недостаточной чувствительностью цитологических исследований [18]. Неправильный забор материала или недостаточная квалификация врача-цитолога могут приводить к большому количеству ложноотрицательных ответов, требующих дополнительных уточняющих методик. Накопленный опыт в нашей стране показал наилучшие результаты обследований в системах ведомственных лечебных учреждений, где охват прикрепленного контингента женщин достигает 100%, что в результате приводит к отсутствию случаев инвазивного РШМ в течение 2–5 лет [17].
Следующим после цитологического исследования важным диагностическим методом профилактического осмотра женщин является кольпоскопия. Среди задач, поставленных Министерством здравоохранения РФ на ближайшие годы, по внедрению стандартов диагностики и лечения в повседневную клиническую практику кольпоскопическое исследование является обязательным для первичных пациенток женских консультаций с ненормальными цитологическими мазками, женщин с патологией шейки матки и любыми заболеваниями влагалища, вульвы, шейки (код кольпоскопии А03.20.001) [17]. Таким образом, кольпоскопия является одним из ведущих методов обследования женщин, дополняющих цитологическое исследование.
Поскольку основная роль в генезе заболеваний шейки матки принадлежит ВПЧ, то тестирование на этот вирус является также важнейшим инструментом профилактических мероприятий. Особую озабоченность представляют пациентки с длительной персистенцией высокоонкогенных типов ВПЧ в сочетании с ASCUS. Женщинам, инфицированным ВПЧ, особенно типами высокого онкологического риска, требуется более активная диагностическая и терапевтическая тактика, соблюдение курсов терапии, строгий комплаенс.
При активном выявлении заболеваний шейки матки в ходе профилактических осмотров, а также при их ранней диагностике у женщин, самостоятельно обратившихся к гинекологу, чрезвычайно важным является выделение группы пациенток с минимальными субклиническими формами болезни для своевременного лечения и диспансерного наблюдения в женских консультациях [17]. В этой связи важное значение приобретает необходимость длительного контроля и фармакотерапии, направленной на подавление вируса, а также готовность пациентки следовать рекомендованному лечению.
Ранняя диагностика и принципы лечения начальных проявлений CIN остаются одной из дискутабельных проблем в акушерско-гинекологической практике. При небольшом поражении чаще рекомендуют оставить женщину под наблюдением и периодически выполнять обследования — тесты на ВПЧ, кольпоскопию, цитологию. Очень важно при этом диагностировать и лечить воспалительные, дисгормональные и другие заболевания урогенитального тракта. Большую роль в определении тактики ведения больных в этих случаях имеет желание пациентки и ее возможность регулярного посещения врача для проведения обследования и желание следовать рекомендациям врача в выборе медикаментозной терапии. Выжидательная тактика при ПВИ часто связана с тем, что носительство и персистенция свидетельствуют не о предраковом процессе как таковом, а о многократно повышенном риске возникновения последнего, усугубляющегося при дополнительных факторах риска у ряда пациенток [25]. Так, G. Но и соавт. [10] показали, что персистенция ВПЧ более 6 мес встречалась с увеличением возраста женщины и обусловлена типом ВПЧ.
Появление патологических изменений в цитологических мазках возрастает по мере персистенции ВПЧ высокого канцерогенного риска у большинства женщин. Согласно данным литературы после инфицирования ВПЧ CIN II–III развивается уже через 3 года у 27% женщин. При анализе исходов CIN, ассоциированных с ВПЧ, было показано, что при CIN I регрессия наблюдается в 57%, персистенция — в 32%, прогрессия — 11%, а развитие инвазивного рака — только в 1% случаев. При CIN II регрессия наблюдается в 43%, персистенция — в 35%, прогрессия — в 22%, а развитие инвазивного рака — в 5% случаев. В то же время при CIN III малигнизация происходит более чем в 12% случаев, а регрессия — лишь в 32% [26, 27].
В связи с вышесказанным, другим подходом в тактике ведения пациенток с начальными проявлениями CIN может быть назначение противовирусной терапии и контроль со стороны врача за четким выполнением рекомендаций и схем медикаментозной терапии.
Этиопатогенез минимальных изменений эпителия (легкая дисплазия или атипические изменения неясной причины) связан с ВПЧ, который на этой стадии заболевания еще находится в клетке в эписомальном состоянии и не повреждает ее геном. Следовательно, именно на этом этапе развития системный и местный иммунитет будет играть ведущую роль в прогнозе развития болезни. По данным биопсий шейки матки латентные формы инфекции выявляются у 8,1% женщин, а субклинические у 40–60% [25, 28]. Именно поэтому медикаментозная терапия при начальных формах поражения эпителия должна быть направлена на подавление вируса при соблюдении комплаенса, понимании пациенткой необходимости завершения курса для повышения эффективности лечения.
В своем исследовании R. Richard и B. Barron [29] показали, что среднее время для развития карциномы in situ составляет примерно 5 лет для больных со слабой дисплазией, 3 года — с умеренной и 1 год — с выраженной дисплазией. Это позволило предположить, что 66% всех дисплазий будет прогрессировать до карциномы, но достаточно длительное время, которое необходимо использовать для раннего выявления и лечения. В клинической ситуации, несмотря на то, что имеется достаточный период безопасного времени для динамического наблюдения, многие врачи и пациентки после информирования о диагнозе не хотят длительно наблюдаться даже с начальной патологией эпителия. Женщины хотят быть излеченными сразу, что часто предопределяет активную тактику ведения больных, включая деструкцию активной зоны трансформации и иммуно/противовирусную терапию [29–33].
Таким образом, у пациенток с «минимальным» повреждением эпителия шейки матки, например ASCUS, с наличием цитоплазматического эффекта ВПЧ (койлоцитоз при цитологическом исследовании) и положительном ВПЧ-тесте и его высоком титре, может оказаться актуальным применение препарата с двойным противовирусным действием — инозин пранобекс (Изопринозин).
Это один из немногих иммунотропных и противовирусных препаратов, в инструкции по применению которого указана терапия заболеваний, вызванных ВПЧ. Он также входит в Европейскую классификацию методов лечения аногенитальных бородавок [34]. В настоящее время накоплен огромный опыт применения Изопринозина, так как используется он с 1970-х гг. и зарегистрирован в большинстве стран Европы.
Изопринозин — иммуномодулятор, стимулирующий противовирусную защиту организма. Помимо иммунотропного, Изопринозин обладает прямым противовирусным действием, угнетая синтез вирусов путем встраивания инозин-оротовой кислоты в полирибосомы пораженной вирусом клетки и нарушая присоединение адениловой кислоты к вирусной РНК.
Таким образом, обладая противовирусным действием и оказывая влияние на противовирусный иммунитет, Изопринозин прямо и косвенно способен подавлять репликацию ВПЧ и образование вирусных белков. Эти эффекты могут изменять механизм взаимодействия ВПЧ и макроорганизма, препятствуя переходу вируса из транзиторной в персистирующую форму, а также влияя на клиническую манифестацию инфекции.
Одним из показаний применения препарата являются инфекции, вызванные вирусом папилломы человека: остроконечные кондиломы, ПВИ вульвы, вагины и шейки матки (в составе комплексной терапии).
При инфекциях, вызванных ВПЧ, Изопринозин назначают по 3 г/сут (2 таблетки 3 раза в сутки) как дополнение к местной терапии или хирургическому вмешательству в течение 14–28 дней или 5 дней в неделю последовательно в течение 1–2 недель в месяц в течение 3 месяцев. При дисплазии шейки матки, ассоциированной с ВПЧ: по 2 таблетки (1000 мг) 3 раза в сутки в течение 10 дней, далее 2–3 курса с интервалом 10–14 дней.
Улучшение морфологической картины эпителия вульвы показано в исследовании Sun Kuie Tay [32]. Инозин пранобекс назначали по 1 г 3 раза в сутки в течение 6 недель. Положительный эффект был достигнут у 63,5% больных, а в группе, принимавшей плацебо, — у 16,7%.
В другом исследовании при монотерапии Изопринозином по 3 г в сутки у 44 женщин с CIN I (длительность лечения 10 дней) и CIN II (длительность лечения 21 день) установлено, что выраженный клинический эффект наблюдался у 88,6% пациенток — полностью исчезало поражение эпителия экзоцервикса, что подтверждалось кольпоскопически и гистологически [35].
В работе Т. В. Клинышковой и соавт. [36] показана высокая частота регресса CIN I (70%) и прекращения выделения ВПЧ (83,3%) при использовании Изопринозина в режиме монотерапии и комбинированного лечения в сочетании с деструкцией у пациенток с ВПЧ-ассоциированными поражениями шейки матки. Изопринозин назначали по 3 г в сутки двумя 10-дневными курсами — за 1 месяц до деструкции и с 1-го дня деструкции при четком контроле за выполнением курса лечения.
В. Н. Прилепская сообщает о прекращении выделения ВПЧ у 65,6% больных после комбинированной терапии (Изопринозин + деструкция очагов) CIN низкой степени [3]. При использовании только деструкции очагов этот результат был достигнут у 46,9% больных. Изопринозин назначали по 1 г 3 раза в сутки в течение 5 дней за 7–10 дней до проведения деструкции.
Похожие результаты — прекращение выделения ВПЧ у 77% больных — показаны в исследовании И. В. Шевниной (2009 г.) при комбинированной терапии женщин с CIN и аногенитальными бородавками. Изопринозин назначали по 1 г 3 раза в сутки в течение 10 дней, затем по 0,5 грамма 3 раза в сутки в течение 20 дней.
В другом исследовании Изопринозин назначали женщинам с патологией шейки матки, ассоциированной с ВПЧ [37]. Препарат назначали после проведения обследования и противовоспалительной терапии по 3 г в сутки в течение 10 дней. Элиминация ВПЧ достигнута у 95,3% пациенток.
Есть и другие исследования, в которых показано прекращение выделения ВПЧ из очагов поражения у 69,6–97,8% женщин, принимавших Изопринозин [30, 38, 39].
Представленные данные свидетельствуют о возможной эффективности монотерапии Изопринозином при бессимптомном вирусовыделении, когда применение деструктивных методик не показано.
Сравнительная оценка лечения с применением Изопринозина и без него показала преимущество дополнительной лекарственной терапии вне зависимости от степени онкологического риска. Так, в группе женщин с начальными изменениями эпителия самостоятельное улучшение после санации влагалища достигнуто в 64,9% наблюдений, а при применении Изопринозина в 80,4% случаев [17]. У пациенток с изменениями легкой степени тяжести, выявленными при кольпоскопическом или цитологическом исследованиях, даже в случаях отсутствия самостоятельных улучшений более 3 мес Изопринозин был эффективен почти в 85% наблюдений [17].
Результаты исследования, проведенного в ФГБУ НЦАГиП им. акад. В. И. Кулакова [40, 41], показали, что инозин пранобекс подавляет репликацию высокоонкогенных типов ВПЧ и способствует исчезновению койлоцитарной атипии у 94% пациенток с поражением эпителия шейки матки.
При использовании Изопринозина в режиме монотерапии и в комбинации с деструкцией у пациенток с ВПЧ-ассоцированными поражениями низкой степени получена высокая частота регресса CIN I, прекращение выделения ВПЧ, снижение вирусной нагрузки, активация интерферонового ответа в сравнении с традиционными подходами [16]. Через 4 мес у пациенток, принимавших Изопринозин, в 2 раза снизилась частота экспрессии онкобелка Е7 по сравнению с контрольной группой. Кроме этого были отмечены и другие значимые позитивные изменения в отличие от контрольной группы, где имелась лишь тенденция к этому. Выявленные различия позволяют расценивать их как патогенетические предпосылки неполного клинического эффекта и отдаленного рецидивирования заболевания у пациенток контрольной группы. Эффективность лечения в группе пациенток, принимавших Изопринозин, по окончании лечения была в 1,4 раза выше, чем при традиционном лечении.
Заключение
Таким образом, основными профилактическими мероприятиями, направленными на раннее выявление и преодоление прогрессирования ВПЧ-ассоциированной патологии шейки матки, могут быть:
Многочисленные исследования, проведенные во многих странах мира, в том числе и в России, показали, что при применении Изопринозина (в комбинации с деструкцией или в виде монотерапии), благодаря его двойному противовирусному и иммуномодулирующему действию, подавляющему репликацию ВПЧ, повышается эффективность терапии заболеваний шейки матки, ассоциированных с ПВИ.
Для достижения этих результатов важным является соблюдение дозировок и продолжительности лечения. Как было указано выше, наиболее опасной с точки зрения прогрессирования дисплазии является персистенция ВПЧ, при которой вирус встраивается в геном эпителиальной клетки. Противовирусное действие при этом должно продолжаться несколько месяцев, чтобы захватить несколько циклов полного обновления эпителия. Именно поэтому для консервативной терапии дисплазий предлагается длительное многокурсовое лечение — два-три 10-дневных курса с интервалом 10–14 дней. Такие курсы, как показали результаты многочисленных исследований, приведенные в данной работе, позволяют достичь высокой эффективности лечения. Чем ниже уровень выполнения пациентками предписаний врача, тем ниже уровень эффективности лечения и выше риск рецидивирования и прогрессирования патологии.
Литература
А. М. Соловьев*, кандидат медицинских наук
Д. В. Логвинова**
*ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
**НПЦДК ДЗМ, Москва