Чем лечить атрофический гастрит
Хронический атрофический гастрит
МКБ-10
Общие сведения
Хронический атрофический гастрит – диагноз морфологический, для верификации которого обязательны результаты ЭГДС. Клинические проявления данной патологии не всегда соответствуют выявляемым при проведении биопсии изменениям. Хронический атрофический гастрит может развиться как на поздних стадиях хеликобактерного гастрита (из-за длительной персистенции инфекции происходит постепенная гибель значительного количества желудочных желез), так и в результате аутоиммунных нарушений в организме (антитела к эпителиальным клеткам желудка вызывают их гибель, постепенно развивается ахлоргидрия).
H.pylori выявляется более чем у 80% населения России, при этом хроническое воспаление слизистой желудка обнаруживается примерно у 50%. Аутоиммунный гастрит у женщин диагностируется в три раза чаще, чем у мужчин, однако является достаточно редким заболеванием. Исследования в области гастроэнтерологии подтверждают, что заболеваемость хроническим гастритом повышается на 1,5% ежегодно.
Причины
Наиболее значимыми причинами хронического атрофического гастрита являются инфекция H.pylori и аутоиммунные процессы. Атрофия эпителия желудка развивается на поздних стадиях хронического хеликобактер-ассоциированного гастрита. Бактерии сначала колонизируют слизистую антрального отдела, вызывая хронический воспалительный ответ. По мере прогрессирования инфекции процесс распространяется сначала на тело желудка, а затем и на остальные его отделы, инициируя пангастрит. На этой стадии уже четко визуализируются атрофические изменения слизистой, формируется хронический атрофический гастрит. Обычно на данном этапе хеликобактерии перестают выявляться, так как желудочные железы атрофируются, происходит замена желудочного эпителия на кишечный, к которому H.pylori не имеет тропности.
При аутоиммунном гастрите поражение основных желез желудка наблюдается в начале заболевания. Диффузная атрофия эпителия желудка очень быстро прогрессирует, что связано с выработкой аутоантител к микросомальным антигенам париетальных клеток, гастринсвязывающим белкам, внутреннему фактору. Антитела принимают непосредственное участие в деструкции эпителиальных клеток желудка.
Причина образования аутоантител на сегодняшний день не определена, но гастроэнтерологи не исключают наследственной предрасположенности к хроническому атрофическому гастриту. Известно, что для запуска аутоиммунного процесса в эпителии желудка титр антител должен достичь некой критической цифры, индивидуальной для каждого человека. Повлиять на скорость этого процесса могут различные эндогенные и экзогенные провоцирующие факторы:
Симптомы
Для хронического атрофического гастрита характерны как местные, так и общие проявления. Некоторые симптомы зависят от этиологии заболевания (HP-ассоциированный или аутоиммунный тип) и локализации воспалительного процесса.
При бактериальном генезе хронического атрофического гастрита с локализацией в антральном отделе пациенты предъявляют жалобы на тяжесть в желудке во время или сразу после еды. Если хронический гастрит длительно протекал как гиперацидный, больного могут беспокоить диспепсические нарушения: диарея или запоры, повышенный метеоризм, урчание в животе.
Аутоиммунный гастрит характеризуется тетрадой признаков: аутоиммунный процесс, наличие в крови антител к обкладочным клеткам желудка, В12-фолиеводефицитная анемия, ахлоргидрия. При любом виде хронического атрофического гастрита беспокоят боли в эпигастрии во время или после еды, тошнота, неприятный запах и привкус во рту, отрыжка и срыгивания, жжение в подложечной области или изжога.
Общие проявления выражаются слабостью, раздражительностью, склонностью к артериальной гипотонии, колющими болями в сердце. Для хронического атрофического гастрита характерен демпинг-синдром: после еды возникает резкая слабость, бледность кожи, потливость, сонливость, икота, неустойчивый стул.
Осложнения
При аутоиммунном гастрите антитела поражают не только клетки желудка, но и внутренний фактор Касла, участвующий в метаболизме витамина В12. В результате этого развивается пернициозная анемия, проявляющаяся жжением в языке, симметричными парестезиями в руках и ногах, утомляемостью, сонливостью, депрессией. Помимо В12-дефицитной анемии, хронический аутоиммунный гастрит может осложняться язвенной болезнью желудка и ДПК, ахлоргидрией, раком желудка.
Диагностика
При подозрении на хронический гастрит пациент в обязательном порядке нуждается в консультации гастроэнтеролога и врача-эндоскописта. На первичном приеме назначается ряд анализов и исследований. После получения результатов проводится повторная консультация, на которой обычно и выставляется диагноз хронического атрофического гастрита.
Лечение хронического атрофического гастрита
Перед началом лечения рекомендуется отказаться от вредных привычек (курения, приема алкоголя). Диета не является основным методом терапии хронического атрофического гастрита. Медикаментозное лечение планируется в зависимости от этиологии заболевания (хеликобактерный или аутоиммунный гастрит).
При хроническом атрофическом гастрите, сопровождающемся тяжелыми аутоиммунными нарушениями, показано назначение коротких курсов глюкокортикоидных гормонов в невысоких дозах. После стабилизации процесса и регресса клинических проявлений лечение прекращается. Если секреторная функция желудка не восстановилась, назначают натуральный желудочный сок, прокинетики, ферменты поджелудочной железы. Проводится коррекция В12-дефицитной анемии.
Лечение хеликобактер-ассоциированного хронического атрофического гастрита стандартное: ингибиторы протонной помпы в сочетании с антибактериальными препаратами (кларитромицин, амоксициллин, фуразолидон, метронидазол, тетрациклин), препаратами висмута. Использование препаратов висмута вместо ИПП показано пациентам с пониженной секреторной функцией желудка.
Атрофический гастрит — симптомы, лечение хронического атрофического гастрита
Атрофический гастрит — разновидность хронической формы заболевания. Из-за изменений в париетальных клетках желудка истончается слизистая оболочка, железы, которые вырабатывают соляную кислоту, атрофируются. В результате нарушается процесс переваривания пищи.
Атрофический гастрит — опасное прогрессирующее заболевание, относится к предраковым состояниям. При длительном течении болезни вместо желудочных клеток появляются клетки, характерные для тонкого кишечника, разрастаются клетки слизистой, что приводит к раку желудка. Патологию выявляют у 50-70% людей старше 50 лет.
Выделяют 2 основных причины развития и прогрессирования атрофического гастрита. Первая — инфекция хеликобактер пилори. Бактерию выявляют у 80% пациентов с атрофическим гастритом. Заразиться H. pylori можно через слюну больного человека, зараженную воду и пищи. Но основной механизм инфицирования до конца не изучен.
Вторая — аутоиммунный гастрит, при котором вырабатываются антитела к собственным париетальным клеткам. Заболевание редкое, преимущественно встречается у женщин.
Атрофический гастрит может быть осложнением следующих патологий:
Провоцирующие факторы — курение, злоупотребление алкоголем, кофе, газированными напитками, увлечение острой, холодной и горячей пищей, длительный прием НПВС, антибиотиков, гормональных препаратов. Атрофию желудка могут вызвать химические вещества, поэтому заболевание нередко выявляют у людей, которые работают на вредном производстве.
Негативно на слизистую желудка влияет рефлюкс — заброс содержимого кишечника в желудок. Происходит повреждение слизистой желудка, постепенно развиваются атрофические изменения.
Виды и стадии развития
При постановке диагноза учитывают локализацию патологических изменений, результаты гистологии и эндоскопии, возможные причины развития болезни.
Атрофический гастрит часто протекает бессимптомно, особенно у людей преклонного возраста. Появление негативных проявлений связано с дисфункцией желудка.
Признаки атрофического гастрита:
Один из характерных внешних признаков — лакированный язык, покрытый густым налетом белого цвета.
При аутоиммунном гастрите развивается анемия на фоне дефицита витамина B12, значительно снижается секреция соляной кислоты. Признаки заболевания — слабость, повышенная потливость, боль в сердце, аритмия, снижение артериального давления. Беспокоит жжение во рту, нарушается чувствительность конечностей.
Диагностика атрофического гастрита
Лечением заболевания занимается гастроэнтеролог. Диагноз ставят только после изучения состояния слизистой оболочки желудка, проведения морфологического исследования.
Лечение атрофического гастрита
Терапия направлена на устранение причин и симптомов заболевания, предотвращение осложнений.
При гастрите эффективна бальнеотерапия — лечение минеральной водой с высоким содержанием солей. Предварительно необходимо удалить газ, пить в теплом виде за полчаса до еды. Помогают и физиопроцедуры — электрофорез, магнитотерапия, тепловое воздействие на область эпигастрия.
При атрофическом гастрите нарушается работа тонкого и толстого кишечника, поджелудочной железы. Развивается хроническая B 12-дефицитная анемия, что негативно сказывается на работе нервной системы.
Атрофический гастрит
Атрофический гастрит – это хронический гастрит типа А, при котором уменьшается количество желудочных желез, снижается кислотообразующая функция. Считается предраковым состоянием. Проявляется тяжестью и тупыми болями в желудке, тошнотой, изжогой, диспепсическими явлениями, анемией. Наиболее значимыми методами диагностики являются: гастроскопия с забором и гистологией биоптатов, различные исследования для определения наличия хеликобактерной инфекции. Менее информативны гастрография, УЗИ органов брюшной полости. Так как 90% атрофий желудка связаны с воздействием хеликобактерий, специфическое лечение включает в себя эрадикацию инфекции. Назначается заместительная и симптоматическая терапия, санаторное лечение и физиотерапия.
МКБ-10
Общие сведения
Атрофический гастрит – хроническое прогрессирующее воспаление слизистой желудка, в результате которого полностью утрачиваются обкладочные железы желудка, происходит постепенная атрофия с последующей метаплазией участков слизистой. Основным признаком, который указывает на высокую вероятность рака, является не вид перестройки клеток, а площадь процесса – при распространенности метаплазии на 20% площади слизистой желудка и более вероятность развития рака практически 100%.
По наблюдениям специалистов в сфере практической гастроэнтерологии, хронический атрофический гастрит в 13% случаев заканчивается развитием онкологической патологии. По сравнению с неатрофическим процессом вероятность такого осложнения при атрофическом гастрите в пять раз выше. Основной задачей гастроэнтерологов сегодня является разработка новых, простых и неинвазивных методов достоверной диагностики атрофии, а также ранней диагностики рака желудка. Замечено, что своевременная диагностика и полная эрадикация инфекционного процесса уже через пять лет приводят к восстановлению слизистой желудка и значительному уменьшению площади метаплазии.
Причины
Основными причинами развития атрофического гастрита являются длительно текущая хеликобактерная инфекция и аутоиммунный процесс, при котором собственные антитела повреждают G-клетки желудка (они являются основной составляющей обкладочных желез). Атрофии железистого эпителия могут способствовать различные сопутствующие заболевания и состояния: бесконтрольный прием медикаментов, алкоголизм, стрессы и выраженное физическое переутомление, различные профессиональные вредности, наследственные особенности работы ЖКТ, тяжелые фоновые заболевания.
Патогенез
H.pylori вызывает хроническое повреждение клеток, ослабляя местные защитные свойства слизистой желудка, что в результате позволяет токсинам и свободным радикалам беспрепятственно проникать в ткани и повреждать ядра клеток. В финале этого процесса клетки приобретают свойства нескольких типов тканей – так называемые гибридные клетки, которые имеют свойства предраковых. Данный процесс называется кишечная метаплазия. Вначале эти участки слизистой приобретают вид тонкокишечного эпителия, затем толстокишечного. Чем дальше зашел процесс метаплазии, тем больше вероятность развития аденокарциномы желудка. На сегодняшний день хеликобактерная инфекция включена в список биологических канцерогенов, ведь без надлежащего лечения она рано или поздно приводит к раку желудка.
Механизм развития аутоиммунного процесса несколько иной. При этом в организме из-за нарушения иммунитета начинают образовываться антитела, которые распознают собственные ткани желудка как чужеродные. Чаще всего антитела вырабатываются к G-клеткам и фактору Касла, который отвечает за всасывание витамина В12. Из-за этого постепенно снижается кислотность желудка, клетки перестраиваются и начинают производить слизь вместо соляной кислоты. В желудке перестают всасываться железо и витамины, развивается тяжелая пернициозная анемия. Если же аутоиммунному гастриту сопутствует хеликобактерная инфекция, предраковое состояние разовьется гораздо быстрее.
Симптомы атрофического гастрита
Патология развивается медленно, поражение при этом начинается со дна желудка, переходя на его тело, а затем и на остальную слизистую. В начале заболевания особой симптоматики может и не быть, что затрудняет диагностику и мешает раннему началу лечения. После развития полной клинической картины у пациента могут выявляться несколько симптомокомплексов.
Анемический синдром развивается из-за нарушения всасывания железа и витаминов (особенно В12, фолиевой кислоты) в полости желудка. Проявляется он выраженной слабостью, утомляемостью, сонливостью, постоянной усталостью (порой даже нарушается обычная деятельность пациента). Кожные покровы и слизистые бледнеют. Пациент отмечает постоянные боли в языке, жжение, слизистая языка становится лаковой. Также больной предъявляет жалобы на нарушения чувствительности в конечностях, обычно симметричные. Характерны сухие волосы и ломкие ногти, беспокоит одышка при незначительных нагрузках, колющие боли в сердце.
Диспепсический синдром проявляется выраженной тяжестью в эпигастрии, реже тупыми ноющими болями в верхней половине живота. Боли связаны с растяжением стенок желудка пищевыми массами из-за нарушений пищеварения. Также пациента беспокоят изжога (забрасывание кислого содержимого в пищевод), срыгивание (забрасывание пищи из желудка в ротовую полость), отрыжка (непроизвольный выход воздуха из желудка). Сопровождаются эти симптомы тошнотой, иногда рвотой, после которой боль в эпигастрии уменьшается. В рвотных массах – большое количество съеденной пищи, слизь, желчь. Аппетит значительно снижен.
Нарушения пищеварения распространяются на другие отделы ЖКТ – появляется дискомфорт в животе, стул становится неустойчивым – запоры сменяются поносами. По утрам во рту неприятный привкус, беспокоит постоянный запах изо рта. Язык обложен сероватым налетом, на нем видны отпечатки зубов. Нарушенное пищеварение и снижение аппетита могут приводить к потере веса, а при отсутствии лечения – к выраженной алиментарной дистрофии. Развивается полигиповитаминоз, который приводит к значительному снижению иммунитета, присоединению различных инфекций.
Диагностика
Сегодня все больше внимания уделяется ранней неинвазивной диагностике атрофического гастрита. Для этого врачами-гастроэнтерологами разработана специальная панель диагностики. При проведении обычной гастроскопии выявить очаги дисплазии эпителия, а тем более определить их площадь не представляется возможным. Из-за этого зачастую возникают ошибки, связанные как с гипердиагностикой, так и гиподиагностикой: площадь гиперплазии может быть оценена неправильно, а воспалительные изменения могут быть приняты за метаплазию эпителия. Для того, чтобы правильно оценить площадь измененного эпителия, взять биопсию из всех измененных участков, во время гастроскопии производится окрашивание слизистой (чаще всего метиленовым синим) – краситель хорошо воспринимается участками с кишечной метаплазией.
Специальная гематологическая панель Biohit позволяет быстро и эффективно определить степень метаплазии эпителия, атрофии слизистой и обкладочных желез, избежать ошибок диагностики. В этой панели исследуется уровень сывороточного пепсиногена, определяется соотношение пепсиногена 1 к пепсиногену 2, гистамина 17. Снижение этих показателей говорит о выраженной атрофии клеток железистого эпителия, а низкий уровень гастрина 17 говорит о гибели G-клеток желез желудка.
В то же время, повышение уровня гастрина 17 и пепсиногена 1 часто ассоциируется с хеликобактерной инфекцией. Значительное повышение уровня гастрина 17 чаще всего связано с аутоиммунным гастритом, при котором наблюдается ахлоргидрия или гипохлоргидрия, сохранена функция антрального отдела желудка. Если же в антральном отделе также имеются очаги атрофии (мультифокальная атрофия), то уровни всех этих показателей будут низкими. Данная панель имеет не менее 80% достоверности, используется на начальных этапах обследования и позволяет определиться с типом гастрита, его локализацией и причиной, выявить предраковое состояние и определить правильную тактику лечения.
В сравнении с гематологической панелью и эндоскопическим исследованием с забором биопсии, остальные методы диагностики атрофического гастрита менее информативны. Так, при гастрографии отмечается сглаженность складок слизистой и замедление перистальтики желудка, размеры его уменьшены. Такая же картина обнаруживается при проведении УЗИ желудка. Внутрижелудочная рН-метрия обнаруживает снижение кислотности желудочного сока. Для уточнения диагноза желательно проводить суточное измерение кислотности.
При подозрении на малигнизацию необходимо провести МСКТ органов брюшной полости для исключения опухолевого процесса. Также обязательно проводятся все необходимые исследования для выявления инфицированности H.pylori: ПЦР-диагностику хеликобактер, дыхательный тест, выявление в крови антител к хеликобактер.
Лечение атрофического гастрита
Основной задачей гастроэнтеролога является предупреждение дальнейшей кишечной метаплазии, раковой трансформации. При своевременном начале лечения атрофического гастрита уже через пять лет наступает значительное улучшение состояния эпителия. Обязательно назначается лечебная диета, которая на начальном этапе включает в себя химически, термически и механически щадящую пищу.
После нормализации состояния допускается употребление химически активных продуктов: разведенных соков (лимонный, капустный, клюквенный). Свежие фрукты из диеты исключаются, можно есть только бананы. К пище предъявляются особые требования – она должна быть теплой (нельзя принимать холодные и горячие продукты), приемы пищи должны быть частыми и дробными. Необходимо исключить спиртные напитки и курение.
При обнаружении хеликобактерной инфекции обязательным условием выздоровления является эрадикация инфекционного агента. Современные протоколы лечения предусматривают назначение двух- или трехкомпонентной схемы, включающей антихеликобактерные антибиотики, ингибиторы протонной помпы, препараты висмута. Только полное излечение от хеликобактерий может привести к восстановлению слизистой и снижению риска малигнизации.
Глюкокортикоидные гормоны при атрофическом гастрите назначаются только при развитии В12-фолиеводефицитной анемии. Также назначается симптоматическое лечение: заместительная терапия натуральным желудочным соком, ферментами, недостающими витаминами, препаратами железа. Для стимуляции секреции соляной кислоты необходимо пить минеральные воды с высоким содержанием солей, отвары трав (подорожник, полынь, фенхель), кислые соки, растворы лимонной и янтарной кислот.
Используются гастропротекторы (мизопростол, карбеноксолон), стимуляторы регенерации (облепиховое масло), обволакивающие средства на основе алюминия и висмута, препараты для улучшения перистальтики. Активно применяется физиотерапия: электрофорез с лекарственными препаратами, электро- и магнитотерапия, тепловые процедуры на область эпигастрия. Санаторно-курортное лечение вне периода обострения включает терапию минеральными водами на бальнеологических курортах.
Хронический атрофический гастрит (K29.4)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
I. По локализации:
— антральный гастрит;
— гастрит (преимущественно или только) тела желудка;
— мультифокальный гастрит.
II. По морфологии.
Для морфологической оценки хронического гастрита российские авторы (Аруин Л.И., Капуллер Л.Л., Исаков В.А., 1998) предлагают использовать визуально-аналоговую шкалу. При ХПГ данная шкала позволяет оценить степень выраженности воспаления с помощью полуколичественных критериев.
Визуальная аналоговая шкала морфологической оценки хронического гастрита
| Признак | Норма | Слабая | Умеренная | Выраженная |
| Обсеменение H.pylori | ||||
| Инфильтрация нейтрофилами | ||||
| Хроническое воспаление | ||||
| Атрофия привратника | ||||
| Атрофия тела желудка | ||||
| Кишечная метаплазия |
Примечание к таблице. В данной таблице отмечается наличие морфологических признаков согласно прилагаемому ниже изображению.
Хроническое воспаление, вызванное Н. pylori: в настоящее время считается, что при исследовании (объектив Х40) СОЖ содержит в норме не более 2-5 лимфоцитов, плазматических клеток и макрофагов в поле зрения или 2-3 мононуклеара в одном валике. Наличие 1-2 плазмоцитов в поле зрения уже свидетельствует о хроническом воспалении.
Не требуют полуколичественной оценки, но указываются следующие признаки: потеря муцина, наличие лимфатических узелков, фовеолярная гиперплазия, пилорическая метаплазия, панкреатическая метаплазия, гиперплазия эндокринных клеток.
В зависимости от степени распространенности дистрофически измененных клеток среди «нормальных» клеток поверхностного эпителия в поле зрения, а также от глубины проникновения воспалительной инфильтрации в толщину слизистой оболочки, среди поверхностных гастритов выделяют:
— слабо выраженный (первая стадия воспалительной активности);
— умеренно выраженный (вторая стадия воспалительной активности);
— сильно выраженный (третья стадия воспалительной активности).
В классификации ХАГ по выраженности атрофии и ее виду выделены три категории изменений слизистой оболочки желудка (СОЖ).
3. Атрофия желудочных желез. Подразделяется на два главных типа:
3.1 Метапластический тип атрофии характеризуется утратой желудочных желез, свойственных данному отделу, с замещением их кишечными, а применительно к слизистой оболочке тела желудка – пилорическими железами.
3.2 Неметапластический тип атрофии: в слизистой оболочке сохраняются железы, характерные для соответствующего отдела желудка, но наблюдается уменьшение объема железистой ткани. Железы становятся редкими и неглубокими. Наблюдается фиброз и фибромускулярная пролиферация собственной пластинки слизистой оболочки.
В данной классификации сохранена полуколичественная оценка степени тяжести атрофии: слабая, умеренная и тяжелая.
При практическом использовании эта классификация показала очень высокий уровень согласованности в интерпретации гистологической картины (до 78%) между разными морфологами. По критериям данной классификации большинство патологоанатомов одинаково оценивали состояние СОЖ.
При слабой неметапластической атрофии в антральном отделе уменьшается количество и глубина пилорических желез, разделенных фиброзным матриксом, а при тяжелой – пилорические железы практически полностью замещены соединительной тканью.
Умеренная неметапластическая атрофия слизистой оболочки тела желудка сопровождается уменьшением количества главных желез, отмечается углубление желудочных ямок и разрастание соединительной ткани в собственной пластинке слизистой оболочки.
При тяжелой неметапластической атрофии слизистой оболочки тела желудка главные железы полностью отсутствуют.
При тяжелой метапластической атрофии в антральном отделе пилорические железы, а в слизистой оболочке тела желудка – главные железы полностью замещены железами кишечного типа.
Раздельная оценка атрофических изменений в антральном и фундальном отделах желудка имеет высокую клиническую значимость, однако затрудняет интегративное восприятие общего состояния СОЖ. Помимо этого, в категорию неопределенных атрофий попадает большое количество случаев с продолжающейся воспалительной реакцией, а также изолированная атрофия СОЖ без воспаления встречается очень редко.
IV. По степени и стадии хронического гастрита (ХГ).
А
Н
Т
Р
У
М
Атрофический гастрит. Диагностика с помощью Гастропанели
Очень часто на прием приходят пациенты, которым по поводу болей в верхней половине живота, тяжести после еды в подложечной области, отрыжки была проведена гастродуоденоскопия и сделано заключение, на основании которого врачом ставится диагноз «атрофический гастрит». Возникает тревога у человека, что делать и не может ли этот гастрит перейти в рак желудка?
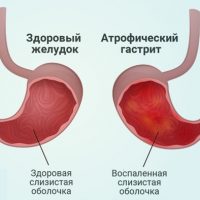
Среди болезней желудка наиболее часто встречаемым и выставляемым практическими врачами диагнозом является «хронический гастрит».
Хронический гастрит занимает центральное место среди болезней желудка, является наиболее распространенным заболеванием желудочно-кишечного тракта. Считается, что треть взрослого населения страдает хроническим гастритом, но только 10-15% обращается к врачам. Важным является то, что хронический гастрит предшествует или сопровождает серьезные по течению и прогнозу болезни желудка — язвенную болезнь, рак желудка, а также близко лежащих органов пищеварительной системы.
Атрофический гастрит – что это
Что мы понимаем под атрофическим гастритом? В основе лежат атрофические процессы в слизистой оболочке желудка, воспалительные и дистрофические процессы, которые приводят к функциональной недостаточности слизистой. Атрофия желез слизистой оболочки желудка заключается в уменьшении численности клеток, продуцирующих ферменты (пепсины) и париетальные клетки, выделяющие соляную кислоту, и клеток, которые вырабатывают фактор Кастла.
Анатомия желудка
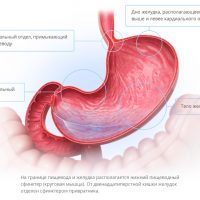
Атрофия клеток желудка может затрагивать все отделы желудка, и тогда мы говорим о тотальном поражении органа или затрагивать конкретные отделы – фундальный (поражение тела желудка), антральный (выходной отдел желудка), или избирательно поражать часть клеток желудка. Клинические проявления атрофии в разных отделах желудка будут разные.
Известно, что желудок — это полый орган, куда пища попадает из ротовой полости и где происходит желудочное переваривание пищи: депонирование пищи, механическая и химическая переработка пищи и эвакуация ее из желудка в кишечный тракт.
Цитология желудка
В слизистой каждого отдела имеются различные клетки, отвечающие за переваривание пищи и участие в кроветворении:
Добавочные слетки слизистой оболочки желудка образуют слизь практически во всех отделах желудка. Эта слизь выполняет защитную функцию от желчи, лекарств, которые принимает пациент, соляной кислоты.
В выходном отделе желудка имеются эндокринные клетки — G клетки, которые вырабатывают стимулятор образования пепсиногенов, соляной кислоты, отвечают за состояние моторной функции желудка.
Атрофический гастрит — причины развития
Наиболее частой причиной, вызывающей атрофический гастрит в настоящее время, считается инфекция Helicobacter pylori. В желудке развивается поверхностный гастрит и при длительном существовании инфекции переходит в атрофический.
Инфекция желудка ассоциируется с поражением антрального отдела желудка в виде ограниченного или тотального поражения этого отдела – атрофический гастрит антрального отдела и тела желудка. Развитие атрофических процессов в желудке может быть результатом возрастных изменений слизистой, генетических особенностей, обусловленных гипо- или атрофией слизистой желудка, лекарственным поражением желудка, длительным приемом антисекреторных препаратов (ИПП).
Аутоиммунный атрофический гастрит, когда организм начинает вырабатывать антитела против своих клеток слизистой оболочки желудка встречается достаточно редко.
Как подтвердить диагноз «атрофический гастрит»
Диагноз хронического атрофического гастрита является морфологическим. Если проводится эндоскопическое обследование, то при подозрении на атрофические процессы в желудке должны быть взяты биопсии слизистой оболочки желудка и дана гистологическая интерпретация изменений в ней.
В морфологическом диагнозе должны быть учтены: поражение отдела желудка, состояние желез, выраженность и глубина воспаления и перестройки слизистой (метаплазия, дисплазия). Клинический диагноз «хронический атрофический гастрит» без морфологического подтверждения не имеет смысла.
Наиболее точным методом диагностики является эндоскопическое исследование с биопсией. Однако в связи с неравномерностью распространения атрофических процессов в слизистой оболочке желудка гистологические исследования могут давать ложноотрицательные результаты. Кроме того, биопсия является дорогим и трудоемким методом и не может проводиться каждому пациенту, а само эндоскопическое исследование является серьезным инвазивным методом исследования.
В настоящее время существует альтернатива биопсии слизистой оболочки желудка — скрининговый метод исследования «сывороточная биопсия», способный объективно отражать функциональное состояние слизистой оболочки желудка и его морфологическую основу по образцам сыворотки крови.
Сывороточная биопсия или Гастропанель (или тестовая панель) обеспечивает простой и достоверной путь для получения большой информации о структуре и функции слизистой оболочки желудка, с большой чувствительностью и специфичностью выявить пациентов, имеющих атрофический гастрит и тех, кто нуждается в дальнейшем обследовании – эндоскопическом исследовании желудка. Если тестовая панель выявляет атрофический гастрит, то проведение эндоскопического исследования обязательно с онконастороженностью.
Как проводится Гастропанель
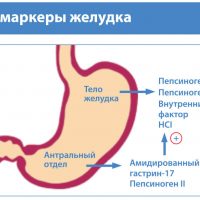
По анализу сыворотки крови определяются маркеры хронического атрофического гастрита. Маркерами атрофии слизистой оболочки фундального и антрального отделов желудка являются:
Тесты основаны на технологии иммуноферментного анализа.
Несколько слов о сывороточных маркерах
Мы имеем диагностический алгоритм выявления заболеваний желудка, который показано проводить всем пациентам, имеющим боль или дискомфорт в верхних отделах живота.
Пепсиногены
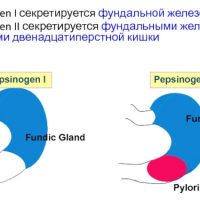
Снижение уровня Пепсиногена I говорит о степени выраженности атрофического гастрита тела желудка, а поскольку активизация Пепсиногена I в активный пепсин происходит при участии соляной кислоты, то по уровню Пепсиногена I можно условно представить уровень кислотности желудка. Пепсиноген II вырабатывается во всех отделах желудка и в 12-перстной кишке. По мере увеличения тяжести атрофии уменьшается соотношение сывороточного уровня Пепсиногена I и Пепсиногена II, что свидетельствует о тяжести атрофии и распространении процесса.
Гастрин

Гомоцистеин
Гомоцистеин — ранний маркер клеточного функционального дефицита В12, В6, фолиевой кислоты вследствие развития атрофического гастрита и других причин – возраст, курение, хеликобактерная инфекция и др. При атрофическом гастрите уровень гомоцистеина повышается в крови и становится токсичным для организма. При сдаче крови на гомоцистеин следует отказаться за 1 день до исследования от белковой пищи, витаминов, гормональных контрацептивов. Этот тест может быть дополнением к Гастропанели или самостоятельным тестом при других заболеваниях.
Достоинства Гастропанели для постановки диагноза «атрофический гастрит»

Какие же достоинства Гастропанели можно отметить: это простой неинвазивный серологический тест, отмечена высокая чувствительность, специфичность, безопасность и удобство для пациента, быстрое получение результатов, отвечает принципам доказательной медицины.
Что делать, если у вас выявили атрофический гастрит
Несколько слов о принципах лечения хронического атрофического гастрита. Подходы к лечению индивидуальные, всё зависит от выраженности атрофических процессов, наличия хеликобактера, дефицита витамина В12.
Проблемой будет заниматься врач, который назначит:
Наиболее трудно устранить аутоиммунные механизмы поражения слизистой желудка, вопрос назначения гормональных препаратов встает только при сопровождении гастрита анемией. Эрадикационная терапия хеликобактер пилори имеет свои особенности. Прежде всего встает вопрос о кислотности желудочного сока, и чаще лечение проводят без антисекреторных препаратов. Исследование кислотности желудочного сока рН-метрическим методом проводят в настоящее время редко (чаще суточное мониторирование в условиях стационара), но возможна ориентация кислотности по уровню Пепсиногена I.
Высокий уровень Пепсиногена, периодические изжоги у пациента могут свидетельствовать о сохраненной секреции желудка. При атрофическом гастрите при гипо или анацидном состоянии с поражением тела и выходного отдела желудка исключаются антисекреторные препараты и эрадикация хеликобактекр пилори проводится антибиотиками. Эффективная эрадикация инфекции улучшает процессы в слизистой желудка, и ее возможно рассматривать как профилактику развития рака желудка.
Питание при хроническом атрофическом гастрите

Чаще всего врачи назначают диету 2, цель которой механическое щажение слизистой желудка и сохранение химических раздражителей.
Но врачебный опыт показывает, что строгих ограничений не требуется. Необходимый режим питания – еда малыми порциями с препаратами заместительной терапии позволяет иметь хорошее желудочное пищеварение, при котором в желудке переваривается и белковая пища.
Атрофический гастрит — лечение
Заместительная терапия
Проведение заместительной терапии включает применение препаратов соляной кислоты и ферментов желудочного сока:
Стимулирующая терапия
Некоторые средства, стимулирующие секрецию желудочного сока:
Состав: дягиль, тысячелистник, одуванчик, береза, вахта трёхлистная, подорожник, тмин, кровохлебка, солодка голая, дымянка лекарственная, календула, ромашка аптечная.
Применение: 1 десертную ложку смеси залить 500 мл кипятка, настаивать в термосе по объему ночь, процедить.
Принимать по 150 мл 3 раза в день за час до еды. Перед употреблением подогреть, разбавив горячей водой. Хранить в холодильнике.
Прием: 10 дней прием — 2 дня перерыв, 3-4 месяца.
В период относительной ремиссии атрофического гастрита главными препаратами являются средства заместительной и стимулирующей терапии, которые влияют на секреторную недостаточность желудка.
Лекарственная терапия
Кроме этих препаратов, применяют препараты, влияющие на трофику и регенерацию слизистой оболочки желудка (Солкосерил, Ребагит), обволакивающие средства (семя льна, средства, содержащие висмут, алюминий (Фосфолюгель, Де-нол), но они чаще назначаются при обострении гастрита и наличии эрозий.
Для улучшения эвакуации пищи из желудка применяются прокинетики (например, Мотилиум).
При наличии у пациента В12 дефицитной анемии проводится лечение инъекциями витамина В12 и фолиевой кислоты.
Эрадикация хеликобактер пилори проводится обязательно. Эти курсы лечения назначаются врачом.
Таким образом, будьте внимательны к своим ощущениям в желудке, своевременно проведите диагностическое обследование, начиная не с гастроскопии, а с анализа крови — Гастропанели, уточните состояние желудка, проведите по необходимости дополнительные обследования (по рекомендации врача), а затем лечебно-профилактическое лечение и будьте здоровы!
Атрофический гастрит – скрытая угроза: как поставить диагноз и помочь больному
Оксана Михайловна Драпкина, профессор:
– Приступим к дальнейшей программе. У нас будет лекция доцента Лапиной Татьяны Львовны, посвященная атрофическому гастриту (АГ).
Татьяна Львовна Лапина, доцент:
– Уважаемые коллеги! Тема моей лекции: «Атрофический гастрит – скрытая угроза: как поставить диагноз и помочь больному».
Зачем вообще нужно ставить диагноз атрофического гастрита?
Все дело в том, что уже многие десятилетия ясно, что АГ и такое изменение слизистой оболочки желудка, которое называется кишечной метаплазией (это маркер, признак АГ), являются предраковыми заболеваниями желудка.
Хронический гастрит и АГ, как правило, не имеют своей симптоматики. Не имея явной симптоматики, гастрит «молчит» о себе. Атрофия слизистой оболочки о себе никак не заявляет. Но молчание это очень громкое и грозное, потому что в итоге мы можем получить опухоль желудка.
Открытие пилорического хеликобактера в этой цепочке патогенетических событий от хронического гастрита к раку желудка позволило очень четко показать, что именно этот микроорганизм является причиной хронического воспаления слизистой оболочки желудка.
Действительно, абсолютно четко доказано, что для инфекции пилорического хеликобактера связь с АГ очевидна.
Посмотрите, пожалуйста. Это данные недавнего мета-анализа, которые четко связывают наличие инфекции пилорического хеликобактера с частотой случаев АГ. Суммарный относительный риск составляет 5. Многократно наличие инфекции пилорического хеликобактера усиливает риск АГ.
Естественно, пилорический хеликобактер как таковой связан с тем раком желудка, который в качестве своего предракового изменения имеет АГ. С некардиальным раком желудка, а именно с диффузной аденокарциномой кишечного типа по классификации Lauren.
Посмотрите, пожалуйста. Специально представляю данные мета-анализа по связи с инфекцией пилорического хеликобактера некардиального рака желудка и рака кардии. Рак кардии не связан с АГ. Четко видно, что нет связи с инфекцией пилорического хеликобактера.
Дистальный рак желудка кишечного типа имеет в качестве стадии определенный, предшествующий своему развитию АГ. Он четко связан с инфекцией пилорического хеликобактера.
Почему пилорический хеликобактер может привести к формированию рака желудка? В первую очередь, через воспалительные изменения слизистой оболочки – через гастрит.
Сама бактерия непосредственна. Например, благодаря тем эпигенетическим изменениям, которые инфекция пилорического хеликобактера вызывает в эпителиоцитах слизистой оболочки желудка.
На этой схеме, которая взята из очень хорошего обзора (он так и называется «Воспаление, атрофия и рак желудка») очень четко показано, что на молекулярном уровне ясно, какие события в эпителиоците желудка запускает инфекция пилорического хеликобактера. В результате может происходить дисбаланс процессов пролиферации, апоптоза, накапливаться генетические мутации.
Конечно, интересно понять, можно ли с помощью эрадикации пилорического хеликобактера добиться профилактики рака желудка.
Самые яркие работы – это работы по проведении эрадикационной терапии у пациентов, у которых диагностирован ранний рак желудка. Это работы японские. Вы знаете, что в этой стране очень хороший алгоритм ведения таких пациентов. Пациенты с ранним раком желудка подлежат эндоскопической резекции опухоли.
Посмотрите, пожалуйста: 544 больных после эндоскопической резекции раннего рака желудка наблюдались три года. Половине из них провели эрадикацию инфекции пилорического хеликобактера, половине не провели.
Через три года у пациентов после эрадикационной терапии случаи нового обнаружения опухолей желудка составили 3%. Пациенты, у которых осталась инфекция пилорического хеликобактера, в течение 3-х лет наблюдения – практически 9%. В три раза чаще выявлялась новая опухоль желудка.
Очень легко все представить на этой модели эндоскопической резекции рака желудка. На самом деле, эпидемиологические исследования по предотвращению рака желудка с помощью эрадикации пилорического хеликобактера очень сложно претворить в жизнь, очень сложно составить правильный план таких исследований.
Тем не менее, видно, что такие исследования проводятся. Действительно, из анализа этих исследований делается вывод, что эрадикация пилорического хеликобактера статистически значимо снижает частоту рака желудка примерно на 1/3.
Исходя из этих расчетов, в качестве некоторых рекомендаций определенных сообществ врачей даются рекомендации по возможному проведению скрининга инфекции пилорического хеликобактера в популяции. Особенно в тех популяциях, где высока частота инфекции пилорического хеликобактера.
Эрадикация инфекции у серопозитивных лиц как стратегия и мера профилактики рака желудка.
С точки зрения разработки такого алгоритма по профилактике рака желудка в Японии интересна эта статья очень известных исследователей. Благодаря их расчетам для Японии: возраст пациентов, когда была проведена эрадикационная терапия инфекции пилорического хеликобактера, и возможное снижение частоты рака желудка.
Вы видите, чем более молодой возраст (в зависимости от пола), тем более эффективна эрадикационная терапия как мера профилактики рака желудка.
С точки зрения диагностики атрофии рекомендуется использовать так называемый уровень сывороточного пепсиногена I. Это белок, который вырабатывается главными клетками желез тела желудка. При АГ утрачиваются железы и главные клетки, поэтому уровень сывороточного пепсиногена достоверно понижается. Определенные пороговые значения могут свидетельствовать о наличии атрофии тела желудка.
В зависимости от наличия инфекции пилорического хеликобактера и наличия сывороточного пепсиногена в низком титре как маркера атрофии выделяются определенные группы лиц популяции, которые могут подлежать (а могут и не подлежать) дальнейшему наблюдению.
Естественно, лица без инфекции пилорического хеликобактера и те, у кого сывороточный пепсиноген в норме, не требуют дальнейшего наблюдения. Но если речь идет о наличии инфекции пилорического хеликобактера, обязательно имеется в виду эрадикационная терапия.
Особенно тяжелая группа: пилорический хеликобактер + и сывороточный пепсиноген как маркер атрофии низкий. Есть специальная группа больных, когда атрофия зашла настолько глубоко, что пепсиноген низкий. Даже не определяется антитело к пилорическому хеликобактеру.
Эти пациенты должны подлежать эндоскопическому исследованию ежегодно после проведения эрадикационной терапии.
Наиболее интересна работа, которая говорит о профилактических мероприятиях с точки зрения профилактики рака желудка. Это работа Ванга (B. C. Wahg) и соавторов. Она выполнена в регионе с высокой частотой рака желудка. Наблюдалась в течение многих лет когорта из 1630 лиц. При этом почти 1000 из них на момент вовлечения в исследования не имели АГ и маркера АГ (кишечной метаплазии). У них не было выявлено дисплазии.
После эрадикационной терапии и группа сравнения, которая получала плацебо. Частота выявления рака желудка спустя годы наблюдения 7 человек и 11 человек с раком желудка.
Разницы вроде бы никакой нет. Но когда посмотрели пациентов, у которых эрадикационная терапия была начата до формирования признаков АГ, кишечной метаплазии, без дисплазии, то в результате наблюдения ноль случаев опухоли желудка. Шесть случаев диагностированного рака желудка при отсутствии эрадикации пилорического хеликобактера.
Конечно, присутствуют независимые факторы риска: курение, возраст пациентов. Тем не менее, в этом исследовании прекрасно доказано, что чем раньше начата эрадикационная терапия (может быть, до развития АГ), тем лучше эта мера действует с точки зрения профилактики.
Кому и когда проводить лечение?
Вы видите, перечислен ряд болезней и состояний, которые могут считаться показаниями для эрадикации инфекции пилорического хеликобактера.
Действительно, здесь присутствует АГ. Но будем ли мы проводить широкомасштабный скрининг на сывороточный пепсиноген и на антитела к пилорическому хеликобактеру? Пока мало регионов в России, в которых такие работы ведутся широкомасштабно.
Что делать практическому врачу?
Практическому врачу нужно использовать рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции пилорического хеликобактера у взрослых. Они были разработаны группой экспертов в результате, на мой взгляд, очень живого и длительного обсуждения и опубликованы в № 1 российского журнала «Гастроэнтерология, гепатология, колопроктология» за текущий (2012-й) год.
Назначение эрадикационной терапии желательно при хроническом гастрите, вызванном инфекцией пилорического хеликобактера. В том числе при АГ.
Пациент, у которого НПВС-гастропатия, гастроэзофагеально-рефлюксная болезнь, функциональная диспепсия, который пришел к доктору, предъявляя определенные жалобы, который настроен на проведение эзофагогастродуоденоскопии, гастроэнтерологического обследования – конечно, всегда следует иметь в виду диагностику инфекции пилорического хеликобактера. По возможности широкое назначение эрадикационной терапии, если это показано и если нет противопоказаний.
Как мы будем назначать эрадикационную терапию?
Мы будем назначать, конечно, хорошо зарекомендовавшую себя стандартную тройную терапию.
Ингибитор протонной помпы (ИПП) в стандартной дозе 2 раза в сутки. «Кларитромицин» («Clarithromycin») – грамм в сутки. «Амоксициллин» («Amoxicillin») – 1 грамм в сутки. Возможна комбинация «Кларитромицина» с «Метронидазолом» («Metronidazolum»).
Российские рекомендации по ведению пациентов с инфекцией пилорического хеликобактера рекомендуют определенные методы, которые могут усилить эффект от стандартной тройной терапии.
Например, назначение дважды в сутки высокой дозы ИПП, удвоенной по сравнению со стандартной дозировкой.
Мне бы хотелось обратить ваше внимание на тот пункт, который помечен восклицательным знаком. Добавление к стандартной тройной терапии препарата «Висмута трикалия дицитрата» («Bismuthate tripotassium dicitrate»).
ИПП в стандартной дозе 2 раза в сутки. «Кларитромицин», «Амоксициллин» и «Висмут трикалия дицитрат» 240 мг 2 раза в сутки.
Я должна сказать, что соли «Висмута» крайне интересны и с точки зрения включения их в эрадикационную терапию, и с точки зрения возможного назначения при хроническом гастрите и АГ.
Одна из самых надежных схем лечения включает соль «Висмута». Например, «Висмут трикалия дицитрат». Это классическая квадротерапия с препаратом «Висмута». Она рекомендуется и в качестве терапии 1-й линии, и как стандартная тройная терапия.
Например, в ситуации, когда вы хотите однозначно добиться эрадикации, потому что квадротерапия – это очень мощное лечение.
Когда у нас встретилась MALT-лимфома желудка, ассоциированная с пилорическим хеликобактером, мы пациентке назначили квадротерапию, нисколько не сомневаясь в нашем решении.
Возможно, пациент не переносит антибиотики пенициллинового ряда, поэтому стандартная тройная терапия, которая может включать «Амоксициллин», в этой ситуации невозможна к применению. Мы обращаемся к квадротерапии.
Если мы провели стандартную тройную терапию, и все-таки она не оказалась эффективной, в качестве 2-й лечебной линии выбираем квадротерапию с препаратом «Висмута».
Это действительно очень надежное лечение. Посмотрите, пожалуйста, работу 2011-го года. Квадротерапия на 14 и 10 дней. Даже по очень жесткому критерию эффективности Intention to treat (ITT) 92% эрадикации, причем и 10, и 14 дней.
На предыдущем слайде в рекомендациях Российской гастроэнтерологической ассоциации вы видели рекомендуемую продолжительность квадротерапии – 10 дней.
Препараты «Висмута» – это препараты, с самого начала «хеликобактерной эры», применявшиеся для эрадикации пилорического хеликобактера.
Первооткрыватель бактерии H.pylori Барри Маршалл (Barry Marshall) придумал назначать препараты «Висмута» для проведения эрадикационной терапии инфекции пилорического хеликобактера.
В результате многолетних исследований сформировался более или менее ясный алгоритм проведения эрадикационной терапии, который и положен в основу рекомендаций Российской гастроэнтерологической ассоциации по этому вопросу.
Конечно, есть разные исследования. Есть исследования, которые говорят о низкой эффективности тройной терапии. Вот работа, которая показывает низкую эффективность и тройной терапии, и не очень высокую эффективность квадротерапии.
Хотя для реальной клинической практики 77-78%. По большому счету, это очень близко к желанным 80%. Можно поспорить, насколько этот показатель для реальной практической деятельности является показателем провала схемы.
Мне бы хотелось обратить ваше внимание на поиски эффективности комбинации различных препаратов. Я вам показывала, что рекомендует Российская гастроэнтерологическая ассоциация: усиление стандартной тройной терапии препаратом «Висмута».
Недавно проведенное исследование в регионе, где резистентность к «Метронидазолу» 42%, к «Кларитромицину» 18%. Высокие уровни резистентности. Неизвестно, что назначить.
Назначили стандартную тройную терапию с препаратом «Висмута». Получили прекрасный процент эрадикации – 80% по жесткому критерию подсчета эффективности по критерию ITT (Intention to treat).
Этот подход – прибавление «Висмута» к эрадикационной терапии – не новый. Это подход, который в разные годы поисков оптимальной эрадикационной терапии занимает то одну ступеньку, то другую. То он ближе к терапии 1-й линии, то чуть-чуть дальше от нее.
Огромный мета-анализ. 93 рандомизированных контролируемых исследования. Ели вы посмотрите последнюю группу работ, это четырехкомпонентные терапии. Это та самая терапия «Метранидазол»-«Тетрациклин»-«Висмут» и антисекреторный препарат.
Вместе с тем различные другие варианты присоединения «Висмута» к стандартной тройной терапии.
Такое добавление этого специального антихеликобатерного препарата, конечно, существенно может прибавить к эффективности эрадикации.
Как нам вести пациентов с гастритом, в том числе с АГ.
Это рекомендации Российской гастроэнтерологической ассоциации, основанные на алгоритме, предложенном Владимиром Трофимовичем Ивашкиным, в 2008-м году.
Мы рекомендуем с точки зрения профилактики рака желудка при гастрите:
• возможно, прием антиоксидантов;
• отказ от курения, концентрированного алкоголя.
Специфическая профилактика при наличии инфекции пилорического хеликобактера – это эрадикация пилорического хеликобактера. Но препараты «Висмута», безусловно, занимают здесь определенную нишу.
Посмотрите, пожалуйста, как рекомендует Российская гастроэнтерологическая ассоциация. При хроническом гастрите, в том числе атрофическом, после окончания эрадикационной терапии по желанию врача, по его мнению, возможно продолжить лечение препаратом «Висмута» до 4-8 недель для реализации защитных свойств этого препарата.
Вы знаете, что препараты «Висмута», помимо антихеликобактерной активности, обладают очень мощным потенциалом по защите клеток слизистой оболочки желудка.
Наверное, к цитопротективным эффектам «Висмута» мы еще вернемся в следующих лекциях.





