Чем лечить дырки в легких
Туберкулез: формы, симптомы, диагностика, лечение
Туберкулез – это инфекционное заболевание, вызываемое палочкой Коха (Mycobacterium tuberculosis). Патоген чаще всего поражает легкие, но существуют и другие формы: туберкулез костей, суставов, почек, кожи и других органов.
Процент смертности от туберкулеза по всему миру высок, он входит в десятку заболеваний, приводящих к летальным исходам [1]. Это не только медицинская, но и социальная проблема, поскольку на заболеваемость, помимо состояния здоровья, также влияют социальные и экономические причины, качество питания и образ жизни. Ключевыми факторами риска считаются вредные привычки, ослабленная иммунная система и хронический стресс.
Как передается туберкулез
Возбудитель передается от человека к человеку воздушно-капельным путем при чихании и кашле и просто при разговоре, а также иногда контактно (через поврежденную кожу или внутриутробно). Бактерии туберкулеза долго сохраняются активными во внешней среде в плохо проветриваемом помещении и попадают в организм здорового человека через предметы быта и продукты питания.
Заражение туберкулезом еще не означает начало заболевания: оно развивается только у 5-15% инфицированных. До развития первых симптомов может пройти несколько недель или месяцев, и основным фактором риска считается ослабление иммунных сил организма [1].
Классификация туберкулеза
Симптомы туберкулеза
Признаки заражения различаются в зависимости от органа, пораженного микобактерией. Общие симптомы включают утомляемость, сниженную трудоспособность, плохой аппетит, повышенную температуру тела, потерю веса, появление румянца на щеках.
Клинические признаки туберкулеза у детей развиваются быстрее и более выражены. Риск заражения у этой группы пациентов выше. Это связано с возрастными особенностями строения органов и нестойкостью иммунитета ребенка к агрессивным инфекциям. Помимо «взрослых» симптомов у детей также отмечаются капризность, плаксивость, необоснованная беспокойность и нарушения сна.
Диагностика туберкулеза
Это заболевание, особенно закрытая форма, сложно диагностируется. Переход из латентной фазы в активную смазанный, а клинические симптомы не позволяют установить точный диагноз или отсутствуют. В связи с этим решающее значение имеет лабораторная диагностика.
Проба Манту (или туберкулиновая проба). Для проведения этого классического анализа на туберкулез пациенту подкожно в области предплечья вводят очищенный туберкулин – смесь белков, характерных для микобактерий. Оценку иммунологической реакции проводят через 48-72 часов на основании диаметра папулы (узелка над поверхностью кожи) или участка покраснения в месте введения туберкулина. У людей, неинфицированных бактерией, папулы не образуются или их размеры незначительны. К основным недостаткам метода относятся непереносимость туберкулина и ложноположительная реакция у людей, вакцинированных от туберкулеза вакциной БЦЖ.
Квантифероновый тест на туберкулез. Этот современный иммунологический метод позволяет выявить латентный туберкулез, а также туберкулезное поражение других органов. Введения туберкулина не требуется, поэтому этот тест подходит уязвимым группам пациентов (беременные и кормящие женщины, пожилые люди, ВИЧ-инфицированные, люди с непереносимостью туберкулина). Для диагностики используется венозная кровь. Наличие в организме активного туберкулеза обуславливает появление в крови особых белков, входящих в состав микобактерий. Т-лимфоциты реагируют на присутствие этих белков и в результате такой сенсибилизации начинают усиленно вырабатывать интерферон-гамма. Квантифероновый тест основан на измерении уровня интерферона-гамма, повышение которого указывает на наличие туберкулезной инфекции в пробе крови.
Метод T-SPOT.TB. Позволяет диагностировать латентную и активную формы легочного и внелегочного туберкулеза. Для исследования используют венозную кровь. В основе метода лежит оценка количества самих сенсибилизированных Т-лимфоцитов. Он также не дает ложноположительных результатов и подходит уязвимым группам пациентов.
Анализ мокроты. Для проведения теста необходимо собрать утреннюю мокроту, которая отделяется при кашле. Во взятом образце определяют наличие самих микобактерий. Анализ подходит только для диагностики туберкулеза легких.
Анализ мочи. Выявляют изменения параметров, характерные для туберкулеза: появление лейкоцитов, эритроцитов, бактерий, белка, гноя, сдвиг реакции мочи в кислую сторону.
Отрицательные лабораторные анализы не гарантируют отсутствие туберкулеза. Пациенты с подозрением на заболевание проходят флюорографию и/или рентгенографию легких. Для выявления внелегочных форм туберкулеза проводят МРТ, КТ и другие инструментальные исследования. Также применяют биопсию (взятие образца тканей) для микроскопических исследований и посевов на питательные среды.
Дифференциальную диагностику проводят с широким рядом заболеваний в тех случаях, когда ни одно исследование не подтвердило наличие микобактерий, присутствуют атипичные симптомы или отсутствует адекватный ответ на противотуберкулезное лечение.
Лечение туберкулеза
Полное выздоровление не гарантирует отсутствие рецидива заболевания в будущем.
Фиброз после коронавируса
Специалисты реабилитационного центра “Лаборатория Движения” помогут в восстановлении после перенесенной коронавирусной инфекции (COVID-19)
У четверти пациентов с COVID-19 развивается отягощенное пневмонией течение болезни. Многоочаговое поражение лёгких влечет вероятность появления тяжелых осложнении, таких как фиброз после коронавируса. Последствия воспалительного процесса, в ходе которых происходит замещение легочной ткани соединительной. Простыми словами, фиброз — это возникновение рубцов и шрамов. Если поражения малого размера, то рубцевание не влияет на легочную функцию. Если обширные, то снижается газообмен, возникают необратимые изменения легочной функции и дыхательная недостаточность.
Рассказывает специалист РЦ «Лаборатория движения»
Дата публикации: 29 Октября 2021 года
Дата проверки: 30 Ноября 2021 года
Содержание статьи
Фиброз легких – что это, причины
Фиброз легких или пневмофиброз после ковида — это замена ткани легких соединительным рубцом, происходящая под влиянием воспалительного процесса. При выраженном воспалении в легком образуются области по типу «матового стекла». Под воздействием терапии области сжимаются, уплотняются, на их месте остается шрам или фиброзное изменение.
В отличие от альвеол, соединительная ткань не обладает эластичностью и воздухопроницаемостью, снижается объем легких и потребляемого кислорода. Ковидная пневмония отличается от внебольничной, риск необратимого поражения легочной ткани минимален при своевременной терапии в начале заболевания и дальнейшей реабилитации пациента в постковидном периоде.
На формирование пневмофиброза или пневмосклероза легких после коронавируса уходит не меньше трех месяцев. Сформировавшийся фиброз необратим, но на стадии развития процесса фиброзные изменения благоприятно минимизируются медикаментозным и физиотерапевтическим лечением.
Симптомы
Фиброз легких после коронавируса — симптомы выражены следующими признаками:
Для подтверждения диагноза назначают КТ легких, на котором рентгенолог увидит все произошедшие изменения. Фиброз легких, симптомы после ковида на снимках компьютерной томографии выражены:
По совокупности признаков врачи определяют объем медикаментозного лечения и дальнейшей реабилитации.
Вероятность развития фиброза после коронавируса
На склонность к фиброобразованию влияет
Также в группе риска пациенты с тяжелым течением SARS-CoV-2, находившиеся на искусственной вентиляции легких.
Как долго сохраняются аномальные изменения в органах дыхательной системы
Постковидные патологические изменения сохраняются в легких сроком от трех до шести-восьми месяцев. Продолжительность индивидуальна в каждом клиническом случае и зависит от состояния иммунной системы, наличия сопутствующих заболеваний, раннего или поздно начатого лечения.
При появлении даже незначительного проявления симптомов, указывающих на образование пневмофиброза, необходимо посетить врача и пройти рекомендуемое обследование. Чем раньше начато лечение и пульмонологическое восстановление, тем меньше риск осложнений.
Лечение фиброза легких после пневмонии
Ведение пациентов с перенесенной ковидной пневмонией предусматривает комплексную диагностику и лечение. Перед назначением врач учитывает результаты обследования, подбирает тактику индивидуального курса терапии.
Наряду с медикаментозным лечением используют физиотерапевтические процедуры, специальные комплексы дыхательной гимнастики, лечебной физкультуры.
Как избежать осложнений
Чем опасен фиброз легких после коронавируса — при большой площади фиброзных разрастаний страдают не только легкие. Появление очагов кальцинатов в легких после коронавируса снижает объем вдыхаемого и выдыхаемого воздуха. Возникают осложнения в работе сердечно-сосудистой системы — сердце, чтобы насытить органы кислородом, начинает быстрее перекачивать кровь. Появляется деформация сосудов, наблюдается повышение давления, образуются тромбы.
Последствия со стороны нервной системы выражены проявлениями кислородного голодания мозга: снижением когнитивных функций, работоспособности, проблемами с памятью, быстрой утомляемостью, развитием стойкого депрессивного состояния.
Своевременное лечение фиброза легких после коронавируса дают благоприятный прогноз. Дальнейшая реабилитация направлена на устранение патологического состояния и минимизации риска осложнений.
Бронхиальный свищ
Бронхиальный свищ – это патология бронхиального дерева, характеризующаяся наличием патологического сообщения бронха с внешней средой, полостью плевры или просветом внутренних органов. Клиническая картина определяется взаимоотношениями бронха с другими анатомическими структурами. Общими признаками являются одышка, цианоз, кашель с выделением содержимого дренируемых органов (гноя, пищевых масс, примеси желчи и пр.). Диагноз бронхиального свища подтверждается данными рентгенодиагностики (рентгенографии легких, фистулографии, бронхографии, КТ), эндоскопии (бронхоскопии, ЭГДС), плевральной пункции с манометрией. Тактика в отношении бронхиальных свищей может быть консервативной или хирургической.
МКБ-10
Общие сведения
Бронхиальный свищ – фистула, обусловливающая аномальное сообщение бронха с какой-либо полостью, органом или поверхностью кожи. Бронхиальные свищи являются одной из наиболее сложных проблем пульмонологии и торакальной хирургии, поскольку трудно поддаются консервативному лечению, поддерживают хронические гнойные процессы, существенно отягощают послеоперационный прогноз. Частота формирования бронхиальных свищей тесно связана с их этиологией. Так, врожденные пищеводно-трахеальные и пищеводно-бронхиальные сообщения встречаются у 0,03% новорождённых. В структуре приобретенных бронхиальных свищей преобладают послеоперационные дефекты – на их долю приходится 2-30% осложнений резекции легкого.
Причины
Формирование врожденных бронхиальных свищей происходит внутриутробно. Возникновение бронхопищеводных и трахеопищеводных свищей обусловлено неполным разделением дыхательной и пищеварительной систем на определенном этапе эмбриогенеза под влиянием различных факторов, воздействующих на плод (авитаминоза, внутриутробных инфекций, травм, радиации и пр.). В большинстве случаев при таком пороке развития имеется свищевой ход между главным бронхом (обычно правым) и пищеводом. Этиология приобретенных бронхиальных свищей может быть различной:
Патогенез
Вначале бронхиальный свищ представляет собой патологическое сообщение, стенки которого выстланы некротическими массами. По мере отторжения нежизнеспособных тканей формируется канал, покрытый грануляционной или эпителиальной тканью. Этот канал может соединять бронх с грудной стенкой, плевральной полостью, близлежащими органами, обусловливая специфическую клиническую картину. Со временем стенки свищевого хода становятся ригидными, препятствуя самостоятельному закрытию дефекта. Любой инфекционный процесс в бронхиальном дереве, полости плевры, легочной ткани поддерживает течение бронхиального свища.
Классификация
Кроме деления на врожденные и приобретенные, бронхиальные свищи подразделяются на единичные (62%) и множественные (38%, в т. ч. «решетчатое легкое»). С учетом этиологического фактора они могут иметь посттравматическое, постинфекционное, послеоперационное происхождение. В зависимости от уровня локализации различают свищи главных, долевых, сегментарных, субсегментарных бронхов и альвеолярные фистулы. В клинической практике наибольшую ценность представляет анатомическая классификация, в рамках которой выделяют:
Наружные (торакобронхиальные) свищи
Внутренние свищи
Симптомы бронхиальных свищей
Критериями, определяющими симптоматику бронхиальных свищей, выступают их анатомические особенности, диаметр, сроки образования дефекта, наличие или отсутствие инфекционного процесса. К числу общих симптомов, сопровождающих развитие патологии, относятся признаки интоксикации (лихорадка с ознобами, слабость, разбитость, головная боль, плохой аппетит) и дыхательной недостаточности (цианоз, одышка, боли в грудной клетке). Кроме этого, для различных видов бронхиальных свищей характерны свои специфические проявления.
Наружные (бронхокожные, бронхоплеврокожные) свищи характеризуются наличием видимого дефекта на коже грудной стенки, из которого периодически отходит слизистое или слизисто-гнойное отделяемое, а при кашле и натуживании может выделяться воздух. Попадание в свищевой ход воды провоцирует возникновение резкого приступообразного кашля и приступа удушья. Иногда снятие окклюзионной повязки вызывает усиление кашля, одышки и цианоза, нарушение голоса вплоть до афонии.
Бронхиальные свищи, сообщающиеся с «сухой» плевральной полостью, проявляются сухим кашлем или откашливанием незначительного количества слизистой мокроты. При бронхоплевральных свищах, развившихся на фоне гнойного плеврита, общее состояние больных отягощается гнойно-резорбтивной лихорадкой, интоксикацией, истощением. Отмечается отхождение большого объема гнойной, зловонной мокроты при кашле, выраженная одышка, выделение воздуха из плеврального дренажа, подкожная эмфизема. Клинику бронхолегочных свищей определяют субфебрилитет, кашель с выделением слизисто-гнойной мокроты, потливость, слабость.
Основным признаком бронхоорганных свищей служит откашливание больным содержимого того органа, с которым сообщается бронх: съеденной пищи, желчи, желудочного или кишечного содержимого. Врожденные трахео- и бронхопищеводные свищи могут быть заподозрены вскоре после рождения ребенка на основании поперхивания при кормлении, вздутия желудка, развития аспирационной пневмонии. Основным проявлением приобретенных свищей служит кашель, связанный с приемом жидкости и пищи, иногда – удушье.
Осложнения
Длительное течение бронхиальных свищей может привести к возникновению пневмонии и хронической эмпиемы плевры. Возможны осложнения в виде кровохарканья или легочного кровотечения, аспирационной пневмонии другого легкого. Системные последствия представлены сепсисом, массивным внутренним кровотечением, висцеральным амилоидозом.
Диагностика
При осмотре пациента с предполагаемым диагнозом «бронхиальный свищ» обращает внимание цианоз кожи и слизистых, одышка, тахикардия, характерная деформация концевых фаланг пальцев («барабанные палочки», «часовые стекла»). Аускультация выявляет рассеянные разнокалиберные хрипы.
Бронхокожные свищи, открывающиеся на поверхности грудной стенки, обнаруживаются визуально. С диагностической целью может быть проведено зондирование свища с введением водного раствора метиленового синего. Возникновение кашля с выделением окрашенной мокроты подтверждает наличие бронхиального свища. Для получения информации о протяженности и конфигурации свищевого хода производится фистулография с контрастными веществами. В ряде случаев уточнить локализацию, количество, размеры свищевых ходов позволяет диагностическая торакоскопия, выполняемая через свищевое отверстие в грудной стенке.
При внутренних свищах важное диагностическое значение имеет бронхоскопия, позволяющая оценить состояние бронхиального дерева, а также рентгенологические методы диагностики: обзорная рентгенография и КТ легких, бронхография. Бронхоплевральные свищи могут быть выявлены с помощью данных плевральной пункции с манометрией – при сообщении бронхиального дерева с полостью плевры в последней не удается создать отрицательное давление путем аспирации воздуха. В случае подозрения на наличие бронхопищеводного или бронхожелудочного свища показана эзофагогастроскопия.
Лечение бронхиальных свищей
В большинстве случаев бронхиальные свищи требуют оперативного лечения. Вместе с тем, в отношении некоторых фистул бронхов может быть применена консервативная тактика. Лечением данной патологии должны заниматься торакальные хирурги, владеющие всем арсеналом методов ведения больных с бронхиальными свищами. Консервативное лечение бронхиальных свищей предполагает проведение мероприятий по санации гнойных полостей: дренирование плевральной полости, промывание антисептическими растворами, введение протеолитических ферментов и антибиотиков, удаление инородных тел, наложение аппарата активной аспирации и т. п. После облитерации остаточных полостей возможно самострельное закрытие небольших бронхиальных свищей.
Имеется положительный опыт ликвидации свищей с помощью химического прижигания или электрокоагуляции фистулы, позволяющих разрушить эпителиальную выстилку и стимулировать рост соединительной ткани в канале. При крупных фистулах может применяться временное эндоскопическое закрытие свищнесущего бронха специальной поролоновой пломбой – такая тактика позволяет осуществить лаваж гнойной полости и создать благоприятные условия для оперативной ликвидации бронхиального свища.
Консервативное лечение бронхиальных свищей оказывается успешным лишь в 10-12% случаев, поэтому большинству пациентов показано оперативное закрытие дефекта. Для оперативного устранения торакобронхиального свища может выполняться его иссечение с последующим ушиванием, мышечная пластика лоскутом на ножке. При послеоперационных свищах показано выполнение реампутации культи бронха. Устранение пищеводно-бронхиальных свищей требует ушивания дефектов со стороны пищевода и бронха, возможно – резекции измененной части легкого. Закрытие бронхоплеврального свища может производиться с помощью интраплевральной торакопластики или декортикации легкого.
Прогноз и профилактика
Исход и перспективы выздоровления зависят от причины, приведшей к формированию бронхиального свища, полноты, адекватности и своевременности лечебных мероприятий. Наиболее серьезный прогноз и высокая летальность (30-70%) отмечается при послеоперационных свищах, осложненных эмпиемой плевры. При возникновении бронхиального свища выжидательная тактика недопустима; необходимо как можно более раннее начало консервативных мероприятий, проведение хирургического вмешательства после необходимой подготовки. Профилактика приобретенных бронхиальных свищей заключается в соблюдении техники обработки культи бронха, своевременной терапии гнойно-деструктивных заболеваний легких, предупреждении травм грудной клетки.
Абсцедирующая пневмония
Абсцедирующая пневмония или абсцесс легких – сложная форма воспаления легких, протекающая с расплавлением легочных тканей и образованием полостей, заполненных гнойным содержимым. Главная причина абсцедирующего осложнения – затяжная гнойная пневмония. Симптомы заболевания практически ничем не отличаются от обычной пневмонии: у больного критическая температура, которую сложно сбить, дыхательная недостаточность, сильный кашель, сопровождающийся отхождением мокроты с гнойными включениями.
Диагностика абсцедирующей пневмонии предполагает сдачу лабораторных анализов и прохождение аппаратных методик исследования. Лечение в основном сочетает методы консервативного и хирургического воздействия. Отсутствие терапии чревато серьезными последствиями, вплоть до летального исхода.
Причины абсцедирующей пневмонии
Деструкцию и расплавление легочных структур провоцируют различные болезнетворные микроорганизмы:
Зачастую болезнь развивается на фоне поражения тканей легких анаэробными микроорганизмами, которые проникают в органы дыхания вследствие аспирации секрета ротоглотки или распространения из очагов инфекции по лимфо- и кровеносным сосудам.
Аспирационная природа развития болезни чаще всего встречается у таких категорий пациентов:
Само по себе проникновение инфекции в легкие не гарантирует возникновения гнойно-воспалительного процесса. Все зависит от состояния иммунной системы человека. Если иммунитет работает слаженно, защитные клетки моментально уничтожат болезнетворную флору, в противном случае инфекция внедряется в ткани и беспрепятственно размножается, вызывая деструктивные изменения в легких.
После проникновения возбудителя в ткани легких образуется гнойный очаг, вокруг которого формируется воспаленная зона. Она локализует участок гноеобразования от рядом расположенных неповрежденных структур. В результате образуется полость, наполненная гнойным содержимым.
Иммунная система, пытаясь избавиться от патологического очага, удаляет гнойное содержимое через бронхи. Нередко случается прорыв абсцесса в бронхи. После прорыва стенки капсулы слипаются и на этом месте формируется рубец. Если же прорыва абсцесса не случилось, развиваются такие опасные осложнения:
Если при таких осложнениях медицинская помощь оказана больному несвоевременно, высока вероятность летального исхода.
Возможности медцентров
Симптомы абсцедирующей пневмонии
По симптоматике гнойная пневмония у взрослых мало чем отличается от обычного воспаления легких. Человека беспокоят:
При отсутствии лечения состояние стремительно ухудшается. Нарастают признаки общей интоксикации:
Приступ кашля сопровождается отхождением мокроты с гнойным и кровянистым включением. Прогрессирует симптоматика абсцедирующей пневмонии:
В клиниках «Президент-Мед» вы можете
Диагностика абсцедирующей пневмонии
Чтобы подтвердить или опровергнуть диагноз «абсцедирующая пневмония», врач, после первичного осмотра и сбора анамнеза, дает направление на комплексное диагностическое обследование, включающее такие процедуры:
Диагноз поможет подтвердить рентгенологическое исследование. На снимках гнойная пневмония выглядит так:
Ультразвуковое исследование назначается при наличии плевральных осложнений. Во время УЗИ проводится дренирование плевральной полости и удаление гнойного содержимого. При необходимости врач может назначить пункцию плевральной полости, чтобы удостовериться в правильности поставленного диагноза.
Если данных, полученных в результате вышеупомянутых диагностических процедур, недостаточно, врач даст направление на компьютерную или магниторезонансную томографию.
Лечение абсцедирующей пневмонии
После подтверждения диагноза врач подбирает индивидуальную схему терапии, продолжительность которой может составлять от 3 недель до нескольких месяцев. Все зависит от тяжести и запущенности болезни.
Консервативная схема терапии включает:
Для очищения легочной ткани от гнойных очагов проводятся хирургические процедуры:
Если консервативные методы не приносят должного эффекта, врач принимает решение о проведении операции по удалению пораженных участков легких.
Абсцедирующая пневмония, лечение которой назначено правильно и своевременно, имеет относительно благоприятный прогноз. Если же терапия отсутствует и болезнь прогрессирует, развиваются тяжелые, угрожающие жизни осложнения. Прогноз запущенной гнойной пневмонии серьезный: процент летального исхода высокий – 15 – 25 %.
Туберкулез: формы, симптомы, диагностика, лечение
Туберкулез – это инфекционное заболевание, вызываемое палочкой Коха (Mycobacterium tuberculosis). Патоген чаще всего поражает легкие, но существуют и другие формы: туберкулез костей, суставов, почек, кожи и других органов.
Процент смертности от туберкулеза по всему миру высок, он входит в десятку заболеваний, приводящих к летальным исходам [1]. Это не только медицинская, но и социальная проблема, поскольку на заболеваемость, помимо состояния здоровья, также влияют социальные и экономические причины, качество питания и образ жизни. Ключевыми факторами риска считаются вредные привычки, ослабленная иммунная система и хронический стресс.
Как передается туберкулез
Возбудитель передается от человека к человеку воздушно-капельным путем при чихании и кашле и просто при разговоре, а также иногда контактно (через поврежденную кожу или внутриутробно). Бактерии туберкулеза долго сохраняются активными во внешней среде в плохо проветриваемом помещении и попадают в организм здорового человека через предметы быта и продукты питания.
Заражение туберкулезом еще не означает начало заболевания: оно развивается только у 5-15% инфицированных. До развития первых симптомов может пройти несколько недель или месяцев, и основным фактором риска считается ослабление иммунных сил организма [1].
Классификация туберкулеза
Симптомы туберкулеза
Признаки заражения различаются в зависимости от органа, пораженного микобактерией. Общие симптомы включают утомляемость, сниженную трудоспособность, плохой аппетит, повышенную температуру тела, потерю веса, появление румянца на щеках.
Клинические признаки туберкулеза у детей развиваются быстрее и более выражены. Риск заражения у этой группы пациентов выше. Это связано с возрастными особенностями строения органов и нестойкостью иммунитета ребенка к агрессивным инфекциям. Помимо «взрослых» симптомов у детей также отмечаются капризность, плаксивость, необоснованная беспокойность и нарушения сна.
Диагностика туберкулеза
Это заболевание, особенно закрытая форма, сложно диагностируется. Переход из латентной фазы в активную смазанный, а клинические симптомы не позволяют установить точный диагноз или отсутствуют. В связи с этим решающее значение имеет лабораторная диагностика.
Проба Манту (или туберкулиновая проба). Для проведения этого классического анализа на туберкулез пациенту подкожно в области предплечья вводят очищенный туберкулин – смесь белков, характерных для микобактерий. Оценку иммунологической реакции проводят через 48-72 часов на основании диаметра папулы (узелка над поверхностью кожи) или участка покраснения в месте введения туберкулина. У людей, неинфицированных бактерией, папулы не образуются или их размеры незначительны. К основным недостаткам метода относятся непереносимость туберкулина и ложноположительная реакция у людей, вакцинированных от туберкулеза вакциной БЦЖ.
Квантифероновый тест на туберкулез. Этот современный иммунологический метод позволяет выявить латентный туберкулез, а также туберкулезное поражение других органов. Введения туберкулина не требуется, поэтому этот тест подходит уязвимым группам пациентов (беременные и кормящие женщины, пожилые люди, ВИЧ-инфицированные, люди с непереносимостью туберкулина). Для диагностики используется венозная кровь. Наличие в организме активного туберкулеза обуславливает появление в крови особых белков, входящих в состав микобактерий. Т-лимфоциты реагируют на присутствие этих белков и в результате такой сенсибилизации начинают усиленно вырабатывать интерферон-гамма. Квантифероновый тест основан на измерении уровня интерферона-гамма, повышение которого указывает на наличие туберкулезной инфекции в пробе крови.
Метод T-SPOT.TB. Позволяет диагностировать латентную и активную формы легочного и внелегочного туберкулеза. Для исследования используют венозную кровь. В основе метода лежит оценка количества самих сенсибилизированных Т-лимфоцитов. Он также не дает ложноположительных результатов и подходит уязвимым группам пациентов.
Анализ мокроты. Для проведения теста необходимо собрать утреннюю мокроту, которая отделяется при кашле. Во взятом образце определяют наличие самих микобактерий. Анализ подходит только для диагностики туберкулеза легких.
Анализ мочи. Выявляют изменения параметров, характерные для туберкулеза: появление лейкоцитов, эритроцитов, бактерий, белка, гноя, сдвиг реакции мочи в кислую сторону.
Отрицательные лабораторные анализы не гарантируют отсутствие туберкулеза. Пациенты с подозрением на заболевание проходят флюорографию и/или рентгенографию легких. Для выявления внелегочных форм туберкулеза проводят МРТ, КТ и другие инструментальные исследования. Также применяют биопсию (взятие образца тканей) для микроскопических исследований и посевов на питательные среды.
Дифференциальную диагностику проводят с широким рядом заболеваний в тех случаях, когда ни одно исследование не подтвердило наличие микобактерий, присутствуют атипичные симптомы или отсутствует адекватный ответ на противотуберкулезное лечение.
Лечение туберкулеза
Полное выздоровление не гарантирует отсутствие рецидива заболевания в будущем.
Абсцесс легкого
В клинической практике под термином «абсцесс легкого» понимают патологический процесс, характеризующийся формированием более или менее ограниченной полости в легочной ткани в результате ее некроза и последующего гнойного расплав
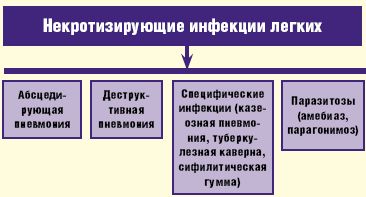
В клинической практике под термином «абсцесс легкого» понимают патологический процесс, характеризующийся формированием более или менее ограниченной полости в легочной ткани в результате ее некроза и последующего гнойного расплавления. Зачастую в описании некротизирующих инфекций в легких используют термин «некротизирующая пневмония» или «гангрена легкого», тем самым выделяя две различные клинические ситуации— легочный некроз с небольшими многофокусными формирующимися полостями и большое кавитарное поражение. Однако фактически мы нередко наблюдаем образование мелкофокусной инфильтрации с тенденцией к слиянию и образованию нескольких небольших по размеру очагов абсцедирования легочной ткани, которые в последующем могут сливаться с формированием единой полости. В группу некротизирующих инфекций легких входит не только абсцедирующая пневмония или собственно абсцесс легкого, но и деструктивная пневмония, которая характеризуется образованием полостей, нечетко отграниченных от воспаленной или малоизмененной легочной ткани; а также ряд специфических инфекций (казеозная пневмония, туберкулезная каверна, сифилитическая гумма), сопровождающихся развитием деструкции легочной ткани и паразитозы (амебиаз, парагонимоз), которые, хотя и рассматриваются вне рамок пневмонии, тем не менее, при локализации поражения в легких могут вызывать деструктивные повреждения соответствующей локализации (рис. 1).
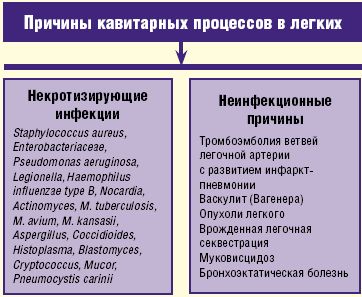
Кроме некротизирующих инфекций кавитарный процесс в легких может быть обусловлен неинфекционными причинами, а именно тромбоэмболией ветвей легочной артерии, васкулитом Вагенера, опухолевым процессом, врожденной легочной секвестрацией, муковисцидозом и бронхоэктатической болезнью (рис. 2).
Выделяют острые или хронические абсцессы легкого, основываясь на продолжительности симптомов, начиная с догоспитального этапа и вплоть до момента оказания специализированной медицинской помощи. Под острым абсцессом понимают патологическую ситуацию длительностью до одного месяца, клинические случаи с более длительным развитием клинической картины рассматриваются как хронические.
Также абсцессы легких подразделяются на первичные и вторичные, исходя из наличия/отсутствия взаимосвязанных патологических процессов. Абсцессы у пациентов, склонных к аспирации содержимого ротоглотки, а также у ранее здоровых пациентов обычно рассматриваются как первичные; вторичные абсцессы легкого обычно связывают с предшествующим возникновением бронхогенной карциномы легкого или развитием системного заболевания с выраженной дисфункцией иммунной системы, либо c ВИЧ-инфицированием, а также они возможны у пациентов, перенесших операцию по пересадке/трансплантации органов.
В основе абсцесса легкого/абсцедирующей пневмонии чаще всего лежит аспирация из верхних отделов дыхательных путей, на долю которой приходится до 70% и более всех случаев заболевания, а среди выявляемых патогенов преобладают разновидности анаэробов, которые колонизируют в десневых карманах ротовой полости. Напротив, распространение инфекции из поддиафрагмального пространства— менее частая причина, обусловливающая развитие абсцесса легкого; еще реже встречается гематогенное распространение инфекционного процесса.
Первым шагом в развитии абсцесса легкого является поступление инфицированного содержимого ротоглотки в нижние отделы дыхательных путей, что обычно происходит при нахождении пациента в лежачем положении. Аспирация содержимого ротоглотки чаще всего наблюдается у пациентов с нарушением сознания, страдающих алкоголизмом и наркоманией, а также в случае развития дисфагии. Сначала возникает пневмонит, в последующем (обычно 7–14 дней) поступивший инфицированный материал приводит к развитию некроза легочной ткани. Некроз в дальнейшем эволюционирует в абсцесс легкого и/или эмпиему; на более позднем этапе возможно открытие бронхоплеврального свища, а также прорыв абсцесса в плевральную полость.
Кроме всего прочего, существует еще ряд механизмов развития легочного абсцедирования инфекционного генеза. Во-первых, необходимо помнить об эндокардите трикуспидального клапана, основным этиологическим агентом которого является Staphylococcus aureus. Заболевание чаще всего наблюдается у молодых пациентов, страдающих внутривенной формой наркомании. Развитие патологического процесса в сердце манифестирует с развитием септической эмболии в легочной ткани.
В другом случае речь идет о так называемом синдроме Лемиера (thrombophlebitis Lemierre)— гнойном тромбофлебите шейных вен. Вначале наблюдается тонзиллит с развитием паратонзиллярного абсцесса с последующим распространением инфекционного процесса на нижележащие отделы шеи, когда затрагивается шейное сосудистое сплетение. Эволюцией процесса является бактериемия, вызываемая Fusobacterium necrophorum, которая приводит к образованию септических эмболов в легких.
Этиология абсцесса легкого известна: в 50% случаев выявляются анаэробы— Peptostreptococcus, Prevotella, Bacteroides sp. и Fusobacterium sp. (табл. 1). В другой половине случаев абсцесс легкого вызывают ассоциации анаэробных и аэробных микроорганизмов— в первую очередь представители семейства Enterobacteriaceae и, прежде всего, Klebsiella pneumoniae и K.oxytoca, реже Staphylococcus aureus, Streptococcus spp. и Haemophilus influenzae. Аэробы сравнительно редко способны вызывать мономикробный абсцесс легкого, однако стоит отметить, что K.рneumoniae и S.aureus обладают наиболее высокой гистолитической активностью.
В отношении последнего необходимо отметить, что в подавляющем большинстве доказанных случаев легочной инфекции, вызванной S.aureus, наблюдается лишь неосложненная бронхопневмония. Исключением является развитие инфекционного эндокардита правых отделов сердца. Заболевание, как уже было отмечено, манифестирует с образованием септических эмболов в легочной ткани.
К сожалению, в практической деятельности микробиологическая диагностика редко приводит к положительному результату вследствие объективных трудностей в выделении культуры анаэробов. Стандартом получения образцов для последующего микробиологического исследования является проведение трансторакальной тонкоигольной биопсии абсцесса, выполнение которой большинству пациентов не представляется возможным. Кроме того, российские лаборатории обладают невысоким опытом работы с анаэробными возбудителями.
В абсолютном большинстве случаев у истоков развития абсцесса легких лежит развитие очагового паренхиматозного воспаления, т.е. пневмонии, что сопровождается такими неспецифическими признаками инфекции нижних дыхательных путей, как лихорадка, кашель, плевральные боли и собственно очаговая инфильтрация, которая подтверждается данными клинического обследования и рентгенографией органов грудной клетки. Появление вышеобозначенных симптомов заставляет пациента обратиться за медицинской помощью, а проведение правильного диагностического алгоритма позволяет врачу диагностировать инфильтрацию легочной ткани.
Безусловно, важным моментом является выявление причинно-следственных факторов— дисфагии, эпизодов нарушения сознания и пр., на фоне которых появилась клиническая симптоматика. Необходимо также учитывать результаты рентгенографии органов грудной клетки, проводимой в обязательном порядке в прямой и боковой проекциях. Чаще всего инфильтративные изменения с очагом некроза паренхимы легкого наблюдаются в тех сегментах легких, которые связаны с так называемым «гравитационным механизмом» (локализация абсцесса в заднем сегменте верхней доли, если аспирация произошла в положении лежа, или верхнем сегменте нижней доли, если аспирация произошла в положении сидя). Определенную роль играет интерпретация результатов общего исследования полученной мокроты— цвет, запах, присутствие крови и пр.
Однако на практике врач чаще всего диагностирует развитие пневмонической инфильтрации, не обращая внимание на анализ факторов риска аспирации и назначает антибактериальную терапию с учетом возбудителей, характерных для внебольничной пневмонии, — Streptococcus pneumoniae, Chlamydophila, Mycoplasma pneumoniae и пр. Следующим этапом естественной эволюции заболевания является некротизирующая пневмония, которая, наряду с лихорадкой и плевральными болями, характеризуется появлением «гнилостной» мокроты и формированием микроабсцессов (менее 1,0 см в диаметре). Последние обычно выявляются при компьютерной томографии органов грудной клетки, поскольку рентгенография зачастую не дает возможность надежно визуализировать полостные образования небольших размеров на фоне пневмонической инфильтрации.
Вслед за некротизирующей пневмонией формируется собственно абсцесс легкого, что сопровождается такими симптомами, как лихорадка, анорексия, похудание, возможная анемизация, плевральные боли, экспекторация «гнилостной» мокроты. Завершает диагностику формирующегося или сформировавшегося абсцесса легкого визуализация толстостенных полостных образований диаметром более 1,0 см с характерным уровнем жидкости и газа. У ряда больных, особенно в случае прилежания полости абсцесса к плевре, нередко происходит спонтанное дренирование полости абсцесса с закономерным формированием эмпиемы плевры.
Проведение дифференциальной диагностики у пациентов с выявленным абсцессом легкого необходимо с единственной целью— определить инфекционный и неинфекционный характер поражения. В обязательном порядке собирается анамнез с настороженностью в вопросах туберкулеза и, как минимум, трехкратно проводится посев мокроты либо образцов бронхиолоальвеолярного лаважа на Mycobacterium tuberculosis. Желательным является проведение бронхоскопии, так как в ряде случаев удается установить причины абсцедирования (инородные тела, опухолевое поражение и пр.).
Лечение абсцесса легкого
В большинстве клинических ситуаций антимикробные препараты при абсцессе легкого назначаются эмпирически, что связано с рядом объективных обстоятельств:
Общепринятым стандартом в лечении абсцесса легкого до настоящего времени остается применение бензилпенициллина по 2 млн ЕД внутривенно с интервалом 4 часа в комбинации с метронидазолом (0,5–1,0 г в/в с интервалом 8–12 ч); в последующем, при достижении отчетливого клинико-рентгенологического улучшения, осуществляется переход на пероральную терапию амоксициллином по 0,5–1,0 г с интервалом 8 часов и метронидазолом (0,5 г с интервалом 8–12 ч) внутрь.
Однако слабой стороной такой терапии является то, что 15–20% штаммов потенциальных возбудителей абсцесса легкого оказываются резистентными к бензилпенициллину (прежде всего, это фузобактерии и бактероиды). Кроме того, на сегодняшний день доказанным является преимущество линкосамидов (клиндамицин по 600 мг в/в с интервалом 6–8 ч с последующим переходом на прием антибиотика внутрь по 300 мг с интервалом 6 ч) по сравнению с традиционной терапией бензилпенициллином. Возможна также высокодозная терапия ингибиторозащищенными аминопенициллинами (амоксициллин/клавуланат по 2,4 г в/в с интервалом 6 часов с последующим переходом на прием антибиотика внутрь по 625 мг с интервалом 6–8 ч), предпочтительно в режиме ступенчатого лечения.
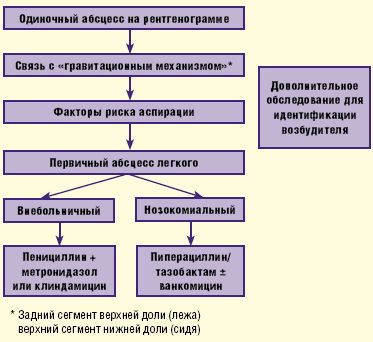
В случае нозокомиального, или внутрибольничного, происхождения абсцесса легкого назначаются ингибиторозащищенные пенициллины с антисинегнойной активностью— пиперациллин/тазобактам, в комбинации с ванкомицином (риск метициллинорезистентных S.aureus) или без него (рис. 3).
Российские эксперты в качестве препаратов выбора рекомендуют ингибиторозащищенные аминопенициллины (амоксициллин/клавуланат, ампициллин/сульбактам) либо цефоперазон/сульбактам. При отсутствии этих антибиотиков либо их неэффективности могут использоваться карбапенемы, ингибиторозащищенные пенициллины (тикарциллин/клавуланат, пиперациллин/тазобактам) либо комбинации клиндамицина с аминогликозидами (АГ) (табл. 2).
Длительность терапии при абсцессе легкого определяется индивидуально, но, как правило, составляет не менее 3–4 недель.
В ряде случаев невозможно добиться излечения пациента без хирургического вмешательства, чаще всего требуется торакотомическое дренирование, реже применяется торакоскопия и декортикация.
Клинический пример
Пациент И., 1946 года рождения, переведен в ГВКГ им Н. Н. Бурденко 23.08.2007 г. из терапевтического отделения базового госпиталя.
Из анамнеза: пенсионер МО РФ, занимается преподавательской деятельностью. Страдает сахарным диабетом 2-го типа, среднетяжелого течения с марта 2007 г., гипертонической болезнью второй стадии, ишемической болезнью сердца, дисциркуляторной энцефалопатией. Рекомендованные лекарственные препараты регулярно не принимает. Курил на протяжении 15 лет до 10 сигарет в сутки, злоупотребляет алкоголем.
Из анамнеза заболевания известно, что заболел остро в начале августа 2007 г., когда после переохлаждения температура тела повысилась до фебрильных цифр, появились озноб, боль в левой половине грудной клетки, усиливающаяся при движениях, перемене положения тела, выраженная слабость, непродуктивный кашель. Обратился в поликлинику по месту жительства, где с 8.08.07 по 13.08.07 г. проходил лечение у невролога по поводу межреберной невралгии. Получал диклофенак, с кратковременным купированием болевого синдрома. Ввиду усиления кашля, сохранения фебрильной лихорадки, болевого синдрома в грудной клетке слева врачом-неврологом заподозрена левосторонняя пневмония. Пациент госпитализирован в терапевтическое отделение базового госпиталя на шестые сутки после начала заболевания, где диагностирована левосторонняя полисегментарная пневмония. На фоне проводимой антибактериальной терапии цефтриаксоном и азитромицином получен незначительный клинический эффект. Сохранялись лихорадка до 38–39°C, озноб, выраженная слабость, боли в грудной клетке, малопродуктивный кашель. При контрольной рентгенографии органов грудной клетки на седьмые сутки от начала антибактериальной терапии отмечено прогрессирование очагово-инфильтративных изменений в легких с двух сторон, выявлен абсцесс нижней доли левого легкого. Для дальнейшего обследования и определения лечебной тактики переведен в торакальное отделение госпиталя имени Н. Н. Бурденко. При поступлении: состояние средней степени тяжести. Правильного телосложения, повышенного питания. Рост 172 см, масса тела 76 кг. Кожные покровы и видимые слизистые физиологической окраски; кожа лица— гиперемирована, умеренный акроцианоз, сосудистые звездочки на лице и груди. Периферические лимфатические узлы не увеличены. Костно-мышечная система без особенностей. Грудная клетка правильной формы, эластична. Левая половина грудной клетки отстает в акте дыхания. Перкуторно над легкими коробочный звук с резким притуплением над задненижними участками левого легкого. Аускультативно дыхание жесткое, справа над базальными отделами выслушиваются звучные мелкопузырчатые хрипы, слева над зоной притупления резкое ослабление дыхания. Частота дыхательных движений 24–26 в минуту. Пульс 100 ударов в минуту, ритмичный, удовлетворительных качеств. Сердечная область не изменена, границы относительной тупости не расширены. Тоны сердца приглушены, артериальное давление– 140/80 мм рт. ст. Учащенное мочеиспускание— до 3–4 раз ночью. В клиническом анализе крови наблюдается палочкоядерный сдвиг в сторону юных форм до 24%, лимфоцитопения, ускоренное СОЭ 55 мм/ч. При компьютерной томографии органов грудной клетки (КТ ОГК) определяются: полисегментарная инфильтрация паренхимы обоих легких, в проекции 6, 9 и 10 сегментов левого легкого жидкостное ограниченное образование 107×94 мм в поперечнике с уровнем жидкости и газа; сдавление нижнедолевого бронха слева; увеличение внутригрудных лимфатических узлов.
Установлен клинический диагноз: двусторонняя внебольничная полисегментарная пневмония (тяжелое течение), осложненная абсцессом нижней доли левого легкого, дыхательной недостаточностью второй степени. В отделении под контролем УЗИ произведено дренирование полости абсцесса с эвакуацией зловонного жидкого гноя до 500 мл и налажено проточно-аспирационное дренирование полости абсцесса. Проводилась комбинированная антибактериальная терапия Тиенамом (2 г/сут), Амикацином (1 г/сут), Метрогилом (300 мг/сут).
В результате проводимой терапии отмечена положительная клинико-рентгенологическая и лабораторная динамика. Улучшилось самочувствие больного, исчезли боли в грудной клетке, уменьшились кашель и общая слабость, на 8 сутки отмечено снижение температуры тела до субфебрильных цифр. При контрольной КТ ОГК на 5 сутки от момента начала активной терапии отмечено уменьшение полости абсцесса до 13×11 мм и интенсивности инфильтрации легочной ткани, выявлены инфильтраты с распадом в 10 сегменте левого легкого. К концу второй недели от начала лечения в госпитале температура тела нормализовалась, лабораторные показатели в пределах нормальных величин, при контрольной рентгенографии ОГК инфильтративных и очаговых изменений легочной ткани, остаточных полостей не выявлено. Пациент выписан из стационара в удовлетворительном состоянии на 51 сутки от начала заболевания и на 36 сутки нахождения в ГВКГ им. Н. Н. Бурденко.
В заключение необходимо отметить, что в диагностике и лечении заболевания у данного пациента присутствуют два важных момента. Во-первых, это поздняя диагностика внебольничной пневмонии на поликлиническом этапе, осложнившаяся формированием абсцесса легкого. Во-вторых, пациенту проводилась комбинированная антибактериальная терапия абсцесса— Тиенам + Амикацин + Метрогил, которая с точки зрения современных рекомендаций представляется избыточной.
А. А. Зайцев, кандидат медицинских наук
М. Б. Миронов, кандидат медицинских наук
А. И. Синопальников, доктор медицинских наук, профессор
Бронхиальный свищ
Бронхиальный свищ – это патология бронхиального дерева, характеризующаяся наличием патологического сообщения бронха с внешней средой, полостью плевры или просветом внутренних органов. Клиническая картина определяется взаимоотношениями бронха с другими анатомическими структурами. Общими признаками являются одышка, цианоз, кашель с выделением содержимого дренируемых органов (гноя, пищевых масс, примеси желчи и пр.). Диагноз бронхиального свища подтверждается данными рентгенодиагностики (рентгенографии легких, фистулографии, бронхографии, КТ), эндоскопии (бронхоскопии, ЭГДС), плевральной пункции с манометрией. Тактика в отношении бронхиальных свищей может быть консервативной или хирургической.
МКБ-10
Общие сведения
Бронхиальный свищ – фистула, обусловливающая аномальное сообщение бронха с какой-либо полостью, органом или поверхностью кожи. Бронхиальные свищи являются одной из наиболее сложных проблем пульмонологии и торакальной хирургии, поскольку трудно поддаются консервативному лечению, поддерживают хронические гнойные процессы, существенно отягощают послеоперационный прогноз. Частота формирования бронхиальных свищей тесно связана с их этиологией. Так, врожденные пищеводно-трахеальные и пищеводно-бронхиальные сообщения встречаются у 0,03% новорождённых. В структуре приобретенных бронхиальных свищей преобладают послеоперационные дефекты – на их долю приходится 2-30% осложнений резекции легкого.
Причины
Формирование врожденных бронхиальных свищей происходит внутриутробно. Возникновение бронхопищеводных и трахеопищеводных свищей обусловлено неполным разделением дыхательной и пищеварительной систем на определенном этапе эмбриогенеза под влиянием различных факторов, воздействующих на плод (авитаминоза, внутриутробных инфекций, травм, радиации и пр.). В большинстве случаев при таком пороке развития имеется свищевой ход между главным бронхом (обычно правым) и пищеводом. Этиология приобретенных бронхиальных свищей может быть различной:
Патогенез
Вначале бронхиальный свищ представляет собой патологическое сообщение, стенки которого выстланы некротическими массами. По мере отторжения нежизнеспособных тканей формируется канал, покрытый грануляционной или эпителиальной тканью. Этот канал может соединять бронх с грудной стенкой, плевральной полостью, близлежащими органами, обусловливая специфическую клиническую картину. Со временем стенки свищевого хода становятся ригидными, препятствуя самостоятельному закрытию дефекта. Любой инфекционный процесс в бронхиальном дереве, полости плевры, легочной ткани поддерживает течение бронхиального свища.
Классификация
Кроме деления на врожденные и приобретенные, бронхиальные свищи подразделяются на единичные (62%) и множественные (38%, в т. ч. «решетчатое легкое»). С учетом этиологического фактора они могут иметь посттравматическое, постинфекционное, послеоперационное происхождение. В зависимости от уровня локализации различают свищи главных, долевых, сегментарных, субсегментарных бронхов и альвеолярные фистулы. В клинической практике наибольшую ценность представляет анатомическая классификация, в рамках которой выделяют:
Наружные (торакобронхиальные) свищи
Внутренние свищи
Симптомы бронхиальных свищей
Критериями, определяющими симптоматику бронхиальных свищей, выступают их анатомические особенности, диаметр, сроки образования дефекта, наличие или отсутствие инфекционного процесса. К числу общих симптомов, сопровождающих развитие патологии, относятся признаки интоксикации (лихорадка с ознобами, слабость, разбитость, головная боль, плохой аппетит) и дыхательной недостаточности (цианоз, одышка, боли в грудной клетке). Кроме этого, для различных видов бронхиальных свищей характерны свои специфические проявления.
Наружные (бронхокожные, бронхоплеврокожные) свищи характеризуются наличием видимого дефекта на коже грудной стенки, из которого периодически отходит слизистое или слизисто-гнойное отделяемое, а при кашле и натуживании может выделяться воздух. Попадание в свищевой ход воды провоцирует возникновение резкого приступообразного кашля и приступа удушья. Иногда снятие окклюзионной повязки вызывает усиление кашля, одышки и цианоза, нарушение голоса вплоть до афонии.
Бронхиальные свищи, сообщающиеся с «сухой» плевральной полостью, проявляются сухим кашлем или откашливанием незначительного количества слизистой мокроты. При бронхоплевральных свищах, развившихся на фоне гнойного плеврита, общее состояние больных отягощается гнойно-резорбтивной лихорадкой, интоксикацией, истощением. Отмечается отхождение большого объема гнойной, зловонной мокроты при кашле, выраженная одышка, выделение воздуха из плеврального дренажа, подкожная эмфизема. Клинику бронхолегочных свищей определяют субфебрилитет, кашель с выделением слизисто-гнойной мокроты, потливость, слабость.
Основным признаком бронхоорганных свищей служит откашливание больным содержимого того органа, с которым сообщается бронх: съеденной пищи, желчи, желудочного или кишечного содержимого. Врожденные трахео- и бронхопищеводные свищи могут быть заподозрены вскоре после рождения ребенка на основании поперхивания при кормлении, вздутия желудка, развития аспирационной пневмонии. Основным проявлением приобретенных свищей служит кашель, связанный с приемом жидкости и пищи, иногда – удушье.
Осложнения
Длительное течение бронхиальных свищей может привести к возникновению пневмонии и хронической эмпиемы плевры. Возможны осложнения в виде кровохарканья или легочного кровотечения, аспирационной пневмонии другого легкого. Системные последствия представлены сепсисом, массивным внутренним кровотечением, висцеральным амилоидозом.
Диагностика
При осмотре пациента с предполагаемым диагнозом «бронхиальный свищ» обращает внимание цианоз кожи и слизистых, одышка, тахикардия, характерная деформация концевых фаланг пальцев («барабанные палочки», «часовые стекла»). Аускультация выявляет рассеянные разнокалиберные хрипы.
Бронхокожные свищи, открывающиеся на поверхности грудной стенки, обнаруживаются визуально. С диагностической целью может быть проведено зондирование свища с введением водного раствора метиленового синего. Возникновение кашля с выделением окрашенной мокроты подтверждает наличие бронхиального свища. Для получения информации о протяженности и конфигурации свищевого хода производится фистулография с контрастными веществами. В ряде случаев уточнить локализацию, количество, размеры свищевых ходов позволяет диагностическая торакоскопия, выполняемая через свищевое отверстие в грудной стенке.
При внутренних свищах важное диагностическое значение имеет бронхоскопия, позволяющая оценить состояние бронхиального дерева, а также рентгенологические методы диагностики: обзорная рентгенография и КТ легких, бронхография. Бронхоплевральные свищи могут быть выявлены с помощью данных плевральной пункции с манометрией – при сообщении бронхиального дерева с полостью плевры в последней не удается создать отрицательное давление путем аспирации воздуха. В случае подозрения на наличие бронхопищеводного или бронхожелудочного свища показана эзофагогастроскопия.
Лечение бронхиальных свищей
В большинстве случаев бронхиальные свищи требуют оперативного лечения. Вместе с тем, в отношении некоторых фистул бронхов может быть применена консервативная тактика. Лечением данной патологии должны заниматься торакальные хирурги, владеющие всем арсеналом методов ведения больных с бронхиальными свищами. Консервативное лечение бронхиальных свищей предполагает проведение мероприятий по санации гнойных полостей: дренирование плевральной полости, промывание антисептическими растворами, введение протеолитических ферментов и антибиотиков, удаление инородных тел, наложение аппарата активной аспирации и т. п. После облитерации остаточных полостей возможно самострельное закрытие небольших бронхиальных свищей.
Имеется положительный опыт ликвидации свищей с помощью химического прижигания или электрокоагуляции фистулы, позволяющих разрушить эпителиальную выстилку и стимулировать рост соединительной ткани в канале. При крупных фистулах может применяться временное эндоскопическое закрытие свищнесущего бронха специальной поролоновой пломбой – такая тактика позволяет осуществить лаваж гнойной полости и создать благоприятные условия для оперативной ликвидации бронхиального свища.
Консервативное лечение бронхиальных свищей оказывается успешным лишь в 10-12% случаев, поэтому большинству пациентов показано оперативное закрытие дефекта. Для оперативного устранения торакобронхиального свища может выполняться его иссечение с последующим ушиванием, мышечная пластика лоскутом на ножке. При послеоперационных свищах показано выполнение реампутации культи бронха. Устранение пищеводно-бронхиальных свищей требует ушивания дефектов со стороны пищевода и бронха, возможно – резекции измененной части легкого. Закрытие бронхоплеврального свища может производиться с помощью интраплевральной торакопластики или декортикации легкого.
Прогноз и профилактика
Исход и перспективы выздоровления зависят от причины, приведшей к формированию бронхиального свища, полноты, адекватности и своевременности лечебных мероприятий. Наиболее серьезный прогноз и высокая летальность (30-70%) отмечается при послеоперационных свищах, осложненных эмпиемой плевры. При возникновении бронхиального свища выжидательная тактика недопустима; необходимо как можно более раннее начало консервативных мероприятий, проведение хирургического вмешательства после необходимой подготовки. Профилактика приобретенных бронхиальных свищей заключается в соблюдении техники обработки культи бронха, своевременной терапии гнойно-деструктивных заболеваний легких, предупреждении травм грудной клетки.