Чем лечить энтеробактерии в горле
Секстафаг пиобактериофаг поливалентный : инструкция по применению
Описание
Бактериофаг представляет собой прозрачную жидкость желтого цвета различной интенсивности, возможен зеленоватый оттенок.
Пиобактериофаг поливалентный обладает способностью специфически лизировать бактерии стафилококков, стрептококков (в том числе энтерококков), протея, клебсиелл пневмонии, синегнойной и кишечной палочек.
Состав
В 1 мл препарата содержится:
Фармакотерапевтическая группа
Прочие терапевтические средства.
Классификация по ICTV: Caudovirales.
Фармакологические свойства
Фармакодинамика. Активность бактериофага при наличии фагочувствительности бактериального штамма проявляется в виде проникновения, внутриклеточного размножения, разрушения бактериальной клетки и выхода фаговых частиц, готовых к заражению новых бактериальных клеток.
После перорального однократного приема бактериофага, фаговые частицы обнаруживаются через 1 час в образцах крови, через 1-1,5 часа на поверхности ожоговых ран и в бронхиальном содержимом, через 2 часа в ликворе и моче. В каловых массах выявлялось фаговых частиц в 3 раза больше, чем в моче.
По данным литературы, клиническая эффективность фаготерапии сопоставима с результатами лечения у пациентов, получающих антибиотикотерапию.
Фармакокинетика. Исследования по фармакокинетике, проведенные на лабораторных животных доказали, что бактериофаг, введенный любым способом, поступает в общий ток крови, но обычно в крови не задерживается, а адсорбируется различными тканями, оседая в первую очередь в лимфатических узлах, в печени и селезенке. Выведение из организма происходит через кишечник и почки.
По литературным данным длительность пребывания бактериофагов и уровень выхода фагов зависят от присутствия гомологичного фагочувствительного штамма-возбудителя инфекции в организме. При отсутствии гомологичного возбудителя через 2 часа после однократного приема наблюдается массивное выделение фагов с мочой, снижающееся до единичных к концу первых суток. Однако низкий уровень выхода фагов может поддерживаться до 6 суток. Высокое содержание фаговых частиц в образцах и длительное его выделение свидетельствует о происходящем в организме процессе размножения бактериофагов в очаге инфекции.
У урологических больных наблюдается тенденция нарастания титра фаговых частиц в крови, достигающая массивного присутствия к 8-10 часам после приема препарата. Длительность обнаружения фага варьирует от 2 до 6-7 суток. У всех больных снижение количества бактериофага сопутствовало снижению уровня бактериурии.
Гематоэнцефалический барьер у здорового животного является барьером для проникновения фагов в центральную нервную систему. Нарушение центрального барьера даже в слабой степени влечет за собой поступление бактериофага из кровяного русла в ликвор.
Показания к применению
Лечение и профилактика гнойно-воспалительных и энтеральных заболеваний, вызванных стафилококками, стрептококками, протеями, клебсиеллами, синегнойной и кишечной палочками:
— посттравматические конъюктивиты, кератоконъюктивиты, гнойные язвы роговицы и иридоциклиты;
— генерализованные септические заболевания;
— другие заболевания, вызванные бактериями стафилококков, стрептококков (в том числе энтерококков), протея, клебсиелл пневмонии, синегнойной и кишечной палочек.
При тяжелых проявлениях инфекций, вызванных стафилококками, стрептококками, протеем, клебсиеллой пневмонии, синегнойной и кишечной палочками, препарат назначается в составе комплексной терапии.
С профилактической целью препарат используют для обработки операционных и свежеинфицированных ран, а также для профилактики внутрибольничных инфекций по эпидемическим показаниям.
Важным условием эффективной фаготерапии является предварительное определение фагочувствительности возбудителя.
Способ применения и дозировка
Перед использованием флакон с бактериофагом необходимо взболтать и просмотреть. Препарат должен быть прозрачным и не содержать осадка.
Лечение гнойно-воспалительных заболеваний с локализованными поражениями должно проводиться одновременно как местно, так и приемом препарата внутрь в течение 7-20 дней (по клиническим показаниям).
В зависимости от характера очага инфекции бактериофаг применяют:
1. Местно в виде орошения, примочек и тампонирования жидким фагом в количестве до 200 мл в зависимости от размеров пораженного участка. При абсцессах бактериофаг вводят в полость очага после удаления гноя с помощью пункции. Количество вводимого препарата должно быть несколько меньше объема удаленного гноя. При остеомиелите после соответствующей хирургической обработки в рану вливают бактериофаг по 10-20 мл.
3. При циститах, пиелонефритах, уретритах препарат принимают внутрь. В случае, если полость мочевого пузыря или почечной лоханки дренированы, бактериофаг вводят через цистостому или нефростому 1-2 раза в день по 20-50 мл в мочевой пузырь и по 5-7 мл в почечную лоханку.
4. При гнойно-воспалительных гинекологических заболеваниях препарат вводят в полость вагины, матки в дозе 5-10 мл ежедневно однократно.
5. При гнойно-воспалительных заболеваниях уха, горла, носа препарат вводят в дозе 2-10 мл 1-3 раза в день. Бактериофаг используют для полоскания, промывания, закапывания, введения смоченных турунд (оставляя их на 1 час).
7. При лечении стоматитов и хронических генерализованных пародонтитов препарат используют в виде полосканий полости рта 3-4 раза в день в дозе 10-20 мл, а также введением в пародонтальные карманы турунд, пропитанных пиобактериофагом, на 5-10 минут.
8. При кишечных формах заболевания, заболеваниях внутренних органов, дисбактериозе бактериофаг применяют через рот и в виде клизм в течение 7-20 дней. Через рот бактериофаг дают 3 раза в сутки натощак за 1 час до еды. В виде клизм назначают 1 раз в день вместо одного приема через рот.
Рекомендуемые дозировки препарата
| Возраст пациента | Доза на 1 прием (мл) | |
| Внутрь | В клизме | |
| 0-6 мес. | 5 | 10 |
| 6-12 мес. | 10 | 20 |
| От 1 года до 3 лет | 15 | 20-30 |
| От 3- до 8 лет | 20 | 30-40 |
| От 8 лет и старше | 20-30 | 40-50 |
В случае, если до применения бактериофага для лечения ран применялись химические антисептики, рана должна быть тщательно промыта стерильным 0,9% раствором натрия хлорида.
Применение бактериофага у детей (до 6 месяцев). При сепсисе, энтероколите новорожденных, включая недоношенных детей, бактериофаг применяют в виде высоких клизм (через газоотводную трубку или катетер) 2-3 раза в сутки (см. табл.). При отсутствии рвоты и срыгивания возможно применение препарата через рот. В этом случае он смешивается с грудным молоком. Возможно сочетание ректального (в клизмах) и перорального (через рот) применения препарата. Курс лечения 5-15 дней. При рецидивирующем течении заболевания возможно проведение повторных курсов лечения. С целью профилактики сепсиса и энтероколита при внутриутробном инфицировании или опасности возникновения внутрибольничной инфекции у новорожденных детей бактериофаг применяют в виде клизм 2 раза в день в течение 5-7 дней.
При лечении омфалитов, пиодермий, инфицированных ран препарат применяют в виде аппликаций ежедневно двукратно (марлевую салфетку смачивают бактериофагом и накладывают на пупочную ранку или на пораженный участок кожи).
Семейство Enterobacteriaceae. Часть 1
Автор: врач – клинический фармаколог Трубачева Е.С.
.jpg)
Автор: врач – клинический фармаколог Трубачева Е.С.
Morganella spp. и Proteus spp.
Особо выдающихся представителей семейства Enterobacteriaceae мы уже разбирали в отдельных статьях, а именно представительницу рода Esherichia — кишечную палочку E.coli, а также одну из представительниц клебсиелл — Klebsiella pneumonia. В ближайших статьях мы постараемся осветить все оставшееся семейство, как, во-первых, одно из самых проблемных в плане развития резистентности к антимикробным препаратам, а во-вторых — как возбудителей, наиболее часто являющихся причиной внутрибольничных инфекций.
Микробиологические аспекты
Основными клинически значимыми представителями родов семейства Enterobacteriaceae, вызывающими заболевания у человека, являются:
Естественно совсем уж экзотику мы рассматривать не станем, но по наиболее часто встречающимся представителям обязательно пробежимся.
Клинические аспекты
Почему данное семейство так актуально? Наверное, потому, что почти ни одна нозология не обходится без его представителей. В самом широком смысле семейство Enterobacteriaceae является причиной следующих заболеваний:
Как мы видим, наши знакомые отметились практически везде. Но надо обязательно помнить, что выявление вышеуказанных представителей у здоровых людей из респираторного тракта, урогенитального и уж тем более желудочно-кишечного ни в коем случае не говорит о том, что человек чем-то болен, так как в большинстве своем эти микробы являются представителями нормальной микрофлоры, а не все люди умеют мыть руки, особенно летом.
Когда можно думать о наличии бактериальной патологии? Во-первых, когда имеется четкая клиника, во-вторых, когда микробы выделены из стерильных в норме сред, таких как кровь и ликвор, брюшная или плевральная полость, точнее, экссудат оттуда и, в-третьих, когда микроорганизмы выделены в клинически значимых концентрациях (тут в помощь будет ваша бак. лаборатория).
Стоит отметить еще один немаловажный момент — не все представители семейства Enterobacteriaceae умеют жить вне организма человека, и поэтому не размножаются во внешней среде, а потому обнаружение оных на пищевых продуктах и всевозможных поверхностях в лечебных учреждениях говорит о фекальном загрязнении, проще говоря, о неумении обрабатывать руки после посещения туалетной комнаты. Одним из таких микробов-детекторов является кишечная палочка, и стоит ее поймать даже не на руках персонала, а, например, на компьютерной мышке, как дальше можно уже ничего не искать, а начинать очередной этап избиения младенцев, пардон, обучения правилам асептики и антисептики, в частности, обработки рук.
Но давайте перейдем к частностям — и первым микроорганизмом, который будем сегодня рассматривать, станет:
Morganella spp.
Зверюшка названа так в честь своего первооткрывателя Гарри Р. Моргана.
Начнем традиционно с микробиологических аспектов
Семейство морганелл включает единственный вид M. morganii, включающий два подвида M. morganii и M. sibonii, которые различаются только ферментацией трегалозы.
Морганеллы являются представителями нормальной микрофлоры как человека, так и животных, а потому могут присутствовать в качестве сапрофитов в окружающей (внебольничной!) среде.
Морганеллы имеют довольно сложные отношения с антибактериальными препаратами и обладают природной резистентностью к:
Проявляют высокую чувствительность к:
Клинические аспекты
Как говорилось выше, морганеллы являются частью нормальной микрофлоры человека, крайне редко вызывая инфекционные заболевания. Чаще всего они являются возбудителями осложненных инфекций мочевыводящих путей.
Факторами риска развития инфекции являются:
В качестве механизмов резистентности морганеллы способны продуцировать бета-лактамазы, чем и объясняется их природная устойчивость к пенициллинам и цефалоспоринам 1-2 поколений. При нерациональном использовании антибиотиков они начинают вырабатывать бета-лактамазы расширенного спектра и факторы устойчивости к фторхинолонам, которыми довольно бодро делятся с соседями по семейству Enterobacteriaceae. Отдельно стоит отметить способность отдельных штаммов морганелл к резистентности к имипенему.
Какие заболевания вызывают чаще всего:
Терапевтические аспекты
Антибактериальная терапия будет полностью зависеть от результата из микробиологической лаборатории. Повторимся еще раз, микроб изначально умеет вырабатывать бета-лактамазы, а потому в случае развития осложненных инфекции мочевыводящих путей, которые чаще всего уже не связанны с кишечной палочкой, препаратами выбора становятся карбопенемы (имипенем, если штамм к нему чувствителен, или меропенем), дозирование которых проводится с учетом клиренса креатинина. Длительность лечения должна быть не менее 7 дней. В качестве альтернативы можно использовать цефалоспорин 4-го поколения Цефипим каждые 8 часов или фторхинолоны.
Аминогликозиды, несмотря на чувствительность к оным, при лечении заболеваний мочевыводящих путей лучше не применять в виду их нефро- и отоксичности, и по этой же причине их невозможно будет использовать около трех месяцев после проведенной терапии, например, в лечении синегнойной инфекции. Цефалоспорины третьего поколения тоже применять не стоит, так как морганеллы довольно быстро обзаводятся бета-лактамазами расширенного спектра, которые, как мы помним, эту генерацию препаратов быстро инактивируют.
Proteus spp.
Микробиологические аспекты
Протей долгое время был практически родным отцом морганеллы, так как последняя рассматривалась как один из видов рода протей. Этот род примечателен тем, что занимает почетное второе место по выявляемости после кишечной палочки в семействе Enterobacteriaceae.
В данный момент представителями рода протей являются P. mirabilis, вызывающий порядка 90% инфекционных заболеваний, а также P. vulgaris и P. penneri.
Клинические аспекты
Протеи выступают возбудителями порядка 10% неосложненных инфекций мочевыводящих путей, с чем могут быть связаны неудачи в лечении последних с использованием аминопенициллинов.
Как и все клинически значимые возбудители семейства Enterobacteriaceae, протей является возбудителем нозокомиальных инфекций, таких как пневмония, вплоть до сепсиса. Кроме того выступает возбудителем интраабдоминальных, а также хирургических инфекций кожи и мягких тканей, сепсиса, связанного с медицинскими вмешательствами как последствий нозокомиальной пневмонии в результате недостаточной дезинфекции, например, бронхоскопов.
Таким образом, мы видим, что, как и в предыдущем случае, проще правильно помыть руки и обработать инструменты, чем лечить это все с учетом природной и приобретенной резистентности.
Терапевтические аспекты
Как и в случае с морганеллой, нам просто необходим результат микробиологического исследования с определением чувствительности по МПК возбудителя либо результаты микробиологического мониторинга, которые помогут предположить зверей в случае неудачи ранее проводимого лечения.
В случае ампициллин-чувствительного P.mirabilis именно ампициллин может выступать препаратом первой линии. Кроме того, возможно использование цефуроксима и фторхинолонов. Обязательным аспектом лечения является его длительность. В случае неосложненных инфекций мочевыводящих путей (цистита) — не менее 3 дней, пиелонефрита — 10–14 дней, осложненных инфекций — 10–21 день. Сепсис является состоянием, требующим индивидуального подхода, но лечим не менее 14 дней.
На этом на сегодня мы закончим, но повторим одну базовую и, чего уж, наиважнейшую истину: в лечении инфекций, связанных с любым представителем семейства Enterobacteriaceae, самым главным будет являться профилактика. А именно правильное и тщательное мытье рук. Обеспечим мытье рук, не будет большинства проблем с инфекциями, вызванными указанным семейством.
Современные подходы к коррекции микробиоценоза ротоглотки
В структуре инфекционной заболеваемости детей ведущее место занимают респираторные инфекции [1–3]. Известно, что всеобщей закономерностью является повышенная восприимчивость к ним детей раннего и дошкольного возраста [6–8].
В структуре инфекционной заболеваемости детей ведущее место занимают респираторные инфекции [1–3]. Известно, что всеобщей закономерностью является повышенная восприимчивость к ним детей раннего и дошкольного возраста [6–8]. Именно среди детей указанной возрастной группы формируется особо выделяемая категория (15–30%) часто болеющих детей (ЧБД), вопросы лечения и оздоровления которых до сих пор остаются нерешенными и являются трудной задачей для педиатров [5–7]. У 67% ЧБД преимущественно рецидивирующей патологией становятся заболевания ЛОР-органов [9]. Характер воспалительного процесса в ротоглотке во многом зависит от реактивности иммунной системы, факторов местной защиты, в том числе микробиоценоза слизистой ротоглотки. Течение инфекционного процесса в ротоглотке могут обусловить различные микроорганизмы, в том числе и условно-патогенные [4, 6, 8, 10]. Вместе с тем состояние микробиоты ротоглотки изучено еще недостаточно. Отсутствуют однозначные представления о нормобиозе и значимости выделения различных видов микробов.
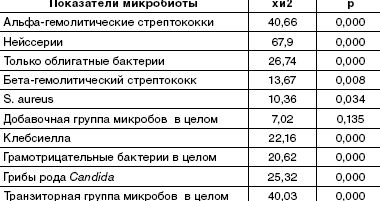
Сравнительный анализ полученных результатов обнаружил достоверные различия в состоянии микроэкологии задней стенки глотки в группах здоровых детей и пациентов с респираторной патологией (табл. 2).
У подавляющего числа здоровых детей (99%) на задней стенке глотки был зарегистрирован рост альфа-гемолитического стрептококка в ассоциации с нейссериями. Причем у половины из них другие виды микробов не обнаруживались.
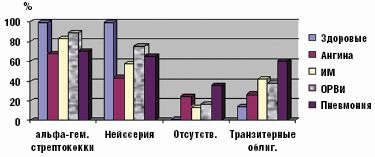
При гнойном или катаральном воспалительном процессе в ротоглотке обнаружено угнетение облигатной ассоциации альфа-гемолитического стрептококка и нейссерий, образующих защитную биопленку. Дисбиоз локуса развивался в 75–100% случаев. Он имел определенные особенности в зависимости от характера инфекционного процесса. Наиболее выраженное угнетение пролиферации облигатных бактерий было обусловлено местным гнойно-воспалительным процессом при ангине и системным поражением при пневмонии (рис. 1).
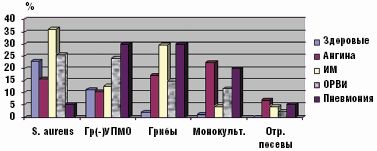
Именно при данной патологии чаще всего отсутствовали облигатные микробы, выделялись монокультуры или ассоциации микроорганизмов, состоящие только из добавочных и/или транзиторных представителей с высокой вероятностью их этиологической значимости, обнаруживались отрицательные посевы (рис. 2). Наиболее устойчивым компонентом облигатной ассоциации был стрептококк, отсутствие нейссерий либо снижение их количества наблюдалось значительно чаще.
Инициация инфекционного процесса респираторными вирусами способствовала преимущественной пролиферации грамотрицательных бактерий (особенно клебсиеллы) в больших количествах (более 104 КОЕ/мл), а также их ассоциаций (р = 0,000, рис. 2). Синегнойная палочка выделялась только у ЧДБ либо больных пневмонией. Лечение в стационаре способствовало нарастанию частоты обнаружения грамотрицательных микробов в 2–3 раза вне зависимости от этиологии инфекционного процесса. Обнаружение грамотрицательных бактерий у здоровых детей являлось следствием перенесенной ОРВИ (20% против 0, р
Л. В. Феклисова, доктор медицинских наук, профессор
Е. Р. Мескина, кандидат медицинских наук
Л. А. Галкина, кандидат медицинских наук
Е. Е. Целипанова, кандидат медицинских наук
Н. А. Савицкая, кандидат медицинских наук
С. П. Казакова, кандидат медицинских наук
Е. А. Воропаева, кандидат медицинских наук
ГУ МОНИКИ им. М. Ф. Владимирского, Москва
Рецидивирующая инфекция в горле и носу
Период лечения: 3 года назад
Лечение: После мазка из горла у лора и нашли золотистый стафилококк, провели курс тонзиллора.
Результат: Сразу после лечения небольшое улучшение. Спустя месяц-другой проблема горла вернулась.
Период лечения: последние 2 года 6 мес
Лечение: наблюдалась у гомеопата, сдавала до и после лечения посевы из зева и носа.
Результат: После лечения (гомеопатическими препаратами) посевы были чистыми и симптомы больного горла пропадали, но спустя пару месяцев снова появлялась инфекция.
Жалобы: Все это время (кроме летнего сезона) почти каждый день приходится полоскать горло ромашкой/шалфеем/хлоргексидином/мирамистином. Без этого появляются неприятные ощущения, которые без лечения перетекают в простуду. Последние года полтора появился небольшой насморк, который также не проходит (беловатые выделения в небольшом объеме и в основном по утрам и после улицы в холодное время года, а также корочки в течение дня).
В сентябре насморк после простуд перерос в гайморит, сделали 5 синусов и физио. Насморк и выделения прошли полностью, но спустя месяц после окончания лечения снова появился. Горло продолжает беспокоить.
Во время лечения у гомеопата обнаружили похожий состав микробов у мужа в горле, лечился со мной гомеопатией, но после окончания лечения посевы не сдавал. Горло и насморк его не беспокоит. Необходимо ли ему лечиться если его ничего не беспокоит? (Он лечиться устал и не хочет)
Свежие анализы в конце письма. Есть предположение, что лаборант при заборе перепутал этикетки нос/горло у мужа, потому что наши анализы противоположны.
Какие есть варианты лечения, только тонзилллор? Эффективно только лечение антибиотиками или есть другие варианты, бактериофаги или что-то еще? Суммы, оставляемые у лора уже порядком напрягают. Посевы сдавала в инвитро, лор из поликлиники направление не дает и лечит ромашкой.
У меня
Нос: Staphylococcus epidermidis 10^5 КОЕ/мл,
Enterobacter aerogenes 10^4 КОЕ/мл»
Горло:
Klebsiella pneumoniae 10^5 КОЕ/мл
Neisseriae sp. 10^8 КОЕ/мл
Streptococcus pneumoniae 10^5 КОЕ/мл
Candida albicans 10^3 КОЕ/мл
У мужа:
Нос: Staphylococcus aureus 10^5 КОЕ/мл
Neisseriae sp. 10^5 КОЕ/млStreptococcus pyogenes 10^5 КОЕ/мл
Candida albicans 10^4 КОЕ/мл
Горло: Staphylococcus epidermidis 10^5 КОЕ/мл
На сервисе СпросиВрача доступна бесплатная консультация лора онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно. Задайте свой вопрос и получите ответ сразу же!
Энтеровирусная инфекция у детей
Содержание
Энтеровирусная инфекция — это группа вирусных заболеваний, поражающих различные системы организма (как правило, кожу, пищеварительный тракт и органы дыхания). После перенесенной болезни формируется устойчивый иммунитет (до нескольких лет), но только к конкретному вирусу, вызвавшему заболевание.
Поэтому болеть ребенок может несколько раз. Из-за этого, к тому же, нет вакцины от этой болезни. У детей на грудном вскармливании есть иммунитет от матери. Но он не стойкий и быстро проходит после прекращения кормления грудью. Чаще всего энтеровирусной инфекцией болеют дети от 3 до 10 лет и подростки. Чем меньше возраст, тем большую опасность представляет собой болезнь.
Энтеровирусную инфекцию вызывают вирусы групп ЕСНО (Эховирусы) и Коксаки. Для них характерно разнообразие симптоматики – от конъюнктивита до диареи. Источник инфекции – другой человек. Она передается фекально-оральным и воздушно-капельным путем. В регионах с умеренным климатом наблюдается сезонность заболевания – чаще болеют в начале осени и конце лета. Энтеровирусы долго живут в воде: 18 дней – в водопроводной, 33 – в речной, 65 – в очищенных стоках. Источник:
Г.П. Мартынова
Энтеровирусная (неполио) инфекция у детей //
Сибирское медицинское обозрение, 2014, №3
Виды энтеровирусов
Существует более 100 возбудителей такой инфекции. Основные – это ЕСНО, полиовирусы (возбудители полиомиелита), вирусы Коксаки А и В, энтеровирусы, не поддающиеся классификации.
Вирусы Коксаки – это несколько серотипов возбудителя, относящихся к группам А, В и С. Вирусы Коксаки типа А – причина тяжелых форм энтеровирусных заболеваний. Это геморрагический конъюнктивит, герпетическая ангина, асептический менингит. Тип В опаснее, потому что провоцирует гепатит, миокардит, перикардит. Источник:
В.В. Ботвиньева, Л.С. Намазова-Баранова, О.Б. Гордеева, О.К. Ботвиньев, Т.Н. Коноплева
Современные возможности диагностики, профилактики и лечения энтеровирусной инфекции Коксаки у детей
// Педиатрическая фармакология, статья поступила: 22.01.2012 г., принята к печати: 12.05.2012 г.
Вирусы ЕСНО наиболее опасны для новорожденных. У них они вызывают менингит, миокардит, гепатит. Это часто становится причиной смерти. У детей постарше осложнений не бывает.
Причины
Группа энтеровирусов очень разнообразна. Они распространены повсеместно: в воде и земле, продуктах питания и организмах людей и животных, в фекалиях (сохраняют жизнеспособность до 6 месяцев). Они устойчивы к факторам внешней среды и химическому воздействию ряда средств, но погибают при температуре выше 50 градусов, высушивании, воздействии формальдегида и хлора. Вспышки заболевания характерны для тёплого времени года.
Основные пути заражения:
Симптомы
В зависимости от типа вируса, наблюдается различная симптоматика энтеровирусной инфекции у ребёнка. Некоторые из них протекают сравнительно легко, другие способны спровоцировать серьёзные осложнения. Для болезни характерен инкубационный период до 10 дней. Большая часть признаков энтеровирусной инфекции схожа с проявлением простудных заболеваний:
В зависимости от типа вируса возможны:
Можно выделить ряд симптомов, которые появляются при осложнении энтеровирусной инфекции:
Методы диагностики
Диагноз в большинстве случаев можно поставить по характерным симптомам, физикальному обследованию и истории болезни.
После осмотра и сбора жалоб, педиатр назначит ряд анализов, направленных на выявление типа вируса. Врач может назначить:
Для точной постановки диагноза также может потребоваться метод дифференциальной диагностики для исключения других заболеваний со схожей клинической картиной.
Выполняются и другие диагностические тесты:
Методы лечения энтеровирусной инфекции
Медикаментозная терапия – это:
Для снятия симптоматики ребенку могут быть назначены препараты разных групп:
Обезболивающие и жаропонижающие, чтобы снять головную и мышечную боль, лихорадку. Это «Ибупрофен», «Парацетамол», «Ибуклин», «Нурофен детский» и др.
Иммуноглобулины стимулируют иммунитет ребенка. Их вводят инъекционно – внутримышечно или внутривенно. Второй вариант более эффективен и распространен.
Важно! Противовирусные препараты не показали высокой эффективности на поздних стадиях и не включены в официальный план лечения. Они помогают на очень ранней стадии, когда с момента заражения прошло 5-10 часов. Но выявить болезнь на этом этапе почти невозможно.
Хорошо поддерживают организм ребенка в этот непростой период – витамины (особенно витамин D) и добавки, содержащие незаменимые микроэлементы (магний, цинк, калий, селен, кальций), помогающие бороться с вирусом.
Важно! Антибиотики против энтеровирусной инфекции не работают, так как это антибактериальные, а не противовирусные препараты.
Ребенку должен быть обеспечен постельный режим, обильное питьё с использованием растворов для восстановления водно-электролитного баланса, специальная щадящая диета. Основное назначение диеты – снизить интоксикацию и повысить иммунитет, при этом в щадящем для органов пищеварения режиме. В рационе должно быть достаточно витаминов, минералов, белка.
Профилактика
Основа профилактики энтеровирусной инфекции у ребёнка — соблюдение правил гигиены:
В педиатрическом отделении медицинского центра «СМ-Клиника» созданы все условия для диагностики и лечения энтеровирусной инфекции у ребёнка. Для тяжёлых больных при отделении работает круглосуточный стационар, где маленький пациент будет находиться под постоянным присмотром квалифицированного медицинского персонала и врачей. Помните что, чем раньше будет поставлен верный диагноз и определён тип вируса, тем легче будет вылечить ребёнка и избежать осложнений.