Чем лечить гепатоз печени после удаления желчного пузыря
Постхолецистэктомический синдром: диагностика и лечение
Желчнокаменная болезнь (ЖКБ) чрезвычайно распространена в цивилизованных странах, в том числе и в России. Особенно высока заболеваемость среди женщин в возрасте 35–40 лет и старше. ЖКБ характеризуется образованием желчных
Желчнокаменная болезнь (ЖКБ) чрезвычайно распространена в цивилизованных странах, в том числе и в России. Особенно высока заболеваемость среди женщин в возрасте 35–40 лет и старше. ЖКБ характеризуется образованием желчных камней в билиарной системе, главным образом в желчном пузыре, и осложнениями, возникающими в связи с прогрессированием патологического процесса.
Основным методом лечения данного заболевания является холецистэктомия. У 25% перенесших холецистэктомию больных или сохраняются, или через некоторое время появляются абдоминальные боли и диспепсические расстройства, требующие лечения. Адекватная терапия больных зависит от правильного понимания патогенеза клинических симптомов, развивающихся после холецистэктомии. Особенности их формирования связаны, с одной стороны, с нарушениями в обмене холестерина, присущими желчнокаменной болезни, с другой — тем обстоятельством, что патологический процесс протекает в новых анатомо-физиологических условиях, т. е. при отсутствии желчного пузыря.
Известно, что удаление желчного пузыря по поводу калькулезного холецистита не избавляет больных от обменных нарушений, в том числе от печеночно-клеточной дисхолии, которая сохраняется и после операции. У большинства больных после холецистэктомии определяется литогенная желчь с низким холатохолестериновым коэффициентом. Выпадение физиологической роли желчного пузыря, а именно концентрация желчи в межпищеварительный период и выброс ее в двенадцатиперстную кишку во время еды, сопровождается нарушением пассажа желчи в кишечник и расстройством пищеварения. Изменение химического состава желчи и хаотическое ее поступление в двенадцатиперстную кишку нарушают переваривание и всасывание жира и других веществ липидной природы, уменьшают бактерицидность дуоденального содержимого, что приводит к микробному обсеменению двенадцатиперстной кишки, ослаблению роста и функционирования нормальной кишечной микрофлоры, расстройству печеночно-кишечной циркуляции и снижению общего пула желчных кислот. Под влиянием микрофлоры желчные кислоты подвергаются преждевременной деконъюгации, что сопровождается повреждением слизистой оболочки двенадцатиперстной, тонкой и толстой кишки с развитием дуоденита, рефлюкс-гастрита, энтерита и колита. Дуоденит сопровождается дуоденальной дискинезией и, в первую очередь, дуоденальной гипертензией с развитием дуодено-гастральных рефлюксов и забросом содержимого в общий желчный проток и проток поджелудочной железы.
В результате формируются дискинезии сфинктера печеночно-поджелудочной ампулы, желчного и панкреатического протоков (сфинктера Одди), а деконъюгированные желчные кислоты обусловливают развитие диареи. Таким образом, у больных с удаленным желчным пузырем имеющиеся клинические проявления могут быть связаны с изменением химического состава желчи, нарушенным пассажем ее в двенадцатиперстную кишку, дискинезией сфинктера Одди, а также с избыточным бактериальным ростом в кишечнике, синдромами мальдигестии и мальабсорбции, дуоденитом и другими патологическими нарушениями в системе пищеварения. Кроме того, у ряда больных могут сохраняться или развиваться вновь органические препятствия для оттока желчи, связанные с проведенной холецистэктомией. Патологические состояния, которые наблюдаются у больных после холецистэктомии, можно разделить на 3 группы.
В настоящее время термином «постхолецистэктомический синдром» принято обозначать только дисфункцию сфинктера Одди, обусловленную нарушением его сократительной функции и препятствующую нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку при отсутствии органических препятствий. При этом предлагается, вместо принятых ранее определений «постхолецистэктомический синдром», «билиарная дискинезия» и др., использовать термин «дисфункция сфинктера Одди».
Клинические проявления дисфункции сфинктера Одди зависят, в первую очередь, от вовлечения в процесс той или иной его структуры. При изолированной дисфункции сфинктера холедоха развиваются билиарные, при преимущественном вовлечении в процесс сфинктера панкреатического протока — панкреатические, а при патологии общего сфинктера — сочетанные билиарно-панкреатические боли. Для дисфункции сфинктера Одди характерны рецидивирующие приступы сильных или умеренных болей продолжительностью 20 и более минут, повторяющиеся в течение 3 и более месяцев. При билиарном типе боль локализуется в эпигастрии или правом подреберье с иррадиацией в спину и правую лопатку, при панкреатическом типе — в левом подреберье с иррадиацией в спину уменьшающаяся при наклоне вперед, при сочетанном типе — имеет опоясывающий характер. Боль может сочетаться со следующими признаками: а) начало после приема пищи; б) появление в ночные часы; в) тошнота и/или рвота.
Однако оценка только клинических симптомов недостаточна для исключения органической патологии билиарной системы. С этой целью используются ряд скрининговых и уточняющих методов (табл.).
Неинвазивные методы, позволяющие предположить дисфункцию сфинктера Одди, включают определение в крови уровня билирубина, щелочной фосфатазы, аминотрансфераз, амилазы и липазы. Лабораторные исследования необходимо проводить во время или не позднее 6 ч после окончания болевого приступа, а также в динамике. Транзиторное повышение в 2 и более раз уровня печеночных или панкреатических ферментов в период не менее чем при 2 последовательных приступах болей является важным в подтверждении дисфункции сфинктера Одди.
Аналогичное значение имеет провокационный морфино-простигминовый тест, когда парентеральное введение препаратов провоцирует развитие болевого приступа, чаще смешанного билиарно-панкреатического типа в сочетании с повышением в крови уровня аминотрансфераз, щелочной фосфатазы, панкреатических ферментов. Однако диагностическая ценность данного теста ограничена его низкой чувствительностью и специфичностью.
При УЗИ важное значение придается расширению холедоха и главного панкреатического протока, которое свидетельствует о нарушении тока желчи и панкреатического секрета на уровне сфинктера Одди. В то же время у 3-4% больных, перенесших холецистэктомию и не имеющих симптомов, отмечается расширение общего желчного протока. Определенное значение имеет ультразвуковое исследование диаметра общего желчного протока с использованием жирных завтраков, стимулирующих выработку эндогенного холецистокинина и увеличивающих холерез. После пробного завтрака измерение диаметра холедоха проводится каждые 15 мин в течение 1 ч. Увеличение его диаметра на 2 мм и более по сравнению с исходным позволяет предположить наличие неполной обтурации холедоха как в результате дисфункции сфинктера Одди, так и из-за органической патологии билиарной системы.
Для оценки состояния панкреатических протоков используется проба с введением секретина в дозе 1 мг/кг. В норме после стимуляции панкреатической секреции секретином при УЗИ отмечается расширение панкреатического протока в течение 30 мин с последующим его уменьшением до исходного уровня. Если проток остается расширенным более 30 мин, это свидетельствует о нарушении его проходимости.
При билисцинтиграфии о наличии дисфункции сфинктера Одди свидетельствует увеличение времени транзита радиофармпрепарата от ворот печени до двенадцатиперстной кишки, при этом оно пропорционально уровню базального давления сфинктера Одди. В то же время при расширенном холедохе данное исследование малоинформативно для оценки функции сфинктера Одди.
К инвазивным методам оценки функции сфинктера Одди относится непрямой способ — эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Косвенными признаками повышения тонуса сфинктера Одди являются диаметр холедоха более 12 мм, задержка контраста в холедохе свыше 45 мин. О дисфункции сфинктера главного панкреатического протока свидетельствуют расширение последнего до более чем 5 мм и замедление эвакуации контраста из его просвета. Однако аналогичные изменения могут наблюдаться и при наличии органической патологии.
Наиболее точным методом, подтверждающим дисфункцию сфинктера Одди, является манометрия. При этом возможно канюлирование раздельно холедоха и вирсунгова протока с проведением манометрии их сфинктеров, что позволяет выделить преимущественно билиарный или панкреатический тип расстройств, а также установить этиологию рецидивирующих панкреатитов у больных, перенесших холецистэктомию и папиллотомию. Признаками дисфункции сфинктера Одди при манометрическом исследовании являются:
Манометрия сфинктера Одди показана далеко не всем больным. Выбор данного исследования основывается на оценке тяжести клинических проявлений и эффективности консервативной терапии.
Таким образом, предположить, что речь идет о дисфункции сфинктера Одди можно в следующих ситуациях:
Примерные формулировки диагнозов у больных, перенесших холецистэктомию:
Диагноз: желчнокаменная болезнь, холецистэктомия в 1994 г. (для случаев, при которых отсутствуют клинические симптомы).
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1999 г.
Диагноз: хронический рецидивирующий (обструктивный) панкреатит с внешнесекреторной и инкреторной недостаточностью в фазе обострения.
Сопутствующее заболевание: желчнокаменная болезнь, холецистэктомия в 1994 г.
Диагноз: синдром раздраженного кишечника с преобладанием запоров в фазе обострения.
Сопутствующий диагноз: желчнокаменная болезнь, холецистэктомия в 1994 г.
Ведение больных, перенесших холецистэктомию. Цель лечения: восстановить нормальное поступление желчи и панкреатического секрета из билиарных и панкреатических протоков в двенадцатиперстную кишку. Задачи лечения: нормализовать химический состав желчи; восстановить проходимость сфинктера Одди; восстановить нормальный состав кишечной микрофлоры; нормализовать процессы пищеварения и моторику тонкой кишки для профилактики дуоденальной гипертензии.
Для профилактики образования желчных сладжей или камней во внепеченочной билиарной системе рекомендуется:
Медикаментозное лечение дисфункции сфинктера Одди направлено на снятие спазма гладкой мускулатуры последнего. С этой целью используется ряд препаратов, обладающих спазмолитическим эффектом. Нитраты: нитроглицерин используется с целью быстрого купирования болей, нитросорбит — для курсового лечения. Механизм действия нитратов сводится к образованию в гладких мышцах свободных радикалов оксида азота (NO), которые активируют гуамилатциклазу и увеличивают содержание цГМФ, что приводит к их расслаблению. Однако выраженные кардиоваскулярные эффекты, побочные действия и развитие толерантности делают их малоприемлемыми для длительной терапии дисфункции сфинктера Одди.
Антихолинергические средства блокируют мускариновые рецепторы на постсинаптических мембранах органов-мишеней. В результате происходит блокада кальциевых каналов, прекращается вход ионов кальция в цитоплазму гладкомышечных клеток и, как следствие, достигается снятие мышечного спазма. В качестве спазмолитиков используются как неселективные (препараты красавки, метацин, платифиллин, бускопан и др.), так и селективные М-холиноблокаторы (гастроцепин и др.). Однако при приеме препаратов данной группы может наблюдаться достаточно широкий спектр побочных эффектов: сухость во рту, задержка мочеиспускания, нарушения зрения, повышение внутриглазного давления, тахикардия, запоры, сонливость. Сочетание довольно низкой эффективности с широким спектром побочных действий ограничивает применение препаратов этой группы при дисфункции сфинктера Одди.
Блокаторы медленных кальциевых каналов — фенилалкиламины (верапамил, галлопамил), 1,4-дигидроперидины (нифедипин, амлодипин) и бензотиазепины (дилтиазем и др.) закрывают кальциевые («медленные») каналы клеточных мембран, препятствуют входу ионов кальция в цитоплазму клеток гладкой мускулатуры и вызывают ее релаксацию. Препараты обладают многочисленными кардиоваскулярными эффектами, в первую очередь вазодилатирующими, в связи с чем не нашли широкого применения при лечении дисфункции сфинктера Одди. Имеются лишь единичные публикации по использованию нифедипина при дисфункции сфинктера Одди, и целесообразность их применения требует дальнейшего изучения.
Миотропные спазмолитики, механизм действия которых сводится к ингибированию фосфодиэстеразы, или к активации аденилатциклазы, или к блокаде аденозиновых рецепторов, что приводит к снижению тонуса и двигательной активности гладкой мускулатуры. Представителями данной группы препаратов являются дротаверин (но-шпа, но-шпа форте), бенциклан (галидор), дицикловерин (триган-Д), альверин (метеоспазмил) и др.
Основными недостатками препаратов всех вышеуказанных групп являются:
В отличие от них, гимекромон (одестон) обладает избирательным спазмолитическим действием на сфинктер Одди и сфинктер желчного пузыря. Кроме того, препарат не повышает давление в желчных путях, не оказывает влияния на секреторную функцию пищеварительных желез и процессы кишечной абсорбции.
В восстановлении нормального оттока желчи при отсутствии желчного пузыря, наряду с проходимостью сфинктера Одди, большое значение имеет уровень давления в двенадцатиперстной кишке. Если он превышает секреторное давление желчи и панкреатического сока, они будут депонироваться в билиарных и панкреатических протоках с соответствующими последствиями.
В связи с этим разрешение дуоденальной гипертензии считается непременным условием ведения больных с дисфункцией сфинктера Одди. При выборе тактики лечения следует учитывать, что основным патогенетическим механизмом развития дуоденальной гипертензии является избыточное содержание жидкости и газа в просвете двенадцатиперстной кишки в результате бродильно-гнилостных процессов, обусловленных микробной контаминацией.
Для деконтаминации двенадцатиперстной кишки проводятся 1-2 семидневных курса антибактериальной терапии со сменой препарата при очередном курсовом лечении. Препаратами выбора являются: доксициклин 0,1 г 2 раза в день, тетрациклин 0,25 г 4 раза в день, бисептол 960 мг 2 раза в день, фуразолидон 0,1 г 3 раза в день, эрсефурил 0,2 г 4 раза в день, ципрофлоксацин 250 мг 2 раза в день, метронидазол 0,25 г 4 раза в день, интетрикс 1 капсула 4 раза в сутки, реже — левомицетин 0,25 г 4 раза в день.
Подбор лекарственных средств проводится, как правило, эмпирически. При выраженных симптомах диспепсии назначаются сразу 2 препарата, один из которых должен действовать преимущественно на анаэробную микрофлору (например, метронидазол). Одновременно с приемом кишечных антисептиков в ряде случаев назначаются пребиотики: при наличии поносов — хилак форте 60 капель 3 раза в день в течение 1 нед, затем по 30 капель 3 раза в день в течение 2 нед; в случаях преобладания запоров — лактулоза по 1-2 столовые ложки 1 раз в день до нормализации стула.
После окончания антибактериальной терапии показаны пробиотики (препараты, содержащие нормальные штаммы кишечной флоры). Одним из известных представителей группы пробиотиков является бифиформ, содержащий в одной капсуле, покрытой энтерорастворимой оболочкой, энтерококки 107, бифидумбактерии 107 и питательную среду, способствующую их росту в тонкой и толстой кишке. Назначается препарат по 1 капсуле 2 раза в день в течение 2 нед. В комплексе с антибактериальными средствами необходимо назначать алюминийсодержащие буферные антациды (алюгастрин, алюмаг, маалокс, фосфалюгель, смекта и др.). Любой из препаратов принимается по 1 дозе через 1 ч после завтрака, обеда и ужина и перед сном (не сочетаются с хилаком форте). Продолжительность лечения составляет 5–7 дней. Целесообразность использования данных препаратов обусловлена следующими их способностями:
Наличие у большинства больных относительной ферментной недостаточности в результате разрушения пищеварительных ферментов дуоденальной и тонкокишечной микрофлорой, снижения интрадуоденального уровня рН, а также нарушения процесса смешивания их с пищевым химусом является обоснованием назначения ферментных препаратов. При склонности к поносам назначаются препараты панкреатина: мезим форте, креон, ликреаза, панцитрат и другие по 1 дозе 2-3 раза в день в начале еды; при склонности к запорам — комбинированные средства, содержащие панкреатин, желчные кислоты, гемицеллюлозу: фестал, энзистал, дигестал по 1 драже 2-3 раза в день в конце приема еды. Продолжительность лечения индивидуальна и, как правило, не превышает 10 дней.
Приведем ориентировочные схемы ведения больных с дисфункцией сфинктера Одди.
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1996 г.
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1989 г. Сопутствующие заболевания: хронический катаральный, преимущественно дистальный дуоденит. Синдром избыточного бактериального роста в тонкой кишке.
Таким образом, своевременная и правильная оценка клинической симптоматики, развивающейся у больных после операции холецистэктомии, дает возможность подобрать адекватную терапию и в результате существенно улучшить качество жизни пациентов с заболеваниями гепатобилиарной системы.
По вопросам литературы обращайтесь в редакцию.
П. Я. Григорьев, доктор медицинских наук, профессор, Э. П. Яковенко, доктор медицинских наук, профессор
Н. А. Агафонова, кандидат медицинских наук, А. С. Прянишникова, кандидат медицинских наук
И. П. Солуянова, кандидат медицинских наук, З. В. Бекузарова, А. В. Яковенко, кандидат медицинских наук
РГМУ, Москва
Фосфоглив® при жировом гепатозе

Механизм развития жирового гепатоза печени
В основе патогенетических механизмов жирового гепатоза лежат:
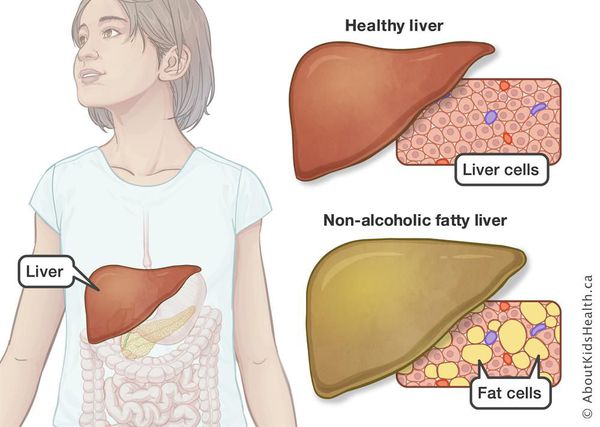
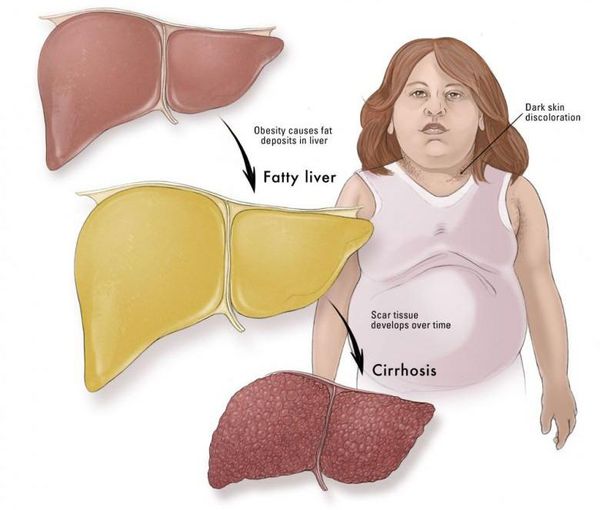
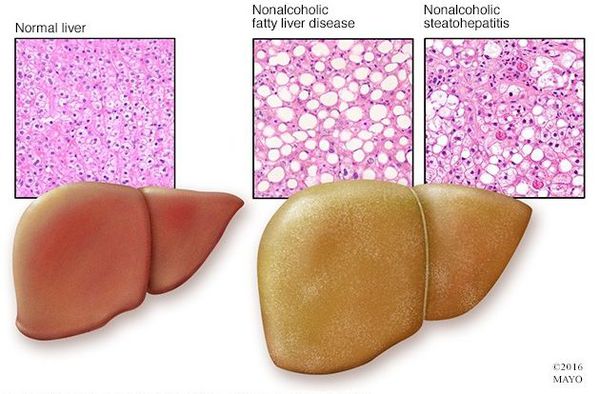
Характерной особенностью патологического состояния является повышение количества триглицеридов более чем на 10 % от общей сухой массы печени. Из-за этого при гепатозе происходит отложение жировых капель в гепатоцитах, развитие «ожирения» печеночных клеток, их последующая гибель и замещение фиброзной соединительной тканью.
Жир в клетках печени может накапливаться по нескольким причинам:
На сегодняшний день распространенность стеатоза в общей популяции достигает 40 %.
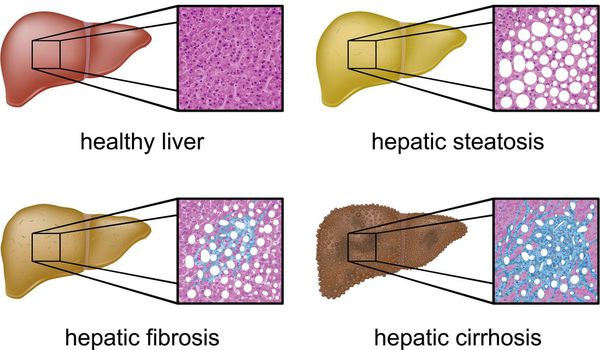
Степени гепатоза
В зависимости от количества и места накопления жира принято выделять 4 степени жирового гепатоза печени:
Причины жирового гепатоза
К основным причинам развития жирового гепатоза печени относят:
Клинические признаки гепатоза
Основные симптомы заболевания
На ранней стадии заболевания симптомы жирового гепатоза печени практически не наблюдаются. Это объясняется способностью гепатоцитов к активной регенерации. Однако по мере накопления жира клетки печени перестают справляться со своей функцией. У пациентов появляются следующие симптомы:
Диагностика
Диагностика жирового гепатоза включает в себя сбор анамнеза, оценку самочувствия и физикального статуса пациента, а также лабораторные и инструментальные методы обследования печени.
Лабораторные методы исследования:
Инструментальные диагностические методики:
Лечение жирового гепатоза печени
В связи с наличием большого разнообразия причин, обуславливающих развитие патологического процесса, лечение жирового гепатоза считается достаточно сложной задачей, требующей грамотного комплексного подхода. Обязательными условиями успешной терапии являются:
Диета
Пациентам с повышенной массой тела рекомендуется диетическое питание, направленное на нормализацию жирового и холестеринового обмена. В соответствии с принципом диеты № 5 в суточный рацион больного гепатозом должны входить:
Блюда готовятся на пару, запекаются или отвариваются и подаются только в теплом виде. Прием горячей, холодной, острой и жареной пищи запрещен. Питание должно быть дробным – 5–6 раз в день.
В список продуктов, рекомендованных при лечении гепатоза печени, входят:
Запрещенные продукты при гепатозе:
Лечение жирового гепатоза печени при помощи здоровой диеты требует строгого соблюдения принципов сбалансированного питания. Оптимальная потеря веса – не более 1 кг за неделю. В случае резкого снижения массы тела возможно развитие стеатоза, способного повлечь за собой воспаление, усиление активности фиброгенеза и увеличение скорости развития фиброза.
Медикаментозная терапия
Медикаментозное лечение жирового гепатоза печени проводится в 2 этапа.
Симптоматическое лечение гепатоза печени предусматривает использование противовоспалительных средств, пищеварительных ферментов, витаминов, препаратов антифиброзного действия и пробиотиков, нормализующих микрофлору кишечника.
Фосфоглив* при лечении жирового гепатоза
Фосфоглив* – современный гепатопротектор, нашедший широкое применение в гастроэнтерологии и гепатологии. Этот препарат патогенетического действия обладает восстанавливающими, противовоспалительными и антифиброзными свойствами и может использоваться для лечения гепатоза. В состав гепатопротектора входят два активных компонента: эссенциальные фосфолипиды и глицирризиновая кислота.
Эссенциальные фосфолипиды способствуют:
Применение Фосоглива* в комплексном лечении гепатоза способствует:
Препарат обладает благоприятным профилем безопасности и имеет доказательства клинической эффективности. Для достижения максимального действия при лечении гепатоза печени Фосфоглив* следует принимать курсами согласно инструкции по применению.
Удаление желчного пузыря и жировая болезнь печени
Приходилось ли вам слышать о желчнокаменной болезни или сокращенно ЖКБ? Скорее всего, ответ будет утвердительным, об этом распространенном заболевании известно каждому. Даже если вы к счастью не попали в те 10-15% взрослого населения, у которых желчнокаменная болезнь диагностирована, у многих могут найтись родственники и знакомые, у которых эта болезнь есть. А вот о неалкогольной жировой болезни печени или сокращенно НЖБП знают намного меньше людей, хотя по данным статистики ее распространенность выше в 1,6 раза. В России эта болезнь более известна под названием жировой гепатоз или жировая дистрофия печени, а также стеатоз и неалкогольный стеатогепатит. С 2016 термин неалкогольная жировая болезнь печени включен в Международную классификацию болезней 10-го пересмотра и объединяет все патологические состояния, связанные с накоплением жира в печени и имеющие неалкогольное происхождение – стеатоз, стеатогепатит и цирроз печени.
Как часто и почему желчнокаменная болезнь сочетается с жировым гепатозом (неалкогольной жировой болезнью печени)?
Согласно данным исследований, проведенных в последние годы, у людей с неалкогольной жировой болезнью печени риск развития желчнокаменной болезни повышен в 1,5 раза, причем почти у 100% людей с ожирением выявляются оба эти заболевания. Ученым пока не ясно, какое из этих заболеваний развивается первым, возможно, они развиваются параллельно.
Причиной сочетаемости желчнокаменной болезни и неалкогольной жировой болезни печени является то, что факторы риска развития этих болезней во многом совпадают:
Если у вас есть в наличии хотя бы некоторые из перечисленных выше факторов риска, рекомендуем посетить своего лечащего врача для профилактики этих заболеваний.
Удаление желчного пузыря может спровоцировать развитие неалкогольной жировой болезни печени (жирового гепатоза)
Кроме схожих факторов риска, дополнительно к факторам риска развития и прогрессирования неалкогольной жировой болезни печени (жирового гепатоза) необходимо добавить холецистэктомию (удаление желчного пузыря). После удаления желчного пузыря риск развития неалкогольной жировой болезни печени возрастает в 2,4 раза, хотя само наличие желчнокаменной болезни этот риск не повышает. Причины такого явления, по мнению специалистов, в нарушении транспорта желчи после удаления желчного пузыря и увеличении поступления свободных жирных кислот в печень из жировой ткани.
Профилактика и лечение желчнокаменной болезни и жирового гепатоза
Если вы давно не были у врача, профилактику рекомендуем начинать с обследования с проведением лабораторных анализов и УЗИ брюшной полости. Оба заболевания долгое время могут протекать без каких-либо заметных симптомов, и человек может не знать, что он уже болен. В ГЦ Эксперт вы можете получить бесплатный первичный прием гастроэнтеролога для назначения обследования, необходима предварительная запись по тел. 602-35-44.
Профилактика эффективно помогает избежать как развития, так и прогрессирования этих заболеваний. Это, прежде всего, коррекция рациона питания, добавление в него цельных злаков, овощей и фруктов, а также увеличение двигательной активности.Для профилактики вы можете использовать средиземноморскую диету или диету №5 по Певзнеру.
При нарушении транспорта желчи в организме необходима лекарственная терапия, которая может помочь предотвратить образование камней в желчном пузыре, для назначения терапии рекомендуем вам обратиться к врачу-гастроэнтерологу. Лекарственная терапия желчнокаменной болезни возможна только на этапе возникновения густой желчи и песка или холестериновых камней не больше 15 мм при сохранении сократительной способности желчного пузыря и проходимости желчных путей.
Не занимайтесь самолечением, при наличии камней в желчном пузыре самолечение очень опасно и может вызвать обострение заболевания, требующее срочного оперативного вмешательства.
При наличии снижения чувствительности к инсулину, сахарного диабета 2 типа и ожирения может потребоваться лекарственная терапия для снижения уровня сахара и триглицеридов в крови.
После удаления желчного пузыря необходима реабилитация
Если у вас есть показания к удалению желчного пузыря, то перед операцией мы рекомендуем провести подготовительное лечение, а после комплексное реабилитационное лечение, направленное на профилактику сразу нескольких заболеваний – постхолецистоэктомического синдрома, рецидивов желчнокаменной болезни и развития или прогрессирования неалкогольной жировой болезни печени (жирового гепатоза).
Фосфоглив® при жировом гепатозе

Механизм развития жирового гепатоза печени
В основе патогенетических механизмов жирового гепатоза лежат:
Характерной особенностью патологического состояния является повышение количества триглицеридов более чем на 10 % от общей сухой массы печени. Из-за этого при гепатозе происходит отложение жировых капель в гепатоцитах, развитие «ожирения» печеночных клеток, их последующая гибель и замещение фиброзной соединительной тканью.
Жир в клетках печени может накапливаться по нескольким причинам:
На сегодняшний день распространенность стеатоза в общей популяции достигает 40 %.
Степени гепатоза
В зависимости от количества и места накопления жира принято выделять 4 степени жирового гепатоза печени:
Причины жирового гепатоза
К основным причинам развития жирового гепатоза печени относят:
Клинические признаки гепатоза
Основные симптомы заболевания
На ранней стадии заболевания симптомы жирового гепатоза печени практически не наблюдаются. Это объясняется способностью гепатоцитов к активной регенерации. Однако по мере накопления жира клетки печени перестают справляться со своей функцией. У пациентов появляются следующие симптомы:
Диагностика
Диагностика жирового гепатоза включает в себя сбор анамнеза, оценку самочувствия и физикального статуса пациента, а также лабораторные и инструментальные методы обследования печени.
Лабораторные методы исследования:
Инструментальные диагностические методики:
Лечение жирового гепатоза печени
В связи с наличием большого разнообразия причин, обуславливающих развитие патологического процесса, лечение жирового гепатоза считается достаточно сложной задачей, требующей грамотного комплексного подхода. Обязательными условиями успешной терапии являются:
Диета
Пациентам с повышенной массой тела рекомендуется диетическое питание, направленное на нормализацию жирового и холестеринового обмена. В соответствии с принципом диеты № 5 в суточный рацион больного гепатозом должны входить:
Блюда готовятся на пару, запекаются или отвариваются и подаются только в теплом виде. Прием горячей, холодной, острой и жареной пищи запрещен. Питание должно быть дробным – 5–6 раз в день.
В список продуктов, рекомендованных при лечении гепатоза печени, входят:
Запрещенные продукты при гепатозе:
Лечение жирового гепатоза печени при помощи здоровой диеты требует строгого соблюдения принципов сбалансированного питания. Оптимальная потеря веса – не более 1 кг за неделю. В случае резкого снижения массы тела возможно развитие стеатоза, способного повлечь за собой воспаление, усиление активности фиброгенеза и увеличение скорости развития фиброза.
Медикаментозная терапия
Медикаментозное лечение жирового гепатоза печени проводится в 2 этапа.
Симптоматическое лечение гепатоза печени предусматривает использование противовоспалительных средств, пищеварительных ферментов, витаминов, препаратов антифиброзного действия и пробиотиков, нормализующих микрофлору кишечника.
Фосфоглив* при лечении жирового гепатоза
Фосфоглив* – современный гепатопротектор, нашедший широкое применение в гастроэнтерологии и гепатологии. Этот препарат патогенетического действия обладает восстанавливающими, противовоспалительными и антифиброзными свойствами и может использоваться для лечения гепатоза. В состав гепатопротектора входят два активных компонента: эссенциальные фосфолипиды и глицирризиновая кислота.
Эссенциальные фосфолипиды способствуют:
Применение Фосоглива* в комплексном лечении гепатоза способствует:
Препарат обладает благоприятным профилем безопасности и имеет доказательства клинической эффективности. Для достижения максимального действия при лечении гепатоза печени Фосфоглив* следует принимать курсами согласно инструкции по применению.
Неалкогольный жировой гепатоз
«В связи с высокой вероятностью неблагоприятного течения НАЖБП, особенно в сочетании с другими проявлениями метаболического синдрома, все больные независимо от тяжести заболевания нуждаются в динамическом наблюдении и лечении»
Главный врач ГЦ «Эксперт», профессор ПСПбГМУ им. акад. И.П. Павлова Мехтиев С.Н.
Лечение неалкогольного жирового гепатоза печени (неалкогольной жировой болезни печени, НАЖБП) проводится с использованием методик обследования и лечения, разработанных главным врачом центра, профессором Мехтиевым Сабиром Насрединовичем на основе российских и зарубежных клинических рекомендаций, а также собственного практического и научно-исследовательского опыта.
Лечение начинается с обследования, составленного с учетом индивидуальных особенностей и состояния здоровья пациента, которое позволит:
По результатам обследования составляется индивидуальная программа лечения, которая будет включать:
Лечение проходит под наблюдением гастроэнтеролога, повторный прием потребуется через 1-2 месяца. Повторные УЗИ и эластография печени для оценки успешности лечения проводятся не раньше чем через полгода.
Способы лечения неалкогольной жировой болезни печени
Лечение неалкогольной жировой болезни печени при отсутствии осложнений, проводится амбулаторно. На сегодняшний момент нет какого-либо одного лекарственного препарата для лечения этого заболевания, поэтому лечение включает комплекс мер, как с использованием лекарственной терапии, так и без нее.
При отсутствии успеха консервативных мероприятий по снижению массы тела, при высокой степени ожирения (ИМТ >40 кг/м) и прогрессировании неалкогольной жировой болезни печени для лечения ожирения используют бариатрическую хирургию.
При необходимости лекарственная терапия корректируется во время лечения. Длительность приема лекарств зависит от стадии жирового гепатоза и состояния здоровья, а вот диету и режим дня с достаточным объемом физической активности необходимо будет соблюдать и после окончания лечения. Если человек после выздоровления возвращается к нездоровому питанию и снова набирает лишний вес, неалкогольный жировой гепатоз возвращается.
Неалкогольный жировой гепатоз может сочетаться с заболеваниями сердечно-сосудистой системы и поджелудочной железы или быть причиной их развития.
Лечение пациентов с неалкогольным жировым гепатозом и болезнями сердечно-сосудистой системы
На лечении пациентов с гипертонией и неалкогольным жировым гепатозом специализируется гастроэнтеролог и кардиолог Мехтиева Ольга Александровна . Она владеет методикой ритмокардиографии, которая выявляет наличие риска развития сердечно-сосудистых заболеваний на ранней стадии. Одновременное лечение гипертонии и неалкогольного жирового гепатоза поможет вернуть здоровье печени, добиться нормализации показателей артериального давления и уменьшить риски развития заболеваний печени и сердечно-сосудистой системы.
Лечение пациентов с неалкогольным жировым гепатозом и диабетом 2 типа
Пациентов со сложными случаями сочетания неалкогольного жирового гепатоза и панкреатита или диабета второго типа ведет главный врач нашего центра Мехтиев Сабир Насрединович . Сабир Насрединович более 12 лет лечит людей с жировым гепатозом и его осложнениями, а также занимается научными исследованиями по данной теме.
При заболеваниях поджелудочной железы и диабете второго типа гастроэнтеролог и эндокринолог в нашем центре лечат пациентов совместно.
Пациент в результате лечения получит
Советы и рекомендации
Узнать больше о неалкогольной жировой болезни печени (НАЖБП) и получить советы как сохранить свою печень здоровой вы можете из статьи главного врача нашего центра Мехтиева С.Н. «Жир в печени разрушает сердце и ведет к диабету» в «Комсомольской правде».
О причинах развития жирового гепатоза, фрагмент выступления профессора Мехтиева Сабира Насрединовича на научно-практическом семинаре «Особенности течения НЖБП у пациента с хроническим билиарнозависимым панкреатитом»
Что такое жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, врача общей практики со стажем в 14 лет.
Определение болезни. Причины заболевания
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печении или жировой гепатоз, неалкогольный стеатогепатит) — это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
Все эти изменения неуклонно приводят к:
Метаболический синдром — широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией. [2] [3] [4]
В большинстве случаев НАЖБП развивается после 30 лет. [7]
Факторами риска данного заболевания являются:
Основными причинам развития НАЖБП являются: [11]
При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %. [3]
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
У 50-75% больных могут появляться симптомы общей (хронической) усталости, снижение работоспособности, недомогание, слабость, тяжесть в области правого подреберья, набор веса, длительное повышение температуры тела без всякой причины, красные точки на коже в области груди и живота. Печень часто увеличена. Возникают расстройства пищеварения, повышенное газообразование, кожный зуд, редко — желтуха, «печёночные знаки».
Часто НАЖБП сопутствуют заболевания желчного пузыря: хронический холецистит, желчнокаменная болезнь. Реже, в запущенных случаях, возникают признаки портальной гипертензии: увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости). Как правило, данные симптомы наблюдаются на стадии цирроза печени. [7]
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
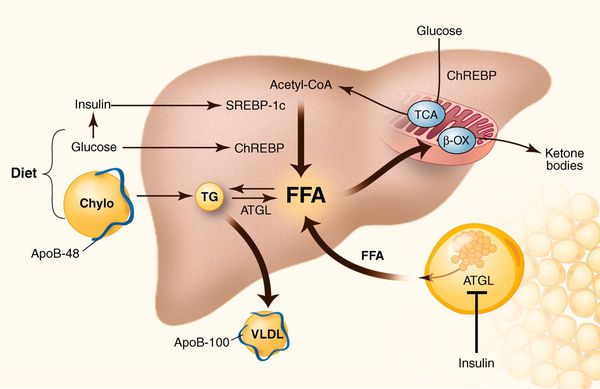
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот, что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид. [2]
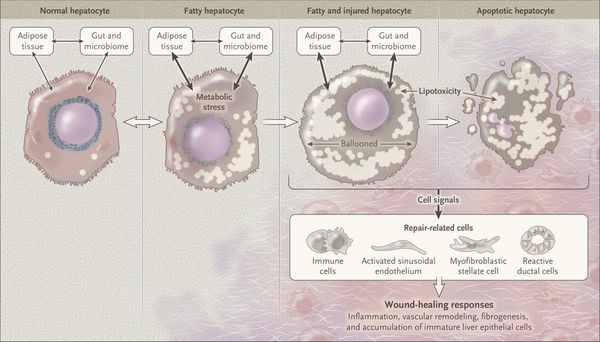
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной, раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах, в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов, которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз. [2]
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов. [7] CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
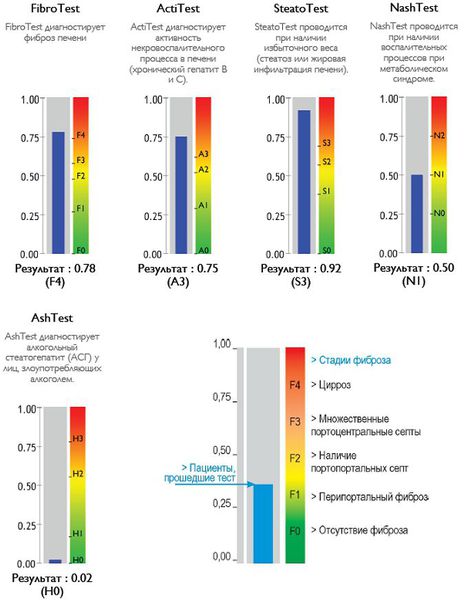
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt: [9] [10] [11]
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
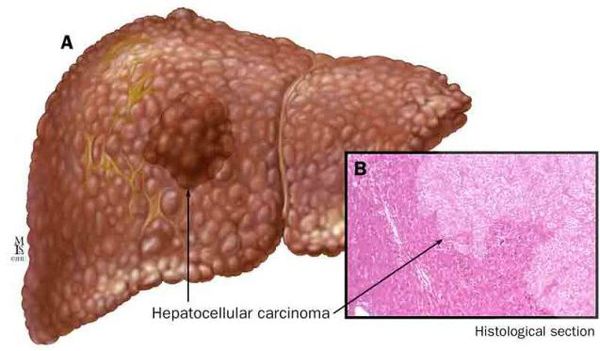
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени — гепатоцеллюлярную карциному. [9] Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов. [7]
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
С помощью эластометрии исследуется эластичность мягких тканей. Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
В процессе лечения производится:
После лечения наступает заметное улучшение дезинтоксикационной (защитной), пищеварительной и метаболической функции печени, пациенты теряют в весе, улучшается общее самочувствие, повышается умственная и физическая работоспособность.
Курсовые программы лечения занимают от трёх до шести месяцев и подбираются в зависимости от степени выраженности метаболических нарушений. К ним относятся:
Программы включают в себя предварительное обследование, постановку диагноза и медикаментозное лечение, которое состоит из двух этапов:
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.
Постхолецистэктомический синдром: диагностика и лечение
Желчнокаменная болезнь (ЖКБ) чрезвычайно распространена в цивилизованных странах, в том числе и в России. Особенно высока заболеваемость среди женщин в возрасте 35–40 лет и старше. ЖКБ характеризуется образованием желчных
Желчнокаменная болезнь (ЖКБ) чрезвычайно распространена в цивилизованных странах, в том числе и в России. Особенно высока заболеваемость среди женщин в возрасте 35–40 лет и старше. ЖКБ характеризуется образованием желчных камней в билиарной системе, главным образом в желчном пузыре, и осложнениями, возникающими в связи с прогрессированием патологического процесса.
Основным методом лечения данного заболевания является холецистэктомия. У 25% перенесших холецистэктомию больных или сохраняются, или через некоторое время появляются абдоминальные боли и диспепсические расстройства, требующие лечения. Адекватная терапия больных зависит от правильного понимания патогенеза клинических симптомов, развивающихся после холецистэктомии. Особенности их формирования связаны, с одной стороны, с нарушениями в обмене холестерина, присущими желчнокаменной болезни, с другой — тем обстоятельством, что патологический процесс протекает в новых анатомо-физиологических условиях, т. е. при отсутствии желчного пузыря.
Известно, что удаление желчного пузыря по поводу калькулезного холецистита не избавляет больных от обменных нарушений, в том числе от печеночно-клеточной дисхолии, которая сохраняется и после операции. У большинства больных после холецистэктомии определяется литогенная желчь с низким холатохолестериновым коэффициентом. Выпадение физиологической роли желчного пузыря, а именно концентрация желчи в межпищеварительный период и выброс ее в двенадцатиперстную кишку во время еды, сопровождается нарушением пассажа желчи в кишечник и расстройством пищеварения. Изменение химического состава желчи и хаотическое ее поступление в двенадцатиперстную кишку нарушают переваривание и всасывание жира и других веществ липидной природы, уменьшают бактерицидность дуоденального содержимого, что приводит к микробному обсеменению двенадцатиперстной кишки, ослаблению роста и функционирования нормальной кишечной микрофлоры, расстройству печеночно-кишечной циркуляции и снижению общего пула желчных кислот. Под влиянием микрофлоры желчные кислоты подвергаются преждевременной деконъюгации, что сопровождается повреждением слизистой оболочки двенадцатиперстной, тонкой и толстой кишки с развитием дуоденита, рефлюкс-гастрита, энтерита и колита. Дуоденит сопровождается дуоденальной дискинезией и, в первую очередь, дуоденальной гипертензией с развитием дуодено-гастральных рефлюксов и забросом содержимого в общий желчный проток и проток поджелудочной железы.
В результате формируются дискинезии сфинктера печеночно-поджелудочной ампулы, желчного и панкреатического протоков (сфинктера Одди), а деконъюгированные желчные кислоты обусловливают развитие диареи. Таким образом, у больных с удаленным желчным пузырем имеющиеся клинические проявления могут быть связаны с изменением химического состава желчи, нарушенным пассажем ее в двенадцатиперстную кишку, дискинезией сфинктера Одди, а также с избыточным бактериальным ростом в кишечнике, синдромами мальдигестии и мальабсорбции, дуоденитом и другими патологическими нарушениями в системе пищеварения. Кроме того, у ряда больных могут сохраняться или развиваться вновь органические препятствия для оттока желчи, связанные с проведенной холецистэктомией. Патологические состояния, которые наблюдаются у больных после холецистэктомии, можно разделить на 3 группы.
В настоящее время термином «постхолецистэктомический синдром» принято обозначать только дисфункцию сфинктера Одди, обусловленную нарушением его сократительной функции и препятствующую нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку при отсутствии органических препятствий. При этом предлагается, вместо принятых ранее определений «постхолецистэктомический синдром», «билиарная дискинезия» и др., использовать термин «дисфункция сфинктера Одди».
Клинические проявления дисфункции сфинктера Одди зависят, в первую очередь, от вовлечения в процесс той или иной его структуры. При изолированной дисфункции сфинктера холедоха развиваются билиарные, при преимущественном вовлечении в процесс сфинктера панкреатического протока — панкреатические, а при патологии общего сфинктера — сочетанные билиарно-панкреатические боли. Для дисфункции сфинктера Одди характерны рецидивирующие приступы сильных или умеренных болей продолжительностью 20 и более минут, повторяющиеся в течение 3 и более месяцев. При билиарном типе боль локализуется в эпигастрии или правом подреберье с иррадиацией в спину и правую лопатку, при панкреатическом типе — в левом подреберье с иррадиацией в спину уменьшающаяся при наклоне вперед, при сочетанном типе — имеет опоясывающий характер. Боль может сочетаться со следующими признаками: а) начало после приема пищи; б) появление в ночные часы; в) тошнота и/или рвота.
Однако оценка только клинических симптомов недостаточна для исключения органической патологии билиарной системы. С этой целью используются ряд скрининговых и уточняющих методов (табл.).
Неинвазивные методы, позволяющие предположить дисфункцию сфинктера Одди, включают определение в крови уровня билирубина, щелочной фосфатазы, аминотрансфераз, амилазы и липазы. Лабораторные исследования необходимо проводить во время или не позднее 6 ч после окончания болевого приступа, а также в динамике. Транзиторное повышение в 2 и более раз уровня печеночных или панкреатических ферментов в период не менее чем при 2 последовательных приступах болей является важным в подтверждении дисфункции сфинктера Одди.
Аналогичное значение имеет провокационный морфино-простигминовый тест, когда парентеральное введение препаратов провоцирует развитие болевого приступа, чаще смешанного билиарно-панкреатического типа в сочетании с повышением в крови уровня аминотрансфераз, щелочной фосфатазы, панкреатических ферментов. Однако диагностическая ценность данного теста ограничена его низкой чувствительностью и специфичностью.
При УЗИ важное значение придается расширению холедоха и главного панкреатического протока, которое свидетельствует о нарушении тока желчи и панкреатического секрета на уровне сфинктера Одди. В то же время у 3-4% больных, перенесших холецистэктомию и не имеющих симптомов, отмечается расширение общего желчного протока. Определенное значение имеет ультразвуковое исследование диаметра общего желчного протока с использованием жирных завтраков, стимулирующих выработку эндогенного холецистокинина и увеличивающих холерез. После пробного завтрака измерение диаметра холедоха проводится каждые 15 мин в течение 1 ч. Увеличение его диаметра на 2 мм и более по сравнению с исходным позволяет предположить наличие неполной обтурации холедоха как в результате дисфункции сфинктера Одди, так и из-за органической патологии билиарной системы.
Для оценки состояния панкреатических протоков используется проба с введением секретина в дозе 1 мг/кг. В норме после стимуляции панкреатической секреции секретином при УЗИ отмечается расширение панкреатического протока в течение 30 мин с последующим его уменьшением до исходного уровня. Если проток остается расширенным более 30 мин, это свидетельствует о нарушении его проходимости.
При билисцинтиграфии о наличии дисфункции сфинктера Одди свидетельствует увеличение времени транзита радиофармпрепарата от ворот печени до двенадцатиперстной кишки, при этом оно пропорционально уровню базального давления сфинктера Одди. В то же время при расширенном холедохе данное исследование малоинформативно для оценки функции сфинктера Одди.
К инвазивным методам оценки функции сфинктера Одди относится непрямой способ — эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Косвенными признаками повышения тонуса сфинктера Одди являются диаметр холедоха более 12 мм, задержка контраста в холедохе свыше 45 мин. О дисфункции сфинктера главного панкреатического протока свидетельствуют расширение последнего до более чем 5 мм и замедление эвакуации контраста из его просвета. Однако аналогичные изменения могут наблюдаться и при наличии органической патологии.
Наиболее точным методом, подтверждающим дисфункцию сфинктера Одди, является манометрия. При этом возможно канюлирование раздельно холедоха и вирсунгова протока с проведением манометрии их сфинктеров, что позволяет выделить преимущественно билиарный или панкреатический тип расстройств, а также установить этиологию рецидивирующих панкреатитов у больных, перенесших холецистэктомию и папиллотомию. Признаками дисфункции сфинктера Одди при манометрическом исследовании являются:
Манометрия сфинктера Одди показана далеко не всем больным. Выбор данного исследования основывается на оценке тяжести клинических проявлений и эффективности консервативной терапии.
Таким образом, предположить, что речь идет о дисфункции сфинктера Одди можно в следующих ситуациях:
Примерные формулировки диагнозов у больных, перенесших холецистэктомию:
Диагноз: желчнокаменная болезнь, холецистэктомия в 1994 г. (для случаев, при которых отсутствуют клинические симптомы).
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1999 г.
Диагноз: хронический рецидивирующий (обструктивный) панкреатит с внешнесекреторной и инкреторной недостаточностью в фазе обострения.
Сопутствующее заболевание: желчнокаменная болезнь, холецистэктомия в 1994 г.
Диагноз: синдром раздраженного кишечника с преобладанием запоров в фазе обострения.
Сопутствующий диагноз: желчнокаменная болезнь, холецистэктомия в 1994 г.
Ведение больных, перенесших холецистэктомию. Цель лечения: восстановить нормальное поступление желчи и панкреатического секрета из билиарных и панкреатических протоков в двенадцатиперстную кишку. Задачи лечения: нормализовать химический состав желчи; восстановить проходимость сфинктера Одди; восстановить нормальный состав кишечной микрофлоры; нормализовать процессы пищеварения и моторику тонкой кишки для профилактики дуоденальной гипертензии.
Для профилактики образования желчных сладжей или камней во внепеченочной билиарной системе рекомендуется:
Медикаментозное лечение дисфункции сфинктера Одди направлено на снятие спазма гладкой мускулатуры последнего. С этой целью используется ряд препаратов, обладающих спазмолитическим эффектом. Нитраты: нитроглицерин используется с целью быстрого купирования болей, нитросорбит — для курсового лечения. Механизм действия нитратов сводится к образованию в гладких мышцах свободных радикалов оксида азота (NO), которые активируют гуамилатциклазу и увеличивают содержание цГМФ, что приводит к их расслаблению. Однако выраженные кардиоваскулярные эффекты, побочные действия и развитие толерантности делают их малоприемлемыми для длительной терапии дисфункции сфинктера Одди.
Антихолинергические средства блокируют мускариновые рецепторы на постсинаптических мембранах органов-мишеней. В результате происходит блокада кальциевых каналов, прекращается вход ионов кальция в цитоплазму гладкомышечных клеток и, как следствие, достигается снятие мышечного спазма. В качестве спазмолитиков используются как неселективные (препараты красавки, метацин, платифиллин, бускопан и др.), так и селективные М-холиноблокаторы (гастроцепин и др.). Однако при приеме препаратов данной группы может наблюдаться достаточно широкий спектр побочных эффектов: сухость во рту, задержка мочеиспускания, нарушения зрения, повышение внутриглазного давления, тахикардия, запоры, сонливость. Сочетание довольно низкой эффективности с широким спектром побочных действий ограничивает применение препаратов этой группы при дисфункции сфинктера Одди.
Блокаторы медленных кальциевых каналов — фенилалкиламины (верапамил, галлопамил), 1,4-дигидроперидины (нифедипин, амлодипин) и бензотиазепины (дилтиазем и др.) закрывают кальциевые («медленные») каналы клеточных мембран, препятствуют входу ионов кальция в цитоплазму клеток гладкой мускулатуры и вызывают ее релаксацию. Препараты обладают многочисленными кардиоваскулярными эффектами, в первую очередь вазодилатирующими, в связи с чем не нашли широкого применения при лечении дисфункции сфинктера Одди. Имеются лишь единичные публикации по использованию нифедипина при дисфункции сфинктера Одди, и целесообразность их применения требует дальнейшего изучения.
Миотропные спазмолитики, механизм действия которых сводится к ингибированию фосфодиэстеразы, или к активации аденилатциклазы, или к блокаде аденозиновых рецепторов, что приводит к снижению тонуса и двигательной активности гладкой мускулатуры. Представителями данной группы препаратов являются дротаверин (но-шпа, но-шпа форте), бенциклан (галидор), дицикловерин (триган-Д), альверин (метеоспазмил) и др.
Основными недостатками препаратов всех вышеуказанных групп являются:
В отличие от них, гимекромон (одестон) обладает избирательным спазмолитическим действием на сфинктер Одди и сфинктер желчного пузыря. Кроме того, препарат не повышает давление в желчных путях, не оказывает влияния на секреторную функцию пищеварительных желез и процессы кишечной абсорбции.
В восстановлении нормального оттока желчи при отсутствии желчного пузыря, наряду с проходимостью сфинктера Одди, большое значение имеет уровень давления в двенадцатиперстной кишке. Если он превышает секреторное давление желчи и панкреатического сока, они будут депонироваться в билиарных и панкреатических протоках с соответствующими последствиями.
В связи с этим разрешение дуоденальной гипертензии считается непременным условием ведения больных с дисфункцией сфинктера Одди. При выборе тактики лечения следует учитывать, что основным патогенетическим механизмом развития дуоденальной гипертензии является избыточное содержание жидкости и газа в просвете двенадцатиперстной кишки в результате бродильно-гнилостных процессов, обусловленных микробной контаминацией.
Для деконтаминации двенадцатиперстной кишки проводятся 1-2 семидневных курса антибактериальной терапии со сменой препарата при очередном курсовом лечении. Препаратами выбора являются: доксициклин 0,1 г 2 раза в день, тетрациклин 0,25 г 4 раза в день, бисептол 960 мг 2 раза в день, фуразолидон 0,1 г 3 раза в день, эрсефурил 0,2 г 4 раза в день, ципрофлоксацин 250 мг 2 раза в день, метронидазол 0,25 г 4 раза в день, интетрикс 1 капсула 4 раза в сутки, реже — левомицетин 0,25 г 4 раза в день.
Подбор лекарственных средств проводится, как правило, эмпирически. При выраженных симптомах диспепсии назначаются сразу 2 препарата, один из которых должен действовать преимущественно на анаэробную микрофлору (например, метронидазол). Одновременно с приемом кишечных антисептиков в ряде случаев назначаются пребиотики: при наличии поносов — хилак форте 60 капель 3 раза в день в течение 1 нед, затем по 30 капель 3 раза в день в течение 2 нед; в случаях преобладания запоров — лактулоза по 1-2 столовые ложки 1 раз в день до нормализации стула.
После окончания антибактериальной терапии показаны пробиотики (препараты, содержащие нормальные штаммы кишечной флоры). Одним из известных представителей группы пробиотиков является бифиформ, содержащий в одной капсуле, покрытой энтерорастворимой оболочкой, энтерококки 107, бифидумбактерии 107 и питательную среду, способствующую их росту в тонкой и толстой кишке. Назначается препарат по 1 капсуле 2 раза в день в течение 2 нед. В комплексе с антибактериальными средствами необходимо назначать алюминийсодержащие буферные антациды (алюгастрин, алюмаг, маалокс, фосфалюгель, смекта и др.). Любой из препаратов принимается по 1 дозе через 1 ч после завтрака, обеда и ужина и перед сном (не сочетаются с хилаком форте). Продолжительность лечения составляет 5–7 дней. Целесообразность использования данных препаратов обусловлена следующими их способностями:
Наличие у большинства больных относительной ферментной недостаточности в результате разрушения пищеварительных ферментов дуоденальной и тонкокишечной микрофлорой, снижения интрадуоденального уровня рН, а также нарушения процесса смешивания их с пищевым химусом является обоснованием назначения ферментных препаратов. При склонности к поносам назначаются препараты панкреатина: мезим форте, креон, ликреаза, панцитрат и другие по 1 дозе 2-3 раза в день в начале еды; при склонности к запорам — комбинированные средства, содержащие панкреатин, желчные кислоты, гемицеллюлозу: фестал, энзистал, дигестал по 1 драже 2-3 раза в день в конце приема еды. Продолжительность лечения индивидуальна и, как правило, не превышает 10 дней.
Приведем ориентировочные схемы ведения больных с дисфункцией сфинктера Одди.
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1996 г.
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1989 г. Сопутствующие заболевания: хронический катаральный, преимущественно дистальный дуоденит. Синдром избыточного бактериального роста в тонкой кишке.
Таким образом, своевременная и правильная оценка клинической симптоматики, развивающейся у больных после операции холецистэктомии, дает возможность подобрать адекватную терапию и в результате существенно улучшить качество жизни пациентов с заболеваниями гепатобилиарной системы.
По вопросам литературы обращайтесь в редакцию.
П. Я. Григорьев, доктор медицинских наук, профессор, Э. П. Яковенко, доктор медицинских наук, профессор
Н. А. Агафонова, кандидат медицинских наук, А. С. Прянишникова, кандидат медицинских наук
И. П. Солуянова, кандидат медицинских наук, З. В. Бекузарова, А. В. Яковенко, кандидат медицинских наук
РГМУ, Москва