Чем лечить гиперплазию эндометрия в 50 лет
Гиперплазия эндометрия – симптомы и лечение

Основная причина чрезмерного разрастания эндометрия – это повышенная выработка эстрогенов и недостаток прогестерона. Чаще всего, данная патология диагностируется у женщин в предменопаузе и у девочек- подростков. Оба состояния связаны с гормональной перестройкой организма. Для гиперплазии эндометрия характерен ановуляторный цикл – отсутствие овуляции.
Что может спровоцировать гиперплазию эндометрия?
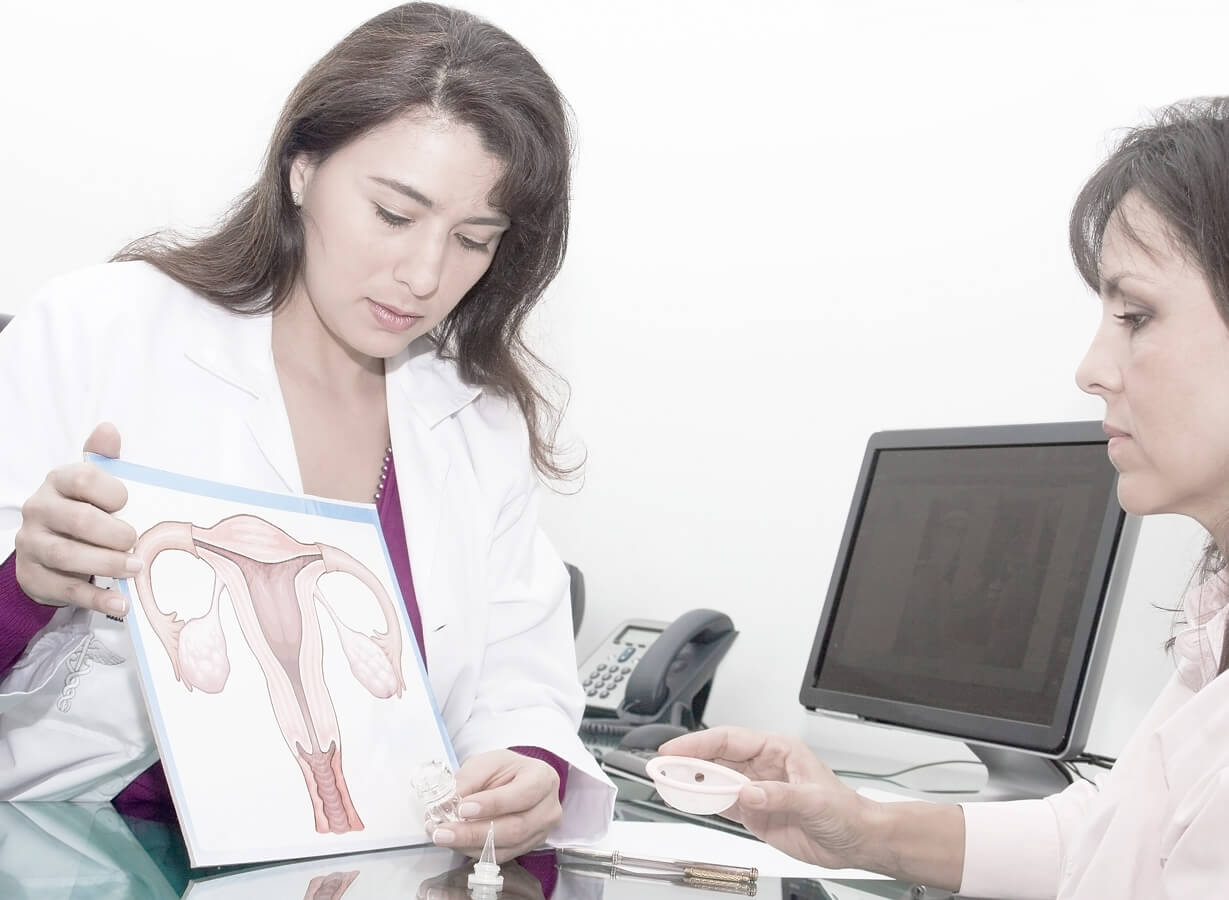
Какие симптомы характерны для гиперплазии эндометрия?
Все эти симптомы могут сопровождать миому матки или даже выкидыш на раннем сроке, поэтому необходимо сделать УЗИ малого таза, чтобы определить причину нециклических выделений.
Способы диагностики гиперплазии эндометрия
Узи органов малого таза влагалищным датчиком определяет толщину эндометрия. Толщина эндометрия меняется на протяжении всего цикла, в период перед месячными фиксируется самое высокое значение. Для диагностики следует проводить УЗИ в первой половине цикла, обычно на 7-10 день. Толщина свыше 15 мм дает повод заподозрить патологию и направить пациентку на гистероскопию – внутреннее обследование матки гистероскопом (специальным оптическим прибором), сопровождающееся диагностическим выскабливанием эндометрия и исследование полученного материала для типирования гиперплазии. Так УЗИ дает лишь 68 процентов информативности при гиперплазии, а для гистероскопии это значение достигает 94 процентов.
Аспирационная биопсия – еще один метод диагностики, когда кусочек эндометрия, взятый из полости матки, направляется на гистологическое исследование.
В некоторых случаях гинеколог может направить пациентку на анализ крови на гормоны: эстроген и прогестерон, гормоны щитовидной железы и надпочечников.
Лечение гиперплазии.
Самым эффективным способом лечения гиперплазии эндометрия является раздельное диагностическое выскабливание. Проводится в условиях стационара, обычно под наркозом. Затем полученный эндометрий отправляется на гистологию, и в зависимости от полученного результата исследования назначается гормональное лечение.
Гормонотерапия нужна для подавления разрастания эндометрия и регулирования гормонального фона. Гормональное лечение зависит от возраста пациентки. Так женщинам до 35 лет назначают комбинированные оральные контрацептивы.
Лечение гестагенами – еще один способ гормонотерапии, подходит для лечения гиперплазии эндометрия любого типа. Спираль Мирена – это один из таких вариантов. Но существует и таблетированная форма – это назначение препаратов Утрожестан или Дюфастон.
Не следует пренебрегать гормональной терапией, так как процент рецидивов высок (полипы могут возникнуть вновь после их удаления и не один раз), а обильные кровотечения осложняются анемией.
Гиперплазия эндометрия матки
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Эндометрий представляет собой нежную тонкую слизистую ткань, которая выстилает полость матки изнутри. Данная ткань каждый месяц быстро растет и утолщается под действием женских половых гормонов. В случае наступления беременности, эндометрий является «пуховой периной» на которую прикрепляется оплодотворенная яйцеклетка. При отсутствии беременности под действием гормонов эндометрий отторгается, выходит в виде менструальной крови.
Классификация гиперплазии эндометрия по локализации
Классификация гиперплазии эндометрия (по гистологической картине)
Причины гиперплазии эндометрия
В настоящее время основной причиной развития гиперплазии считается нарушение баланса женских половых гормонов, который чаще всего встречается в пубертатном периоде и перименопаузе.
Факторы риска развития гиперплазии эндометрия
Симптомы, которые встречаются при гиперплазии эндометрия
Основные из них при гиперплазии эндометрия могут быть:
Обследования, которые помогут выявить и поставить диагноз гиперплазии эндометрия
Лечение гиперплазии эндометрия
Практически в 100% случаев лечение гиперплазии эндометрия хирургическое.
Методами хирургического лечения гиперплазии эндометрия является гистероскопия и гистерорезектоскопия.
Данная операция проводится под общей анестезией. Продолжительность операции не превышает 30 минут, короткий период нахождения под общей анестезией позволяет врачам в тот же день отпустить пациентку домой.
Осложнения гиперплазии
При отсутствии должного и адекватного лечения гиперплазия эндометрия приводит к тяжелой анемии с значительным снижением уровня гемоглобина, появлению слабости, повышенной усталости, сонливости, что связано с большими потерями крови во время менструации. У молодых женщин гиперплазия эндометрия может быть причиной бесплодия и невынашивания беременности. Отдельные формы гиперплазии эндометрия (железистая и кистозная гиперплазии эндометрия) являются предраковым состоянием и в случае длительного наблюдения, при отсутствии лечения, могут переродиться в рак матки.
Профилактические мероприятия при данном заболевании необходимы для того, чтобы снизить риск развития рака эндометрия и предотвратить рецидив гиперплазии.
Гиперплазия эндометрия. Часто задаваемые вопросы
1. Что это такое? Доброкачественный процесс, который характеризуется чрезмерным разрастанием внутреннего слоя матки.
2. Из-за чего она возникает? Из-за постоянного воздействия полового гормона эстрогена на эндометрий, который вызывает его чрезмерное разрастание. Гиперэстрогения возникает из-за нарушения центральной регулиции менструального цикла, гормонопродуцирующих опухолей яичников, неправильного использования гормональных препаратов, дефицита прогестерона (гормон II фазы менструального цикла), обладающего антипролиферативным действием, так же в результате ановуляторных циклов.
3. Это распространенное заболевание? Частота встречаемости в структуре гинекологической заболеваемости 15-50%. По данным обращаемости пациенток частота встречаемости ГПЭ- 30%. В позднем репродуктивном возрасте и в перименопаузе встречается с частотой- 50%
4. Это заболевание очень опасно? Пристального внимания врачей заслуживают:
При отсутствии должного лечения гиперплазия эндометрия может приводить к серьезным маточным кровотечениям, со снижением гемоглобина крови и вытекающими отсюда последствиями.
5. Возможно ли забеременеть на фоне гиперплазии эндометрия? Ответ – нет. Гиперплазия эндометрия не возникает спонтанно, это следствие нарушений в репродуктивной системе женщины. Нарушение баланса между звеньями регуляции менструального цикла вызывает избыток эстрогенов в организме женщины, нехватку прогестерона, вследствие этого отсутствие овуляции (выхода яйцеклетки из фолликула для оплодотворения). Так же сам эндометрий структурно изменен, поэтому является неблагоприятным для имплантации (прикрепление плодного яйца к стенке матки).
7. Как диагностировать атипическую гиперплазию эндометрия? Большую информацию врач получает при опросе пациентки во время общения (возраст менархе или время наступления менопаузы, все особенности менструального цикла- его длительность, характер выделений и т.д.).
УЗ-исследование в зависимости от периода жизни женщины, а также фазы менструального цикла может дать информацию о состоянии эндометрия. По этим данным можно заподозрить проблему, однако подтвердить или опровергнуть атипию в клетках эндометрия нельзя. Только проведение гистероскопии с последующим гистологическим исследованием материала является золотым стандартом для диагностики этого состояния. Информативность метода более 90%.
8. Обязательно ли проводить выскабливание эндометрия при гиперплазии? Раздельное выскабливание цервикального канала и полости матки несет за собой лечебный и диагностический характер. Механическое удаление измененной патогенной ткани из полости матки предотвращает маточное кровотечение, что составляет лечебный эффект. Полученный соскоб отправляется на гистологическое исследование, после которого будет дано заключение о характере ткани, наличии или отсутствии признаков злокачественного поражения.
9. Возможен ли рецидив гиперплазии эндометрия? Да, возможен. Так как причиной гиперплазии эндометрия является нарушение гормонального баланса в организме женщины, то требуется обследование её гормонального фона. Для профилактики рецидива необходимо соответствующее лечение и исключение факторов риска.
Чем лечить гиперплазию эндометрия в 50 лет
ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии» Минздрава Московской области, Москва, Россия
Московский областной НИИ акушерства и гинекологии
Гиперплазия эндометрия в пери- и постменопаузе
Журнал: Российский вестник акушера-гинеколога. 2020;20(3): 35-40
Капитанова О. В., Чечнева М. А. Гиперплазия эндометрия в пери- и постменопаузе. Российский вестник акушера-гинеколога. 2020;20(3):35-40.
Kapitanova O V, Chechneva M A. Endometrial hyperplasia in peri- and postmenopausal women. Russian Bulletin of Obstetrician-Gynecologist. 2020;20(3):35-40.
https://doi.org/10.17116/rosakush20202003135
ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии» Минздрава Московской области, Москва, Россия
Большая клиническая значимость гиперпластических процессов в эндометрии заключается в том, что они являются одной из самых распространенных причин маточных кровотечений у женщин в возрасте 45—55 лет и их госпитализации в стационар. Гиперплазия эндометрия, особенно с атипией, является значительной клинической проблемой, поскольку может предшествовать раку эндометрия. За последние несколько лет оценка состояния эндометрия изменилась в признании того, что патология эндометрия не всегда носит глобальный характер. Толщина эндометрия не может быть единственным признаком гиперплазии эндометрия.
ГБУЗ МО «Московский областной научно-исследовательский институт акушерства и гинекологии» Минздрава Московской области, Москва, Россия
Московский областной НИИ акушерства и гинекологии
Введение
Гиперпластические процессы в эндометрии представляют большую медико-биологическую и социально-экономическую проблему и занимают значительное место в структуре гинекологической заболеваемости [1—6]. Высокая распространенность гиперпластических процессов в эндометрии, отсутствие должной эффективности от гормональной терапии, а также вероятность озлокачествления ставят гиперплазию эндометрия (ГЭ) в ряд наиболее актуальных проблем современной медицины. По данным Е.М. Вихляевой, гиперплазией эндометрия страдают почти 50% женщин позднего репродуктивного возраста и в период перименопаузы [7].
Большая клиническая значимость гиперпластических процессов в эндометрии заключается в том, что они являются одной из наиболее частых причин маточных кровотечений у женщин в возрасте 45—55 лет и их госпитализации в стационар [8—12]. Другая причина пристального внимания к ГЭ — это возможность их злокачественной трансформации. По данным статистики РФ, рак эндометрия (РЭ) занимает 3-е место в структуре онкологической заболеваемости женского населения [13, 14]. Малигнизация железистой гиперплазии и полипа эндометрия встречается в 2—5% и достигает 10% в постменопаузе [15—17]. Атипическая гиперплазия прогрессирует в инвазивный рак с частотой до 50% наблюдений [18, 19]. Однако, по данным разных авторов, РЭ по результатам гистологического исследования подтверждается у 1—10% женщин, имеющих кровотечение в постменопаузе. Практически в 60% наблюдений выявляется атрофия эндометрия и примерно с одинаковой частотой — полипы эндометрия, ГЭ и другие доброкачественные изменения эндометрия [20, 21]. Таким образом, в большинстве случаев причиной кровотечений в постменопаузе служат изменения эндометрия доброкачественного характера.
Факторами риска развития РЭ являются пожилой возраст пациенток (старше 50 лет), ожирение, поздняя менопауза, сахарный диабет, длительная эстрогеновая стимуляция, прием тамоксифена [22, 23].
При ожирении и индексе массы тела (ИМТ) более 25 кг/м 2 повышается риск развития РЭ на 200—400% [24]. Так как более 50% женщин в постменопаузе имеют избыточную массу тела, необходима онконастороженность в данной возрастной группе.
Диагностика патологии эндометрия
В скрининговой диагностике патологии эндометрия наиболее информативным неинвазивным методом обследования является лучевой — ультразвуковое исследование (УЗИ) — неинвазивный, легко выполнимый и высокоинформативный метод обследования больных для выявления количественных и качественных характеристик всех слоев эндометрия с оценкой их кровоснабжения, что позволяет современная аппаратура [25, 26]. Методами лучевой диагностики, в отсутствие клинических проявлений заболевания, могут выявляться различные признаки диффузных (гиперплазия) или очаговых (полипы) изменений эндометрия [27, 28].
В настоящее время согласно клиническим рекомендациям Министерства здравоохранения РФ [29] и международным протоколам [30] за верхнюю границу нормы толщины М-эха принимают 4 мм. Если она ниже этой границы, то вероятность РЭ составляет менее 1% [31—34], в таких случаях биопсия эндометрия не требуется. В ряде случаев увеличение толщины эндометрия по данным УЗИ выявляется у женщин в постменопаузе в отсутствие симптомов заболевания. Однако тактика ведения в таких случаях окончательно не определена. Последнее обстоятельство особенно важно, поскольку в настоящее время среди исследователей прочно укоренилось мнение, что толщина эндометрия является ведущим признаком гиперплазии [35]. Однако в литературе появляются данные о необходимости изменения ультразвуковых критериев толщины эндометрия для определения дальнейшей тактики ведения женщин в отсутствие клинических проявлений в постменопаузе, так как выбор метода лечения и его применение порой ограничены из-за сопутствующей соматической патологии больных. Особые трудности возникают при лечении больных с ГЭ старше 60 лет ввиду высокого риска развития осложнений при оперативном вмешательстве и применении анестезиологического пособия. Поэтому необходимо разграничить группы пациенток с утолщенным эндометрием (по УЗИ в отсутствие клинических проявлений), которым обязательно должны проводиться дальнейшая диагностика и лечение, и группы пациенток, которые могут находиться под динамическим наблюдением (без риска развития РЭ) в связи с возрастом, наличием соматической патологии или нежеланием (отказом) пациентки от дальнейшего лечения (диагностического обследования).
Современные данные литературы о дифференциальной диагностике и тактике ведения женщин в пери- и постменопаузе с патологией эндометрия
В исследовании A. Lev-Sagie и соавт. [36] под наблюдением находились 82 женщины в постменопаузе со случайно выявленным при УЗИ утолщением эндометрия, всем выполнена гистероскопия с выскабливанием стенок полости матки. По результатам гистологического исследования, у 67 (82%) пациенток выявлены неактивные полипы, у 7 — субмукозные узлы, у 6 — атрофия эндометрия, у 1 — простая гиперплазия, еще у 1 — полип с простой гиперплазией. Ни одного случая сложной гиперплазии или РЭ не было. При этом частота развития осложнений оперативного вмешательства составила 3,6%: 2 перфорации матки, 1 осложнение интубации.
R. Ozelci и соавт. [37] проанализировали истории болезни 266 женщин в постменопаузе, которым были выполнены гистероскопия и биопсия эндометрия. В исследование были включены пациентки с отсутствим симптомов, у которых, по данным трансвагинального ультразвукового исследования (ТВУИ), толщина эндометрия равна или превышает 6 мм. По результатам гистологического исследования, наиболее часто выявляемыми очаговыми поражениями у пациенток в отсутствие симптоматики были полипы эндометрия, диагностированные в 168 (63,1%) наблюдениях. У 24 (9%) пациенток была диагностирована простая гиперплазия, у 4 (1%) — атипичная гиперплазия и у 8 (3%) — аденокарцинома эндометрия. По мнению авторов обзора, при толщине эндометрия ≥10,5 мм рекомендованы гистероскопия и кюретаж стенок полости матки.
Другие исследователи [38] провели ретроспективный анализ (с января 2006 г. по январь 2017 г.) медицинских карт 488 женщин в постменопаузе, не имевших клинических проявлений, у которых при ТВУИ выявили эндометрий толщиной ≥5 мм и провели гистероскопию с последующей биопсией эндометрия. Наиболее частыми патологическими находками были полипы (51,0%) и нормальный эндометрий (34,2%). У 15 (3,1%) и 10 (2,0%) больных имелась интраэпителиальная неоплазия и карцинома соответственно. Однако пациентки с карциномой обладали более толстым эндометрием, в котором чаще определялся кровоток при цветовом допплеровском картировании (ЦДК). В исследовании отмечено, что при злокачественных новообразованиях толщина эндометрия была ≥12 мм, и при ЦДК определялись локусы кровотока в эндометрии.
J. Alcázar и соавт. [39] изучили результаты исследований, опубликованных в период с января 1990 г. по декабрь 2016 г., и оценили корреляцию между толщиной эндометрия, измеренной с помощью ТВУИ, и гистологическими находками у женщин, не имевших клинических проявлений в постменопаузе. Научные работы, включавшие исследования у пациенток, которые принимали заместительную гормональную терапию, тамоксифен или ингибиторы ароматазы, были исключены. Было выявлено 289 исследований, и оценены данные по 4751 женщине. Распространенность РЭ или ГЭ с атипией составила 2,4%. В результате исследователи пришли к выводу, что риск развития РЭ или ГЭ с атипией был в 2,6 раза выше у женщин с толщиной эндометрия ≥11 мм в отличие от такового у женщин с толщиной эндометрия 5—10 мм, хотя имелись значительные расхождения в разных исследованиях.
A. Ghoubara и соавт. в своем исследовании [40] также пришли к выводу, что использование порога толщины эндометрия ≥10 мм у женщин без клинических симптомов позволяет не упустить ни одного случая атипичной ГЭ или РЭ.
Целью исследования M. Louie и соавт. [41] было уточнение частоты внутриматочной патологии у 462 женщин с бессимтомно протекающей постменопаузой, не имевших клинических ее проявлений, и обеспечение оптимального порога для взятия у них биоптата эндометрия. В исследование включали женщин без симптомов заболевания эндометрия, если при ТВУИ у них была выявлена толщина эндометрия выше 4 мм.
Среди 462 женщин карцинома была выявлена у 9 (1,9%), атипичная гиперплазия — у 7 (1,5%). Толщина эндометрия, равная или превышающая 14 мм, достоверно ассоциировалась с типичной гиперплазией (отношение шансов — ОШ 4,29; 95% доверительный интервал — ДИ 1,30—14,20; p=0,02), с отрицательным прогностическим значением 98,3%. Толщина более 15 мм была ассоциирована с карциномой (ОШ — 4,53; 95% ДИ — 1,20—17,20; p=0,03), с прогностической значимостью отрицательного результата теста 98,5% и риском развития рака 0,06%. Таким образом, исследователи пришли к выводу, что случайно обнаруженное утолщение эндометрия менее 15 мм не может служить основанием для взятия биопсии эндометрия у женщин в постменопаузе, не имеющих вагинального кровотечения.
W. Wolfman и соавт. [42] изучили материалы публикаций, вышедших с 1970 по 2009 г., о результатах обследования женщин в постменопаузе без аномальных маточных кровотечений, у которых при УЗИ обнаружено утолщение эндометрия. При детальной оценке информативности, рисков и стоимости диагностического выскабливания авторы пришли к выводу, что применение инвазивных методов исследования только на основании увеличения показателя М-эхо является излишней (неоправданной) процедурой.
Однако некоторые исследователи придерживаются другой точки зрения. Целью исследования M. Genc и соавт. [43] было уточнение частоты внутриматочной патологии у 283 женщин в постменопаузе, госпитализированных в гинекологическое отделение для проведения гистерэктомии по причинам, не связанным с патологией эндометрия. По результатам гистологического исследования, у 75,6% из 209 пациенток, не имевших кровотечения в постменопаузе, обнаружена патология полости матки, о которой не подозревали на этапе предоперационной подготовки: ГЭ, полипы, миома матки, аденомиоз — в 1 (0,5%) наблюдение, аденокарциномы. У 87,8% из 74 женщин с кровотечением в постменопаузе обнаружена внутриматочная патология, в том числе 13 (17,6%; p=0,0001) наблюдений РЭ. Таким образом, патология полости матки может иметься и у женщин в постменопаузе, не имеющих симптомов заболевания, поэтому авторы настаивают на ежегодном скрининге и консультировании пациенток пожилого и старческого возраста, не дожидаясь у них эпизода кровотечения.
Л.В. Адамян и соавт. [44] в своем исследовании пациенток без клинических проявлений внутриматочных заболеваний в постменопаузе с подозрением на патологию эндометрия по данным ТВУЗ (толщина эндометрия более 4 мм), чаще всего выявляли полипы эндометрия (63,9%), атрофию эндометрия (30,5%), а частота аденокарциномы составила 2,1%. Авторы исследования акцентируют внимание на том, что риск возникновения злокачественных новообразований достаточно высок, что свидетельствует о важности адекватного обследования и своевременного лечения женщин этой возрастной группы, а также о необходимости скринингового обследования с применением УЗИ.
По данным литературы, у пациенток без клинических проявлений заболевания матки в постменопаузе с утолщеным эндометрием (по данным УЗИ) наиболее часто при гистероскопии и гистологическом исследовании выявляются полипы эндометрия. Однако частота РЭ у женщин с полипами эндометрия составляет 0,3—4,8% [45]. Большинство исследователей настаивают на обращении особого внимания на пациенток в постменопаузе с полипами, проявляющимися маточным кровотечением. Так, E. Ricciardi и соавт. [46] изучали распространенность полипов с атипией у пациенток в постменопаузе. В ретроспективном исследовании проанализированы данные 1027 женщин с полипами эндометрия в пери- и постменопаузе. Доброкачественные полипы выявлены в 95,8% случаев, предраковые — в 2,67% и с атипией — в 1,54% случаев. У женщин в постменопаузе (старше 60 лет) и старческом возрасте риск развития РЭ был выше (ОШ 3,05; 95% ДИ 1,54—6,19; p
Новая технология противорецидивной гормональной терапии гиперпластических процессов эндометрия у женщин позднего репродуктивного возраста
Проведено исследование специфического связывания рецепторов прогестерона с синтетическими гестагенами у женщин позднего репродуктивного возраста. Разработана новая медицинская технология гесагенотерапии гиперпластических процессов эндометрия, позволяющая
The study on specific binding of progesterone receptors and synthetic gestogens in women of late childbearing age, was done. The new medical technology of gestogen therapy of hyperplastic processes of endometrium, which allows to reduce recurrence frequency, was developed.
.jpg)
Патогенез ГПЭ характеризуется сложным взаимодействием общих системных процессов и локальных изменений в эндометрии. В свете современных концепций в основе развития ГПЭ лежит гормональный дисбаланс, который выражается абсолютной или относительной гиперэстрогенемией [4–6]. Эндометрий является самой чувствительной тканью-мишенью половых гормонов. Исследования последних лет показали, что ведущую роль в развитии ГПЭ играет чувствительность слизистой оболочки матки к стероидным гормонам [2, 7–9]. Для противорецидивной терапии ГПЭ применяют гормональные препараты, состав и дозу которых выбирают в зависимости от результатов гистологического исследования соскоба эндометрия, сочетанных гинекологических и соматических заболеваний, возраста женщины и индивидуальной переносимости препарата. В практическом здравоохранении у пациенток позднего репродуктивного возраста наиболее часто используются синтетические гестагены. Однако, по литературным данным, отсутствие эффекта от гестагенотерапии при ГПЭ варьирует от 25,9% до 78,0% [6, 10].
Резервом повышения эффективности терапии ГПЭ является индивидуальный выбор препаратов. Для осуществления персонализованного подбора гормональной терапии мы предложили использовать силу связывания препарата с рецепторами прогестерона из ткани эндометрия конкретной пациентки. Данное предположение основано на тезисе, что сила связывания лиганда с рецептором определяет эффект от лечения, то есть чем выше связывание гестагенов с прогестерон-связывающими участками, тем лучший эффект ожидается от лечения.
С целью проверки данной гипотезы на кафедре молекулярной фармакологии и радиобиологии им. академика П. В. Сергеева ГБОУ ВПО РНИМУ им. Н. И. Пирогова совместно с МОНИИАГ было проведено исследование специфического связывания рецепторов прогестерона с синтетическими гестагенами у женщин позднего репродуктивного возраста с гиперпластическими процессами эндометрия. Проведенные в отделении гинекологической эндокринологии исследования показали, что выбор гестагена с учетом индивидуальной чувствительности эндометрия к препарату позволил значительно снизить частоту рецидивов железистой гиперплазии эндометрия [4, 5, 7]. По результатам исследования была разработана новая медицинская технология и получен патент на изобретение «Способ гестагенотерапии гиперпластических процессов эндометрия» [11].
Материал и методы исследования
В исследование вошли 164 женщины позднего репродуктивного возраста. Критериями включения в исследование явились: наличие ГПЭ (простой железистой гиперплазии и/или железистых полипов эндометрия), отсутствие тяжелой соматической патологии и выраженных метаболических нарушений, препятствующих проведению противорецидивной гормональной терапии.
Клинические методы исследования включали общее стандартное гинекологическое обследование женщин: осмотр шейки матки в зеркалах, влагалищное бимануальное исследование, трансвагинальное ультразвуковое сканирование органов малого таза (на 5–8 день менструального цикла), мазок на флору и ЗППП. Ультразвуковое сканирование органов малого таза у пациенток позднего репродуктивного возраста проводилось на базе НКО МОНИИАГ, аппаратом Siemens Sequoia 512 с использованием вагинального датчика от 6 до 8 мГц, в режиме двухмерной визуализации.
Ткань эндометрия для определения цитозольных рецепторов половых стероидов получали во время выскабливания стенок полости матки при использовании серийного аппарата Circon Acmi на базе эндоскопического отделения МОНИИАГ или путем эндорам-биопсии.
Уровень рецепторов прогестерона и специфическое связывание стандартных гестагенов с прогестерон-связывающими участками определяли в цитозоле биоптатов эндометрия по методу [12].
Цитозольную фракцию получали стандартным методом с помощью ультрацентрифугирования (105 000 g, ультрацентрифуга UP-65 M, 60’). Уровень рецепторов прогестерона (РП) и специфическое связывание гестагенов с прогестерон-связывающими участками определяли в цитозоле биоптатов эндометрия радиолигандным методом [13].
Белок определяли методом Лоури.
Статистическую обработку материала проводили на персональном компьютере, в работе использовалась программа GraphPad Prism 5.0 и стандартные методы статистического анализа.
Результаты и обсуждение
Из 136 обследованных пациенток с ГПЭ 73 (54%) были с рецидивирующим течением (в анамнезе от 1 до 6 раздельных диагностических выскабливаний (РДВ) слизистой стенок матки и цервикального канала), у остальных 63 женщин (46%) гиперплазия эндометрия была выявлена впервые.
В контрольную группу вошли 28 женщин (без измененного эндометрия), в группу с ГПЭ вошли 73 пациентки, при гистологическом исследовании у 51 (37,5%) пациентки были диагностированы железистые полипы эндометрия, а у 85 — простая железистая гиперплазия эндометрия.
У пациенток с ГПЭ в 112 случаях (82%) были гормонзависимые заболевания гениталий (миома матки и/или эндометриоз различной локализации), 58% обследуемых женщин имели избыточную массу тела (ИМТ ≥ 25).
37 (27,2%) пациенткам с ГЭ проводили гистероскопию с РДВ во II фазу менструального цикла в условиях МОНИИАГ. 99 (73%) женщинам РДВ с или без гистероскопии было проведено по месту жительства.
Уровень РП в эндометрии изменялся в зависимости от нозологической формы гиперплазии. Так, при полипах эндометрия средняя величина этого параметра снизилась в 1,4 раза по сравнению с нормой и составила в среднем 16,9 ± 3,7 фмоль/мг белка, а при железистой гиперплазии эндометрия — в 1,2 раза и равнялась 19,2 ± 5,6 фмоль/мг белка (р ≤ 0,05).
В качестве тестируемых гестагенов использовались: медроксипрогестерона ацетат, норэтистерон, дидрогестерон. Приведенные гестагены выбраны по принципу различий структуры и наличия доступных лекарственных форм. Уровень рецепторов прогестерона в цитозоле эндометрия, как и сила специфического связывания с гестагенами, варьировали в широких пределах. При этом усредненные данные показали, что наибольшую силу связывания продемонстрировал медроксипрогестерона ацетат (64,6 ± 7,2 при полипах эндометрия и 73,8 ± 5,2 при гиперплазии (р ≤ 0,001)), наименьшую — норэтистерон (52,7 ± 4,1 при полипах эндометрия и 60,3 ± 2,6 при гиперплазии (р ≤ 0,001)).
При исследовании были выделены следующие группы: контрольная группа (I группа) — 28 пациенток; женщины с рецидивирующим течением ГПЭ, которым была назначена гормональная противорецидивная терапия по методу слепой выборки (II группа) — 41 пациентка; женщины с рецидивирующим течением ГПЭ, которым назначалась гормональная противорецидивная терапия с учетом результатов связывающей активности гестагенов с прогестерон-связывающими участками (III группа) — 32 пациентки.
II группе была назначена гормональная противорецидивная терапия с использованием препаратов, в состав которых входят тестируемые гестагены. Эффективность терапии пациенток данной группы (отсутствие рецидивов в течение 6 месяцев по окончании лечения) сравнивали с результатами индивидуального тестирования аффинитета рецепторов прогестерона, полученных из эндометрия пациенток до начала лечения.
III группе была назначена гормональная терапия с учетом результатов связывающей активности гестагенов с прогестерон-связывающими участками цитозоля эндометрия конкретной пациентки.
Все пациентки, имеющие рецидивирующее течение заболевания, получали:
Оценка эффективности гормональной терапии проводилась по клиническим симптомам, а также по результатам трансвагинального ультразвукового сканирования органов малого таза на 3-м и 6-м месяцах гормональной терапии. Ультразвуковое исследование проводили на 4–8 день менструального цикла, толщина эндометрия считалась нормальной при значениях 0,3–0,6 см, если же она превышала данные значения, то проводилась гистероскопия для уточнения диагноза.
В результате клинико-лабораторного исследования показано, что во II группе частота рецидивов составила 17,1%, в то время как в III группе частота рецидивов составила 6,3%.
Сравнительный анализ противорецидивной эффективности синтетических гестагенов в проведенном исследовании показал, что количество рецидивов при использовании норэтистерона было максимально и составило 18 через 3 месяца во II группе, тогда как при терапии медроксипрогестерона ацетатом рецидивов обнаружено не было через 3 и 6 месяцев.
Выводы
Таким образом, нами рекомендуется алгоритм проведения персонализированной противорецидивной гормональной терапии по схеме, представленной на рис. 2.
Медико-социальная эффективность
Снижение частоты рецидивов гиперпластических процессов эндометрия у женщин позднего репродуктивного возраста ведет к:
Таким образом, предложенная медицинская технология представляет собой подбор индивидуальной гормональной терапии гиперпластических процессов эндометрия на основании индивидуальной оценки связывающих свойств рецепторов прогестерона эндометрия.
Работа выполнена в рамках программы развития НИУ ГБОУ ВПО РНИМУ им Н. И. Пирогова, 2010–2019, приоритетное направление развития ПНР-2, персонализированная медицина.
Литература
В. И. Краснопольский*, доктор медицинских наук, профессор, член-корреспондент РАМН
Н. Д. Гаспарян*, доктор медицинских наук, профессор
Л. С. Логутова*, доктор медициинских наук, профессор
Е. Н. Карева**, доктор медицинских наук, профессор
О. С. Горенкова*, кандидат медицинских наук
Д. А. Тихонов**
*ГБУЗ Московской области МОНИИАГ,
**ГБОУ ВПО РНИМУ им. Н. И. Пирогова, Москва
Гиперплазия эндометрия матки
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Эндометрий представляет собой нежную тонкую слизистую ткань, которая выстилает полость матки изнутри. Данная ткань каждый месяц быстро растет и утолщается под действием женских половых гормонов. В случае наступления беременности, эндометрий является «пуховой периной» на которую прикрепляется оплодотворенная яйцеклетка. При отсутствии беременности под действием гормонов эндометрий отторгается, выходит в виде менструальной крови.
Классификация гиперплазии эндометрия по локализации
Классификация гиперплазии эндометрия (по гистологической картине)
Причины гиперплазии эндометрия
В настоящее время основной причиной развития гиперплазии считается нарушение баланса женских половых гормонов, который чаще всего встречается в пубертатном периоде и перименопаузе.
Факторы риска развития гиперплазии эндометрия
Симптомы, которые встречаются при гиперплазии эндометрия
Основные из них при гиперплазии эндометрия могут быть:
Обследования, которые помогут выявить и поставить диагноз гиперплазии эндометрия
Лечение гиперплазии эндометрия
Практически в 100% случаев лечение гиперплазии эндометрия хирургическое.
Методами хирургического лечения гиперплазии эндометрия является гистероскопия и гистерорезектоскопия.
Данная операция проводится под общей анестезией. Продолжительность операции не превышает 30 минут, короткий период нахождения под общей анестезией позволяет врачам в тот же день отпустить пациентку домой.
Осложнения гиперплазии
При отсутствии должного и адекватного лечения гиперплазия эндометрия приводит к тяжелой анемии с значительным снижением уровня гемоглобина, появлению слабости, повышенной усталости, сонливости, что связано с большими потерями крови во время менструации. У молодых женщин гиперплазия эндометрия может быть причиной бесплодия и невынашивания беременности. Отдельные формы гиперплазии эндометрия (железистая и кистозная гиперплазии эндометрия) являются предраковым состоянием и в случае длительного наблюдения, при отсутствии лечения, могут переродиться в рак матки.
Профилактические мероприятия при данном заболевании необходимы для того, чтобы снизить риск развития рака эндометрия и предотвратить рецидив гиперплазии.
Гиперплазия эндометрия. Часто задаваемые вопросы
1. Что это такое? Доброкачественный процесс, который характеризуется чрезмерным разрастанием внутреннего слоя матки.
2. Из-за чего она возникает? Из-за постоянного воздействия полового гормона эстрогена на эндометрий, который вызывает его чрезмерное разрастание. Гиперэстрогения возникает из-за нарушения центральной регулиции менструального цикла, гормонопродуцирующих опухолей яичников, неправильного использования гормональных препаратов, дефицита прогестерона (гормон II фазы менструального цикла), обладающего антипролиферативным действием, так же в результате ановуляторных циклов.
3. Это распространенное заболевание? Частота встречаемости в структуре гинекологической заболеваемости 15-50%. По данным обращаемости пациенток частота встречаемости ГПЭ- 30%. В позднем репродуктивном возрасте и в перименопаузе встречается с частотой- 50%
4. Это заболевание очень опасно? Пристального внимания врачей заслуживают:
При отсутствии должного лечения гиперплазия эндометрия может приводить к серьезным маточным кровотечениям, со снижением гемоглобина крови и вытекающими отсюда последствиями.
5. Возможно ли забеременеть на фоне гиперплазии эндометрия? Ответ – нет. Гиперплазия эндометрия не возникает спонтанно, это следствие нарушений в репродуктивной системе женщины. Нарушение баланса между звеньями регуляции менструального цикла вызывает избыток эстрогенов в организме женщины, нехватку прогестерона, вследствие этого отсутствие овуляции (выхода яйцеклетки из фолликула для оплодотворения). Так же сам эндометрий структурно изменен, поэтому является неблагоприятным для имплантации (прикрепление плодного яйца к стенке матки).
7. Как диагностировать атипическую гиперплазию эндометрия? Большую информацию врач получает при опросе пациентки во время общения (возраст менархе или время наступления менопаузы, все особенности менструального цикла- его длительность, характер выделений и т.д.).
УЗ-исследование в зависимости от периода жизни женщины, а также фазы менструального цикла может дать информацию о состоянии эндометрия. По этим данным можно заподозрить проблему, однако подтвердить или опровергнуть атипию в клетках эндометрия нельзя. Только проведение гистероскопии с последующим гистологическим исследованием материала является золотым стандартом для диагностики этого состояния. Информативность метода более 90%.
8. Обязательно ли проводить выскабливание эндометрия при гиперплазии? Раздельное выскабливание цервикального канала и полости матки несет за собой лечебный и диагностический характер. Механическое удаление измененной патогенной ткани из полости матки предотвращает маточное кровотечение, что составляет лечебный эффект. Полученный соскоб отправляется на гистологическое исследование, после которого будет дано заключение о характере ткани, наличии или отсутствии признаков злокачественного поражения.
9. Возможен ли рецидив гиперплазии эндометрия? Да, возможен. Так как причиной гиперплазии эндометрия является нарушение гормонального баланса в организме женщины, то требуется обследование её гормонального фона. Для профилактики рецидива необходимо соответствующее лечение и исключение факторов риска.
Гиперплазия эндометрия – симптомы и лечение

Основная причина чрезмерного разрастания эндометрия – это повышенная выработка эстрогенов и недостаток прогестерона. Чаще всего, данная патология диагностируется у женщин в предменопаузе и у девочек- подростков. Оба состояния связаны с гормональной перестройкой организма. Для гиперплазии эндометрия характерен ановуляторный цикл – отсутствие овуляции.
Что может спровоцировать гиперплазию эндометрия?

Какие симптомы характерны для гиперплазии эндометрия?
Все эти симптомы могут сопровождать миому матки или даже выкидыш на раннем сроке, поэтому необходимо сделать УЗИ малого таза, чтобы определить причину нециклических выделений.
Способы диагностики гиперплазии эндометрия
Узи органов малого таза влагалищным датчиком определяет толщину эндометрия. Толщина эндометрия меняется на протяжении всего цикла, в период перед месячными фиксируется самое высокое значение. Для диагностики следует проводить УЗИ в первой половине цикла, обычно на 7-10 день. Толщина свыше 15 мм дает повод заподозрить патологию и направить пациентку на гистероскопию – внутреннее обследование матки гистероскопом (специальным оптическим прибором), сопровождающееся диагностическим выскабливанием эндометрия и исследование полученного материала для типирования гиперплазии. Так УЗИ дает лишь 68 процентов информативности при гиперплазии, а для гистероскопии это значение достигает 94 процентов.
Аспирационная биопсия – еще один метод диагностики, когда кусочек эндометрия, взятый из полости матки, направляется на гистологическое исследование.
В некоторых случаях гинеколог может направить пациентку на анализ крови на гормоны: эстроген и прогестерон, гормоны щитовидной железы и надпочечников.
Лечение гиперплазии.
Самым эффективным способом лечения гиперплазии эндометрия является раздельное диагностическое выскабливание. Проводится в условиях стационара, обычно под наркозом. Затем полученный эндометрий отправляется на гистологию, и в зависимости от полученного результата исследования назначается гормональное лечение.
Гормонотерапия нужна для подавления разрастания эндометрия и регулирования гормонального фона. Гормональное лечение зависит от возраста пациентки. Так женщинам до 35 лет назначают комбинированные оральные контрацептивы.
Лечение гестагенами – еще один способ гормонотерапии, подходит для лечения гиперплазии эндометрия любого типа. Спираль Мирена – это один из таких вариантов. Но существует и таблетированная форма – это назначение препаратов Утрожестан или Дюфастон.
Не следует пренебрегать гормональной терапией, так как процент рецидивов высок (полипы могут возникнуть вновь после их удаления и не один раз), а обильные кровотечения осложняются анемией.
Диагностическая и лечебная тактика у пациенток с патологией эндометрия в периоде перименопаузы
Какие методы исследования применяются на первом диагностическом этапе при обследовании женщин с отягощенным онкоанамнезом в перименопаузе? Какие дополнительные методы исследования можно применять для уточнения диагноза? Рисунок 1. Железиста
Какие методы исследования применяются на первом диагностическом этапе при обследовании женщин с отягощенным онкоанамнезом в перименопаузе?
Какие дополнительные методы исследования можно применять для уточнения диагноза?
 |
| Рисунок 1. Железистая гиперплазия эндометрия климактерического периода (трансабдоминальное сканирование) |
Предшествующий менопаузе продолжительный период постепенного перехода к полному угасанию репродуктивной функции женщины имеет свои особые характеристики, проявляющиеся в изменении отдельных звеньев нейрогуморального контроля функций определенных органов и систем.
На современном уровне развития медицинской науки удается регистрировать самые незначительные отклонения в «нормальном» течении данного процесса с позиции обнаружения патологических изменений, требующих своевременной медицинской коррекции для профилактики предшественников и рака эндометрия.
До сегодняшнего дня в гинекологии не удается радикально изменить онкоэпидемиологическую ситуацию и разработать стратегию, которая позволила бы решить проблему ранней диагностики и эффективного лечения рака эндометрия — опухоли, уносящей ежегодно более 5 тыс. жизней. При этом нельзя не отметить, что вопросы ранней диагностики рака эндометрия в менопаузе решаются достаточно эффективно ввиду разработки и внедрения оптимального алгоритма диагностического исследования.
Между тем возникновение патологических состояний эндометрия начинается задолго до наступления менопаузы, чему предшествует не только широкий спектр доброкачественных заболеваний органов женской половой системы, но и определенный, наследуемый по родительской линии генетический фон, что в совокупности позволяет создать диагностический алгоритм раннего обнаружения предшественников и начального рака эндометрия.
Период перименопаузы остается еще недостаточно изученным по совокупности оценки нейрогуморальных процессов, происходящих в организме женщины и проявляющихся в органах-мишенях, одним из которых является матка и собственно эндометрий.
Нельзя не отметить, что различные аспекты проблемы перименопаузального периода постоянно находятся в зоне повышенного внимания онкологов. Это касается и вопросов выяснения причин аномальных маточных кровотечений этого периода, изучения состояния эндометрия с помощью современных диагностических методов — УЗИ, гистероскопии, МРТ и морфологического исследования, а также определения терапевтической тактики при сопутствующих перименопаузе симптомах и заболеваниях, включая тонкие методы генного анализа и др.
 |
| Рисунок 2. Диагностические маршруты больных с гиперпластическими процессами эндометрия в перименопаузальный период |
Поэтому важно формирование индивидуализированной концепции клинического подхода к признакам патологических состояний этого периода, и в частности аномальных маточных кровотечений, доминирующими причинами развития которых являются гиперпластические процессы и рак эндометрия.
Диагностическое выскабливание, традиционно выполняемое при аномальных маточных кровотечениях, оказывается малоэффективным в диагностике начальных форм рака эндометрия, провоцирует развитие внутреннего эндометриоза, миомы матки, усугубляя и осложняя их течение, что экономически обременительно для гинекологических стационаров.
Вместе с тем практически повсеместное назначение гормонотерапии при гиперпластических процессах, сопровождающихся аномальными маточными кровотечениями, в свою очередь не всегда оправданно, так как существенно повышает стоимость лечения и может оказывать отрицательное влияние на психосоматическое состояние больных, обострять течение хронических заболеваний органов сердечно-сосудистой системы и свертывающей системы крови.
Поэтому сегодня необходимо совершенствование традиционных подходов к диагностике и лечению больных с гиперпластическими процессами эндометрия в перименопаузальном периоде, сопровождающимися аномальными маточными кровотечениями, в строгом соответствии с возрастными характеристиками обследуемых и учетом факторов риска.
Научное рассмотрение данной проблемы, в частности, стало возможным благодаря привлечению современных подходов к оценке реальной клинической ситуации с использованием возможностей компьютерного анкетирования, трансабдоминальной/трансвагинальной сонографии, цветного доплеровского картирования, гистероскопии с прицельной биопсией и морфологического изучения картины эндометрия в периоде перименопаузы в сочетании с анализом результатов остеоденситометрии.
На основе привлеченного клинического материала, обобщающего наблюдения за 392 женщинами в возрасте 45-55 лет в перименопаузальном периоде, нами изучены признаки, характеризующие состояние эндометрия в перименопаузальном периоде в сочетании с оценкой показателей минеральной плотности костной ткани.
Рассматривая ультразвуковое исследование основным, неинвазивным и безвредным, что позволяет применять метод многократно, исследовали объем и качество диагностической информации, предоставляемой с его помощью у женщин перименопаузального периода. При проведении этих работ были выявлены следующие моменты, касающиеся больных с клиникой аномальных маточных кровотечений.
1. Традиционное трансабдоминальное сканирование должно являться первым диагностическим этапом при появлении каких-либо симптомов в течение перименопаузального периода и обязательным для пациенток данной возрастной группы (45-55 лет), особенно при наличии положительных онкоанамнестических данных.
Этот метод позволил установить без диагностического выскабливания подслизистую миому (27,6%), внутренний эндометриоз (9,2%) и в сочетании с аспирационной биопсией — атрофию эндометрия (36,2%), а также осуществлять динамическое наблюдение за больными в рамках диагностического центра.
2. Стойкое увеличение размеров срединных маточных структур (М-эхо) более 7 мм с эхографическими признаками нечеткости М-эхо (появление гиперэхогенных структур и утрата визуализируемой границы эндометрий — миометрий) у 19,3% обследованных потребовало подключения уточняющих современных ультразвуковых технологий — трансвагинального УЗИ, доплеровского цветного картирования. Это позволило уточнить размеры и структуру эндометрия, обнаружить наличие полипов эндометрия (14,3%), а также зон эндометрия, наиболее подозрительных с позиции пролиферативных процессов, не свойственных данному периоду жизни женщины, — атипическая гиперплазия — у 3%, рак эндометрия — у 2% обследованных.
Эффективность трансабдоминального УЗИ в перименопаузальном периоде составила по критерию точности 82,5%, чувствительности — 78,4% и специфичности — 87,3%. Эти показатели выявили целесообразность использования примерно у 15% больных перименопаузального периода возможностей трансвагинального и доплеровского УЗИ, подтвердивших, что размеры М-эхо, устойчиво определяемые при динамическом УЗИ в перименопаузе 6-8 мм с утратой четкости контура эндометрий/миометрий свидетельствуют о вероятности злокачественной трансформации, что особенно согласуется с динамическим снижением индекса резистентности с 0,6-0,8 до 0,4-0,5 при доплеровском сканировании.
 |
| Рисунок 3. Клинические подходы к индивидуальному лечению гинекологической патологии перименопаузального периода |
По данным морфологического исследования, причинами кровотечений в перименопаузальном периоде была и атрофия эндометрия — 5,1%, и полипоз эндометрия — 14,3%, а в части случаев — рак эндометрия — 2%. Однако у большинства больных имели место гиперпластические процессы эндометрия, среди которых потенциальная опасность, по нашим данным, связана с морфологическими признаками эстрогенной стимуляции — 98 (25%) обследованных. Наличие повышенной минеральной плотности костной ткани у таких больных (7,4% из числа обследованных) явилось одной из причин их включения в группу риска по онкопатологии эндометрия.
Таким образом, для периода перименопаузы характерны следующие признаки состояния эндометрия:
Морфологические признаки атипической гиперплазии, обнаруживающиеся в процессе мониторинга при длительном приеме прогестагенов, также свидетельствуют о персистенции патологического процесса, особенно в конце перименопаузального периода.
На основе анализа полученных данных были разработаны индивидуальные диагностические маршруты, позволившие с привлечением соответствующих современных методов исследования уточнить состояние эндометрия у каждой конкретной больной на основе принципов функционально щадящего лечения, исключив применение инвазивных и агрессивных методик при отсутствии объективных медицинских показаний к их использованию.
Интерпретация полученных нами клинико-диагностических данных дала возможность распределить всех обследуемых в перименопаузе пациенток, как обращающихся впервые, так и направленных специалистами других областей, на три самостоятельных потока:
1. Благоприятный анамнез и показатели УЗИ, морфологического исследования аспирата и минеральной плотности костной ткани (М-эхо менее 7 мм, четкие границы; морфология аспирата — атрофия, гиперплазия эндометрия с децидуоподобной реакцией; нормальная или сниженная минеральная плотность костной ткани) ограничивают объем диагностических мероприятий ежегодным трансабдоминальным УЗ-контролем;
2. У женщин до 50 лет с благоприятным онкоанамнезом и показателями трансабдоминального и трасвагинального УЗИ и денситометрии (остеопения, остеопороз, норма) с морфологически верифицированной железистой, железисто-кистозной гиперплазией эндометрия с/без микрофокусов атипической гиперплазии эндометрия в начале перименопаузального периода возможно консервативное ведение с УЗ-контролем в условиях цветного доплеровского картирования с гистероскопией и прицельной биопсией эндометрия;
3. УЗ-признаки увеличения М-эхо с появлением его гетерогенности, снижением индекса резистентности менее 0,5 и атипической гиперваскуляризацией в сочетании с морфологической картиной атипической гиперплазии 2-3-й степени и повышением минеральной плотности костной ткани — специальное лечение.
Была разработана индивидуальная терапевтическая тактика для пациенток перименопаузального периода с различными показателями комплексного динамического диагностического исследования:
1. При благоприятном онкоанамнезе, УЗ-признаках нормального течения перименопаузы или атрофии эндометрия специальное лечение не показано;
2. УЗ-признаки симптомной миомы матки и симптомного внутреннего эндометриоза (неэффективное гормональное лечение) не требуют диагностического выскабливания, а состояние эндометрия оценивают по результатам аспирационной биопсии (по показаниям после гистероскопии) — хирургическое лечение в гинекологическом стационаре;
3. УЗ-признаки гиперплазии эндометрия у больных моложе 50 лет при благоприятном онкоанамнезе и морфологической картине железистой гиперплазии с фокусами атипической гиперплазии 1-й степени и индексом резистентности более 0,5 позволили на I этапе, после терапевтической аблации эндометрия, ограничиться гормонотерапией прогестагенами и ультразвуковым контролем каждые три месяца в условиях диагностического центра;
4. Ультразвуковые морфологические признаки прогрессирующей атипической гиперплазии эндометрия перименопаузального периода требуют хирургического лечения в специализированном стационаре.
Таким образом, данная стратегия позволяет повысить эффективность обнаружения доброкачественных и злокачественных заболеваний эндометрия с обоснованным привлечением современных диагностических методов, а также индивидуализировать тактику ведения женщин перименопаузального периода с патологическими процессами эндометрия.
Диагноз: гиперплазия эндометрия
Поделиться:
Не знаю, «страшно» ли звучит диагноз «гиперплазия эндометрия», но встречается он, во всяком случае, часто. Такой диагноз могут поставить по результатам обследования женщинам с аномальными маточными кровотечениями. Обильные и продолжительные менструации, короткие (менее 24 дней от начала одной менструации до начала другой) циклы, кровянистые выделения из половых путей после менопаузы — серьезный повод для обращения к врачу.
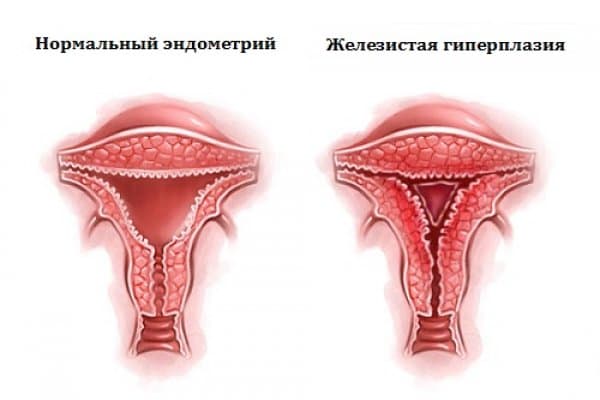
Что значит «гиперплазия»
Эндометрий — внутренняя функционально-активная оболочка матки. На протяжении менструального цикла эндометрий претерпевает ряд циклических изменений, чтобы принять в свои объятия плодное яйцо. Эстрогены в первой фазе цикла заставляют его расти и «толстеть», а прогестерон после овуляции превращает эндометрий в мягкую подстилку. Если беременность не наступила, уровень прогестерона стремительно снижается, давая сигнал «ничего не получилось, сворачиваем подготовку». По сути, менструация — это отторжение эндометрия для того, чтобы начать новый цикл с новой надеждой.
Читайте также:
Болезненные месячные: что делать?
Гиперплазия — это слишком толстый эндометрий. Из-за того, что он очень сильно «растолстел», менструации превращаются в обильные кровотечения. Чаще всего это бывает в ситуациях, когда не происходят овуляции. Нет овуляции, значит, в яичнике не сформируется желтое тело — орган, вырабатывающий прогестерон. Нет прогестерона, значит, эндометрий растет, толстеет, грубеет, но не превращается в нежную подушку, которая могла бы принять плодное яйцо либо спокойно отторгнуться, если беременность не случилась.
Кто в группе риска
Есть несколько категорий женщин, у которых с большой вероятностью может быть гиперплазия:
К развитию гиперплазии эндометрия может привести применение высоких доз эстрогенов, препаратов с антиэстрогенным действием (тамоксифен) или прием препаратов с эстрогеноподобным действием. Гормонпродуцирующие опухоли, иммуносупрессию, инфекции тоже относят к причинам развития заболевания.
Почти всегда это не рак
Симптомы гиперплазии эндометрия очень похожи на клиническую картину рака эндометрия. Более того, раньше мы считали, что любая гиперплазия — предраковое заболевание. Сейчас мнение ученых изменилось. По современной классификации различают две разновидности заболевания: простая (гиперплазия без атипии) и атипическая гиперплазия.
Оказалось, что истинный предрак — атипическая (или аденоматозная) гиперплазия эндометрия — чаще всего не «вырастает» из простой формы, а сразу формируется недоброкачественно. Риск развития рака эндометрия при гиперплазии эндометрия без атипии составляет менее 5 % в течение 20 лет, поэтому серьезных поводов для беспокойства нет. Атипическая гиперплазия встречается реже, но прогноз у этого состояния хуже: риск превращения в рак эндометрия составляет 8 % случаев за 4 года, 27,5 % — за 20 лет. Безусловно, подходы к лечению разных форм будут отличаться, поэтому самое главное — правильно поставить диагноз.
Как ставят диагноз
Диагностика начинается с трансвагинального ультразвукового исследования. Если эндометрий слишком «толстый», необходимо получить образец для гистологического исследования. Раньше всем пациенткам выполняли «чистку» — выскабливание полости матки. Многие женщины до сих пор считают, что «чистка» — это лечение гиперпластических процессов в эндометрии. На самом деле с помощью выскабливания врачи останавливали кровотечение и получали материал для гистологии.
В нашей стране пока не написаны и не утверждены клинические рекомендации по этому заболеванию, поэтому врачам приходится ориентироваться на последние рекомендации по этой проблеме, выпущенные в Великобритании Royal College of Obstetricians and Gynaecologists (RCOG) в 2017 году.
Согласно этим рекомендациям, для гистологического подтверждения лучше всего использовать биопсию эндометрия (с помощью пайпеля или мануальной вакуум-аспирации), которую следует выполнять в амбулаторных условиях. Если это невозможно или полученные результаты неинформативны, проводят диагностическую гистероскопию (осмотр полости матки изнутри с прицельной биопсией под контролем зрения) или выскабливание полости матки. Гистероскопия становится методом выбора при очаговых поражениях (например, при полипах).
Применение дорогостоящих методов — компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) или различных биомаркеров — нецелесообразно, потому что пока нет уверенности, что сложные методы диагностики имеют какие-то существенные преимущества перед рутинными процедурами.
Как гиперплазия эндометрия лечится?
Лечение простой гиперплазии эндометрия заключается в применении гормонотерапии. В зависимости от возраста, сопутствующих заболеваний и репродуктивных планов могут быть применены эстроген-гестагенные контрацептивы или аналоги прогестерона. Удобным способом доставки лекарства непосредственно в полость матки может быть гормонвыделяющая ВМС «Мирена».
При атипической гиперплазии эндометрия методом выбора считают удаление матки. Однако если пациентка молода и планирует беременность, возможно проведение гормонотерапии под строгим врачебным контролем с частыми биопсиями эндометрия. Очень важно, чтобы диагноз «атипическая гиперплазия» был тщательно верифицирован. Для этого стекла и блоки повторно пересматривают врачи-патологоанатомы, специализирующиеся на диагностике рака.
При бессимптомной простой гиперплазии (нет кровотечений, беременность не планируется, диагноз — случайная находка) возможна наблюдательная тактика. Если нет дополнительных факторов риска (таких как ожирение, нерегулярные менструации, применение высоких доз эстрогенов), заболевание может спонтанно регрессировать.

_575.gif)
.gif)
 Читайте также:
Читайте также: 

