Чем лечить кишечный аденовирус
Роспотребнадзор (стенд)
Роспотребнадзор (стенд)
Аденовирусный энтерит
Аденовирусный энтерит
Согласно имеющимся наблюдениям, гастроэнтериты могут вызывать кишечные аденовирусы, относящиеся к серотипам 40 и 41, которые входят в группу F. Из-за недостаточности проведенных исследований на сегодняшний день трудно определить удельный вес аденовирусных гастроэнтеритов в общей структуре вирусных гастроэнтеритов. Если еще в конце 80-х годов им отводили второе место после ротавирусной инфекции в структуре гастроэнтеритов у детей, то в 90-х годах была установлена доминирующая роль калицивирусов. В ходе исследований, проводившихся в Европе, Азии, Северной и Южной Америке, было показано, что кишечные аденовирусы могут вызывать от 2 до 22% случаев гастроэнтеритов у детей в возрасте до 2 лет.
Что провоцирует Аденовирусный энтерит:
Патогенез (что происходит?) во время Аденовирусного энтерита:
Несмотря на способность кишечных аденовирусов к эпидемическому распространению, сезонность развития заболевания, тем не менее, не доказана. Как правило, кишечные аденовирусы становятся причиной заболевания детей до 2-летнего возраста, причем наиболее высок риск заболеть у детей до года. Вирусы могут иметь нозокомиальное распространение, вызывая вспышки заболевания в стационарах. Среди взрослого контингента развитие гастроэнтерита не описано, хотя вполне возможно, что при контакте с больными детьми взрослые инфицируются и переносят субклинические формы инфекции.
Симптомы Аденовирусного энтерита:
Инкубационный период составляет от 8 до 10 дней.
В отличие от других вирусных гастроэнтеритов кишечные аденовирусы вызывают более длительное заболевание (от 5 до 12 дней, а иногда и до 14 дней).
Принципиальное отличие кишечных аденовирусов от респираторных в том, что у больных не развиваются такие типичные клинические признаки, как назофарингит и кератоконъюнктивит, хотя виремия у этих больных также регистрируется.
Заболевание характеризуется умеренно выраженной интоксикацией, невысокой температурой, сохраняющейся в течение нескольких дней. В тех случаях, когда заболевание продолжается до 2 недель, у больных чаще регистрируется лихорадка неправильного типа, которая иногда носит волнообразный характер.
Диспепсические проявления в виде рвоты и диареи выражены умеренно и сохраняются 1-3 дня и более. Больные значительно чаще, чем при других вирусных гастроэнтеритов, отмечают боль в животе, которая бывает обусловлена увеличением мезентериальных лимфоузлов. Описаны случаи, когда лихорадка и боли в животе были чуть ли не единственными проявлениями аденовирусного гастроэнтерита.
В ряде случаев у больных одновременно с признаками гастроэнтерита могут выявляться изменения со стороны респираторного тракта, однако механизмы и характер формирующейся патологии изучены недостаточно.
Прогноз
Заболевание проходит самостоятельно практически без осложнений.
Диагностика Аденовирусного энтерита:
Лабораторная диагностика основана на обнаружении специфического антигена вируса в кале с помощью ИФА. Реже выделяют вирус в культуре клеток. Для определения серотипа используют реакцию нейтрализации цитопатического эффекта с соответствующей антисывороткой. Для ретроспективной диагностики в РТГА исследуют парные сыворотки, взятые на 1-5-й и 15-20-й день болезни. Также используется РСК.
Лечение Аденовирусного энтерита:
Лечение больных с аденовирусным гастроэнтеритом строится на принципах патогенетической терапии. Выбор наиболее оптимального способа лечения больных зависит от своевременной диагностики, а точнее, лабораторной верификации вирусного генеза заболевания.
Из немедикаментозных методов лечения важное место отводится диетотерапии, что определяется патофизиологическими механизмами развития диарейного синдрома. На высоте клинических проявлений заболевания следует исключить из пищи молоко и молочные продукты, ограничить прием углеводов, сахара, овощей и фруктов. По мере купирования клинических признаков заболевания диета постепенно расширяется. Учитывая, что в острый период заболевания у больных формируется ферментопатия, целесообразно назначать им комбинированные ферментные препараты, такие, как фестал, панзинорм, мезим форте и другие. Обоснованной является также терапия адсорбирующими и вяжущими препаратами, которые, в частности, способствуют оформлению кала и урежению кратности дефекации, хотя это мало влияет на развитие дегидратации. К числу таких средств относятся полифепан, смекта, препараты висмута и другие.
В литературе имеются указания на положительное влияние на течение аденовирусного гастроэнтерита различных пробиотиков. Патофизиологическим обоснованием их применения у больных с аденовирусным гастроэнтеритом служит тот факт, что штаммы, входящие в состав пробиотиков, самым непосредственным образом участвуют в процессах пищеварения, обмена веществ и детоксикации. Кроме того, у больных могут выявляться дисбиотические изменения в кишечнике.
Поскольку основным проявлением аденовирусного гастроэнтерита, определяющим тяжесть течения заболевания, является дегидратация, купирование обезвоживания составляет основу патогенетической терапии. Принципы регидратационной терапии на сегодняшний день разработаны достаточно хорошо и носят универсальный характер. В зависимости от степени дегидратации регидратацию проводят пероральным или внутривенным способом.
Пероральная регидратационная терапия проводится в том случае, если у больных отсутствуют выраженные системные проявления обезвоживания. Она проводится глюкозоэлектролитными растворами (цитроглюкосоланом, регидроном и другими), которые принимаются дробно, по 1–1,5 л в час.
Внутривенная терапия назначается больным в случае выраженных системных проявлений или при наличии неукротимой рвоты, затрудняющей оральную регидратацию. Эта терапия проводится сбалансированными полиионными кристаллоидными растворами, такими, как трисоль, квартасоль, хлосоль и другие. Объем вводимых растворов и скорость их введения определяются степенью обезвоживания. В тех случаях, когда у больных проявления интоксикации доминируют над симптомами обезвоживания, допускается введение коллоидных растворов (гемодеза, реополиглюкина и других).
Лечение аденовирусной инфекции у детей с применением ингаляций
Рассмотрены патогенез и клинические симптомы аденовирусной инфекции у детей, описаны подходы к терапии с применением отхаркивающих и иммунотропных препаратов.
Pathogenesis and clinical symptoms of adenovirus infection in children are examined, approaches to therapy with the application of the expectorant and immunotropic preparations are described.
Аденовирусная инфекция (АВ) (МКБ-10: В57) — острое инфекционное заболевание с преимущественным поражением носоглотки, конъюнктивы и лимфоидной ткани. АВ протекает с умеренной интоксикацией, лихорадкой, катаральным синдромом с выраженным экссудативным компонентом [1–3].
Аденовирусы, которые вызывают заболевание у детей, относятся к семейству Adenoviridae, роду Mastadenovirus ДНК-содержащих вирусов средних размеров. В настоящее время выделено около 50 серотипов этого вируса. Наиболее частыми возбудителями аденовирусной инфекции являются 3-й и 7-й серотипы. Аденовирусы обладают тропностью к эпителию дыхательных путей, кишечника и конъюнктивы, а также способностью поражать лимфоидную ткань. Токсичность вирусов этой группы низкая [2].
Источником инфекции является больной или вирусоноситель, пути передачи — воздушно-капельный, водный («болезнь плавательных бассейнов»), а также фекально-оральный. Наиболее восприимчивы к этому вирусу дети от 6 месяцев до 3 лет. АВ регистрируют повсеместно и круглогодично с подъемом заболеваемости в холодное время года. Заболевания наблюдаются в виде спорадических случаев и эпидемических вспышек, для которых характерно медленное развитие и длительное течение. Иммунитет после перенесенного заболевания типоспецифический, продолжительный. Аденовирусы относительно устойчивы в окружающей среде, сохраняются в течение нескольких недель в воде, лекарственных растворах, на предметах обихода, резистентны к эфиру. Разрушаются при температуре +56 °С в течение 30 мин, погибают под воздействием ультрафиолетового облучения и хлорсодержащих препаратов [2, 3].
При заражении вирусы проникают в организм через слизистые оболочки дыхательных путей, а также эпителий тонкой кишки. Благодаря своей лимфотропности, возбудитель внедряется в носоглотку, миндалины, конъюнктиву и вызывает формирование воспалительных очагов. В ходе заболевания увеличиваются все лимфатические узлы, в том числе мезентериальные, возникает гепатоспленомегалия. Инкубационный период длится 4–7 дней. Течение заболевания медленное, волнообразное. Характерен респираторный синдром, конъюнктивит, которые протекают с выраженным экссудативным компонентом. Диарея присоединяется обычно у детей до 2 лет и носит водянистый характер [1].
Патогномоничная форма аденовирусной инфекции — аденофарингоконъюнктивальная лихорадка. Она протекает с подъемом температуры тела до 38–39 °С на протяжении 5–10 дней, фарингитом с зернистостью задней стенки глотки, увеличением и гиперемией миндалин, конъюнктивитом. Нередко развивается тонзиллит, проявляющийся гипертрофией, отечностью и умеренной гиперемией миндалин, а также аденоидит. В ряде случаев на задней стенке глотки, небных миндалинах появляются нежные белесоватые налеты (пленчатый фарингит и тонзиллит) [1, 2].
С первых дней болезни нередко развивается кашель. Характерным для аденовирусной инфекции является синдром полиаденита — увеличение шейных и подчелюстных лимфатических узлов. Наблюдается увеличение печени и селезенки. Возможно развитие мононуклеозоподобного синдрома, для которого характерно сочетание пленчатого тонзиллита, полиаденита и гепатоспленомегалии. Длительность катарального синдрома — 10–15 дней, иногда до 3–4 недель [2, 3].
АВ — одна из распространенных респираторных вирусных инфекций, активно участвующих в формировании у ребенка адекватного противоинфекционного иммунитета, важного для всей последующей жизни.
При нормальном функционировании иммунной системы происходит эффективное взаимодействие интерферона и других лимфокинов, макрофагов, лимфоцитов, специфических антител, приводящее к элиминации возбудителя из макроорганизма и клиническому выздоровлению.
У ребенка раннего возраста направленность иммунной защиты организма изначально носит супрессивный характер. Невысокая активность собственного неспецифического звена иммунитета необходима для профилактики ярких воспалительных реакций, которые могут быстро истощить организм ребенка и привести его к развитию дезадаптации и декомпенсации систем жизнедеятельности. Специфическое звено иммунитета ребенка обусловливает пассивная иммунная защита в виде иммуноглобулинов, транслированных через плаценту, а также попадающих к ребенку вместе с молоком матери при грудном вскармливании.
Формирование надежной и адекватной естественной защиты с преобладанием популяции Тh1-лимфоцитов возможно только при непосредственном контакте ребенка с различными вирусами и «отработке» его иммунной системой паттерна воспалительной реакции, клинически выраженной чаще всего катаральным синдромом с кашлем и лихорадкой. Все проявления острых респираторных инфекций: лихорадка, ринит, кашель, гиперемия сводов зева — носят защитный характер и должны в первую очередь рассматриваться именно в этом контексте, а не представляться досадными помехами, которые надо немедленно купировать. Лихорадка — защитная реакция организма. Только на фоне лихорадки организм дает адекватный иммунный ответ Т-хелперов 1-го типа — продукцию γ-интерферона, интерлейкина-2, фактора некроза опухоли-α, стимулирующих выработку IgG.
Проникновение вируса в организм ребенка запускает каскад иммунных реакций, способствующих стимуляции нейроиммуноэндокринной системы, которая в дальнейшем регулирует процессы дифференцировки и созревания нейроэндокринной оси (рис.).
Защитные реакции кашля и выделения слизи из носовых ходов позволяют качественно осуществить очищение и увлажнение слизистой оболочки дыхательных путей, необходимые для адекватного функционирования мерцательного эпителия. Выделяемая из дыхательных путей мокрота к тому же содержит бесценный материал для выработки специфического иммунитета — фагоциты, которые определили возбудителя и экспрессировали специфические рецепторы для включения в работу высокоспециализированных клеток иммунной системы — лимфоцитов. При заглатывании ребенком мокроты лимфоидная ткань кишечника получает информацию о возбудителе и стимул к выработке регуляторных пептидов.
Покраснение сводов зева сопровождает прилив к слизистой оболочке крови, несущей компоненты гуморального и клеточного иммунитета, и искусственное «тушение» противовоспалительной местной терапией этого проявления неспецифической иммунной реакции мешает первичному этапу иммунной реакции запустить каскад иммунных реакций.
Медикаментозно «притушив» эти проявления, мы никогда не сможем заменить их лекарственными средствами, так как они индивидуальны и адекватны именно этому ребенку с его наследственностью, жизненным опытом и условиями проживания.
К сожалению, отсутствие четкого представления о необходимости некоторого временного периода, в течение которого все неспецифические иммунные процессы должны развернуться и принять участие в формировании гармоничного и полноценного иммунного ответа, в настоящее время приводит к необдуманной агрессивной терапии, целью которой является скорейшее купирование симптомов. По данным С. В. Ключникова (2012), каждому пятому ребенку в возрасте до 1 года назначались антибиотики (в том числе гентамицин, линкомицин). К возрасту 3 года число детей, получавших антибиотики, увеличивается до 28% и достигает 80% к семилетнему возрасту.
Необдуманное применение антибиотиков, недопустимо стремительное купирование естественных проявлений неспецифической иммунной защиты (лихорадка, насморк, кашель, гиперемия и отек сводов зева) ведут к снижению качества защитной биологической пленки на слизистой оболочке дыхательных путей.
В отделении раннего возраста педиатрической клиники МОНИКИ было проведено сравнение результатов микробиологического обследования двух групп детей в возрасте от 4 до 6 лет. Группы были выделены при анкетировании родителей, которым были заданы следующие вопросы:
Дети, родители которых на все вопросы ответили утвердительно, составили первую группу (20 человек). Дети, родители которых ответили на все вопросы, кроме первого и последнего, отрицательно, вошли во вторую группу (15 человек).
Во второй группе количество детей, в мазке которых была выделена грибковая флора, не превысило 11% (2 человека из 15 обследованных), а биотоп был более разнообразным и плотным (8 наименований микробов, количество нормальной флоры 5–6 × 10 5 КОЕ/мл).
По этой причине агрессивное лечение острых респираторных инфекций и резкое неприятие родителями информации о существовании этапа в жизни ребенка, когда частые острые респираторные вирусные инфекции необходимы для его дальнейшего развития, в настоящее время являются базой для полипрагмазии, а организм ребенка становится полигоном для битвы многочисленных лекарственных средств.
Вместе с тем специфической противовирусной терапии при аденовирусной инфекции нет. Антибактериальная терапия в данном случае не показана. В период лихорадки назначают постельный режим, полноценное питание, обильное питье. Рекомендуется давать обильное горячее питье, чай, кисели, теплые морсы и компоты. Симптоматическое лечение включает применение жаропонижающих средств при лихорадке выше 38,5 °С. Если температура ребенка ниже 37,5 °С, нет необходимости в ее снижении медикаментозными препаратами. При более высокой температуре можно применять физические методы охлаждения. На внутреннюю поверхность рук, бедер, боковую поверхность шеи можно прикладывать смоченные в холодной воде компрессы. При насморке можно промывать нос слабым солевым раствором с помощью шприца или закапывать в нос сосудосуживающие капли. Следует избегать длительного применения капель (не более 5–7 дней), так как они могут вызвать временную дисфункцию слизистой оболочки [3, 4].
Оптимальными средствами для элиминации слизистой оболочки, восстановления ее влажности и создания наилучших условий для функционирования эпителия и слизистых клеток, вырабатывающих иммуноглобулин, лизоцим, лактоферрин и другие ферменты, являются изотонические растворы морской воды (Аква Марис, Физиомер, Долфин и пр.). Содержащиеся в морской воде микроэлементы (селен, йод, цинк) ускоряют регенерацию слизистой оболочки.
При выраженном сухом кашле можно начать лечение с приема грудного сбора в виде горячего отвара. Помогает также щелочное питье в виде горячего молока с небольшим количеством (на кончике ложки) соды. Если ребенок отказывается от молока, можно поить его подогретыми щелочными минеральными водами. Если кашель носит влажный характер с трудно отхаркивающейся мокротой, можно применять отхаркивающие препараты, если кашель длительный, сухой, саднящий — целесообразнее будет применять препараты, подавляющие кашель [4].
В лечении кашля при аденовирусной инфекции важно учитывать, что он может быть как сухим (характерное покашливание при гранулезном фарингите), так и с выраженным отделением мокроты. Поэтому препарат для адекватного сопровождения этого симптома должен быть направлен и на стимуляцию отделения мокроты, и на своевременную поддержку регенерации слизистой оболочки, и при этом должен иметь удовлетворяющие ребенка органолептические характеристики и удобный способ применения. Этим условиям соответствует Амбробене (амброксола гидрохлорид) — муколитический препарат с отхаркивающим действием, который обладает секретомоторным, секретолитическим и отхаркивающим свойствами.
Важным достоинством препарата является продуманное разнообразие лекарственных форм. Это дает преимущества в лечении детей любого возраста, поддерживает оптимальную комплаентность родителей и позволяет достичь адекватности в терапии респираторного синдрома у детей.
Например, можно использовать амброксола гидрохлорид в виде сиропов (детям от 5 до 12 лет — 1 мерная ложка (15 мг) — 2–3 раза в день; детям от 2 до 5 лет — 1/2 мерной ложки (7,5 мл) — 3 раза в день, детям до 2 лет — 1/2 мерной ложки (7,5 мл) после еды 2 раза в день).
Ингаляционная терапия имеет преимущества перед другими формами в том, что она совмещает элиминационные свойства (очищение верхних дыхательных путей от патологического содержимого), увлажнение слизистой оболочки и достаточную глубину проникновения для очищения более нижних отделов органов дыхания и таким образом профилактирует рефлекторный бронхоспазм при избытке мокроты. Лекарственное вещество распыляется и в виде аэрозоля оседает на слизистых оболочках верхних дыхательных путей. При этом возрастает интенсивность всасывания в подслизистом слое верхних дыхательных путей и увеличивается его депонирование.
Раствор для ингаляций применяется в зависимости от возраста детям от 5 до 12 лет — 2 мл (15 мг) — 2–3 раза в день; детям младше 5 лет — 1 мл (7,5 мл) — 3 раза в день.
В терапии аденовирусной инфекции можно использовать также иммунотропные препараты (Кипферон, Виферон, ИРС-19, Деринат), регулирующие неспецифические иммунные реакции (интерфероногенез) и дополняющие реакцию организма наличием специфических антител к представителям флоры, которые могут спровоцировать осложнения в виде пневмонии, бронхитов, синуситов.
Таким образом, обдуманная и максимально индивидуальная поддержка естественных защитных реакций организма ребенка при аденовирусной инфекции позволит сохранить и приумножить защитные силы организма ребенка.
Литература
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
«Болит горло и живот», или что вы знаете об аденовирусе
В период сезонных ОРВИ кашель и боль в горле – явление «ожидаемое». Но что, если традиционные симптомы респираторных заболеваний сочетаются с диареей или рвотой? Возможно – это аденовирусная инфекция.
Особые признаки
Аденовирус, в отличие от многих респираторных вирусов, поражает не только дыхательные пути, но и слизистую тонкого кишечника. Кроме того, «под удар» попадает конъюнктива глаза.
При этом, если кишечных симптомов за всю инфекцию может так и не развиться, то «характерные» глаза – важный отличительный признак аденовируса.
Где можно заразиться
Аденовирус отличается крайне высокой заразностью и устойчивостью во внешней среде. А источником заражения могут стать больные люди или предметы обихода, на которых вирус сохраняет активность до 8 дней.
«Подхватить» вирус можно даже в бассейне, при недостаточной дезинфекции воды. И, очевидно, эта вирусная инфекция не редкость в детских коллективах.
Насколько это опасно
Аденовирусная инфекция, в большинстве случаев, угрозы здоровью и жизни не представляет. И обычно завершается без последствий через 7-14 дней. Тогда как у ослабленных пациентов инфекция может затягиваться и достигать 6 недель.
У этой же категории пациентов чаще всего развиваются осложнения, в виде:
Однако эксперты Роспотребназора отмечают, что осложнения аденовирусной инфекции всегда связаны с присоединением патогенной бактериальной флоры (стафило-, стрептококки и другие).
Как выявить аденовирус
Классическая симптоматика аденовирусной инфекции, как правило, не требует дополнительных анализов. А к помощи лабораторных методов диагностики в основном прибегают на самой ранней стадии инфекционного процесса или в случае сомнений в диагнозе.
Наиболее информативным анализом в этом случае служит ПЦР-диагностика материала (мазок из зева или кал) на аденовирус.
Исследование можно заказать отдельно или сразу в комплексе с другими ОРВИ-вирусами (например, «ОРВИ-Скрин»), что позволит сразу же провести дифференциальную диагностику. Правда методика ПЦР резко теряет в достоверности, если уже начато лечение, как местного (полоскания, спреи), так и общего характера.
Этих недостатков лишен анализ крови на антитела IgA к аденовирусу.
Они появляются в крови в начальном периоде заболевания, и некоторое время продолжают циркулировать после выздоровления.
Однако дети, как известно, анализы крови «не любят», поэтому такой формат обследования скорее подходит для взрослых.
Вирусные гастроэнтериты
Oстрые кишечные инфекции (ОКИ), несмотря на успехи медицины, до сих пор остаются одной из наиболее значимых проблем здравоохранения во всех без исключения странах мира [16]. По частоте распространенности они уступают лишь гриппу, а также острым респирато
Oстрые кишечные инфекции (ОКИ), несмотря на успехи медицины, до сих пор остаются одной из наиболее значимых проблем здравоохранения во всех без исключения странах мира [16]. По частоте распространенности они уступают лишь гриппу, а также острым респираторно-вирусным инфекциям. Наиболее высокий уровень заболеваемости и смертности от ОКИ регистрируется в развивающихся странах, однако эпидемиологические исследования последних лет свидетельствуют, что и в индустриально развитых странах проблема ОКИ также стоит достаточно остро. Согласно недавно опубликованным данным, в Великобритании около 20% населения ежегодно переносят ОКИ [22]. По данным американских исследователей, общее число регистрируемых ежегодно случаев ОКИ составляет 250-300 млн, около 450 тыс. взрослых и 160 тыс. детей госпитализируются в стационары и более 4000 случаев заканчиваются летальным исходом [15, 17].
Причиной развития ОКИ могут быть различные микроорганизмы, в том числе бактерии, вирусы и паразиты. Прогресс лабораторных методов диагностики позволил существенно расширить наши представления об этиологических факторах [21]. Согласно общепринятому мнению, этиологическое значение вирусов особенно велико у больных с гастроэнтеритами (ГЭ).
Этиология. Этиологическая расшифровка гастроэнтеритов способствовала выделению из стула больных различных вирусов, однако роль многих из них в развитии заболевания до сих пор до конца не выяснена. Причастность вирусов к развитию ГЭ определяется сегодня на основании следующих критериев [13]: значительно более частое обнаружение вируса в стуле больных с диареей, чем в группе здоровых лиц; развитие специфической иммунной реакции организма на данный вирус в процессе развития заболевания; установление факта санации организма от вируса в периоде реконвалесценции.
В табл. 1 представлены современные сведения относительно роли различных вирусов, обнаруживаемых в стуле, в развитии ГЭ.
Ротавирусы
Ротавирусы традиционно рассматриваются как один из ведущих этиологических факторов ГЭ в мире [1, 2, 3, 5].
Род ротавирусов включает в себя большое количество вирусов, которые вызывают ГЭ не только у людей, но и у других млекопитающих, а также птиц. Вирион состоит из ядра, включающего геном, представленный 11 фрагментированными сегментами двунитчатой РНК, окруженной сложной белковой оболочкой. В зависимости от состава протеинов капсида ротавирусы разделяют на группы, подгруппы и серотипы. Ротавирусы подразделяются на 7 больших групп, которые обозначаются буквами латинского алфавита (от А до G). Наибольшее значение в патологии человека имеет группа А, хотя регистрируются заболевания, обусловленные группами В и С.
Эпидемиология. Ротавирусы имеют повсеместное распространение. Считается, что до 95% всех детей в возрасте от 3 до 5 лет инфицируются ротавирусами [10]. Раньше полагали, что ротавирусная инфекция (РИ) встречается преимущественно у детей, однако современные эпидемиологические данные свидетельствуют о том, что РИ все чаще обнаруживается и у взрослого населения [4]. Вероятно, это может быть следствием качественного улучшения лабораторной диагностики. Наиболее часто вспышки РИ бывают обусловлены группой А, хотя, по имеющимся наблюдениям, зарегистрированы крупные вспышки заболеваемости, обусловленные ротавирусами группы В. Спорадические же случаи заболевания, как правило, вызываются ротавирусами группы С.
Несмотря на высокую степень гомологичности ротавирусов, выделяемых у людей и животных, источником инфекции при РИ является только человек. Возможность передачи вируса от животных к человеку пока не доказана. Установлено, что переболевший человек способен выделять ротавирус с фекалиями в течение 30 и более дней после клинического выздоровления, причем этот период может значительно удлиняться, особенно у лиц с иммунодефицитами. Наиболее интенсивное выделение вируса регистрируется в острый период заболевания или в первую неделю после инфицирования.
Таким образом, фекально-оральный путь представляет собой основной механизм распространения возбудителя, который может реализовываться всеми типичными для данного механизма путями (контактным, водным и пищевым). Кроме того, выделение вируса во внешнюю среду может осуществляться и с секретом дыхательных путей. О том, что существует множество механизмов распространения РИ, может косвенно свидетельствовать тот факт, что инфекция быстро распространяется на значительные территории, особенно в весенний период.
Для РИ типична сезонность заболеваемости, которая зависит от климатогеографических условий. В большинстве стран, в том числе и в России, подъем заболеваемости отмечается осенью и весной, хотя спорадические случаи заболевания могут регистрироваться в течение всего года.
Патогенез. Ротавирус, попадая в кишечник, внедряется в клетки ворсинчатого эпителия преимущественно верхних отделов тонкой кишки, где происходит его репликация. По мере репликации вируса происходит повреждение и слущивание эпителиальных клеток с выделением вируса в просвет кишечника, что и обусловливает последующее поражение дистальных отделов тонкой кишки. Распространение инфекции вплоть до проксимального отдела тонкой кишки происходит в течение первых двух дней заболевания. Повреждение клеток ворсинчатого эпителия сопровождается нарушением пищеварительной и абсорбционной функций тонкой кишки. Диарейный синдром у больных при РИ обусловлен накоплением в просвете кишечника осмолярно-активных веществ. Хотя ротавирусы могут обнаруживаться в собственной пластинке и даже регионарных лиматических узлах, тем не менее данные, свидетельствующие об их способности реплицироваться в этих отделах, отсутствуют. Как правило, у больных без признаков иммунодефицита РИ развивается только в слизистой оболочке тонкой кишки.
Формирование вирусспецифического иммунитета после перенесенной РИ способствует санации организма от вируса [7].
Клиника. Наиболее часто РИ регистрируется у детей в возрасте от 3 месяцев до 3 лет. Именно тогда наиболее высок риск тяжелого течения заболевания, сопровождающегося развитием дегидратации и требующего госпитализации. По современным представлениям, от 12 до 71% (среднее 34%) всех случаев госпитализации детей до 2 лет обусловлены именно РИ [8]. До 3-месячного возраста дети, как правило, не болеют РИ, что объясняется наличием у них трансплацентарных антител. У взрослых РИ в большинстве случаев протекает субклинически. Однако у отдельных контингентов взрослых больных, таких, как лица пожилого возраста, лица, имеющие признаки иммунодефицита, включая ВИЧ-инфекцию, родители, ухаживающие за больными детьми, путешественники, заболевание имеет типичные проявления.
Инкубационный период при РИ составляет от одного до трех дней. Обычно у взрослых РИ клинически манифестирует в форме гастроэнтерита или энтерита. Как и в случаях заболевания другими формами инфекционного гастроэнтерита, клиническая картина РИ лишена каких-либо характерных проявлений, что существенно затрудняет проведение дифференциального диагноза, особенно на ранних стадиях.
Обычно заболевание начинается остро, с подъема температуры тела до фебрильных цифр, а в отдельных случаях и выше. При легком течении лихорадка нетипична, и у больных может отмечаться лишь субфебрильная температура. Температурная реакция обычно бывает непродолжительной (2–4 дня). Интоксикационный синдром носит неспецифический характер и характеризуется такими симптомами, как слабость, недомогание, утомляемость, озноб, головная боль, миалгии и др. В большинстве случаев развернутая клиническая картина заболевания выявляется уже в первые сутки.
Признаки гастроэнтерита появляются у больных практически одновременно с интоксикационным синдромом и характеризуются урчанием и неприятными ощущениями (чувство дискомфорта) в области живота, болью в животе, снижением аппетита, тошнотой, повторной рвотой и частым жидким стулом. При РИ боль в животе не столь типична, как неприятные ощущения в животе (чувство дискомфорта), и регистрируется только в 30–40% случаев. Боль в животе чаще носит диффузный характер, но может локализоваться в эпигастральной области. Урчанию в животе часто сопутствуют болевые ощущения.
Тошнота и рвота у больных с РИ, по данным разных авторов, наблюдаются в 68–85% случаев, что зависит от тяжести течения заболевания.
Диарейный синдром носит более выраженный характер и выявляется у всех больных с клинически манифестными формами РИ с первого дня заболевания. Стул, как правило, бывает относительно обильным, водянистым, желтоватого цвета и зловонным без патологических примесей. Почти в половине случаев отмечается пенистость стула. Кратность дефекаций может быть различной — от 2–3 раз до 10–15 и даже более раз в сутки, что зависит от тяжести течения заболевания. Позывы к дефекации носят императивный характер. Диарейный синдром обычно бывает непродолжительным, нормализация стула в большинстве случаев наступает не позднее 5–6-го дня болезни. По многочисленным наблюдениям, у большинства взрослых пациентов прекращение диареи регистрируется к 3-му дню, а при легком течении — и ко 2-му дню заболевания.
Хотя увеличение печени и селезенки для РИ не типично, тем не менее в отдельных случаях, особенно у детей, эти признаки могут выявляться.
Несмотря на то что тяжесть течения РИ определяется выраженностью интоксикационного синдрома и гастроэнтерита, следует помнить, что далеко не во всех случаях эти два синдромокомплекса бывают выражены в равной степени. Как и при других видах инфекционных гастроэнтеритов, у отдельных больных могут доминировать признаки либо интоксикации, либо гастроэнтерита (обезвоживания).
В клинических исследованиях последних лет большое внимание уделяется респираторному синдрому как важному дифференциально-диагностическому признаку, выявляемому у больных РИ в остром периоде заболевания. Обычно больные жалуются на насморк, заложенность носа, першение в горле, сухой кашель, а при объективном обследовании выявляются гиперемия и зернистость мягкого неба, передних дужек, язычка, задней стенки глотки. Катаральные явления бывают непродолжительными и полностью купируются через 3–4 дня. Поскольку вспышки РИ могут по времени совпадать с подъемом заболеваемости гриппом и другими острыми респираторно-вирусными инфекциями, врачи общей практики, не имея возможности провести адекватное лабораторное обследование больных, нередко ставят больным диагноз «грипп с кишечным синдромом», ошибочно полагая, что катаральные явления не типичны для РИ.
Бытует мнение, что РИ у взрослых протекает преимущественно в легкой и среднетяжелой формах; тем не менее нельзя исключать и возможность тяжелого течения заболевания. Факторами риска тяжелого течения РИ являются сопутствующие соматические заболевания, микст-инфекция, дети моложе 1,5 лет и пожилой возраст.
Осложнения для РИ не типичны. Имеются единичные наблюдения, свидетельствующие о возможном развитии энцефалопатии и вторичных бактериальных осложнений у детей.
Калицивирусы человека
Несмотря на то что именно представители калицивирусов впервые были идентифицированы как возбудители вирусных ГЭ, тем не менее они по-прежнему изучены хуже, чем ротавирусы, что связано со сложностями в их культивировании и идентификации.
Впервые выделенный из кала Norwalk-вирус на основании морфологической картины был отнесен к группе малых, округлых, структурированных вирусов [12]. Только в начале 90-х годов, когда удалось клонировать Norwalk-вирус и секвестрировать его геном, появилась реальная возможность изучения его таксономического положения и разработки современных методов молекулярной диагностики. Проведенные исследования позволили установить два основных патогенных для человека рода вирусов — Norwalk-подобный и Sapporo-подобный, которые входят в семейство Caliciviridae. В роде Norwalk-подобного вируса выделяют две геногруппы.
Эпидемиология. Калицивирусы на сегодняшний день рассматриваются как основные возбудители острых небактериальных ГЭ в различных странах мира, на долю которых приходится до 90% всех случаев заболевания [9, 19]. Причем, как показывают исследования последних лет, они ответственны не только за групповые, но и за спорадические случаи заболевания [9, 11].
Несмотря на широкое распространение калицивирусов в природе, источником инфекции при ГЭ являются только больные лица или вирусоносители. В ходе исследований было установлено, что выделение вируса с калом во внешнюю среду начинается уже через 15 часов после инфицирования. Длительность выделения вируса с калом составляет до 2 недель. Основной механизм передачи возбудителя — фекально-оральный, который наиболее часто реализуется водным и пищевым путем. Кроме того, установлено, что инфицирование может происходить контактным и аэрогенным путями. При контактном пути передачи возбудителя важное значение могут иметь такие факторы внешней среды, как дверные ручки, телефонные трубки, краны в душевых комнатах и др. Исключительно высокая скорость распространения возбудителя при некоторых вспышках заболевания объясняется тем, что вирус распространяется аэрогенным путем.
В отличие от РИ для ГЭ, обусловленных Norwalk-подобным вирусом, сезонность не типична.
Патогенез. Несмотря на то что многие стороны патогенеза остаются неясными, клинические данные свидетельствуют о том, что характер поражения слизистой желудочно-кишечного тракта у больных с ГЭ, обусловленными ротавирусами и Norwalk-подобными вирусами, имеет сходные черты. В частности, развитие диарейного синдрома обусловлено, прежде всего, вторичной дисахаридазной недостаточностью вследствие поражения вирусами проксимальных отделов тонкой кишки. Исследования, проведенные на волонтерах, показывают, что у больных с ГЭ также отмечается нарушение моторной функции желудка, тогда как изменения в слизистой желудка отсутствуют.
Клиника. Инкубационный период составляет от 12 до 48 ч.
Инфекция, обусловленная калицивирусами, как и при РИ, часто может протекать бессимптомно. В типичных случаях заболевание протекает по типу гастроэнтерита. Для Norwalk-вирусной инфекции характерно острейшее начало заболевания — температура в течение 6–8 ч повышается до высоких цифр, отмечаются озноб, ломота в теле, миалгии, головокружение, головная боль. Появляются тошнота и рвота, часто многократная. На высоте интоксикации у пациентов появляются боли в животе и жидкий стул, кратность которого в течение суток достигает 5–8, а иногда и более.
На фоне острейшего развития заболевания и быстрого нарастания интоксикации у больных может отмечаться ортостатический коллапс.
При объективном обследовании обращают на себя внимание бледность кожных покровов, выраженная слабость и адинамия. Достаточно часто у больных наблюдаются катаральные явления со стороны верхних дыхательных путей и заложенность носа.
Особенностью течения Norwalk-вирусной инфекции является кратковременность клинических признаков заболевания. В большинстве случаев уже через 1–2 дня от начала заболевания отмечается купирование клинических признаков болезни. Состояние больных очень быстро полностью восстанавливается.
Следует иметь в виду, что на пике клинических признаков болезни пациентов целесообразно госпитализировать, поскольку они часто нуждаются в дезинтоксикационной и регидратационной терапии.
Кишечные аденовирусы
Согласно имеющимся наблюдениям, ГЭ могут вызывать кишечные аденовирусы, относящиеся к серотипам 40 и 41, которые входят в группу F. Из-за недостаточности проведенных исследований на сегодняшний день трудно определить удельный вес аденовирусных ГЭ в общей структуре вирусных ГЭ. Если еще в конце 80-х годов им отводили второе место после РИ в структуре ГЭ у детей, то в 90-х годах была установлена доминирующая роль калицивирусов. В ходе исследований, проводившихся в Европе, Азии, Северной и Южной Америке, было показано, что кишечные аденовирусы могут вызывать от 2 до 22% случаев ГЭ у детей в возрасте до 2 лет.
Эпидемиология. Несмотря на способность кишечных аденовирусов к эпидемическому распространению, сезонность развития заболевания, тем не менее, не доказана. Как правило, кишечные аденовирусы становятся причиной заболевания детей до 2-летнего возраста, причем наиболее высок риск заболеть у детей до года. Вирусы могут иметь нозокомиальное распространение, вызывая вспышки заболевания в стационарах. Среди взрослого контингента развитие ГЭ не описано, хотя вполне возможно, что при контакте с больными детьми взрослые инфицируются и переносят субклинические формы инфекции.
Механизм передачи инфекции изучен недостаточно. Полагают, что основной путь передачи вируса — контактный.
Клиника. Инкубационный период составляет от 8 до 10 дней.
В отличие от других вирусных ГЭ кишечные аденовирусы вызывают более длительное заболевание (от 5 до 12 дней, а иногда и до 14 дней).
Принципиальное отличие кишечных аденовирусов от респираторных в том, что у больных не развиваются такие типичные клинические признаки, как назофарингит и кератоконъюнктивит, хотя виремия у этих больных также регистрируется.
Заболевание характеризуется умеренно выраженной интоксикацией, невысокой температурой, сохраняющейся в течение нескольких дней. В тех случаях, когда заболевание продолжается до 2 недель, у больных чаще регистрируется лихорадка неправильного типа, которая иногда носит волнообразный характер.
Диспепсические проявления в виде рвоты и диареи выражены умеренно и сохраняются 1-3 дня и более. Больные значительно чаще, чем при других вирусных ГЭ, отмечают боль в животе, которая бывает обусловлена увеличением мезентериальных лимфоузлов. Описаны случаи, когда лихорадка и боли в животе были чуть ли не единственными проявлениями аденовирусного ГЭ.
В ряде случаев у больных одновременно с признаками ГЭ могут выявляться изменения со стороны респираторного тракта, однако механизмы и характер формирующейся патологии изучены недостаточно.
Астровирусы
Изучение роли астровирусов в развитии острых небактериальных ГЭ началось в 1975 году, когда при использовании метода электронной микроскопии их впервые удалось обнаружить в стуле детей с диареями. При изучении распространенности астровирусной инфекции среди детей по обнаружению сывороточных антител удалось установить, что до 71% детей в возрасте от 3 до 4 лет имеют антитела к астровирусам, хотя в анамнезе у них признаки заболевания отсутствовали. Интересные данные получены в ходе исследования, в котором приняли участие 17 взрослых [14]. Было установлено, что астровирусы обладают низкой патогенностью, поскольку, несмотря на инфицирование, клинические признаки заболевания были зарегистрированы только у одного человека, тогда как антительный ответ выявлялся у большинства испытуемых.
На сегодняшний день идентифицировано 8 серотипов астровирусов, из которых только один серотип (HAstV-1) имеет существенное значение в развитии патологии человека.
Только благодаря разработке современных методов диагностики появилась возможность изучения особенностей течения астровирусной инфекции.
Эпидемиология. Изучение этиологической структуры вирусных ГЭ у детей в возрасте от 2 месяцев до 2 лет, проведенное в Японии, позволило установить, что доля астровирусов составляет около 10% [20]. Популяционный мониторинг заболеваемости астровирусными ГЭ, проведенный в Египте в период с 1995 по 1998 год на 397 детях в возрасте до 3 лет, показал, что количество эпизодов болезни в год у детей до 6 месяцев составляет 0,38; в возрасте от 6 до 11 месяцев — 0,40; от 12 до 23 месяцев — 0,16 и от 24 до 35 месяцев — 0,05 [18]. Таким образом, накопленные данные позволяют сделать заключение, что астровирусной инфекцией болеют преимущественно дети до 7 лет, причем наиболее часто заболевание регистрируется у детей до года.
Исследование, проведенное в Египте [18], показало, что по своей эпидемиологической значимости (в сторону уменьшения) астровирусы могут быть расположены следующим образом: HAstV-1; HAstV-5; HAstV-8; HAstV-3; HAstV-6; HAstV-4; HAstV-2.
Согласно имеющимся наблюдениям, сезонность при астровирусных ГЭ не типична. Путь распространения возбудителя — контактный.
Клиника. Инкубационный период при астровирусных ГЭ составляет 1–2 дня. Достаточно часто, даже при установленном инфицировании и обнаружении астровирусов в стуле, у детей отсутствуют клинические признаки заболевания, что свидетельствует о превалировании бессимптомных форм инфекции.
Клинически развитие болезни напоминает РИ, хотя протекает более легко с превалированием водянистой диареи.
В последние годы все чаще стали обращать внимание на возрастающее значение астровирусов в развитии диарей у лиц с иммунодефицитами, включая ВИЧ-инфекцию, а также при нозокомиальных инфекциях.
Диагностика вирусных гастроэнтеритов
Поскольку клиническая картина при вирусных ГЭ отличается неспецифичностью, диагноз должен подтверждаться лабораторными исследованиями. Принципы диагностики вирусных ГЭ разрабатываются с момента расшифровки их этиологической структуры. Поскольку открытие вирусов произошло благодаря внедрению метода электронной микроскопии, именно этот метод длительное время оставался основным, а в некоторых случаях и единственным способом верификации диагноза вирусных ГЭ. Однако высокая стоимость проведения анализа и его относительно невысокая чувствительность потребовали разработки новых, более доступных методов верификации диагноза.
К сожалению, на сегодняшний день имеются реальные проблемы, связанные с верификацией вирусов у больных с ГЭ, поскольку единой «панели» какого-либо метода исследования на различные вирусы не существует.
Наиболее подробно разработаны методы диагностики РИ. В зависимости от принципа, на котором основана диагностика, применяемые методы могут быть разделены на две группы: методы, основанные на определении самого вируса или его компонентов; методы, основанные на определении антител к компонентам ротавирусов (табл. 2).
Исследования последних лет свидетельствуют о том, что одним из наиболее перспективных методов диагностики вирусных ГЭ является полимеразная цепная реакция (ПЦР), чувствительность и специфичность которой оцениваются исключительно высоко. В научных исследованиях эти методы используются достаточно широко, однако пока ни один из них не зарегистрирован в нашей стране.
Лечение вирусных гастроэнтеритов
Несмотря на то что основные возбудители вирусных ГЭ уже известны, методы этиотропной терапии по-прежнему не разработаны. Если учесть скоротечность развития вирусных ГЭ, можно предположить, что в ближайшие десятилетия этиотропная терапия вряд ли сможет занять достойное место в лечении этих больных. Куда большее внимание на сегодняшний день уделяется разработке вакцин для профилактики вирусных ГЭ. Если ротавирусные вакцины уже разработаны и применяются в ряде стран [2], то в отношении других вирусов вакцины находятся только в стадии разработки. Целесообразность госпитализации больных в стационар определяется клинико-эпидемическими показаниями.
Таким образом, лечение больных с вирусными ГЭ строится на принципах патогенетической терапии. Выбор наиболее оптимального способа лечения больных зависит от своевременной диагностики, а точнее, лабораторной верификации вирусного генеза заболевания. Несмотря на то что промывание желудка у больных с бактериальными ГЭ, проводимое в первые часы заболевания, способствует улучшению самочувствия больных, при вирусных ГЭ эффективность этого мероприятия крайне низка.
Из немедикаментозных методов лечения важное место отводится диетотерапии, что определяется патофизиологическими механизмами развития диарейного синдрома. На высоте клинических проявлений заболевания следует исключить из пищи молоко и молочные продукты, ограничить прием углеводов, сахара, овощей и фруктов. По мере купирования клинических признаков заболевания диета постепенно расширяется. Учитывая, что в острый период заболевания у больных формируется ферментопатия, целесообразно назначать им комбинированные ферментные препараты, такие, как фестал, панзинорм, мезим форте и другие. Обоснованной является также терапия адсорбирующими и вяжущими препаратами, которые, в частности, способствуют оформлению кала и урежению кратности дефекации, хотя это мало влияет на развитие дегидратации. К числу таких средств относятся полифепан, смекта, препараты висмута и другие.
В литературе имеются указания на положительное влияние на течение вирусных ГЭ различных пробиотиков. Патофизиологическим обоснованием их применения у больных с вирусными ГЭ служит тот факт, что штаммы, входящие в состав пробиотиков, самым непосредственным образом участвуют в процессах пищеварения, обмена веществ и детоксикации. Кроме того, у больных могут выявляться дисбиотические изменения в кишечнике [1].
Поскольку основным проявлением вирусных ГЭ, определяющим тяжесть течения заболевания, является дегидратация, купирование обезвоживания составляет основу патогенетической терапии. Принципы регидратационной терапии на сегодняшний день разработаны достаточно хорошо и носят универсальный характер. В зависимости от степени дегидратации регидратацию проводят пероральным или внутривенным способом.
Пероральная регидратационная терапия проводится в том случае, если у больных отсутствуют выраженные системные проявления обезвоживания. Она проводится глюкозоэлектролитными растворами (цитроглюкосоланом, регидроном и другими), которые принимаются дробно, по 1–1,5 л в час.
Внутривенная терапия назначается больным в случае выраженных системных проявлений или при наличии неукротимой рвоты, затрудняющей оральную регидратацию. Эта терапия проводится сбалансированными полиионными кристаллоидными растворами, такими, как трисоль, квартасоль, хлосоль и другие. Объем вводимых растворов и скорость их введения определяются степенью обезвоживания. В тех случаях, когда у больных проявления интоксикации доминируют над симптомами обезвоживания, допускается введение коллоидных растворов (гемодеза, реополиглюкина и других).
Заключение
Накопленные к сегодняшнему дню данные наглядно свидетельствуют о существенном удельном весе вирусных ГЭ в патологии человека. К числу установленных возбудителей вирусных ГЭ относятся ротавирусы, калицивирусы человека, кишечные аденовирусы и астровирусы, однако этот список далеко не полный. Даже применение современных молекулярно-генетических методов диагностики позволяет верифицировать диагноз только в половине регистрируемых случаев острых небактериальных ГЭ. Последнее может служить наглядным свидетельством недостаточной изученности этой группы инфекционных болезней.
На основании вышеизложенного следует сделать вывод, что при любых вспышках ОКИ, особенно возникающих в детских организованных коллективах, пациентов необходимо обязательно обследовать на вирусную этиологию (включая весь спектр известных вирусов, а не только на ротавирусы), что позволит оптимизировать не только способы лечения больных, но и противоэпидемические мероприятия.
По вопросам литературы обращайтесь в редакцию
В. А. Малов, доктор медицинских наук, профессор
А. Н. Горобченко, кандидат медицинских наук
Е. А. Городнова
ММА им. И. М. Сеченова, Москва
Аденовирусная инфекция у детей
Приходят холода, дети начинаю болеть гораздо чаще. Родители упорно вызывают врачей, а те упорно ставят диагноз ОРВИ.
Заболевание поражает детей в любом возрасте, но особо тяжело переносится до трех лет. Аденовирусная инфекция может проникать в организм круглогодично, но основной подъем заболеваемости отмечается в зимне-весенний период, повсеместно начинают образовываться локальные вспышки, особенно в закрытых детских коллективах.
Что такое аденовирусная инфекция?
Выяснив, что аденовирусная инфекция является разновидностью ОРВИ, следует рассмотреть ее более детально.
Главными воротами инфекции являются верхние отделы дыхательных путей, реже конъюнктива глаз. Отмечено, что вирус размножается с огромной скоростью, из пораженного участка легко проникает в кровь и распространяется дальше по организму. В качестве дороги, помимо кровеносных сосудов, аденовирусы могут использовать лимфоузлы и лимфатические пути.
Распространенность и пути заражения
По факту, человеческий организм должен защититься от инфекционного заболевания сам, на помощь приходит иммунитет. Но на деле, ослабленный холодным временем года, местный иммунитет ребенка не в состоянии противостоять вирусу в главных воротах проникновения. Общий иммунитет, в связи с возрастом, также недостаточно противостоит вирусному заражению. Отсюда и появляется статистика, по которой дети болеют гораздо чаще, чем взрослые люди.
Практически всегда аденовирусная инфекция наблюдается в форме эпидемической вспышки, то есть поражается группа детей, контактирующих друг с другом. Вирус может распространяться по организму, усердно размножаясь, в течение 1-3 недель.
Симптомы аденовирусной инфекции у детей и их частота проявления
Попав в детский организм, вирус переходит в стадию инкубационного периода, то есть созревания. На протяжении от 4 до 14 дней, чаще 5-7 дней, ребенок может не проявлять никаких признаков заболевания. Заболевание проявляется остро или нарастает постепенно.
К внешним симптомам, которые может выявить любой врач, относятся 2 :
После многих лет изучения различных проявлений ОРВИ, включая аденовирусную инфекцию, врачи вывели частоту проявления тех или иных симптомов, что может указывать на конкретный вирус.
Родителям стоит обратить внимание на три отрезка проявления симптомов у своего ребенка, которые указаны в памятке ниже. Уже после первого отрезка необходимо обратиться за врачебной помощью:
По степени тяжести выделяют следующие формы:
Диагностика аденовирусной инфекции
Диагностировать аденовирусную инфекцию в большинстве случаев не составляет особого труда. Врач собирает анамнез, проводит обследование, определяет характерные симптомы и на их основании ставит диагноз. Подобный способ называют клиническим. Особенно он точен, когда болезнь носит распространенный характер, в зимний или весенний период.
Существует точная методика выявления аденовирусной инфекции посредством исследования крови.
В качестве дополнительных диагностических мероприятий могут быть проведены микроскопические исследования содержимого носа и ротоглотки, для исключения бактериальной инфекции.
Чем лечить аденовирусную инфекцию у детей и профилактические рекомендации
Вылечить инфекцию можно, но не всегда понятно, какие действия или лекарства необходимо применять. После диагностики и определения симптомов аденовирусной инфекции у детей, вероятней всего, будет назначено лечение в домашних условиях. Госпитализация возможна, но только в самых серьезных случаях тяжелой формы заболевания.
Чудо лекарства, которое моментально избавит организм от аденовируса не существует, используется симптоматическое лечение и общие терапевтические мероприятия.
Рекомендации по лечению аденовирусной инфекции у детей, включают в себя 5 :
Лекарства для симптоматического лечения доступны в большинстве аптек, но должны выписываться только лечащим врачом-педиатром. К таким лекарствам относят:
В качестве профилактических мероприятий (до начала заболевания) используют:
Профилактика важна, но если ребенка поразила аденовирусная инфекция, то от закаливания стоит сразу отказаться, так как возможны неприятные последствия. При развитии бактериального осложнения могут потребоваться антибиотики, но без согласования с врачом их прием крайне нежелателен. Основная проблема лечения заключается в том, что аденовирус уже попал в организм, иммунитет пытается его победить, а в этот момент через входные ворота могут проникнуть другие вирусы и бактерии. На помощь приходят специальные медикаментозные препараты.
Лечение аденовирусной инфекции у детей с применением ингаляций
Рассмотрены патогенез и клинические симптомы аденовирусной инфекции у детей, описаны подходы к терапии с применением отхаркивающих и иммунотропных препаратов.
Pathogenesis and clinical symptoms of adenovirus infection in children are examined, approaches to therapy with the application of the expectorant and immunotropic preparations are described.
Аденовирусная инфекция (АВ) (МКБ-10: В57) — острое инфекционное заболевание с преимущественным поражением носоглотки, конъюнктивы и лимфоидной ткани. АВ протекает с умеренной интоксикацией, лихорадкой, катаральным синдромом с выраженным экссудативным компонентом [1–3].
Аденовирусы, которые вызывают заболевание у детей, относятся к семейству Adenoviridae, роду Mastadenovirus ДНК-содержащих вирусов средних размеров. В настоящее время выделено около 50 серотипов этого вируса. Наиболее частыми возбудителями аденовирусной инфекции являются 3-й и 7-й серотипы. Аденовирусы обладают тропностью к эпителию дыхательных путей, кишечника и конъюнктивы, а также способностью поражать лимфоидную ткань. Токсичность вирусов этой группы низкая [2].
Источником инфекции является больной или вирусоноситель, пути передачи — воздушно-капельный, водный («болезнь плавательных бассейнов»), а также фекально-оральный. Наиболее восприимчивы к этому вирусу дети от 6 месяцев до 3 лет. АВ регистрируют повсеместно и круглогодично с подъемом заболеваемости в холодное время года. Заболевания наблюдаются в виде спорадических случаев и эпидемических вспышек, для которых характерно медленное развитие и длительное течение. Иммунитет после перенесенного заболевания типоспецифический, продолжительный. Аденовирусы относительно устойчивы в окружающей среде, сохраняются в течение нескольких недель в воде, лекарственных растворах, на предметах обихода, резистентны к эфиру. Разрушаются при температуре +56 °С в течение 30 мин, погибают под воздействием ультрафиолетового облучения и хлорсодержащих препаратов [2, 3].
При заражении вирусы проникают в организм через слизистые оболочки дыхательных путей, а также эпителий тонкой кишки. Благодаря своей лимфотропности, возбудитель внедряется в носоглотку, миндалины, конъюнктиву и вызывает формирование воспалительных очагов. В ходе заболевания увеличиваются все лимфатические узлы, в том числе мезентериальные, возникает гепатоспленомегалия. Инкубационный период длится 4–7 дней. Течение заболевания медленное, волнообразное. Характерен респираторный синдром, конъюнктивит, которые протекают с выраженным экссудативным компонентом. Диарея присоединяется обычно у детей до 2 лет и носит водянистый характер [1].
Патогномоничная форма аденовирусной инфекции — аденофарингоконъюнктивальная лихорадка. Она протекает с подъемом температуры тела до 38–39 °С на протяжении 5–10 дней, фарингитом с зернистостью задней стенки глотки, увеличением и гиперемией миндалин, конъюнктивитом. Нередко развивается тонзиллит, проявляющийся гипертрофией, отечностью и умеренной гиперемией миндалин, а также аденоидит. В ряде случаев на задней стенке глотки, небных миндалинах появляются нежные белесоватые налеты (пленчатый фарингит и тонзиллит) [1, 2].
С первых дней болезни нередко развивается кашель. Характерным для аденовирусной инфекции является синдром полиаденита — увеличение шейных и подчелюстных лимфатических узлов. Наблюдается увеличение печени и селезенки. Возможно развитие мононуклеозоподобного синдрома, для которого характерно сочетание пленчатого тонзиллита, полиаденита и гепатоспленомегалии. Длительность катарального синдрома — 10–15 дней, иногда до 3–4 недель [2, 3].
АВ — одна из распространенных респираторных вирусных инфекций, активно участвующих в формировании у ребенка адекватного противоинфекционного иммунитета, важного для всей последующей жизни.
При нормальном функционировании иммунной системы происходит эффективное взаимодействие интерферона и других лимфокинов, макрофагов, лимфоцитов, специфических антител, приводящее к элиминации возбудителя из макроорганизма и клиническому выздоровлению.
У ребенка раннего возраста направленность иммунной защиты организма изначально носит супрессивный характер. Невысокая активность собственного неспецифического звена иммунитета необходима для профилактики ярких воспалительных реакций, которые могут быстро истощить организм ребенка и привести его к развитию дезадаптации и декомпенсации систем жизнедеятельности. Специфическое звено иммунитета ребенка обусловливает пассивная иммунная защита в виде иммуноглобулинов, транслированных через плаценту, а также попадающих к ребенку вместе с молоком матери при грудном вскармливании.
Формирование надежной и адекватной естественной защиты с преобладанием популяции Тh1-лимфоцитов возможно только при непосредственном контакте ребенка с различными вирусами и «отработке» его иммунной системой паттерна воспалительной реакции, клинически выраженной чаще всего катаральным синдромом с кашлем и лихорадкой. Все проявления острых респираторных инфекций: лихорадка, ринит, кашель, гиперемия сводов зева — носят защитный характер и должны в первую очередь рассматриваться именно в этом контексте, а не представляться досадными помехами, которые надо немедленно купировать. Лихорадка — защитная реакция организма. Только на фоне лихорадки организм дает адекватный иммунный ответ Т-хелперов 1-го типа — продукцию γ-интерферона, интерлейкина-2, фактора некроза опухоли-α, стимулирующих выработку IgG.
Проникновение вируса в организм ребенка запускает каскад иммунных реакций, способствующих стимуляции нейроиммуноэндокринной системы, которая в дальнейшем регулирует процессы дифференцировки и созревания нейроэндокринной оси (рис.).
Защитные реакции кашля и выделения слизи из носовых ходов позволяют качественно осуществить очищение и увлажнение слизистой оболочки дыхательных путей, необходимые для адекватного функционирования мерцательного эпителия. Выделяемая из дыхательных путей мокрота к тому же содержит бесценный материал для выработки специфического иммунитета — фагоциты, которые определили возбудителя и экспрессировали специфические рецепторы для включения в работу высокоспециализированных клеток иммунной системы — лимфоцитов. При заглатывании ребенком мокроты лимфоидная ткань кишечника получает информацию о возбудителе и стимул к выработке регуляторных пептидов.
Покраснение сводов зева сопровождает прилив к слизистой оболочке крови, несущей компоненты гуморального и клеточного иммунитета, и искусственное «тушение» противовоспалительной местной терапией этого проявления неспецифической иммунной реакции мешает первичному этапу иммунной реакции запустить каскад иммунных реакций.
Медикаментозно «притушив» эти проявления, мы никогда не сможем заменить их лекарственными средствами, так как они индивидуальны и адекватны именно этому ребенку с его наследственностью, жизненным опытом и условиями проживания.
К сожалению, отсутствие четкого представления о необходимости некоторого временного периода, в течение которого все неспецифические иммунные процессы должны развернуться и принять участие в формировании гармоничного и полноценного иммунного ответа, в настоящее время приводит к необдуманной агрессивной терапии, целью которой является скорейшее купирование симптомов. По данным С. В. Ключникова (2012), каждому пятому ребенку в возрасте до 1 года назначались антибиотики (в том числе гентамицин, линкомицин). К возрасту 3 года число детей, получавших антибиотики, увеличивается до 28% и достигает 80% к семилетнему возрасту.
Необдуманное применение антибиотиков, недопустимо стремительное купирование естественных проявлений неспецифической иммунной защиты (лихорадка, насморк, кашель, гиперемия и отек сводов зева) ведут к снижению качества защитной биологической пленки на слизистой оболочке дыхательных путей.
В отделении раннего возраста педиатрической клиники МОНИКИ было проведено сравнение результатов микробиологического обследования двух групп детей в возрасте от 4 до 6 лет. Группы были выделены при анкетировании родителей, которым были заданы следующие вопросы:
Дети, родители которых на все вопросы ответили утвердительно, составили первую группу (20 человек). Дети, родители которых ответили на все вопросы, кроме первого и последнего, отрицательно, вошли во вторую группу (15 человек).
Во второй группе количество детей, в мазке которых была выделена грибковая флора, не превысило 11% (2 человека из 15 обследованных), а биотоп был более разнообразным и плотным (8 наименований микробов, количество нормальной флоры 5–6 × 10 5 КОЕ/мл).
По этой причине агрессивное лечение острых респираторных инфекций и резкое неприятие родителями информации о существовании этапа в жизни ребенка, когда частые острые респираторные вирусные инфекции необходимы для его дальнейшего развития, в настоящее время являются базой для полипрагмазии, а организм ребенка становится полигоном для битвы многочисленных лекарственных средств.
Вместе с тем специфической противовирусной терапии при аденовирусной инфекции нет. Антибактериальная терапия в данном случае не показана. В период лихорадки назначают постельный режим, полноценное питание, обильное питье. Рекомендуется давать обильное горячее питье, чай, кисели, теплые морсы и компоты. Симптоматическое лечение включает применение жаропонижающих средств при лихорадке выше 38,5 °С. Если температура ребенка ниже 37,5 °С, нет необходимости в ее снижении медикаментозными препаратами. При более высокой температуре можно применять физические методы охлаждения. На внутреннюю поверхность рук, бедер, боковую поверхность шеи можно прикладывать смоченные в холодной воде компрессы. При насморке можно промывать нос слабым солевым раствором с помощью шприца или закапывать в нос сосудосуживающие капли. Следует избегать длительного применения капель (не более 5–7 дней), так как они могут вызвать временную дисфункцию слизистой оболочки [3, 4].
Оптимальными средствами для элиминации слизистой оболочки, восстановления ее влажности и создания наилучших условий для функционирования эпителия и слизистых клеток, вырабатывающих иммуноглобулин, лизоцим, лактоферрин и другие ферменты, являются изотонические растворы морской воды (Аква Марис, Физиомер, Долфин и пр.). Содержащиеся в морской воде микроэлементы (селен, йод, цинк) ускоряют регенерацию слизистой оболочки.
При выраженном сухом кашле можно начать лечение с приема грудного сбора в виде горячего отвара. Помогает также щелочное питье в виде горячего молока с небольшим количеством (на кончике ложки) соды. Если ребенок отказывается от молока, можно поить его подогретыми щелочными минеральными водами. Если кашель носит влажный характер с трудно отхаркивающейся мокротой, можно применять отхаркивающие препараты, если кашель длительный, сухой, саднящий — целесообразнее будет применять препараты, подавляющие кашель [4].
В лечении кашля при аденовирусной инфекции важно учитывать, что он может быть как сухим (характерное покашливание при гранулезном фарингите), так и с выраженным отделением мокроты. Поэтому препарат для адекватного сопровождения этого симптома должен быть направлен и на стимуляцию отделения мокроты, и на своевременную поддержку регенерации слизистой оболочки, и при этом должен иметь удовлетворяющие ребенка органолептические характеристики и удобный способ применения. Этим условиям соответствует Амбробене (амброксола гидрохлорид) — муколитический препарат с отхаркивающим действием, который обладает секретомоторным, секретолитическим и отхаркивающим свойствами.
Важным достоинством препарата является продуманное разнообразие лекарственных форм. Это дает преимущества в лечении детей любого возраста, поддерживает оптимальную комплаентность родителей и позволяет достичь адекватности в терапии респираторного синдрома у детей.
Например, можно использовать амброксола гидрохлорид в виде сиропов (детям от 5 до 12 лет — 1 мерная ложка (15 мг) — 2–3 раза в день; детям от 2 до 5 лет — 1/2 мерной ложки (7,5 мл) — 3 раза в день, детям до 2 лет — 1/2 мерной ложки (7,5 мл) после еды 2 раза в день).
Ингаляционная терапия имеет преимущества перед другими формами в том, что она совмещает элиминационные свойства (очищение верхних дыхательных путей от патологического содержимого), увлажнение слизистой оболочки и достаточную глубину проникновения для очищения более нижних отделов органов дыхания и таким образом профилактирует рефлекторный бронхоспазм при избытке мокроты. Лекарственное вещество распыляется и в виде аэрозоля оседает на слизистых оболочках верхних дыхательных путей. При этом возрастает интенсивность всасывания в подслизистом слое верхних дыхательных путей и увеличивается его депонирование.
Раствор для ингаляций применяется в зависимости от возраста детям от 5 до 12 лет — 2 мл (15 мг) — 2–3 раза в день; детям младше 5 лет — 1 мл (7,5 мл) — 3 раза в день.
В терапии аденовирусной инфекции можно использовать также иммунотропные препараты (Кипферон, Виферон, ИРС-19, Деринат), регулирующие неспецифические иммунные реакции (интерфероногенез) и дополняющие реакцию организма наличием специфических антител к представителям флоры, которые могут спровоцировать осложнения в виде пневмонии, бронхитов, синуситов.
Таким образом, обдуманная и максимально индивидуальная поддержка естественных защитных реакций организма ребенка при аденовирусной инфекции позволит сохранить и приумножить защитные силы организма ребенка.
Литература
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
Аденовирус (Аденовирусная инфекция)
Аденовирусная инфекция — патологический процесс, возникающий на фоне попадания в организм человека аденовируса (Adenoviridae). Заболевание сопровождается поражением органов дыхания, глаз, желудочно-кишечного тракта и лимфатической системы. Инфицированные пациенты страдают от интоксикации, лихорадки, потери голоса, кашля, кишечных расстройств. Постановка диагноза осуществляется на основании клинической картины заболевания и результатов лабораторных исследований. В процессе лечения взрослые и дети получают противовирусные препараты, иммуномодуляторы и средства, снимающие острые симптомы инфекции.
Общие сведения о патологии
Аденовирус относится к группе респираторно-вирусных инфекций. Течение заболевания осложняется конъюнктивитом, ринофарингитом, лимфаденопатией, диспепсическим синдромом. Доля аденовирусных инфекций в общей структуре ОРВИ достигает 20%.
В группу риска входят пациенты в возрасте от полугода до трех лет. Почти все дети дошкольного возраста были инфицированы аденовирусом хотя бы один раз. Патология не обладает выраженной сезонностью: уровень заболеваемости остается стабильным на протяжении всего года. Лечение заболевания осуществляется под надзором педиатра и отоларинголога.
Причины развития патологии
Вирусологи выявили три десятка патогенов, относящихся к семейству Adenoviridae. Возбудители инфекции приспособлены к длительному выживанию в неблагоприятных условиях, хорошо переносят отрицательные температуры и низкую влажность окружающей среды. ДНК патогенов разрушается под воздействием ультрафиолетового излучения и химических соединений на основе хлора.
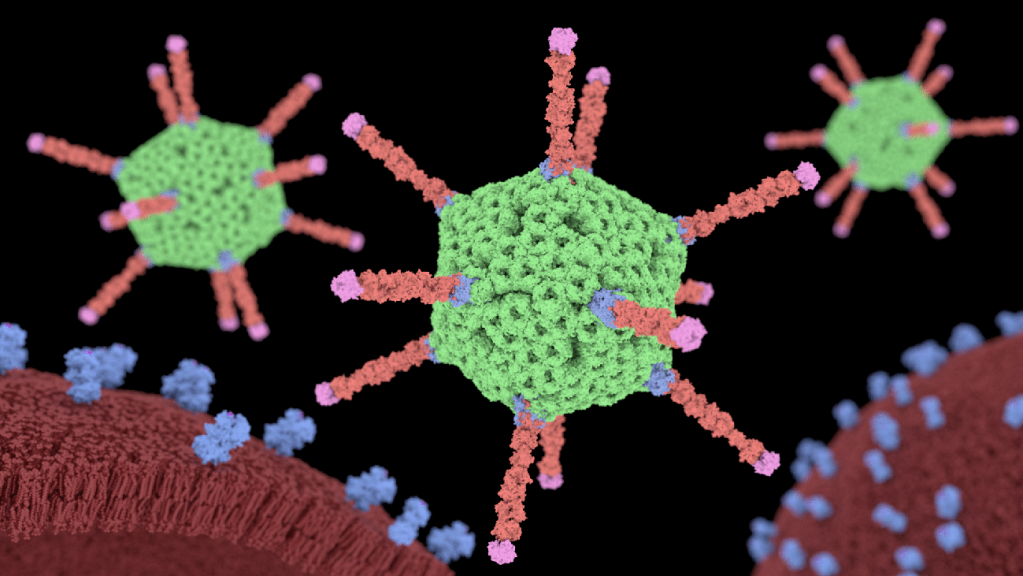
Пациент, перенесший аденовирусную инфекцию, обладает иммунитетом к определенному типу вируса. Ребенок или взрослый может повторно заболеть, столкнувшись с носителем другого серотипа Adenoviridae. Подобный механизм передачи аденовируса от человека к человеку характерен для внутрибольничных инфекций.
 Механизм инфицирования
Механизм инфицирования
Первые проявления аденовируса начинают беспокоить пациента после попадания патогенов на слизистые оболочки дыхательных путей и кишечника или конъюнктиву глаза. Вирусы репродуцируются в клетках эпителия, лимфатических узлах и лимфоидных образованиях кишечника. После завершения инкубационного периода пораженные клетки гибнут — вирусы попадают в кровеносную систему человека.
В местах первичного поражения слизистых формируются отёки. Типичная локализация очага воспаления — задняя стенка глотки. Воспалительный процесс протекает на фоне обильного отделения экссудата. При отсутствии лечения пациент может столкнуться с поражением бронхов, почек, печени и селезенки.
Симптоматика патологии
Симптомы попадания аденовируса в организм человека специфичны и зависят от формы, которую приняла инфекция. При поражении дыхательных путей могут развиться фарингиты, тонзиллофарингиты и бронхиты. В случае проникновения инфекции к тканям конъюнктивы пациенты страдают от фарингоконъюнктивной лихорадки и острого конъюнктивита. Попадание вирусов семейства Adenoviridae на слизистые оболочки кишечника провоцирует развитие диарейного синдрома.
Пациенты могут столкнуться с легким, средним и тяжелым течением заболевания. В некоторых случаях патология осложняется присоединением вторичной инфекции. Инкубационный период длится от пяти до семи дней. По его завершении пациент ощущает резкое повышение температуры тела (до 38–39 градусов). Позднее проявляются типичные признаки аденовирусной инфекции:
Перечисленные симптомы аденовируса развиваются у детей и взрослых в течение нескольких часов после повышения температуры. При отсутствии лечения состояние пациентов быстро ухудшается.
Поражение органов дыхания
Распространение инфекции в дыхательных путях провоцирует появление гнойно-слизистого отделяемого из носа. Дыхание человека учащается. При осмотре пациента отоларинголог обнаружит белый налет на миндалинах и выраженный отек слизистой оболочки глотки. Подчелюстные и шейные лимфатические узлы значительно увеличиваются в размерах. Голос ребенка или взрослого обретает характерную осиплость. В некоторых случаях врачи диагностируют у пациентов сухой кашель и одышку.
Поражение конъюнктивы
Репродуцирование вирусов в тканях конъюнктивы приводит к развитию конъюнктивитов различных форм: катаральной, фолликулярной и пленчатой. Патологический процесс начинает развиваться в одном глазу, но постепенно затрагивает и второй. Пациенты жалуются на рези, жжение, ощущение инородного тела. Офтальмологический осмотр позволяет выявить покраснение и отечность кожи век. В некоторых случаях врачи фиксируют образование плотной белесой пленки на конъюнктиве. Запущенная аденовирусная инфекция осложняется кератитом.
Поражение желудочно-кишечного тракта
Проникновение Adenoviridae в кишечник человека провоцирует развитие острого болевого синдрома в околопупочной области. Пациент страдает от диареи, систематических приступов тошноты и рвоты. Частично клиническая картина заболевания совпадает с острым аппендицитом.
Возможные осложнения
Тяжелое течение аденовирусной инфекции может привести к развитию менингоэнцефалита. Младенцы страдают от аденовирусной пневмонии и дыхательной недостаточности. Взрослые часто сталкиваются со вторичными инфекциями, на фоне которых развиваются синуситы, отиты и бактериальные пневмонии.
 Диагностические мероприятия
Диагностические мероприятия
Диагностика выполняется терапевтом или отоларингологом — врач проводит осмотр пациента с признаками инфицирования аденовирусом. В анамнез ребенка или взрослого вносятся объективные данные о симптомах: лихорадке, конъюнктивите, дыхательной недостаточности, кишечных расстройствах. Подтверждение первичного диагноза выполняется в ходе лабораторных исследований биоматериалов пациента — крови, мазков из носоглотки, соскобов с конъюнктивы, каловых масс.
Дифференциальная диагностика позволяет исключить из анамнеза человека грипп, инфекционный мононуклеоз, дифтерию глотки, микоплазменную инфекцию. При неясных результатах лабораторных анализов терапевт может направить пациента на офтальмологический осмотр.
 Лечение патологии
Лечение патологии
Медикаментозный курс, назначаемый врачами на фоне подтвержденного диагноза, основан на противовирусных препаратах. Стационарное или амбулаторное лечение лиц, страдающих от аденовируса, предполагает назначение глазных капель, мазей (накладываются на веко), жаропонижающих и противокашлевых средств. При поражении органов дыхания пациенту потребуются регулярные ингаляции и отхаркивающие препараты. Лечение осложненного аденовируса у детей и взрослых может потребовать применения антибиотиков.
Прогноз и профилактические меры
При неосложненном течении заболевания пациенты добиваются полного выздоровления за пять–семь дней. Осложненная форма аденовирусной инфекции может потребовать госпитализации ребенка или взрослого. В этом случае сроки выздоровления увеличиваются в 1,5–2 раза.
При резком росте инфицирования аденовирусом в детских садах или школах врачи рекомендуют проводить специфическую профилактику. Носителей вируса необходимо направить на амбулаторной или стационарное лечение. Все помещения образовательных учреждений следует обработать антисептическими растворами.
Диагностика и лечение аденовирусной инфекции в Москве
АО «Медицина» (клиника академика Ройтберга) обладает всем необходимым оборудованием для диагностики и лечения аденовирусной инфекции у детей и взрослых. Прием пациентов осуществляется в современном диагностическом комплексе, построенном с учетом последних достижений медицины.
Вопросы и ответы
Какой врач лечит аденовирусную инфекцию?
Лечение детей осуществляется под надзором педиатра. Взрослые могут обратиться к терапевту. При наличии показаний врач направит пациента на консультацию с офтальмологом или отоларингологом.
Существуют ли вакцины, стимулирующие выработку антител к возбудителям аденовирусной инфекции?
Нет, поскольку патогены группы Adenoviridae отличаются значительным разнообразием.
.gif)

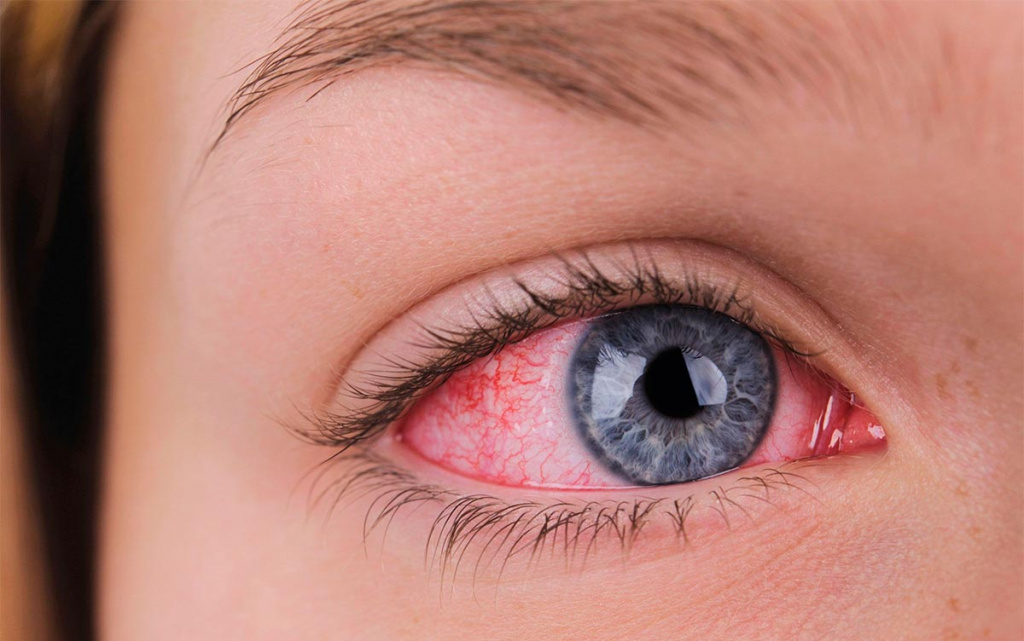 Механизм инфицирования
Механизм инфицирования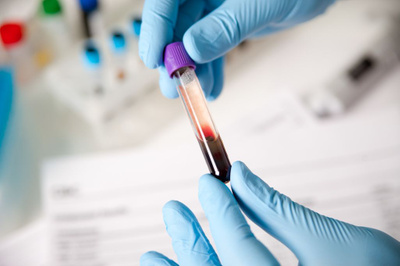 Диагностические мероприятия
Диагностические мероприятия Лечение патологии
Лечение патологии