Чем лечить коли бактерии
Пробиотики для кишечника: список препаратов
Ребенок появляется на свет со стерильным кишечником, но уже к году состав микрофлоры совпадает со взрослым человеком. На протяжении жизни под влиянием питания, болезней и других факторов баланс микроорганизмов в пищеварительном тракте изменяется, но постепенно восстанавливается до нормальных концентраций. Иногда этот процесс затягивается. Тогда врач может рекомендовать пребиотики и пробиотики для кишечника.
Виды пробиотиков
Для восстановления кишечника применяют два типа лечебных средств. Пробиотики – это препараты, которые содержат полезные бактерии в высушенном или растворенном виде. Чаще всего это микроорганизмы из рода Lactobacillus и Bifidobacterium, которые в норме доминируют в пищеварительном тракте человека.
Пребиотиками называются вещества, необходимые для роста хорошей микрофлоры. В некоторых случаях без них можно обойтись, но после тяжелых болезней, лечения антибиотиками или отравления они ускорят восстановление за счет создания благоприятной среды для бактерий.
В пищеварительном тракте здорового взрослого человека обитает несколько десятков видов бактерий, но преобладают два типа микробов: бифидобактерии и лактобактерии. Другие находятся в меньшинстве. Поэтому выделяют следующие виды пробиотиков в зависимости от состава:
Восстанавливать нормальную микрофлору можно разными формами препаратов. Пробиотики выпускают в сухой форме, из которой перед применением самостоятельно готовят суспензию. Существуют готовые жидкие формы лекарства, которые удобно давать маленькому ребенку. Некоторые средства производят в капсулах в желатиновой оболочке. Она не повреждается в желудке и растворяется только в кишечнике. Это защищает бактерии от действия соляной кислоты.
Создание препаратов для решения проблем с пищеварением проходило в несколько этапов. Поэтому фармацевты выделяют несколько поколений пробиотиков:
Какой препарат подойдет в конкретном случае, должен решать врач с учетом состояния пациента, его возраста. Для взрослых требуется большая дозировка и кратность приема пробиотиков.
ТОП-10 лучших пробиотиков
В аптеках продается большое количество пробиотиков, из которых тяжело выбрать нужный препарат. Правильное решение – обратиться к врачу-гастроэнтерологу или терапевту, чтобы назначили лекарственное средство с хорошим эффектом.
Чтобы решить, какой из них лучше, можно ориентироваться на список ТОП-10:
Советы по выбору
Какой из перечисленных пробиотиков поможет справиться с проблемами пищеварения, зависит от заболевания. Если организму необходима помощь после курса лечения антибиотиками, лучше использовать комплексные препараты, где добавлен пребиотик. Он ускорит заселение бактериями слизистой кишечника.
Вне зависимости от названия, для взрослых походят препараты в виде порошка, капсул или раствора. Капли разработаны специально для маленьких детей, которым необходима небольшая доза препарата. Их хорошо смешивать с напитками или молоком матери.
При использовании средств с пробиотическими эффектами, симптомы вздутия живота, урчания, метеоризм могут усилиться из-за процесса брожения. Но это проходит самостоятельно и не требует отмены терапии. Если на фоне приема пробиотиков появилась аллергическая сыпь, лечение прекращают.
Кишечная палочка
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
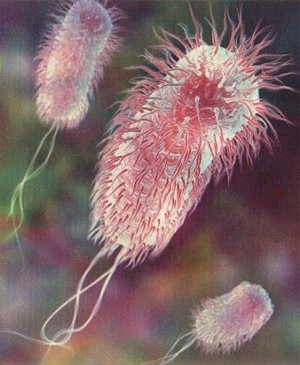
Этой статьей мы начинаем рассмотрение представителей микробиологического мира, с которыми чаще всего встречаем в ежедневной клинической практике, и темой сегодняшнего разговора будет кишечная палочка, она же Escherichia coli (E.coli).
Актуальность обсуждения данного микроорганизма состоит в том, что кишечная палочка – это чемпион по созданию проблем как для пациентов, так и для медицинского персонала стационаров и в амбулаторной службе. Хуже нее только клебсиелла, но о ней поговорим попозже. При этом E.coli не летает по воздуху и не имеет ножек для самостоятельного перемещения и инфицирование ею – это почти всегда «болезнь грязных рук». С патологией, вызванной этим возбудителем, пациент может прийти к любому врачу, а медицинский персонал может принести уже на своих руках кишечную палочку любому пациенту с одной лишь разницей – это будет не дикий и симпатичный зверек, убиваемый обычным амоксицилином, а вооруженная до зубов особь, умеющая очень эффективно убивать сама. То есть это один из тех врагов, которых совершенно точно надо знать в лицо.
Микробиологические аспекты
E.coli относится к типичным представителям семейства Enterobacteriaceae, являясь грамотрицательной бактерией, факультативным анаэробом в составе нормальной кишечной микрофлоры человека. Но тут же становится патогеном, выбравшись из среды нормального обитания, хотя отдельные штаммы являются патогенными и для желудочно-кишечного тракта. То есть кишечная палочка относится к кишечным комменсалам, кишечным патогенам и внекишечным патогенам, каждый из которых мы кратко разберем.
К штаммам E.coli, действующим как кишечные патогены и встречающимся чаще других, относятся:
Затем тот же штамм обнаружился при вспышке ПТИ в Финляндии, но к тому времени пациентов с диареями до появления микробиологических результатов перестали лечить бактерицидными антибиотиками и ситуация была купирована в зародыше.
И третий громкий (для нашей страны) случай – это массовое заболевание питерских школьников в Грузии, где так же был выявлен этот штамм (пресс-релиз Роспотребнадзора по данному случаю лежит здесь).
Когда кишечная палочка выступает внекишечным патогенном? Почти всегда, когда обнаруживается вне места своего нормального обитания.
Этот факт объясняется близким анатомическим расположением двух систем и огрехами в личной гигиене, что позволяет на этапе эмпирической терапии вышеперечисленных заболеваний сразу же назначать препараты, активные в отношении кишечной палочки.
(часть вторая) Практические вопросы диагностики и лечения.
Когда мы можем заподозрить, что перед нами пациент с инфекцией, вызванной кишечной палочкой?
Подтвердить или полностью исключить кишечную палочку из возбудителей может только микробиологическое исследование. Конечно, в современных условиях микробиология уже становится практически эксклюзивом, но мы пришли учиться, а учится надо на правильных примерах, поэтому далее будет рассмотрен ряд антибиотикограмм, выполненных автоматизированными системами тестирования. Вдруг вам повезет, и в вашем лечебном учреждении все уже есть или в ближайшее время будет, а вы уже умеете с этим всем работать?
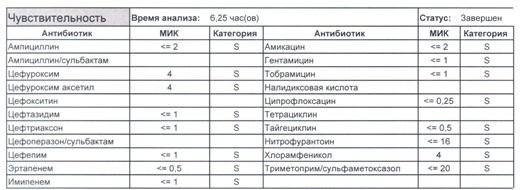
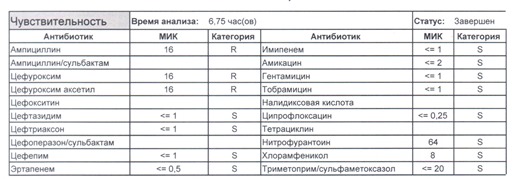
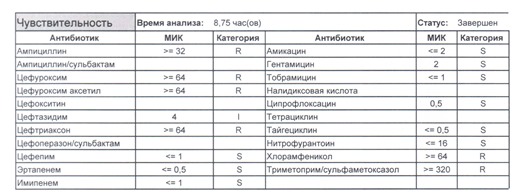
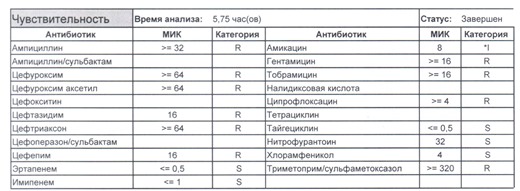
Если вы читаете данный цикл по порядку, то в базовом разделе по микробиологии был выложен ряд антибиотикограмм некоего микроорганизма в контексте нарастания антибиотикорезистентности, и это была наша сегодняшняя героиня – кишечная палочка.
Если такая кишечная палочка окажется внекишечным патогенном, и перед вами будет беременная и ИМП (самый частый случай), то нам необходимо преодолеть резистентность к пенициллинам, то есть подавить деятельность пенициллиназ. Соответственно высокую эффективность продемонстрируют препараты с ингибиторами бета-лактамаз, чаще всего амоксициллина/клавуланат, как наиболее безопасный и эффективный. Единственное, пациентку необходимо предупредить, что в результате стимуляции рецепторов кишечника может развиться антибиотик-ассоциированная диарея.
В каких ситуациях мы можем увидеть (или подумать) о таком звере:
Подобный пациент не придет к вам своими ногами, его не увидит амбулаторная служба, это абсолютно стационарные больные, и если их привезут, то только из другого лечебного учреждения. Чаще всего это пациенты палат интенсивной терапии или реанимации, и такой возбудитель носит на 100% нозокомиальный характер.
Когда можем его обнаружить:
И всегда это будет ятрогенное поражение как следствие неправильной гигиены рук персонала либо обработки инструментария. Можно возразить «но как же тяжелые перитониты?». Отвечу тем, что для тяжелых перитонитов без дефектов ухода наиболее характерен штамм на третьем рисунке, так как для того, чтобы вырастить такую зверюгу, тяжелому перитониту здоровья не хватит, он от осложнений погибнуть успеет, а сама кишечная палочка ножками ходить не умеет, мы ее исключительно неправильно мытыми ручками разносим, и доказать это элементарно, так как точно такие же штаммы будут высеваться при плановых проверках эпидемиологической службы.
А теперь подведем небольшой итог нашего непростого разговора:
Резюмируя вышесказанное, и как бы обидно это ни прозвучало, но почти всегда инфекции, вызванные кишечной палочкой, – это «болезни грязных рук» и показатель микробиологического неблагополучия. И одна из серьезных проблем медико-профилактических служб, так как при всем желании они не смогут полностью изъять источник инфицирования, так как он в прямом смысле находится во всех нас, и только соблюдение санитарных правил и санпросвет. работа могут значительно поспособствовать в сдерживании развития вышеуказанных заболеваний.
ИНСТРУКЦИЯ
по медицинскому применению лекарственного препарата
Торговое наименование препарата
Международное непатентованное наименование
Лекарственная форма
лиофилизат для приготовления раствора для приема внутрь
Состав
В одной дозе препарата содержится;
Описание
Препарат имеет вид кристаллической или пористой массы различных оттенков бежевого или беловато-серого цвета со специфическим запахом.
Фармакотерапевтическая группа
Код АТХ
Фармакодинамика:
Показания:
Лечение хронических колитов состояний после острых кишечных инфекций дисфункций кишечника возникающих в результате дисбактериозов различной этиологии у взрослых и детей с 6 месячного возраста.
-при затяжной и хронической дизентерии;
-колитах и энтероколитах различной этиологии;
-дисбактериозах различной этиологии;
-аллергическом и алиментарном гастроэнтерите и колите;
— острых сосудистых болезнях кишечника;
-протозойных кишечных болезнях шигелеллезе других кишечных инфекциях;
-диарее и гастроэнтерите предположительно инфекционного происхождения;
-в комплексном лечении при хронических заболеваниях желудочно-кишечного тракта (неспецифических и специфических хронических колитах и энтероколитах с выраженными дисбиотическими нарушениями) в случаях необходимости выраженного стимулирующего воздействия на организм;
-после острых кишечных инфекций.
Противопоказания:
Детский возраст с рождения до 6 месяцев.
Специфические и неспецифические язвенные колиты.
Беременность и лактация:
Способ применения и дозы:
Содержимое флакона растворить кипяченой водой комнатной температуры из расчета 5 мл (чайная ложка) воды на 1 дозу препарата.
Препарат принимать не менее чем за 20-30 мин до еды и через 1-2 часа после еды. Грудным детям препарат можно давать непосредственно перед кормлением.
Препарат принимают внутрь в следующих суточных дозах:
Суточные дозы можно делить на 2-3 приема.
Количество доз и продолжительность лечения определяет врач в зависимости от тяжести длительности заболевания и выраженности дисбактериоза.
При необходимости курсы лечения могут быть повторены но не ранее чем через 3-6 месяцев с предварительным исследованием микрофлоры желудочно-кишечного тракта. В промежутках между назначениями колибактерина больным показаны бифидо-или лактосодержащие препараты.
Особенности действия препарата при первом приеме или его отмене. Не выявлено.
При пропуске приема одной или нескольких доз следует повторно принять последнюю принятую дозу и далее продолжать лечение по указанной схеме.
Побочные эффекты:
Применение колибактерина обычно не вызывает побочных реакций. В редких случаях в процессе лечения возможно появление легких диспептических расстройств которые обычно проходят самостоятельно и не требуют отмены препарата или назначения лечения. В случае более выраженной реакции целесообразна временная отмена препарата или прекращение лечения колибактерином. Если любые из указанных в инструкции побочных эффектов усугубляются или Вы заметили любые другие побочные эффекты не указанные в инструкции сообщите об этом врачу.
Передозировка:
Взаимодействие:
Не рекомендуется одновременное проведение химиотерапии и лечение антибиотиками.
Особые указания:
Влияние на способность управлять трансп. ср. и мех.:
Форма выпуска/дозировка:
Упаковка:
По 5 доз во флаконе.
По 5 флаконов в контурной ячейковой упаковке из пленки поливинилхлоридной запаянной алюминиевой фольгой или без неё. В пачке из картона две контурные ячейковые упаковки или 10 флаконов с разделяющей змейкой инструкция по применению.
Условия хранения:
Хранить в сухом защищенном от света месте при температуре не выше 10 °С.
Срок годности:
1 год. Не применять после окончания срока годности.
Условия отпуска
Производитель
Эшерихиозы
Эшерихиозы ( ЮEscherichioses ) — коли-инфекция, коли-энтерит, диарея путешественников — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечных палочек, протекающих с симптомами общей интоксика
Эшерихиозы (ЮEscherichioses) — коли-инфекция, коли-энтерит, диарея путешественников — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечных палочек, протекающих с симптомами общей интоксикации и поражением желудочно-кишечного тракта (ЖКТ) с развитием гастроэнтерита или энтероколита, в редких случаях — как генерализованная форма болезни с внекишечными проявлениями.
Согласно Международной классификации болезней 10-го пересмотра (МКБ-10, 1997) регистрация эшерихиозов проводится под шифрами:
А04,0 — энтеропатогенный эшерихиоз;
А04,1 — энтеротоксигенный эшерихиоз;
А04,2 — энтероинвазивный эшерихиоз;
А04,3 — энтерогеморрагический эшерихиоз;
А04,4 — эшерихиоз других патогенных серогрупп.
История и распространение. Возбудитель открыт немецким педиатром T. Эшерихом в 1886 г. Он выделил его из кишечника детей и определил как Bacterium coli commune, предположив, что она может быть причиной поносов у детей. В его честь микроб назван Еscherichia coli.
Эшерихии — постоянные обитатели кишечника человека, но некоторые из них могут вызывать поражения ЖКТ, что доказано экспериментально Г. Н. Габричевским в 1894 г. и подтверждено клинически в 1922 г. А. Адамом. Различие по антигенной структуре патогенных и непатогенных кишечных палочек, выявленное Ф. Кауфманном в 1942–1945 гг., легло в основу классификации патогенных эшерихий. По рекомендации ВОЗ эшерихии, вызывающие поражение ЖКТ, называются диареегенными.
Эшерихиоз — повсеместно распространенное заболевание, чаще диагностируемое у детей до 1 года; у взрослых оно регистрируется как диарея путешественников. Групповые вспышки зарегистрированы в последние годы в Канаде, США, Японии, России и других странах. Показатель заболеваемости эшерихиозом остается высоким в Калининграде, Санкт-Петербурге, Ненецком автономном округе. Так, в Калининграде с 1999 по 2002 г. зарегистрировано более 1000 случаев заболевания на 100 тыс. населения. В Москве выявлено около 1000 случаев заболевания эшерихиозом на 100 тыс. населения за последние 10 лет; летальных исходов нет.
Этиология. Эшерихии — подвижные грамотрицательные палочки, аэробы, относящиеся к виду Еscherichia (Е.) coli, роду Escherichia, семейству Enterobacteriaceae. Растут на обычных питательных средах, выделяют бактерицидные вещества — колицины. Серовары не имеют морфологических отличий. Эшерихии содержат соматические антигены (О-Аг) 173 серотипов, капсульные (К-Аг) — 80 сероваров и жгутиковые (Н-Аг) — 56 серотипов. Диареегенные кишечные палочки подразделяются на пять типов: энтеротоксигенные (ЭТКП, ETEC), энтеропатогенные (ЭПКП, EPEC), энтероинвазивные (ЭИКП, EIEC), энтерогеморрагические (ЭГКП, EHEC), энтероадгезивные (ЭАКП, EAEC).
Фактор патогенности ЭТКП — пили (разновидность ворсинок), или фимбриальные факторы, которые определяют способность к адгезии и колонизации нижних отделов тонкого кишечника, а также к токсинообразованию. Термолабильный и термостабильный энтеротоксины ответственны за повышенную экскрецию жидкости в просвет кишки. ЭИКП, имеющие плазмиды, способны проникать в клетки кишечного эпителия и размножаться в них. Патогенность ЭПКП обусловлена способностью к адгезии. ЭГКП выделяют цитотоксин, шигоподобные токсины 1-го и 2-го типов, содержат плазмиды, которые облегчают адгезию к энтероцитам. Факторы патогенности энтероадгезивных кишечных палочек изучены недостаточно.
Эшерихии устойчивы в окружающей среде, могут месяцами сохраняться в воде, почве, испражнениях. Сохраняют жизнеспособность в молоке до 34 дней, в детских питательных смесях — до 92 дней, на игрушках — до 3–5 мес. Хорошо переносят высушивание, обладают способностью размножаться в пищевых продуктах, особенно в молоке. Быстро погибают при воздействии дезинфицирующих средств и при кипячении. У многих штаммов Е. соli отмечается резистентность к ряду антибиотиков (неомицин, ампициллин, цефалотин и др.). Устойчивость к антибиотикам выявлена у 13–35,1% штаммов патогенных эшерихий.
Эпидемиология. Основной источник эшерихиозов — больные со стертыми формами заболевания; меньшую роль играют реконвалесценты и носители. Значимость последних возрастает, если они работают на предприятиях по приготовлению и реализации пищевых продуктов. Однако, по мнению W. Robson et al. (1993), B. Bell et al. (1994), источник инфекции при энтерогеморрагических эшерихиозах (О157) — крупный рогатый скот. Инфицирование людей происходит при употреблении продуктов, которые были недостаточно термически обработаны. Зарегистрированы групповые вспышки заболеваний эшерихиозом О157 в США, Канаде, Японии — странах, где распространено употребление в пищу гамбургеров. Это и дало основание данным исследователям рассматривать эшерихиоз О157 как антропозоонозное заболевание. Механизм передачи — фекально-оральный, который реализуется пищевым путем, реже — водным и бытовым. По данным ВОЗ, пищевой путь характерен для энтеротоксигенных и энтероинвазивных эшерихий, бытовой — для энтеропатогенных.
Из пищевых продуктов фактором передачи чаще являются молочные изделия, готовые мясные продукты, напитки (квас, компот и др.).
В детских коллективах распространение инфекции может происходить через игрушки, загрязненные предметы обихода, через руки больных матерей и персонала. Реже регистрируется водный путь передачи эшерихиозов. Наиболее опасно загрязнение открытых водоемов, которое происходит в результате сброса необезвреженных хозяйственно-бытовых сточных вод, особенно из детских учреждений и инфекционных больниц.
Восприимчивость к эшерихиозам высокая, особенно среди новорожденных и ослабленных детей. Около 35% детей, которые общались с источником инфекции, становятся носителями. У взрослых восприимчивость повышается в связи с переездом в другую климатическую зону, изменением характера питания и т. д. (диарея путешественников).
Эпидемический процесс, вызванный разными возбудителями Е. соli, может различаться. Заболевания, вызванные эшерихиями ЕТЕС, чаще регистрируются в развивающихся странах тропических и субтропических зон в виде спорадических случаев, а групповые случаи — среди детей 1–3 лет. Эшерихиозы, вызванные ЕIЕС, хотя и регистрируются во всех климатических зонах, преобладают в развивающихся странах. Заболевания носят групповой характер среди детей 1–2 лет в летне-осенний период. ЕРЕС вызывает спорадическую заболеваемость во всех климатических зонах, чаще всего среди детей до 1 года, которые находились на искусственном вскармливании. Эшерихиозы, вызванные ЕНЕС и ЕАЕС, выявлены в странах Северной Америки и Европы среди взрослых и детей старше 1 года; для них характерна летне-осенняя сезонность. Вспышки среди взрослых чаще регистрировались в домах для престарелых.
Патоморфологические данные определяются локализацией патологического процесса и малохарактерны.
Патогенез. Эшерихии проникают через рот, минуя желудочный барьер, и, в зависимости от типовой принадлежности, оказывают свое патогенное действие.
Энтеротоксигенные штаммы способны к выработке энтеротоксинов и фактора колонизации, с помощью которого осуществляется прикрепление и колонизация тонкой кишки.
Энтеротоксины — это термолабильные или термостабильные вещества, воздействующие на биохимические функции эпителия крипт, не вызывая видимых морфологических изменений. Энтеротоксины усиливают активность аденилатциклазы и гуанилатциклазы. При их участии и под стимулирующим влиянием простагландинов увеличивается образование циклического аденозинмонофосфата. В результате в просвет кишки секретируется большое количество воды и электролитов, которые не успевают реабсорбироваться в толстой кишке, и развивается диарея с последующими нарушениями водно-электролитного баланса.
Заражающая доза ЭТКП составляет 108–1010 микробных клеток.
ЭИКП обладают способностью внедряться в клетки эпителия толстой кишки. Проникновение ЭИКП в слизистую оболочку приводит к развитию воспалительной реакции и образованию эрозий кишечной стенки. Повреждение эпителия способствует увеличению всасывания в кровь эндотоксинов. У больных в испражнениях появляются слизь, кровь и полиморфноядерные лейкоциты. Заражающая доза ЭИКП — 5х105 микробных клеток.
Механизм патогенности ЭПКП малоизучен. У штаммов 055, 086, 0111 и др. выявлен фактор адгезии к клеткам Нер-2, за счет которого обеспечивается колонизация тонкого кишечника. У других штаммов (018, 044, 0112 и др.) этот фактор не обнаружен. Видимо, они имеют иные факторы патогенности, которые пока неизвестны. Заражающая доза ЭПКП — 10х1010 микробных клеток.
ЭГКП выделяют цитотоксин SLT (Shiga-like toxin), который вызывает разрушение клеток эндотелия мелких кровеносных сосудов кишечной стенки проксимальных отделов толстой кишки. Сгустки крови и фибрин приводят к нарушению кровоснабжения кишки, появлению в кале крови. Происходит развитие ишемии кишечной стенки вплоть до некроза. У некоторых больных наблюдаются осложнения с развитием синдрома диссеменированного сосудистого свертывания, инфекционного токсического шока и острой почечной недостаточности (ОПН).
ЭАКП способны к колонизации эпителия тонкой кишки. Вызванные ими заболевания взрослых и детей протекают длительно, но легко. Это связано с тем, что бактерии прочно закрепляются на поверхности эпителиальных клеток.
После перенесенного заболевания формируется кратковременный непрочный типоспецифический иммунитет.
Клиника. Клинические проявления эшерихиозов зависят от типа возбудителя, возраста больного, иммунного статуса.
Принята следующая клиническая классификация эшерихиозов (Н. Д. Ющук, Ю. Я. Венгеров, 1999).
По этиологическим признакам:
По форме заболевания:
По тяжести течения:
При эшерихиозе, вызванном энтеротоксигенными штаммами, инкубационный период продолжается от 16 до 72 ч. Характерно холероподобное течение болезни, протекающее с поражением тонкой кишки без выраженного синдрома интоксикации (диарея путешественников).
Заболевание начинается остро; больных беспокоят слабость, головокружение, температура нормальная или субфебрильная. Появляются тошнота, повторная рвота, разлитые боли в животе схваткообразного характера, стул частый (до 10–15 раз в сутки), жидкий, обильный, водянистый, нередко напоминающий рисовый отвар. Живот вздут, при пальпации определяется урчание, небольшая разлитая болезненность.
Заболевание может иметь как легкое, так и тяжелое течение. Тяжесть течения определяется степенью дегидратации. Возможна молниеносная форма заболевания с быстрым развитием эксикоза. Длительность болезни — 5–10 дней.
Энтероинвазивные эшерихии вызывают дизентериеподобное заболевание, которое протекает с симптомами общей интоксикации и преимущественным поражением толстой кишки. Инкубационный период длится 6–48 ч. Начало острое, характеризуется повышением температуры до 38–39 °С, ознобом, слабостью, головной болью, болью в мышцах, снижением аппетита. У части больных температура нормальная или субфебрильная. Через несколько часов присоединяются симптомы поражения ЖКТ (боли схваткообразного характера, преимущественно в нижней части живота, ложные позывы на дефекацию, тенезмы, жидкий стул — обычно калового характера с примесью слизи и крови до 10 и более раз в сутки. При более тяжелом течении заболевания — стул в виде «ректального плевка». Сигмовидная кишка — спазмированная, уплотненная и болезненная. Печень и селезенка не увеличены. При ректороманоскопии — катаральный, реже — катарально-геморрагический или катарально-эрозивный проктосигмоидит.
Течение болезни доброкачественное. Лихорадка длится 1–2, реже — 3–4 дня; длительность заболевания — 5–7 дней. Через 1–2 дня стул нормализуется, спазм и болезненность толстой кишки сохраняются в течение 5–7 дней болезни. Восстановление слизистой оболочки толстой кишки наступает к 7–10-му дню болезни.
У детей энтеропатогенный эшерихиоз, вызываемый Е. соli 1-го класса, протекает в виде различной тяжести энтеритов, энтероколитов, а у новорожденных и недоношенных детей — в септической форме. Для кишечной формы у детей характерно острое начало болезни, температура — 38–39 °С, слабость, рвота, водянистая диарея, стул желтого или оранжевого цвета. Быстро развивается токсикоз и эксикоз, масса тела снижается. Септическая форма заболевания протекает с выраженными симптомами интоксикации (повышение температуры, анорексия, срыгивание, рвота). Возникают множественные гнойные очаги.
Энтеропатогенный эшерихиоз, вызываемый Е. соli 2-го класса, регистрируется у взрослых и детей. Инкубационный период — 1–5 дней. Характерно острое начало заболевания (температура — 38–38,5 °С, озноб, нечастая рвота, боли в животе, стул без патологических примесей, жидкий, до 5–8 раз в сутки), течение доброкачественное. У некоторых больных отмечаются гипотония, тахикардия.
При эшерихиозе, вызванном энтерогеморрагическими штаммами, заболевание характеризуется синдромом общей интоксикации и поражением проксимального отдела толстой кишки. Инкубационый период составляет 1–7 дней. Заболевание начинается остро с болей в животе, тошноты, рвоты. Температура субфебрильная или нормальная, стул жидкий, до 4–5 раз в день, без примеси крови. Состояние больных ухудшается на 2–4-й день болезни, когда стул учащается, появляются примесь крови, тенезмы. При эндоскопическом исследовании выявляется катарально-геморрагический или фибринозно-язвенный колит. Более выраженные патоморфологические изменения обнаруживаются в слепой кишке. Наиболее тяжело протекает заболевание, вызванное штаммом 0157.Н 7. У 3–5% больных через 6–8 дней от начала заболевания развивается гемолитико-уремический синдром (синдром Гассера), который проявляется гемолитической анемией, тромбоцитопенией и развитием ОПН и токсической энцефалопатии (судороги, парезы, сопор, кома). Летальность в этих случаях может составлять 3–7%. Синдром Гассера чаще регистрируется у детей до 5 лет.
Особенности эшерихиоза, вызванные энтероадгезивными штаммами, изучены мало. Заболевание регистрируется у пациентов с ослабленной иммунной системой. Чаще выявляются внекишечные формы — поражение мочевыводящих (пиелонефрит, цистит) и желчевыводящих (холецистит, холангит) путей. Возможны септические формы (коли-сепсис, менингит).
Чаще эшерихиозы протекают доброкачественно, но возможны осложнения — такие как инфекционный токсический шок, гиповолемический шок с дегидратацией 3–4-й степени, ОПН, сепсис, пневмония, пиелоцистит, пиелонефрит, холецистит, холангит, менингит, менингоэнцефалит.
Диагностика. Клиническая картина эшерихиозов сходна с другими кишечными инфекциями, поэтому основу подтверждения диагноза составляют бактериологические методы исследования. Материал (испражнения, рвотные массы, промывные воды желудка, кровь, мочу, ликвор, желчь) следует брать в первые дни болезни до назначения больным этиотропной терапии. Посевы производят на среды Эндо, Левина, Плоскирева, а также на среду обогащения Мюллера.
Применяются серологические методы исследования — реакция агглютинации, реакция непрямой гемагглютинации — в парных сыворотках, но они неубедительны, так как возможны ложно-положительные результаты из-за антигенного сходства с другими энтеробактериями, и используются для ретроспективной диагностики, особенно во время вспышки.
Перспективным методом диагностики является полимеразная цепная реакция (ПЦР). Инструментальные методы обследования (ректороманоскопия, колоноскопия) при эшерихиозах малоинформативны.
Дифференциальный диагноз эшерихиозов проводят с другими острыми диарейными инфекциями: холерой, шигеллезом, сальмонеллезом, кампилобактериозом, пищевыми токсикоинфекциями стафилококковой этиологии и вирусными диареями: ротавирусной, энтеровирусной, Норволк-вирусной инфекцией и др.
В отличие от эшерихиозов, холера характеризуется отсутствием интоксикации, лихорадки, болевого синдрома, наличием многократной рвоты, быстрым развитием дегидратации 3–4-й степени. Помогает в постановке диагноза эпидемиологический анамнез — пребывание в эндемичных регионах холеры.
Шигеллезу, в отличие от эшерихиозов, свойственна высокая лихорадка; боли локализуются в левой подвздошной области; пальпируется спазмированная, болезненная сигмовидная кишка; стул скудный, в виде «ректального плевка».
Сальмонеллез, в отличие от эшерихиозов, характеризуется более выраженной интоксикацией, разлитыми болями в животе, болезненностью при пальпации в эпигастральной и околопупочной областях, урчанием. Характерен зловонный стул зеленоватого цвета.
При проведении дифференциальной диагностики эшерихиозов с кампилобактериозом также выявляются определенные различия. Для кампилобактериоза более характерно начало заболевания с продромального периода (артралгий, слабости, озноба). Боли в животе, диарея присоединяются на 2–3-й день болезни. Боль в животе локализуется чаще в левой подвздошной области. Возможны сыпь, увеличение печени. Заражение чаще всего происходит при употреблении в пищу инфицированного мяса (свинины, говядины, мяса птиц).
Для пищевых токсикоинфекций стафилококковой этиологии, в отличие от эшерихиозов, характерно острое, бурное начало заболевания, короткий инкубационный период (30–60 мин). Более выражены симптомы интоксикации — рвота неукротимая, боли в животе режущего характера с локализацией в эпигастральной и околопупочной областях. Характерен групповой характер заболевания, связь заболевания с пищевым фактором, быстрый регресс болезни.
Для ротавирусного гастроэнтерита, в отличие от эшерихиозов, характерны катаральные явления, изменения слизистой ротоглотки (гиперемия, зернистость), слабость, адинамия. Боли в животе диффузные, стул жидкий, «пенистый», с резким кислым запахом, позывы на дефекацию носят императивный характер. При пальпации отмечается «крупнокалиберное» урчание в области слепой (реже — сигмовидной) кишки.
При проведении дифференциального диагноза эшерихиозов с энтеровирусной инфекцией также можно выявить определенные отличия. Для энтеровирусной инфекции характерны катаральные явления, субфебрильная температура (до недели), многократная мучительная рвота, продолжительность диареи до 2 нед, увеличение печени и селезенки.
Для Норволк-вирусной инфекции, в отличие от эшерихиозов, характерны короткий инкубационный период от 10 ч до 2 сут, ломота в мышцах, головокружение, боли в эпигастральной и околопупочной областях. Продолжительность заболевания короткая — от нескольких часов до 3 сут.
Лечение. Госпитализация больных с эшерихиозами проводится по клиническим и эпидемиологическим показаниям. Больные при среднетяжелом и тяжелом течении заболевания госпитализируются в инфекционные больницы. В легких случаях заболевания больные могут лечиться амбулаторно при наличии благоприятных бытовых санитарно-гигиенических условий.
По эпидемиологическим показаниям госпитализации подлежат лица из декретированных групп, больные из организованных коллективов, а также пациенты, проживающие в коммунальных квартирах, общежитиях.
Госпитализируются больные, если в семье есть лица, относящиеся к декретированным группам.
В остром периоде болезни больным рекомендуется щадящая диета (стол № 4, при нормализации стула — № 2, в период реконвалесценции — стол № 13).
В легких случаях заболевания достаточно назначения пероральной регидратационной терапии (Глюкосалан, Цитроглюкосалан, Регидрон и др.), количество которых должно в 1,5 раза превышать потери воды с испражнениями.
Показаны ферменты (Панзинорм форте, Фестал, Мезим форте, Креон), энтеросорбенты (Энтеросгель, Энтеродез, Полифепан, Полисорб — в течение 1–3 дней). При легком течении болезни целесообразно использование кишечных антисептиков (Интетрикс по 2 капсулы 3 раза в день, Неоинтестопан после каждого акта дефекации по 2 таблетки — до 14 в сутки, Энтерол по 2 капсулы 2 раза в день) в течение 5–7 дней. Легкие и стертые формы эшерихиозов не требуют назначения этиотропных препаратов.
При лечении больных в условиях стационара показан постельный режим в первые 2–3 дня. Назначается этиотропная терапия. С этой целью при среднетяжелых формах используется один из следующих препаратов: ко-тримоксазол (Бактрим, Бисептол, Септрин) по 2 таблетки 2 раза в день. Из препаратов фторхинолонового ряда назначается ципрофлоксацин — Ципролет — фторхинолон для широкого клинического применения, сочетающий мощное бактерицидное действие, широкий антимикробный спектр и благоприятную фармакокинетику. Механизм действия препарата, связанный с ингибированием ДНК-гиразы и топоизомеразы, обусловливает отсутствие перекрестной резистентности. Максимальные концентрации ципрофлоксацина (Ципролета) в плазме крови достигаются через 60–90 мин. Для препарата характерно быстрое начало действия. Биодоступность препарата более 63–77% и высокий показатель проникновения в ткани, жидкости и клетки обеспечивают его эффективность при назначении в небольших дозировках. Препарат отличается хорошим профилем безопасности и положительной динамикой, проявляющейся в короткие сроки. Также рекомендуются Ципробай, Ципросол по 500 мг 2 раза в сутки перорально, пефлоксацин (Абактал) по 400 мг 2 раза в сутки, офлоксацин (Таривид) по 200 мг 2 раза в сутки, длительность терапии — 5–7 дней.
В тяжелых случаях фторхинолоны применяются вместе с цефалоспоринами II поколения (цефуроксим 750 мг 4 раза в сутки внутривенно или внутримышечно; цефаклор 750 мг 3 раза в сутки внутримышечно; цефтриаксон 1 г 1 раз в сутки внутривенно) и III поколения (цефоперазон 1 г 2 раза в сутки внутривенно или внутримышечно; цефтазидим 2 г 2 раза в сутки внутривенно или внутримышечно).
При дегидратации 2–3-й степени назначают регидратационную терапию внутривенно кристаллоидными растворами (Хлосоль, Ацесоль, Лактосоль, Квартасоль).
Объем регидратационной терапии определяется на основании учета степени обезвоживания и массы тела больного. Лечение проводят в два этапа: ликвидация имеющегося обезвоживания и коррекция продолжающихся потерь жидкости.
Скорость введения полиионных растворов составляет от 60 до 80 мл/мин в зависимости от степени дегидратации. При выраженных симптомах интоксикации используются коллоидные растворы (Гемодез, Реополиглюкин и др.) в объеме 400–800 мл в сутки.
Особое внимание должно быть уделено терапии больных эшерихиозом 0157, так как у них возможно появление тяжелых осложнений.
После приема антибактериальных препаратов при продолжающейся диарее используют эубиотики для коррекции дисбактериозов (Бифиформ, Бифистим, Бифидумбактерин форте, Аципол, Хилак форте, Пробифор и др.) в течение 7–10 дней.
Выписка реконвалесцентов проводится после полного клинического выздоровления при отрицательных результатах бактериологического исследования. Для больных из декретированных групп необходимо наличие двукратного отрицательного бактериологического исследования кала, проведенного через 2 дня после окончания этиотропной терапии.
После выписки из стационара больные находятся на диспансерном наблюдении в кабинете инфекционных заболеваний поликлиник в течение 1 мес. В конце срока наблюдения проводят двукратное бактериологическое исследование кала с интервалом в 2–3 дня (лицам, относящимся к декретированным группам).
Коли-инфекция у взрослых протекает благоприятно, перехода в хронические формы не наблюдается.
Профилактические мероприятия. Основу профилактики эшерихиозов составляют меры по пресечению путей передачи возбудителя. Особенно важно соблюдение санитарно-гигиенических требований на объектах общественного питания, водоснабжения, предупреждение контактно-бытового пути заражения в детских учреждениях, родильных домах, стационарах (использование индивидуальных стерильных пеленок, обработка рук дезинфицирующими растворами после работы с каждым ребенком, дезинфекция посуды, пастеризация, кипячение молока, молочных смесей). Готовые к употреблению и сырые продукты должны разделываться на разных разделочных досках разными ножами. Посуду, в которой транспортируют пищу, необходимо обработать кипятком.
При подозрении на эшерихиоз необходимо обследовать беременных до родов, рожениц, родильниц и новорожденных. Специфической профилактики эшерихиозов нет.
Мероприятия в очаге. Контактировавших с больными в очаге заболевания наблюдают в течение 7 дней. Дети, контактировавшие с больным эшерихиозом по месту жительства, допускаются в детские учреждения после разобщения с больным и трехкратных отрицательных результатов бактериологического исследования кала.
При выявлении больных эшерихиозом в детских учреждениях и родильных домах прекращается прием поступающих детей и рожениц. Персонал, матери, дети, бывшие в контакте с больным, а также дети, выписанные домой незадолго до заболевания, обследуются трехкратно (проводится бактериологическое исследование кала). При выявлении лиц с положительными результатами обследования их изолируют.
Литература
Г. К. Аликеева, кандидат медицинских наук
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
Г. М. Кожевникова, профессор
МГМСУ, Москва
Бактерийные и биологические препараты для коррекции дисбиозов и их рациональное применение
Статья опубликована в «Омской медицинской газете» №8 (29), май 1997 г.
В последние годы получили распространение новые подходы к лечению, связанные с восстановлением естественной экологии организма и основанные на использовании активных биологических продуктов. Одним из аспектов такого подхода является нормализация измененного микробного пейзажа организма при помощи бактерийных и биопрепаратов. В настоящее время усилиями новых промышленных и коммерческих структур традиционно существовавший дефицит бактерийных и биопрепаратов в основном снят. Более того, помимо таких давно знакомых препаратов, как бифидумбактерин, лактобактерин, колибактерин и бификол, появилось множество новых средств, среди которых трудно ориентироваться врачам, фармацевтам и пациентам. Надеемся, что предложенная в данной публикации систематизация бактерийных препаратов, предназначенных для коррекции биоценоза слизистых оболочек, поможет более полному и эффективному использованию всего их богатого арсенала в повседневной практике.
1.1.Препараты семейства бифидобактерий.
Самым известным и широко применяемым препаратом-эубиотиком является Бифидумбактерин, содержащий бифидобактерии вида бифидум. Именно этот вид бифидобактерий преобладает в кишечнике у новорожденных и детей первых лет жизни, поэтому бифидумбактерин является базовым препаратом для коррекции биоценоза кишечника у детей. Показания к применению бифидумбактерина очень широкие, но основными из них являются дисфункции кишечника вследствие дисбактериоза, острые кишечные инфекции (ОКИ), применение с профилактической целью у ослабленных детей с анемией, рахитом, диатезом и при раннем переводе детей с грудного на искусственное вскармливание и т.д..
Существует четыре основные формы выпуска Бифидумбактерина: флаконная, ампульная, таблетированная и в порошках в пакетах из ламинированной фольги. Применение бифидумбактерина в педиатрии диктует чрезвычайно жесткие требования к качеству препарата, и, прежде всего по отсутствию посторонней микрофлоры. В связи с этим, таблетированная форма бифидумбактерина разрешена к применению только с трех лет. С неонатального периода разрешен к применению только Бифидумбактерин в порошке, флаконах или ампулах. Ряд существенных преимуществ имеет форма Бифидумбактерина в порошке производства АО «Партнер», которая представляет собой смесь сухих бифидобактерий с химически чистой лактозой, упакованную в газонепроницаемые пакеты из ламинированной алюминиевой фольги. Технология производства этого препарата предусматривает удаление среды культивирования и практически полное отсутствие (менее 10%) мертвых бактериальных клеток. Поэтому при растворении препарата образуется почти бесцветная опалесцирующая взвесь без выраженного запаха и вкуса. Лактоза, способствующая росту бифидобактерий в кишечнике, несколько увеличивает время растворения препарата.
Бифидумбактерин в свечах используется для лечения дисфункции кишечника с поражением его дистальных отделов (колиты, проктиты) и в гинекологической практике (сенильные неспецифические бактериальные кольпиты, бактериальные вагинозы, нарушение чистоты влагалища 3-4 степени, подготовка родовых путей к родам и т.п.).
Бифидин в качестве действующего вещества содержит бифидобактерии вида адолесцентис, которые обладают более широким спектром ферментации углеводов. Однако данный вид бифидобактерий вегетирует в кишечнике взрослых и детей старше трех лет. У детей до года бифидобактерии адолесцентис встречаются только в случае их искусственного вскармливания. Препарат назначается детям старше трех лет при кишечных расстройствах сопровождающихся дисбактериозом, больным детям на раннем искусственном вскармливании, при затяжном течении кишечных дисфункций, при повторном выделении возбудителей после ОКИ.
Бифилонг содержит бифидобактерии вида лонгум, являющимися вторыми по количественному содержанию после бифидобактерий вида бифидум представителями нормальной микрофлоры детей, находящихся на грудном вскармливании. Промышленный выпуск Бифидина и Бифилонга в настоящее время не осуществляется.
В Новосибирске, в ЗАО «НПФ Вектор-Биомед» освоен выпуск Концентрата бифидобактерий, представляющего собой взвесь бифидобактерий, вида бифидум в культуральной молочной среде. Препарат зарегистрирован как пищевая добавка и распространяется через дистрибьютерскую сеть врачей. В качестве достоинства Концентрата указывается на то, что бифидобактерии в препарате находятся в фазе роста и, следовательно, они более активные. Однако тот факт, что для достижения клинического эффекта требуется прием Концентрата в дозах, в десятки раз превышающий те, что используются при лечении фармакопейным бифидумбактерином (соответственно 8000 и 300 доз) позволяет усомниться в этом.
В Новосибирске в ООО «Био-Веста», выпускается почти аналогичный препарат — Жидкий концентрат бифидобактерий (Биовестин), действующим веществом в котором выступают бифидобактерии вида адолесцентис, особенности применения которых названы выше.
1.2. Препараты семейства лактобактерий
Лактобактерии вместе с бифидобактериями являются также основными представителями нормальной микрофлоры человека. Лактобактерии присутствуют во всех отделах пищеварительного тракта, начиная с полости рта и, кончая толстой кишкой, являются превалирующей флорой генитального тракта, обнаруживаются в грудном молоке.
Первые попытки лечебного применения лактобактерий для коррекции биохимических процессов, протекающих в кишечнике, предпринимались И.И.Мечниковым еще 100 лет назад. В последующем была обнаружена выраженная антагонистическая активность лактобактерий против гнилостных условно-патогенных микроорганизмов и возбудителей острых кишечных и инфекций, которая связывается со способность лактобацилл образовывать молочную кислоту, перекись водорода, лизоцим и другие вещества с противомикробным действием к широкому спектру грампозитивных и грамнегатиивных бактерий. Выявлены репаративные свойства и иммунномодулирующая роль лактобактерий, проявляющаяся в частности в способности повышать общий уровень секреторного Ig A и титры специфических секреторных антител, усиливать фагоцитоз и др. Обсуждается роль лактобактерий в снижении уровня холестерина в крови, в предупреждении продукции канцерогенов и в разрушении щавелевой кислоты, препятствуя тем самым образованию в организме оксалатов.
В нашей стране широко используется препарат Лактобактерин, созданный в начале 70-х годов на основе лактобактерий вида плантарум (plantarum), оказывающие как и бифидобактерии, антагонистическое действие в отношении патогенных и условно-патогенных микроорганизмов. Показания к его применению схожи с таковыми у бифидумбактерина.
В Московском НИИ Эпидемиологии и Микробиологии им.Г.Н.Габричевского был разработан новый препарат Ацилакт, в состав которого входят лактобактерии вида ацидофилус (acidophilus). В отличие от лактобактерий вида плантарум, используемые для приготовления Ацилакта ацидофильные лактобактерии принадлежат к категории облигатных для человека микроорганизмов. Критериями для отбора нового промышленного вида лактобактерий служили способность бактерий к кислотообразованию, противомикробная активность, адгезивные свойства, способствующие длительному сохранению в кишечнике, устойчивость к действию пищеварительных секретов и применяемым антибиотикам. Всем этим условиям соответствуют новый препарат Ацилакт.
Ацилакт применяют по показаниям, общими с другими бактерийными препаратами: дисбактериозы кишечника, острые кишечные инфекции, хронические энтероколиты, а также воспалительные заболевания слизистой оболочки полости рта. Поскольку Ацилакт характеризуется повышенной кислотообразующей активностью, он предпочтителен для лечения дисбактериозов у больных с гипоацидными состояниями и сниженной перистальтикой кишечника.
Уменьшенное содержание в Ацилакте лактозы, в сочетании с высокой способностью составляющих основу препарата ацидофильных лактобактерий расщеплять лактозу, делают Ацилакт средством выбора для лечения дисбактериозов кишечника у пациентов с непереносимостью молока (лактазной недостаточностью).
Применение Ацилакта в течение 2-3-х курсов у детей с атопическим дерматитом приводит к нормализации исходно угнетенного иммунитета и улучшению клинической симптоматики.
Ацилакт может использоваться для лечения гинекологических заболеваний, сопровождающихся нарушением вагинальной микрофлоры, однако в данном случае более удобно применение Ацилакта в свечах. В норме микрофлора влагалища представлена преимущественно лактобактериями, так называемыми палочками Дедерлейна, которые поддерживают во влагалище кислую среду и подавляют рост условно-патогенных микроорганизмов. Ацилакт в свечах применяют при патологических состояниях, связанных с дефицитом лактофлоры женских половых путей, которые особо значимы при следующих заболеваниях:
Противопоказанием к назначению Ацилакта в свечах является кандидоз, так как в некоторых случаях быстрое смещение pH в кислую сторону способствует росту грибков. Ацилакт в данном случае используется после специфической противогрибковой терапии или после применения Бифидумбактерина в свечах.
Выпускается также Ацилакт в таблетках, применение которого путем рассасывания во рту показано при воспалительных заболеваниях десен и слизистой ротовой полости
1.3.Препараты семейства колибактерий
Комбинированный препарат Бификол содержит бифидобактерии вида бифидум и кишечную палочку штамма М-17, следовательно, его действие и показания к применению во многом схожи с таковыми у Бифидумбактерина и Колибактерина.
За рубежом также выпускается немало препаратов-эубиотиков, однако из-за высокой стоимости попытки их широкого внедрения на российском фармацевтическом рынке до сих пор успеха не имели.
Бифиформ (Ferrosan) выпускается в капсулах с желудочнонерастворимым покрытием и содержит бифидобактерии вида бифидум и энтерококки.
Другой большой класс биопрепаратов, используемых для коррекции дисбактериоза и лечения диарейных заболеваний составляют пробиотики. Пробиотики являются активаторами роста нормальной микрофлоры и выделяют вещества, подавляющие размножение патогенных микроорганизмов.
Все препараты на основе спор бактерий Bacillus subtilis имеют схожий механизм действия. Споры бацилл прорастают в вегетативную форму в тонкой кишке. Этот процесс достигает максимума в илеоцекальной области. При прорастании спор высвобождаются ферменты, способствующие расщеплению белков, жиров и углеводов, а также образуется кислая среда, препятствующая процессам гниения и росту патогенных бактерий. Кроме того, ферменты вызывают непосредственный лизис клеточных стенок протея, кишечной палочки, патогенного стафилококка. Поскольку данный штамм бацилл получен искусственным путем и не является физиологическим компонентом биоценоза кишечника, при назначении препаратов из спорообразующих микроорганизмов рекомендуется осторожность: применение их короткими курсами и при слабом эффекте от предшествующего использования бактерийных препаратов-эубиотиков.
Более физиологично действие препарата Линекс (Lek), содержащего в качестве активных действующих веществ ацидофильные лактобактерии бактерии, бифидобактерии вида инфантис и фекальные стрептококки. Молочнокислые бактерии продуцируют молочную, уксусную и пропионовые кислоты. Создаваемая ими в кишечнике кислая среда является неблагоприятной для роста патогенных микроорганизмов. Молочнокислые бактерии участвуют в резорбции моносахаридов, стабилизируют мембраны клеток кишечного эпителия и регулируют всасываемость электролитов. Представители нормальной микрофлоры (бифидобактерии и фекальные стрептококки) способствую при этом восстановлению биоценоза кишечника.
Энтерол (Biocodex) содержит лиофилизированные грибки Sacchoromyces boulardii. Препарат нормализует нарушенное равновесие кишечной микрофлоы, способствует выработке лимфоидными клетками слизистой кишечника секреторного Ig A. Энтерол эффективен при диареях, обусловленных приемом антибиотиков, в том числе при псевдомембранозном колите, вызываемом клостридиальной спорообразующей микрофлорой.
Необычные свойства обнаружены у синтетического ингибитора протеолитических ферментов препарата ПАМБА (BYK GULDEN). ПАМБА увеличивает рост лактобацилл, бифидобактерий и кишечных палочек, одновременно снижая в протеолитическую активность протеев, псевдомонад и других микроорганизмов и усиливая макрофагальный фагоцитоз.
Бифидогенными свойствами обладает также пантотеновая кислота (Кальция пантотенат, Пантенол), входящая в состав многих поливитаминных препаратов, или используемая в виде отдельного препарата.
Для санации слизистых оболочек, кожных покровов и раневых поверхностей от патогенных и условнопатогенных бактерий с успехом применяются специфические бактериофаги. Бактериофаги являются вирусами, поражающими исключительно бактерии, относятся к экологически безопасным для человека биологическим объектам и могут быть использованы для лечения дисбактериозов, ОКИ, гнойных инфекций кожи в любом возрасте.
Бактериофаги, подобно другим вирусам, являются абсолютными внутриклеточными паразитами, их размножение происходит в живой клетке. Проникнув в бактерию через расположенные на ее поверхности фагоспецифические рецепторы, ДНК фага изменяет синтезирующие механизмы клетки, заставляя бактерию синтезировать ДНК и белки фага. На определенном этапе бактерия разрушается, и из нее выходит новое поколение дочерних бактериофагов. Важным свойством бактериофагов является их высокая специфичность, они избирательно лизируют бактерии не только определенного вида, но даже их отдельные серологические группы. Бактериофаги безошибочно находят и уничтожают только те бактерии, против которых направлено их действие, не затрагивая нормальную микрофлору организма, не говоря уже о его собственных клетках. Именно этим и объясняется отсутствие побочных эффектов и противопоказаний к применению бактериофагов, что делает особенно привлекательным их использование в педиатрической практике. Возникновение у бактерий антибиотикоустойчивости не сказывается на их чувствительности к бактериофагам, поэтому последние зачастую активны даже в отношении полирезистентной госпитальной микрофлоры. Однако следует учитывать специфичность бактериофагов: каждый вид фага распознают в качестве своей мишени только те серотипы бактерий, которые имеют определенные фагоспецифические рецепторы. Поэтому назначать бактериофаги необходимо под микробиологическим контролем чувствительности к ним данного возбудителя.
Отечественная промышленность выпускает большой спектр лекарственных бактериофагов: Стафилококковый, Стрептококковый, Коли, Протейный, Синегнойный, Клебсиеллезный, Брюшнотифозный, Дизентерийный, Сальмонеллезный. Имеются и их комбинированные формы: Колипротейний бактериофаг, Интести бактериофаг (содержит фаги шигелл Флекснера серовара 1,2,3,4,6 и Зонне, сальмонелл (паратифа А и В, энтерилитис, тифимуриум, холера суис, ораниенбург), энтеропатогенных групп кишечной палочки, протея вульгарис и мирабилис, стафилококков, синегнойной палочки и патогенных энтерококков), Пиобактериофаг комбинированный (содержит фаги стафилококков, стрептококков, патогенной кишечной палочки, протея и синегнойной палочки). Созвучный, но все-таки иной препарат Пиобактериофаг поливалентный очищенный содержит фаги стафилококков, стрептококков, патогенной кишечной палочки, синегнойной палочки, протея и клебсиелл пневмонии. Данный препарат отличается наиболее высокой степенью очистки от бактериальных метаболитов, что значительно улучшает его вкусовые качества и делает средством первого выбора у детей до года. Бактериофаг клебсиелл поливалентный очищенный активен в отношении клебсиелл пневмонии, озены, риносклеромы. Бактериофаг обычно выпускаются в жидкой форме или в таблетках, в настоящее время также налажен выпуск Пиобактериофага комбинированного и Стафилококкового бактериофага в форме линимента.
Пока наибольшее распространение бактериофаги нашли в лечении дисбактериозов кишечника, острых кишечных инфекций, энтероколитов, гнойно-воспалительных заболеваний горла и носа. Однако область их клинического применения значительно шире и они могут быть с успехом использованы для лечения хирургической, уро-генитальной, кожной и других инфекций.
4. ИММУНОГЛОБУЛИНОВЫЕ ПРЕПАРАТЫ
Принципиально новое направление в терапии дисбактериозов и ОКИ связано с созданием на шей стране оригинального лекарственного средства Комплексный иммуноглобулиновый препарат (КИП) КИП содержит иммуноглобулины человека трех классов: Ig A (15-25%), Ig M (15-25% ) и Ig G (50-70%). От всех других иммуноглобулиновых препаратов, применяемых в России, КИП отличает высокое содержание Ig A и Ig M, повышенная концентрация антител к энтеропатогенным бактериям кишечной группы (шигеллы, сальмонеллы, эшерихии, клебсиеллы и др.), высокая концентрация антител к ротавирусам, а также пероральный способ применения.
Входящий в состав КИПа Ig M оказывает бактерицидный эффект на патогенные микроорганизмы, Ig A затрудняет их прикрепление к эпителию слизистой оболочки, размножение и обеспечивает быстрое удаление из кишечника, Ig G нейтрализует микробные токсины и вирусы, опосредует «прилипание» бактерий к макрофагам с последующим их фагоцитозом. Помимо выведения из организма патогенных и условно-патогенных микроорганизмов, КИП способствует росту нормальной микрофлоры кишечника (бифидобактерий, лактобактерий, энтерококков и непатогенных кишечных палочек), повышает выработку секреторного Ig A и нормализует измененные показатели системного иммунитета. Пероральный способ приема КИПа обеспечивает поступление больших доз действующего вещества к месту поражения с последующим снижением адсорбции патогенов на клетках эпителия слизистой оболочки кишечника и местным иммуномодулирующим эффектом.
В ходе крупного сравнительного исследования показано, что среди всевозможных схем лечения ОКИ у детей именно терапия КИПом дает наилучшие результаты, оцениваемые по таким параметрам, как продолжительность симптомов интоксикации и диарейного синдрома, повторный высев возбудителей, изменения биоценоза кишечника и динамика основных показателей иммунитета.
Отмечено положительное влияние КИПа при терапии аллергодерматозов. Это объясняется повышением уровня секреторного Ig A, в результате чего усиливается местная резистентность слизистой ЖКТ и увеличивается выведение из кишечника поступающих с пищей аллергенов.
Основными показаниями к применению КИПа являются следующие заболевания и патологические процессы:
В НИИ эпидемиологии и микробиологии им Г.Н.Габричесвского совместно с ффирмой «Алфарм» разработан комбинированной препарат Кипферон в ректальных и вагинальных свечах, в состав которого входит КИП в количестве 50 мг и рекомбинантный интерферон- альфа2а в дозе 500.000 МЕ.
Для коррекции кишечной микрофлоры применяются специальные пищевые добавки, содержащие пищевые волокна, относящиеся к углевадам, которые не подвергаются перевариванию под действием пищеварительных ферментов, но служат питательным субстратом для микрофлоры толстого кишечника. К пищевым волокнам, оказывающим стимулирующий эффект на кишечную микрофлору относятся олигосахариды, в частности фруктоолигосахариды, наиболее известным представителем которых является инулин. Большое количество инулина содержится в корнеплодах топинамбура. Существуют несколько пищевых добавок содержащих концентрат топинамбура (Концентрат топинамбура, Топивит, Концентрат иерусалимского артишока и др.). Фруктоолигосахариды и, в частности, инулин существенно стимулируют рост бифидобактерий в кишечнике, изменяют pH толстого кишечника в кислую сторону, способствуют образованию в кишечнике короткоцепочных жирных кислот и других биологически активных веществ оказывающих благоприятное действие на биоценоз кишечника.
6. ЛЕЧЕБНЫЕ КИСЛОМОЛОЧНЫЕ ПРОДУКТЫ
7. РАЦИОНАЛЬНАЯ ТЕРАПИЯ БОЛЬНЫХ С ДИСБАКТЕРИОЗОМ КИШЕЧНИКА
Схема коррекции дисбактериоза кишечника может быть разделена на несколько этапов.
1. Санация кишечника от условно-патогеной микрофлоры. Традиционное лечение больных с дисбактериозом кишечника предусматривает предварительную деконтаминацию кишечника при помощи противомикробных средств. Однако последние нередко вызывают побочные эффекты, затрудняющие составление рациональной программы лечения, особенно для ребенка. В большинстве случаев возможна эффективная и безопасная деконтаминация кишечника от условно-патогенных бактерий путем замены противомикробных средств на более безопасные и высокоэффективные бактерийные препараты: КИП и бактериофаги. Энтеральный прием КИПа по 1 дозе 1-2 раза в день оказывает санирующее действие в отношении большинства грамотрицательных энтеропатогенных бактерий (эшерихий, клебсиелл, протеев, а также шигелл и сальмонел). В зависимости от присутсвующей условно-патогенной микрофлоры дополнительно внутрь назначаются бактериофаги (Интести-бактериофаг, Пиобактериофаг комбинированный, Пиобактериофаг поливалентный очищенный, Стафилококковый или Клебсиеллезный бактериофаги). При наличии избыточного роста клостридий применяется Энтерол.
Одновременно с началом лечения больной принимает витамины А, Е и группы В в составе поливитаминных препаратов (Глутамевит, Компливит, Квадевит, Юникап-М, Центрум и др.), ферментные препараты: Фестал, Панзинорм-Форте, Дигестал (при запорах) или Мезим-Форте, Панкреатин, Панкурмен, Панцинтрат (при диарейном синдроме).
При проведении данной терапии необходимо иметь ввиду, что дисбактериоз является не самостоятельной нозологической единицей, а только патогенетическим звеном основного заболевания, поэтому главное внимание должно быть направлено именно на его расшифровку и лечение.
Таким образом, врачи и пациенты сегодня имеют достаточный выбор средств для сохранения и поддержания равновесия нормальной микрофлоры организма. Задача состоит в рациональном и направленном их применении с учетом индивидуальных особенностей биоценоза у конкретного больного, что зависит от понимания различий в действии отдельных препаратов и ясным представлением терапевтических целей, преследуемых при их назначении.
Эшерихиозы
Эшерихиозы ( ЮEscherichioses ) — коли-инфекция, коли-энтерит, диарея путешественников — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечных палочек, протекающих с симптомами общей интоксика
Эшерихиозы (ЮEscherichioses) — коли-инфекция, коли-энтерит, диарея путешественников — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечных палочек, протекающих с симптомами общей интоксикации и поражением желудочно-кишечного тракта (ЖКТ) с развитием гастроэнтерита или энтероколита, в редких случаях — как генерализованная форма болезни с внекишечными проявлениями.
Согласно Международной классификации болезней 10-го пересмотра (МКБ-10, 1997) регистрация эшерихиозов проводится под шифрами:
А04,0 — энтеропатогенный эшерихиоз;
А04,1 — энтеротоксигенный эшерихиоз;
А04,2 — энтероинвазивный эшерихиоз;
А04,3 — энтерогеморрагический эшерихиоз;
А04,4 — эшерихиоз других патогенных серогрупп.
История и распространение. Возбудитель открыт немецким педиатром T. Эшерихом в 1886 г. Он выделил его из кишечника детей и определил как Bacterium coli commune, предположив, что она может быть причиной поносов у детей. В его честь микроб назван Еscherichia coli.
Эшерихии — постоянные обитатели кишечника человека, но некоторые из них могут вызывать поражения ЖКТ, что доказано экспериментально Г. Н. Габричевским в 1894 г. и подтверждено клинически в 1922 г. А. Адамом. Различие по антигенной структуре патогенных и непатогенных кишечных палочек, выявленное Ф. Кауфманном в 1942–1945 гг., легло в основу классификации патогенных эшерихий. По рекомендации ВОЗ эшерихии, вызывающие поражение ЖКТ, называются диареегенными.
Эшерихиоз — повсеместно распространенное заболевание, чаще диагностируемое у детей до 1 года; у взрослых оно регистрируется как диарея путешественников. Групповые вспышки зарегистрированы в последние годы в Канаде, США, Японии, России и других странах. Показатель заболеваемости эшерихиозом остается высоким в Калининграде, Санкт-Петербурге, Ненецком автономном округе. Так, в Калининграде с 1999 по 2002 г. зарегистрировано более 1000 случаев заболевания на 100 тыс. населения. В Москве выявлено около 1000 случаев заболевания эшерихиозом на 100 тыс. населения за последние 10 лет; летальных исходов нет.
Этиология. Эшерихии — подвижные грамотрицательные палочки, аэробы, относящиеся к виду Еscherichia (Е.) coli, роду Escherichia, семейству Enterobacteriaceae. Растут на обычных питательных средах, выделяют бактерицидные вещества — колицины. Серовары не имеют морфологических отличий. Эшерихии содержат соматические антигены (О-Аг) 173 серотипов, капсульные (К-Аг) — 80 сероваров и жгутиковые (Н-Аг) — 56 серотипов. Диареегенные кишечные палочки подразделяются на пять типов: энтеротоксигенные (ЭТКП, ETEC), энтеропатогенные (ЭПКП, EPEC), энтероинвазивные (ЭИКП, EIEC), энтерогеморрагические (ЭГКП, EHEC), энтероадгезивные (ЭАКП, EAEC).
Фактор патогенности ЭТКП — пили (разновидность ворсинок), или фимбриальные факторы, которые определяют способность к адгезии и колонизации нижних отделов тонкого кишечника, а также к токсинообразованию. Термолабильный и термостабильный энтеротоксины ответственны за повышенную экскрецию жидкости в просвет кишки. ЭИКП, имеющие плазмиды, способны проникать в клетки кишечного эпителия и размножаться в них. Патогенность ЭПКП обусловлена способностью к адгезии. ЭГКП выделяют цитотоксин, шигоподобные токсины 1-го и 2-го типов, содержат плазмиды, которые облегчают адгезию к энтероцитам. Факторы патогенности энтероадгезивных кишечных палочек изучены недостаточно.
Эшерихии устойчивы в окружающей среде, могут месяцами сохраняться в воде, почве, испражнениях. Сохраняют жизнеспособность в молоке до 34 дней, в детских питательных смесях — до 92 дней, на игрушках — до 3–5 мес. Хорошо переносят высушивание, обладают способностью размножаться в пищевых продуктах, особенно в молоке. Быстро погибают при воздействии дезинфицирующих средств и при кипячении. У многих штаммов Е. соli отмечается резистентность к ряду антибиотиков (неомицин, ампициллин, цефалотин и др.). Устойчивость к антибиотикам выявлена у 13–35,1% штаммов патогенных эшерихий.
Эпидемиология. Основной источник эшерихиозов — больные со стертыми формами заболевания; меньшую роль играют реконвалесценты и носители. Значимость последних возрастает, если они работают на предприятиях по приготовлению и реализации пищевых продуктов. Однако, по мнению W. Robson et al. (1993), B. Bell et al. (1994), источник инфекции при энтерогеморрагических эшерихиозах (О157) — крупный рогатый скот. Инфицирование людей происходит при употреблении продуктов, которые были недостаточно термически обработаны. Зарегистрированы групповые вспышки заболеваний эшерихиозом О157 в США, Канаде, Японии — странах, где распространено употребление в пищу гамбургеров. Это и дало основание данным исследователям рассматривать эшерихиоз О157 как антропозоонозное заболевание. Механизм передачи — фекально-оральный, который реализуется пищевым путем, реже — водным и бытовым. По данным ВОЗ, пищевой путь характерен для энтеротоксигенных и энтероинвазивных эшерихий, бытовой — для энтеропатогенных.
Из пищевых продуктов фактором передачи чаще являются молочные изделия, готовые мясные продукты, напитки (квас, компот и др.).
В детских коллективах распространение инфекции может происходить через игрушки, загрязненные предметы обихода, через руки больных матерей и персонала. Реже регистрируется водный путь передачи эшерихиозов. Наиболее опасно загрязнение открытых водоемов, которое происходит в результате сброса необезвреженных хозяйственно-бытовых сточных вод, особенно из детских учреждений и инфекционных больниц.
Восприимчивость к эшерихиозам высокая, особенно среди новорожденных и ослабленных детей. Около 35% детей, которые общались с источником инфекции, становятся носителями. У взрослых восприимчивость повышается в связи с переездом в другую климатическую зону, изменением характера питания и т. д. (диарея путешественников).
Эпидемический процесс, вызванный разными возбудителями Е. соli, может различаться. Заболевания, вызванные эшерихиями ЕТЕС, чаще регистрируются в развивающихся странах тропических и субтропических зон в виде спорадических случаев, а групповые случаи — среди детей 1–3 лет. Эшерихиозы, вызванные ЕIЕС, хотя и регистрируются во всех климатических зонах, преобладают в развивающихся странах. Заболевания носят групповой характер среди детей 1–2 лет в летне-осенний период. ЕРЕС вызывает спорадическую заболеваемость во всех климатических зонах, чаще всего среди детей до 1 года, которые находились на искусственном вскармливании. Эшерихиозы, вызванные ЕНЕС и ЕАЕС, выявлены в странах Северной Америки и Европы среди взрослых и детей старше 1 года; для них характерна летне-осенняя сезонность. Вспышки среди взрослых чаще регистрировались в домах для престарелых.
Патоморфологические данные определяются локализацией патологического процесса и малохарактерны.
Патогенез. Эшерихии проникают через рот, минуя желудочный барьер, и, в зависимости от типовой принадлежности, оказывают свое патогенное действие.
Энтеротоксигенные штаммы способны к выработке энтеротоксинов и фактора колонизации, с помощью которого осуществляется прикрепление и колонизация тонкой кишки.
Энтеротоксины — это термолабильные или термостабильные вещества, воздействующие на биохимические функции эпителия крипт, не вызывая видимых морфологических изменений. Энтеротоксины усиливают активность аденилатциклазы и гуанилатциклазы. При их участии и под стимулирующим влиянием простагландинов увеличивается образование циклического аденозинмонофосфата. В результате в просвет кишки секретируется большое количество воды и электролитов, которые не успевают реабсорбироваться в толстой кишке, и развивается диарея с последующими нарушениями водно-электролитного баланса.
Заражающая доза ЭТКП составляет 108–1010 микробных клеток.
ЭИКП обладают способностью внедряться в клетки эпителия толстой кишки. Проникновение ЭИКП в слизистую оболочку приводит к развитию воспалительной реакции и образованию эрозий кишечной стенки. Повреждение эпителия способствует увеличению всасывания в кровь эндотоксинов. У больных в испражнениях появляются слизь, кровь и полиморфноядерные лейкоциты. Заражающая доза ЭИКП — 5х105 микробных клеток.
Механизм патогенности ЭПКП малоизучен. У штаммов 055, 086, 0111 и др. выявлен фактор адгезии к клеткам Нер-2, за счет которого обеспечивается колонизация тонкого кишечника. У других штаммов (018, 044, 0112 и др.) этот фактор не обнаружен. Видимо, они имеют иные факторы патогенности, которые пока неизвестны. Заражающая доза ЭПКП — 10х1010 микробных клеток.
ЭГКП выделяют цитотоксин SLT (Shiga-like toxin), который вызывает разрушение клеток эндотелия мелких кровеносных сосудов кишечной стенки проксимальных отделов толстой кишки. Сгустки крови и фибрин приводят к нарушению кровоснабжения кишки, появлению в кале крови. Происходит развитие ишемии кишечной стенки вплоть до некроза. У некоторых больных наблюдаются осложнения с развитием синдрома диссеменированного сосудистого свертывания, инфекционного токсического шока и острой почечной недостаточности (ОПН).
ЭАКП способны к колонизации эпителия тонкой кишки. Вызванные ими заболевания взрослых и детей протекают длительно, но легко. Это связано с тем, что бактерии прочно закрепляются на поверхности эпителиальных клеток.
После перенесенного заболевания формируется кратковременный непрочный типоспецифический иммунитет.
Клиника. Клинические проявления эшерихиозов зависят от типа возбудителя, возраста больного, иммунного статуса.
Принята следующая клиническая классификация эшерихиозов (Н. Д. Ющук, Ю. Я. Венгеров, 1999).
По этиологическим признакам:
По форме заболевания:
По тяжести течения:
При эшерихиозе, вызванном энтеротоксигенными штаммами, инкубационный период продолжается от 16 до 72 ч. Характерно холероподобное течение болезни, протекающее с поражением тонкой кишки без выраженного синдрома интоксикации (диарея путешественников).
Заболевание начинается остро; больных беспокоят слабость, головокружение, температура нормальная или субфебрильная. Появляются тошнота, повторная рвота, разлитые боли в животе схваткообразного характера, стул частый (до 10–15 раз в сутки), жидкий, обильный, водянистый, нередко напоминающий рисовый отвар. Живот вздут, при пальпации определяется урчание, небольшая разлитая болезненность.
Заболевание может иметь как легкое, так и тяжелое течение. Тяжесть течения определяется степенью дегидратации. Возможна молниеносная форма заболевания с быстрым развитием эксикоза. Длительность болезни — 5–10 дней.
Энтероинвазивные эшерихии вызывают дизентериеподобное заболевание, которое протекает с симптомами общей интоксикации и преимущественным поражением толстой кишки. Инкубационный период длится 6–48 ч. Начало острое, характеризуется повышением температуры до 38–39 °С, ознобом, слабостью, головной болью, болью в мышцах, снижением аппетита. У части больных температура нормальная или субфебрильная. Через несколько часов присоединяются симптомы поражения ЖКТ (боли схваткообразного характера, преимущественно в нижней части живота, ложные позывы на дефекацию, тенезмы, жидкий стул — обычно калового характера с примесью слизи и крови до 10 и более раз в сутки. При более тяжелом течении заболевания — стул в виде «ректального плевка». Сигмовидная кишка — спазмированная, уплотненная и болезненная. Печень и селезенка не увеличены. При ректороманоскопии — катаральный, реже — катарально-геморрагический или катарально-эрозивный проктосигмоидит.
Течение болезни доброкачественное. Лихорадка длится 1–2, реже — 3–4 дня; длительность заболевания — 5–7 дней. Через 1–2 дня стул нормализуется, спазм и болезненность толстой кишки сохраняются в течение 5–7 дней болезни. Восстановление слизистой оболочки толстой кишки наступает к 7–10-му дню болезни.
У детей энтеропатогенный эшерихиоз, вызываемый Е. соli 1-го класса, протекает в виде различной тяжести энтеритов, энтероколитов, а у новорожденных и недоношенных детей — в септической форме. Для кишечной формы у детей характерно острое начало болезни, температура — 38–39 °С, слабость, рвота, водянистая диарея, стул желтого или оранжевого цвета. Быстро развивается токсикоз и эксикоз, масса тела снижается. Септическая форма заболевания протекает с выраженными симптомами интоксикации (повышение температуры, анорексия, срыгивание, рвота). Возникают множественные гнойные очаги.
Энтеропатогенный эшерихиоз, вызываемый Е. соli 2-го класса, регистрируется у взрослых и детей. Инкубационный период — 1–5 дней. Характерно острое начало заболевания (температура — 38–38,5 °С, озноб, нечастая рвота, боли в животе, стул без патологических примесей, жидкий, до 5–8 раз в сутки), течение доброкачественное. У некоторых больных отмечаются гипотония, тахикардия.
При эшерихиозе, вызванном энтерогеморрагическими штаммами, заболевание характеризуется синдромом общей интоксикации и поражением проксимального отдела толстой кишки. Инкубационый период составляет 1–7 дней. Заболевание начинается остро с болей в животе, тошноты, рвоты. Температура субфебрильная или нормальная, стул жидкий, до 4–5 раз в день, без примеси крови. Состояние больных ухудшается на 2–4-й день болезни, когда стул учащается, появляются примесь крови, тенезмы. При эндоскопическом исследовании выявляется катарально-геморрагический или фибринозно-язвенный колит. Более выраженные патоморфологические изменения обнаруживаются в слепой кишке. Наиболее тяжело протекает заболевание, вызванное штаммом 0157.Н 7. У 3–5% больных через 6–8 дней от начала заболевания развивается гемолитико-уремический синдром (синдром Гассера), который проявляется гемолитической анемией, тромбоцитопенией и развитием ОПН и токсической энцефалопатии (судороги, парезы, сопор, кома). Летальность в этих случаях может составлять 3–7%. Синдром Гассера чаще регистрируется у детей до 5 лет.
Особенности эшерихиоза, вызванные энтероадгезивными штаммами, изучены мало. Заболевание регистрируется у пациентов с ослабленной иммунной системой. Чаще выявляются внекишечные формы — поражение мочевыводящих (пиелонефрит, цистит) и желчевыводящих (холецистит, холангит) путей. Возможны септические формы (коли-сепсис, менингит).
Чаще эшерихиозы протекают доброкачественно, но возможны осложнения — такие как инфекционный токсический шок, гиповолемический шок с дегидратацией 3–4-й степени, ОПН, сепсис, пневмония, пиелоцистит, пиелонефрит, холецистит, холангит, менингит, менингоэнцефалит.
Диагностика. Клиническая картина эшерихиозов сходна с другими кишечными инфекциями, поэтому основу подтверждения диагноза составляют бактериологические методы исследования. Материал (испражнения, рвотные массы, промывные воды желудка, кровь, мочу, ликвор, желчь) следует брать в первые дни болезни до назначения больным этиотропной терапии. Посевы производят на среды Эндо, Левина, Плоскирева, а также на среду обогащения Мюллера.
Применяются серологические методы исследования — реакция агглютинации, реакция непрямой гемагглютинации — в парных сыворотках, но они неубедительны, так как возможны ложно-положительные результаты из-за антигенного сходства с другими энтеробактериями, и используются для ретроспективной диагностики, особенно во время вспышки.
Перспективным методом диагностики является полимеразная цепная реакция (ПЦР). Инструментальные методы обследования (ректороманоскопия, колоноскопия) при эшерихиозах малоинформативны.
Дифференциальный диагноз эшерихиозов проводят с другими острыми диарейными инфекциями: холерой, шигеллезом, сальмонеллезом, кампилобактериозом, пищевыми токсикоинфекциями стафилококковой этиологии и вирусными диареями: ротавирусной, энтеровирусной, Норволк-вирусной инфекцией и др.
В отличие от эшерихиозов, холера характеризуется отсутствием интоксикации, лихорадки, болевого синдрома, наличием многократной рвоты, быстрым развитием дегидратации 3–4-й степени. Помогает в постановке диагноза эпидемиологический анамнез — пребывание в эндемичных регионах холеры.
Шигеллезу, в отличие от эшерихиозов, свойственна высокая лихорадка; боли локализуются в левой подвздошной области; пальпируется спазмированная, болезненная сигмовидная кишка; стул скудный, в виде «ректального плевка».
Сальмонеллез, в отличие от эшерихиозов, характеризуется более выраженной интоксикацией, разлитыми болями в животе, болезненностью при пальпации в эпигастральной и околопупочной областях, урчанием. Характерен зловонный стул зеленоватого цвета.
При проведении дифференциальной диагностики эшерихиозов с кампилобактериозом также выявляются определенные различия. Для кампилобактериоза более характерно начало заболевания с продромального периода (артралгий, слабости, озноба). Боли в животе, диарея присоединяются на 2–3-й день болезни. Боль в животе локализуется чаще в левой подвздошной области. Возможны сыпь, увеличение печени. Заражение чаще всего происходит при употреблении в пищу инфицированного мяса (свинины, говядины, мяса птиц).
Для пищевых токсикоинфекций стафилококковой этиологии, в отличие от эшерихиозов, характерно острое, бурное начало заболевания, короткий инкубационный период (30–60 мин). Более выражены симптомы интоксикации — рвота неукротимая, боли в животе режущего характера с локализацией в эпигастральной и околопупочной областях. Характерен групповой характер заболевания, связь заболевания с пищевым фактором, быстрый регресс болезни.
Для ротавирусного гастроэнтерита, в отличие от эшерихиозов, характерны катаральные явления, изменения слизистой ротоглотки (гиперемия, зернистость), слабость, адинамия. Боли в животе диффузные, стул жидкий, «пенистый», с резким кислым запахом, позывы на дефекацию носят императивный характер. При пальпации отмечается «крупнокалиберное» урчание в области слепой (реже — сигмовидной) кишки.
При проведении дифференциального диагноза эшерихиозов с энтеровирусной инфекцией также можно выявить определенные отличия. Для энтеровирусной инфекции характерны катаральные явления, субфебрильная температура (до недели), многократная мучительная рвота, продолжительность диареи до 2 нед, увеличение печени и селезенки.
Для Норволк-вирусной инфекции, в отличие от эшерихиозов, характерны короткий инкубационный период от 10 ч до 2 сут, ломота в мышцах, головокружение, боли в эпигастральной и околопупочной областях. Продолжительность заболевания короткая — от нескольких часов до 3 сут.
Лечение. Госпитализация больных с эшерихиозами проводится по клиническим и эпидемиологическим показаниям. Больные при среднетяжелом и тяжелом течении заболевания госпитализируются в инфекционные больницы. В легких случаях заболевания больные могут лечиться амбулаторно при наличии благоприятных бытовых санитарно-гигиенических условий.
По эпидемиологическим показаниям госпитализации подлежат лица из декретированных групп, больные из организованных коллективов, а также пациенты, проживающие в коммунальных квартирах, общежитиях.
Госпитализируются больные, если в семье есть лица, относящиеся к декретированным группам.
В остром периоде болезни больным рекомендуется щадящая диета (стол № 4, при нормализации стула — № 2, в период реконвалесценции — стол № 13).
В легких случаях заболевания достаточно назначения пероральной регидратационной терапии (Глюкосалан, Цитроглюкосалан, Регидрон и др.), количество которых должно в 1,5 раза превышать потери воды с испражнениями.
Показаны ферменты (Панзинорм форте, Фестал, Мезим форте, Креон), энтеросорбенты (Энтеросгель, Энтеродез, Полифепан, Полисорб — в течение 1–3 дней). При легком течении болезни целесообразно использование кишечных антисептиков (Интетрикс по 2 капсулы 3 раза в день, Неоинтестопан после каждого акта дефекации по 2 таблетки — до 14 в сутки, Энтерол по 2 капсулы 2 раза в день) в течение 5–7 дней. Легкие и стертые формы эшерихиозов не требуют назначения этиотропных препаратов.
При лечении больных в условиях стационара показан постельный режим в первые 2–3 дня. Назначается этиотропная терапия. С этой целью при среднетяжелых формах используется один из следующих препаратов: ко-тримоксазол (Бактрим, Бисептол, Септрин) по 2 таблетки 2 раза в день. Из препаратов фторхинолонового ряда назначается ципрофлоксацин — Ципролет — фторхинолон для широкого клинического применения, сочетающий мощное бактерицидное действие, широкий антимикробный спектр и благоприятную фармакокинетику. Механизм действия препарата, связанный с ингибированием ДНК-гиразы и топоизомеразы, обусловливает отсутствие перекрестной резистентности. Максимальные концентрации ципрофлоксацина (Ципролета) в плазме крови достигаются через 60–90 мин. Для препарата характерно быстрое начало действия. Биодоступность препарата более 63–77% и высокий показатель проникновения в ткани, жидкости и клетки обеспечивают его эффективность при назначении в небольших дозировках. Препарат отличается хорошим профилем безопасности и положительной динамикой, проявляющейся в короткие сроки. Также рекомендуются Ципробай, Ципросол по 500 мг 2 раза в сутки перорально, пефлоксацин (Абактал) по 400 мг 2 раза в сутки, офлоксацин (Таривид) по 200 мг 2 раза в сутки, длительность терапии — 5–7 дней.
В тяжелых случаях фторхинолоны применяются вместе с цефалоспоринами II поколения (цефуроксим 750 мг 4 раза в сутки внутривенно или внутримышечно; цефаклор 750 мг 3 раза в сутки внутримышечно; цефтриаксон 1 г 1 раз в сутки внутривенно) и III поколения (цефоперазон 1 г 2 раза в сутки внутривенно или внутримышечно; цефтазидим 2 г 2 раза в сутки внутривенно или внутримышечно).
При дегидратации 2–3-й степени назначают регидратационную терапию внутривенно кристаллоидными растворами (Хлосоль, Ацесоль, Лактосоль, Квартасоль).
Объем регидратационной терапии определяется на основании учета степени обезвоживания и массы тела больного. Лечение проводят в два этапа: ликвидация имеющегося обезвоживания и коррекция продолжающихся потерь жидкости.
Скорость введения полиионных растворов составляет от 60 до 80 мл/мин в зависимости от степени дегидратации. При выраженных симптомах интоксикации используются коллоидные растворы (Гемодез, Реополиглюкин и др.) в объеме 400–800 мл в сутки.
Особое внимание должно быть уделено терапии больных эшерихиозом 0157, так как у них возможно появление тяжелых осложнений.
После приема антибактериальных препаратов при продолжающейся диарее используют эубиотики для коррекции дисбактериозов (Бифиформ, Бифистим, Бифидумбактерин форте, Аципол, Хилак форте, Пробифор и др.) в течение 7–10 дней.
Выписка реконвалесцентов проводится после полного клинического выздоровления при отрицательных результатах бактериологического исследования. Для больных из декретированных групп необходимо наличие двукратного отрицательного бактериологического исследования кала, проведенного через 2 дня после окончания этиотропной терапии.
После выписки из стационара больные находятся на диспансерном наблюдении в кабинете инфекционных заболеваний поликлиник в течение 1 мес. В конце срока наблюдения проводят двукратное бактериологическое исследование кала с интервалом в 2–3 дня (лицам, относящимся к декретированным группам).
Коли-инфекция у взрослых протекает благоприятно, перехода в хронические формы не наблюдается.
Профилактические мероприятия. Основу профилактики эшерихиозов составляют меры по пресечению путей передачи возбудителя. Особенно важно соблюдение санитарно-гигиенических требований на объектах общественного питания, водоснабжения, предупреждение контактно-бытового пути заражения в детских учреждениях, родильных домах, стационарах (использование индивидуальных стерильных пеленок, обработка рук дезинфицирующими растворами после работы с каждым ребенком, дезинфекция посуды, пастеризация, кипячение молока, молочных смесей). Готовые к употреблению и сырые продукты должны разделываться на разных разделочных досках разными ножами. Посуду, в которой транспортируют пищу, необходимо обработать кипятком.
При подозрении на эшерихиоз необходимо обследовать беременных до родов, рожениц, родильниц и новорожденных. Специфической профилактики эшерихиозов нет.
Мероприятия в очаге. Контактировавших с больными в очаге заболевания наблюдают в течение 7 дней. Дети, контактировавшие с больным эшерихиозом по месту жительства, допускаются в детские учреждения после разобщения с больным и трехкратных отрицательных результатов бактериологического исследования кала.
При выявлении больных эшерихиозом в детских учреждениях и родильных домах прекращается прием поступающих детей и рожениц. Персонал, матери, дети, бывшие в контакте с больным, а также дети, выписанные домой незадолго до заболевания, обследуются трехкратно (проводится бактериологическое исследование кала). При выявлении лиц с положительными результатами обследования их изолируют.
Литература
Г. К. Аликеева, кандидат медицинских наук
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
Г. М. Кожевникова, профессор
МГМСУ, Москва