Чем лучше лечить ревматоидный артрит
Самые эффективные препараты от ревматоидного артрита
Ревматоидному артриту подвержены от 1 до 5% людей старше 45 лет, при этом женщины болеют в среднем в 3-5 раз чаще мужчин из-за природно высокого иммунитета. Поэтому важно быть внимательными к малейшим проявлениям заболевания, вовремя диагностировать его и выбирать хорошие препараты от ревматоидного артрита в соответствии с предписаниями врача.
Отличительные признаки ревматоидного артрита
Симптомы ревматоидного артрита обычно носят комплексный характер и наблюдаются не только в суставах. Но чаще всего о начале болезни возвещает:
К этим симптомам может добавляться боль в животе и/или грудной клетке, воспаление сосудистой оболочки глаза (увеит), высыпания на коже.
Первые симптомы болезни обычно проявляются после потрясения для организма: физического или психоэмоционального перенапряжения, инфекции, аллергии, гормональной перестройки или воздействия других неблагоприятных факторов.
Форма выпуска препаратов от ревматоидного артрита
В зависимости от стадии и специфики протекания болезни, а также удобства пациента, медикаментозная терапия ему может быть назначена в виде средств для перорального приема и инъекций.
Таблетки и капсулы
Препараты от ревматоидного артрита в таблетках и капсулах легко дозируются и не требуют проведения манипуляций медицинскими работниками. Их минусом является сравнительно невысокая биодоступность активных веществ (70-80%). Некоторые группы медикаментов для лечения артрита (например, нестероидные противовоспалительные средства, глюкокортикоиды) могут поражать слизистые и не применяются для пациентов с язвенной болезнью, гастритом, дуоденитом, диспепсией и другими заболеваниями желудочно-кишечного тракта. Поэтому они также требуют подключения гастропротективных лекарств на время курса, обычно не подходят для постоянного применения. Препараты в таблетках и капсулах обычно следует принимать строго после еды.
Как правило, препараты в таблетках несколько дешевле капсул или растворов для инъекций, а иногда содержат более высокую концентрацию действующих веществ. При этом таблетки начинают действовать медленнее, зато обеспечивают более длительный терапевтический эффект. Из-за перорального приема действующие вещества таблеток подвергаются частичному разрушению в пищеварительном тракте и, увы, не полностью усваиваются организмом в желудке. Капсулы, напротив, быстродействующая форма выпуска, которая имеет защитную оболочку от соляной кислоты, не имеют вкуса и запаха, но гораздо проще портится (например, при ношении в сумке). При трудностях с подвижностью пальцев, во время воспалительных болезней горла извлечение из блистера проглатывание таблеток и капсул может представлять дополнительные неудобства.
Уколы препаратами для лечения ревматоидного артрита
Инъекционное лечение ревматического артрита препаратами может проводиться внутрисуставно, внутримышечно или внутривенно.
Внутрисуставное введение медикаментов от артрита считается крайней мерой, поскольку вызывает дополнительную микротравматизацию сустава, может вызывать усиление иммунного ответа и риск прогрессирования вторичного артроза. Кроме того, препараты для лечения ревматоидного артрита в уколах имеют мелкокристаллическую структуру, а потому могут травмировать суставной хрящ.
В/м и в/в инфекции минуют желудок, а потому не разрушают слизистые ЖКТ. Однако для правильного проведения инъекций нужны специальные навыки. Также препараты для лечения ревматоидного артрита в уколах не подходят для длительного применения в силу болезненности введения.
Саше от ревматоидного артрита
Фармакологические группы препаратов от ревматоидного артрита
Ревматоидный артрит требует комплексного лечения, направленного на снятие воспаления и болевого синдрома, подавление иммунной реакции, заживление эрозий на суставных поверхностях, восстановление питания сустава и околосуставных тканей. Этой цели служат различный фармгруппы медикаментов для лечения артрита.
Иммуноподавляющие препараты для лечения ревматоидного артрита
Иммуномодуляторы всегда сочетают с противовоспалительными средствами и хондропротекторами.
Как правило, средства базисной терапии принимают 1 раз в неделю.
Базисные препараты для лечения ревматоидного артрита применяются курсами или на постоянной основе пожизненно. Обратите внимание, что при ОРВИ и других заболеваниях прием иммунодепрессантов следует прекратить до полного выздоровления.
Иммунодепрессанты выпускают в таблетках, капсулах и растворах для инъекций. Наилучший эффект достигается при комбинации 2-3 базисных препаратов одновременно.
Нестероидные противовоспалительные препараты для лечения ревматоидного артрита
Нестероидные противовоспалительные препараты при лечении ревматоидного артрита помогают снизить активность медиаторов воспаления (простагландинов, ферментов). Они снимают отек и воспаление, убирают болевой синдром нормализуют кровообращение и метаболизм тканей вокруг сустава, облегчают движение в больном сочленении. НПВП раздражают слизистые желудка и кишечника, а потому применяются короткими курсами по 10-12 дней, для снятия обострений. Эта группа медикаментов для лечения артрита оказывает лишь симптоматический эффект и не помогает восстановить сустав или остановить прогрессирование болезни.
НПВП выпускают в форме таблеток, капсул, инъекционных растворов, гелей и суппозиториев.
Глюкокортикоидные средства
Глюкокортикостероидные (гормональные) препараты применяют лишь в тех случаях, когда действия НПВП недостаточно, чтобы снять боль. Поскольку такие лекарства имеют серьезные противопоказания и осложнения, ревматологи рекомендуют использовать их короткими курсами не чаще 1-3 раз в год. В тяжелых случаях возможно применение преднизолона до 6-12 месяцев. Более частый и длительный их прием оправдан лишь при резко неблагоприятном течении болезни, быстром ее прогрессировании, тяжелых осложнениях от базисной терапии.
Глюкокортикоиды можно принимать только по назначению врача и в строгом соответствии с дозировкой, иначе состояние суставов может даже ухудшиться.
Существует множество видов препаратов от ревматоидного артрита
Хондропротективные препараты от ревматоидного артрита
Для достижения стойкого эффекта хондропротекторы принимают длительными курсами по 3-6 месяцев 1-2 раза в год. Поскольку они практически не имеют противопоказаний и не могут вызвать осложнения, эта группа препаратов остается одной из предпочтительных в лечении ревматоидного артрита.
Хондропротекторы выпускают в форме таблеток и капсул, инъекций, саше и гелей. Одним из лучших хондропротекторов считается Артракам.
Ангиопротекторы и корректоры микроциркуляции
Корректоры микроциркуляции применяются в качестве вспомогательных лекарственных средств для профилактики осложнений. От качества кровообращения, в т.ч. в мелких капиллярах, зависит питание сустава. В тяжелых случаях сбои в работе кровеносной системы и субхондральный склероз суставных поверхностей могут приводить к отмиранию (некрозу) костных головок, образующих сустав.
Отек, воспалительный процесс могут вызывать сдавление суставных стенок; нередок при ревматоидном артрите и васкулит (воспаление сосудов).
Спазмолитики и миорелаксанты
Воспалительный процесс в суставе оказывает воздействие и на мягкие околосуставные ткани. Мышцы и связки не становятся исключением. Постоянное мышечное напряжение ускоряет атрофию мышц при ревматоидном артрите из-за их разрушения, усиливает ощущение усталости. Спазмы также могут причинять серьезный дискомфорт: усиливать или вызывать болевые ощущения (спастические боли), мешать нормальному сну, передвижению пациента и выполнению им бытовых дел, вызывать нарушения мелкой моторики.
Препараты нового поколения для лечения ревматоидного артрита
Под лекарствами нового поколения в лечении ревматоидного артрита подразумевают генно-инженерные биологические препараты, которые контролируют течение болезни. Т.н. таргетная терапия синтетическими препаратами длится около 3-6 месяцев с момента выявления симптомов РА.
Применение средств нового поколения обусловлено тем, что при ревматоидном артрите хрящ “самоповреждается” ферментами из пораженных клеток. Повышенная выработка цитокинов при этом запускает каскадную реакцию в клетках, провоцируя хроническое воспаление и, как следствие, инвалидизацию пациента.
Современные биопрепараты помогают затормозить этот процесс за счет блокировки цитокинов (информационные молекулы, которые отвечают за иммунные реакции организма) или выработки антител к ним, инактивации Т-лимфоцитов, либо иначе предотвращают передачу сигналов атакующим иммунным клеткам.
В некоторых случаях, по мнению ревматологов, можно обойтись препаратами нового поколения для лечения ревматоидного артрита.
Препараты для лечения ревматоидного артрита на разных стадиях
Специфика лечения зависит от того, насколько далеко зашли изменения в хрящевой и костной ткани сустава. Поскольку многие лекарства от ревматоидного артрита при длительном приеме отрицательно сказываются на состоянии внутренних органов, врачи стараются идти от безопасных препаратов к сильнодействующим.
1-я стадия заболевания
После купирования первого воспаления при ревматоидном артрите показан прием хондропротекторов и иммунодепрессантов. Такая поддерживающая терапия дает организму возможность восстановиться самостоятельно
НПВС применяются только в острой фазе заболевания. Также на ранних этапах РА возможна длительная ремиссия, которая поддерживается не применением тяжелых препаратов, а соблюдением диеты. Важно одеваться по погоде, чередовать периоды нагрузки и периоды отдыха, поменьше нервничать, принимать витамины курсами 2 раза в год.
На ранних стадиях артрита важно соблюдать умеренный образ жизни и режим дня
2-я стадия заболевания
3-я стадия заболевания
Для ревматоидного артрита 3-й стадии характерна выраженная деструкция суставов, поэтому базисная терапия, препараты для лечения ревматоидного артрита нового поколения, НПВС и глюкокортикоиды выходят на первое место, а хондропротекторы принимаются исключительно как вспомогательное поддерживающее средство. Также больным могут назначать дополнительные медикаменты, чтобы сгладить побочные эффекты от основной терапии.
4-я стадия заболевания
На последней стадии болезни медикаментозное лечение неэффективно. Больным показана операция.
Надеемся, эта статья поможет вам в лечении ревматоидного артрита у вас и ваших близких!
Раннее лечение ревматоидного АРТРИТА
Как врачу общей практики провести раннюю диагностику ревматоидного артрита? Как помочь пациенту с ревматоидным артритом в системе общей практике? Когда и каким образом следует применять препараты второго ряда? Рисунок 1.
Как врачу общей практики провести раннюю диагностику ревматоидного артрита?
Как помочь пациенту с ревматоидным артритом в системе общей практике?
Когда и каким образом следует применять препараты второго ряда?
 |
| Рисунок 1. Многочисленные данные свидетельствуют о том, что уже на ранних стадиях РА развивается стойкое поражение суставов, поэтому не так уж редко у пациента с первично выявленным РА обнаруживаются рентгенологические изменения |
Начало РА может выражаться по-разному: от взрывоподобного воспаления за одну ночь до повторяющихся мигрирующих поражений суставов, длящихся годами и затрудняющих раннюю диагностику.
Однако очень важно установить воспалительную природу заболевания. Признаки, отличающие воспалительный артрит от дегенеративного, включают:
Ревматоидный фактор не является решающим в диагностике ревматоидного артрита, и, как правило, его не определяют при отсутствии каких-либо из указанных признаков. Однако его обнаружение подтверждает диагноз, а высокий титр, как и СОЭ, указывает на более активное и тяжелое заболевание.
При подозрении на РА нельзя дожидаться рентгенологических изменений, свидетельствующих о стойком поражении. Надо сказать, что нередко у первичных пациентов обнаруживаются некоторые рентгенологические изменения, и многочисленные данные свидетельствуют о том, что стойкие поражения суставов развиваются в самом начале РА.
В самом деле, трудно предсказать тяжесть РА. В таблице приведены факторы, часто связанные с неблагоприятным исходом. Но будучи достоверными для групп больных РА, эти данные мало применимы к конкретному пациенту.
Ситуацию осложняют многочисленные варианты течения болезни. Факты подтверждают, что большинство препаратов второго ряда, используемых для терапии, скорее приостанавливают или замедляют развитие заболевания, чем восстанавливают поврежденные ткани. Кроме того, все они чреваты потенциально опасными побочными эффектами.
Учитывая все это, приходится принимать тяжелые решения.
Подход ревматологов к препаратам второго ряда существенным образом изменился, и сейчас большинству пациентов с РА рекомендуется ранняя ударная терапия. Это привело к широкому использованию препаратов, модифицирующих заболевание.
В нашем отделении количество пациентов, принимающих такие препараты, увеличилось с 20% в 1984 году до 60% в 1998 году.
Другим главным фактором, диктующим лечебные мероприятия, является пациент.
Пациент имеет собственное мнение о приоритетах и целях лечения, а личные обстоятельства могут навязывать схему терапии, не применимую к другим пациентам.
Пациенты по-разному оценивают отношение риск/успех, и они имеют на это право.
Врачи обязаны предоставить пациенту все возможности для лечения и дать реалистическую оценку эффективности и токсичности имеющихся препаратов. Это относится как к лекарственной, так и к нелекарственной терапии.
Первой задачей лекарственной терапии является оптимизация выбора препаратов первого ряда. Большинство пациентов с воспалительным артритом выбирают нестероидные противовоспалительные (НПВП). Около 76% больных, находящихся под наблюдением в нашем отделении, принимают НПВП.
По нашим данным, пациенты с РА старше 50 лет ведут более активный образ жизни, если принимают НПВП, чем и объясняется большая популярность именно этих средств, несмотря на негативное отношение к ним со стороны средств массовой информации.
Правильная оценка своего состояния позволяет пациенту более адекватно реагировать на ситуацию; доказано, что это способствует благоприятному исходу.
Больному можно порекомендовать рациональный отдых, правильную нагрузку, удобную обувь и различные приспособления, необходимые в каждом конкретном случае. Полезно знать, что тренировочная обувь великолепно подходит артритической стопе.
Совет по артриту и ревматизму выпускает широкий набор печатной продукции с информацией и рекомендациями. (Чтобы бесплатно получить материалы, напишите в ARC, Copeman House, St Marys Court, St Marys Gate, Chesterfield, Derbyshire, S41 7TD.)
Я рекомендую изучить эту литературу тем, кому поставлен данный диагноз.
Если согласованное лечение оказывается недостаточным или врач диагностирует тяжелое течение, обычно переходят на препараты второго ряда. Я не располагаю данными, но предполагаю, что ревматологи по-разному оценивают использование этих препаратов в рамках первичной помощи.
Кто-то придерживается мнения, что сульфасалазин не намного более токсичен, чем НПВП, и некоторые врачи общей практики активно назначают его еще до направления к специалисту. Другие, напротив, отказываются проводить необходимое мониторирование даже после рекомендации ревматолога.
Трудность состоит в том, что препараты второго ряда изменяют течение заболевания и у ревматолога остается меньше информации, что затрудняет принятие последующих решений.
Например, при первичном осмотре пациента, эффективно пролеченного сульфасалазином, может показаться, что у него нет РА. С другой стороны, неопытный врач общей практики может слишком рано отменить препарат, из-за незначительного эффекта.
В идеале пациента с подозрением на воспаление суставов нужно как можно раньше отправить к ревматологу для подтверждения диагноза и назначения раннего ударного лечения. Ревматологи выполнят свою часть работы, обеспечив таким пациентам быструю консультацию и обследование.
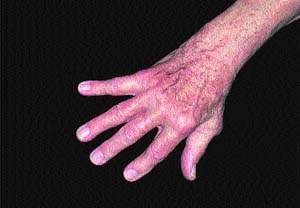 |
| Рисунок 2. В настоящее время ведется изучение молекул, направленных как против воспаления, так и против деструктивных процессов при артрите |
Наиболее токсичные препараты второго ряда, такие как метотрексат и золото, обычно назначаются специалистом, и время, потраченное на выяснение предшествующей терапевтической тактики, оправданно и способствует выбору более подходящих данному пациенту лекарственных средств.
Возможности нелекарственной терапии также шире у системы вторичной помощи, в основном благодаря работе профессиональных команд здоровья. Ядро команды составляют обученные медсестры и физио- и трудотерапевты. Сюда также могут входить психологи, метрологи и добровольцы.
Специализация команды затрудняет ее работу в условиях общей практики и служит еще одной причиной для направления больных к специалистам.
Сегодня лекарственная индустрия демонстрирует тенденцию к выпуску препаратов, модифицирующих течение РА. Продолжаются исследования веществ, направленных одновременно против воспалительных и деструктивных процессов в суставе.
Эти препараты внушают надежду, что финансовая выгода от их применения может заключаться в отсутствии необходимости других видов лечения, особенно замены суставов и вовлечения служб социальной помощи. Проблема в том, что затраты на эти средства окупятся лишь по прошествии длительного времени.
Обратите внимание!
Разрабатываемые лекарственные средства для лечения артрита
Все крупные фармацевтические компании ощущают необходимость создания лекарств против артрита. Лекарственных средств, удовлетворяющих и врача, и пациента, явно недостает. С увеличением средней продолжительности жизни ожидается рост заболеваемости, соответственно необходимо появление лекарств, способных контролировать заболевание.
Анализ патологических процессов, развертывающихся при ревматоидных заболеваниях, предоставляет нам множество потенциальных мишеней для лекарственного воздействия.
В общем, больной, пораженный ревматоидным артритом, — это генетически предрасположенный индивидуум, у которого сорваны механизмы самораспознавания и, таким образом, запущен аутоимунный процесс.
В развитии воспалительных заболеваний, таких как РА, принимает участие иммунная система. Процесс воспаления развивается, постепенно приводя к разрушению сустава и стойкой потере хряща. Некоторые основные этапы этого процесса, возможно, одинаковы для РА и дегенеративных заболеваний.
Генетика. Вероятно, в будущем появится возможность заменять предрасположенные гены и снижать риск артрита. Но путь к этому долог.
Иммуномодулирование. Многие современные препараты, модифицирующие заболевание, угнетают иммунную систему, особенно это относится к кортикостероидам и циклоспорину. Поэтому логично их использование на ранних стадиях заболевания. Наибольшее внимание разработчиков новых лекарств привлекает циклоспорин. Многие препараты исследуются на предмет снижения токсичности и, как следствие, необходимости в постоянном наблюдении за больным в процессе лечения. В эту категорию попадают также различные биологические агенты, из которых наиболее известны анти-CD4-препараты. При ревматоидном артрите временный эффект приносит удаление CD4-позитивных Т-клеток. Мишенями могут служить и другие клеточные компоненты. Блокирование любой части каскада воспаления снижает воспалительный процесс, а с ним и проявления РА. Это также может изменять течение заболевания. Эффективность определяется биологической системой, которая не может с легкостью обойти блок.
В этой связи многообещающим является фактор некроза опухолей (TNF), а также ингибирование, вызываемое другими соединениями.
Вовлеченные в процесс клетки посылают сигналы, известные как интерлейкины, другим клеткам, что приводит к развитию воспаления. Идентифицируются все новые посредники, блокирование которых также может быть эффективным при РА.
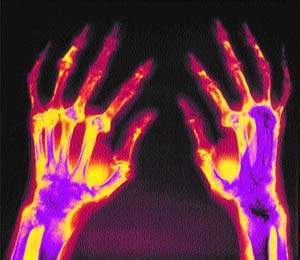 |
| Рисунок 3. Перспектива применения новых антиартритных препаратов тесно связана с вопросами цены и временных затрат |
Мишенью является также механизм, посредством которого клетки мигрируют к месту воспаления. Клетки и стенки сосудов экспрессируют “молекулы адгезии”, которые обозначают место, в котором клетки выходят из циркуляторного русла в ткани.
Ингибирование экспрессии молекул адгезии предполагает не только уменьшение воспаления, но и возможность направленного воздействия на определенные ткани.
Селективное снижение экспрессии молекул адгезии на эндотелии сосудов в суставах может ликвидировать воспаление без системных эффектов.
Повреждение хряща происходит на поздних стадиях РА и дегенеративных заболеваний. Поддержание структуры хряща обеспечивается коллагеновой основой; другие составляющие могут быть заменены, но при условии сохранности основы: потеря коллагенового матрикса приводит к стойкому разрушению хряща. Коллагеназы, разрушающие хрящ, присутствуют в суставах, но, как правило, количество ингибиторов превышает количество коллагеназ. Однако при некоторых заболеваниях это соотношение меняется на обратное, что приводит к повреждению хряща.
Тканевые ингибиторы металлопротеаз (TIMPs) могут блокировать избыточную активность коллагеназ. Подобные препараты могут замедлять прогрессирование и РА, и дегенеративных заболеваний.
Следует иметь в виду, что вмешательство в ферментное равновесие чревато возникновением проблем. Например, в случае с ингибиторами коллагеназ последние, похоже, играют важную роль в удалении внутренней выстилки синовиальных влагалищ сухожилий. Применение некоторых соединений может вызвать осложнение в виде теносиновиита.
С большинством новых препаратов против артрита связаны две проблемы — цена и время, затрачиваемое на лечебные процедуры.
Эти препараты будут дорогостоящими и применяться в дополнение к уже существующим. Ожидается большая экономия средств, но проявится это не сразу, а по мере снижения необходимости хирургического вмешательства и социальной поддержки. Поэтому на начальных этапах необходимо изыскивать новые средства.
Что касается сроков, то в настоящее время к ревматологам выстроились длинные очереди, а клиники, занимающиеся ведением больных, переполнены — и это при том, что большинство больных дегенеративными заболеваниями не нуждаются в наблюдении. И если у нас будут возможности модифицировать течение дегенеративных заболеваний.
Современная медикаментозная терапия ревматоидного артрита
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает
Ревматоидный артрит — это заболевание, находящееся в фокусе внимания ревматологов всего мира в течение десятилетий. Это связано с большим медицинским и социальным значением этой болезни. Ее распространенность достигает 0,5–2% от общей численности населения в промышленно развитых странах [1, 2]. У больных ревматоидным артритом наблюдается уменьшение продолжительности жизни по сравнению с общей популяцией на 3–7 лет [3]. Трудно переоценить колоссальный ущерб, наносимый этим заболеванием обществу за счет ранней инвалидизации пациентов, которая при отсутствии своевременно начатой активной терапии может наступать в первые 5 лет от дебюта болезни.
Ревматоидный артрит — хроническое воспалительное заболевание неясной этиологии, для которого характерно поражение периферических синовиальных суставов и периартикулярных тканей, сопровождающееся аутоиммунными нарушениями и способное приводить к деструкции суставного хряща и кости, а также к системным воспалительным изменениям.
Патогенез заболевания весьма сложен и во многом недостаточно изучен. Несмотря на это, к настоящему времени хорошо известны некоторые ключевые моменты в развитии ревматоидного воспаления, которые определяют основные методы лечебного воздействия на него (рис. 1). Развитие хронического воспаления в данном случае связано с активацией и пролиферацией иммунокомпетентных клеток (макрофагов, Т- и В-лимфоцитов), что сопровождается выделением клеточных медиаторов — цитокинов, факторов роста, молекул адгезии, а также синтезом аутоантител (например, антицитруллиновых антител) и формированием иммунных комплексов (ревматоидные факторы). Эти процессы ведут к формированию новых капиллярных сосудов (ангиогенез) и разрастанию соединительной ткани в синовиальной оболочке, к активации циклооксигеназы-2 (ЦОГ-2) с повышением синтеза простагландинов и развитием воспалительной реакции, к выделению протеолитических ферментов, активации остеокластов, а в результате — к деструкции нормальных тканей суставов и возникновению деформаций.
Лечение ревматоидного артрита
Исходя из патогенеза заболевания, становится очевидным, что эффективно воздействовать на развитие заболевания можно на двух уровнях:
Поскольку, помимо собственно воспаления, активация иммунной системы сопровождается многими другими патологическими процессами, воздействие на первом уровне является существенно более глубоким и эффективным, нежели на втором. Медикаментозная иммуносупрессия представляет собой основу лечения ревматоидного артрита. К иммуносупрессорам, применяющимся для лечения данного заболевания, относятся базисные противовоспалительные препараты (БПВП), биологические препараты и глюкокортикостероиды. На втором уровне действуют нестероидные противовоспалительные препараты (НПВП) и глюкокортикостероиды.
В целом иммуносупрессивная терапия сопровождается более медленным развитием клинического эффекта (в широких рамках — от нескольких дней в случае биологической терапии до нескольких месяцев в случае применения некоторых БПВП), который в то же время бывает очень выраженным (вплоть до развития клинической ремиссии) и стойким, а также характеризуется торможением деструкции суставов.
Собственно противовоспалительная терапия (НПВП) может давать клинический эффект (обезболивание, уменьшение скованности) очень быстро — в течение 1–2 ч, однако при помощи такого лечения практически невозможно полностью купировать симптоматику при активном ревматоидном артрите и, по-видимому, оно совсем не влияет на развитие деструктивных процессов в тканях.
Глюкокортикостероиды обладают как иммуносупрессивным, так и непосредственным противовоспалительным эффектом, поэтому клиническое улучшение может развиваться быстро (в течение нескольких часов при внутривенном или внутрисуставном введении). Имеются данные о подавлении прогрессирования эрозивного процесса в суставах при длительной терапии низкими дозами глюкокортикостероидов и о положительном их влиянии на функциональный статус больного. В то же время из практики хорошо известно, что назначение только глюкокортикостероидов, без других иммуносупрессивных средств (БПВП), редко дает возможность достаточно эффективно контролировать течение болезни.
Немедикаментозные способы терапии ревматоидного артрита (физиотерапия, бальнеотерапия, диетотерапия, акупунктура и др.) представляют собой дополнительные методики, с помощью которых можно несколько улучшить самочувствие и функциональный статус пациента, но не купировать симптоматику и достоверно повлиять на деструкцию суставов.
Ортопедическое лечение, включающее ортезирование и хирургическую коррекцию деформаций суставов, а также реабилитационные мероприятия (лечебная физкультура и др.) имеют особое значение преимущественно на поздних стадиях заболевания для поддержания функциональной способности и улучшения качества жизни больного.
Основными целями лечения при РА являются [2, 6]:
Надо иметь в виду, что цели лечения могут существенно изменяться в зависимости от длительности болезни. На ранней стадии болезни, т. е. при длительности болезни 6–12 мес, достижение клинической ремиссии — вполне реальная задача, так же как и торможение развития эрозий в суставах. С помощью современных методов активной медикаментозной терапии удается добиться ремиссии у 40–50% пациентов [4, 5], показано также отсутствие появления новых эрозий по данным рентгенографии [7] и магнитно-резонансной томографии [8] у значительного количества больных при длительности наблюдения 1–2 года.
При длительно текущем ревматоидном артрите, особенно при недостаточно активной терапии в первые годы заболевания, достижение полной ремиссии теоретически тоже возможно, однако вероятность этого значительно ниже. То же самое можно сказать и о возможности остановить прогрессирование деструкции в суставах, уже существенно разрушенных за несколько лет болезни. Поэтому при далеко зашедшем ревматоидном артрите возрастает роль реабилитационных мероприятий, ортопедической хирургии. Кроме того, на поздних стадиях заболевания длительная поддерживающая базисная терапия может использоваться для вторичной профилактики осложнений болезни, таких как системные проявления (васкулит и др.), вторичный амилоидоз.
Базисная терапия ревматоидного артрита. БПВП (синонимы: базисные препараты, болезнь-модифицирующие антиревматические препараты, медленно действующие препараты) являются главным компонентом лечения ревматоидного артрита и при отсутствии противопоказаний должны быть назначены каждому пациенту с этим диагнозом [9]. Особенно важно максимально быстрое назначение БПВП (сразу после установления диагноза) на ранней стадии, когда имеется ограниченный период времени (несколько месяцев от появления симптоматики) для достижения наилучших отдаленных результатов — так называемое «терапевтическое окно» [10].
Классические БПВП обладают следующими свойствами.
БПВП существенно различаются между собой по механизму действия и особенностям применения. Основные параметры, характеризующие БПВП, представлены в таблице 1.
БПВП условно могут быть подразделены на препараты первого и второго ряда. Препараты первого ряда обладают наилучшим соотношением эффективности (достоверно подавляют как клиническую симптоматику, так и прогрессирование эрозивного процесса в суставах) и переносимости, в связи с чем назначаются большинству пациентов.
К БПВП первого ряда относятся следующие.
БПВП второго ряда применяются значительно реже в связи с меньшей клинической эффективностью и/или большей токсичностью. Они назначаются, как правило, при неэффективности или непереносимости БПВП первого ряда.
БПВП способны вызвать значительное улучшение (хороший клинический ответ) приблизительно у 60% пациентов. В связи с медленным развитием клинического эффекта назначение БПВП на сроки менее 6 мес не рекомендуется. Длительность лечения определяется индивидуально, типичная продолжительность «курса» лечения одним препаратом (в случае удовлетворительного ответа на терапию) составляет 2–3 года и более. Большинство клинических рекомендаций подразумевают неопределенно долгое применение поддерживающих дозировок БПВП для сохранения достигнутого улучшения.
При недостаточной эффективности монотерапии каким-либо базисным препаратом может быть избрана схема комбинированной базисной терапии, т. е. сочетания двух-трех БПВП. Наиболее хорошо зарекомендовали себя следующие сочетания:
В комбинированных схемах препараты обычно применяются в средних дозировках. В ряде клинических исследований было продемонстрировано превосходство комбинированной базисной терапии над монотерапией, однако более высокая эффективность комбинированных схем не считается строго доказанной. Комбинация БПВП ассоциирована с умеренным повышением частоты побочных эффектов.
Биологические препараты в лечении ревматоидного артрита. Термин биологические препараты (от англ. biologics) применяется по отношению к лекарственным средствам, производимым с использованием биотехнологий и осуществляющим целенаправленное («точечное») блокирование ключевых моментов воспаления с помощью антител или растворимых рецепторов к цитокинам, а также другим биологически активным молекулам. Таким образом, биологические препараты не имеют никакого отношения к «биологически активным пищевым добавкам». В связи с большим количеством «молекул-мишеней», воздействие на которые потенциально может подавлять иммунное воспаление, разработан целый ряд лекарственных средств из этой группы и еще несколько препаратов проходят клинические испытания.
К основным зарегистрированным в мире для лечения ревматоидного артрита биологическим препаратам относятся:
Для биологических препаратов характерны выраженный клинический эффект и достоверно доказанное торможение деструкции суставов. Эти признаки позволяют относить биологические препараты к группе БПВП. В то же время особенностью группы является быстрое (нередко в течение нескольких дней) развитие яркого улучшения, что объединяет биологическую терапию с методами интенсивной терапии. Характерная черта биологических средств — потенцирование эффекта в сочетании с БПВП, в первую очередь с метотрексатом. В связи с высокой эффективностью при ревматоидном артрите, в том числе у резистентных к обычной терапии пациентов, в настоящее время биологическая терапия выдвинулась на второе по значимости место (после БПВП) в лечении этого заболевания.
К отрицательным сторонам биологической терапии относятся:
Биологические методы терапии показаны, если лечение препаратами из группы БПВП (такими, как метотрексат) не является адекватным вследствие недостаточной эффективности или неудовлетворительной переносимости.
Одной из наиболее важных молекул-мишеней служит ФНО-a, который имеет множество провоспалительных биологических эффектов и способствуют персистенции воспалительного процесса в синовиальной оболочке, деструкции хряща и костной ткани за счет прямого действия на синовиальные фибробласты, хондроциты и остеокласты. Блокаторы ФНО-α являются наиболее широко применяемыми биологическими средствами в мире.
В России зарегистрирован препарат из этой группы инфликсимаб (ремикейд), представляющий собой химерное моноклональное антитело к ФНО-α. Препарат, как правило, назначается в сочетании с метотрексатом. У пациентов с недостаточной эффективностью терапии средними и высокими дозами метотрексата инфликсимаб существенно улучшает ответ на лечение и функциональные показатели, а также приводит к выраженному торможению прогрессирования сужения суставной щели и развития эрозивного процесса.
Показанием к назначению инфликсимаба в комбинации с метотрексатом является неэффективность одного или более БПВП, применявшихся в полной дозе (в первую очередь метотрексата), с сохранением высокой воспалительной активности (пять и более припухших суставов, скорость оседания эритроцитов (СОЭ) более 30 мм/ч, С-реактивный белок (СРБ) более 20 мг/л). При раннем ревматоидном артрите с высокой воспалительной активностью и быстрым нарастанием структурных нарушений в суставах комбинированная терапия метотрексатом и инфликсимабом может быть назначена сразу.
До назначения инфликсимаба требуется провести скрининговое обследование на туберкулез (рентгенография грудной клетки, туберкулиновая проба). Рекомендуемая схема применения: начальная доза 3 мг/кг массы тела больного в/в капельно, затем по 3 мг/кг массы тела через 2, 6 и 8 нед, далее по 3 мг/кг массы тела каждые 8 нед, при недостаточной эффективности доза может повышаться вплоть до 10 мг/кг массы тела. Длительность лечения определяется индивидуально, обычно не менее 1 года. После отмены инфликсимаба поддерживающая терапия метотрексатом продолжается. Следует иметь в виду, что повторное назначение инфликсимаба после окончания курса лечения этим препаратом ассоциировано с повышенной вероятностью реакций гиперчувствительности замедленного типа.
Вторым зарегистрированным в нашей стране препаратом для проведения биологической терапии является ритуксимаб (мабтера). Действие ритуксимаба направлено на подавление В-лимфоцитов, которые не только являются ключевыми клетками, отвечающими за синтез аутоантител, но и выполняют важные регуляторные функции на ранних стадиях иммунных реакций. Препарат обладает выраженной клинической эффективностью, в том числе у больных, недостаточно отвечающих на терапию инфликсимабом.
Для лечения ревматоидного артрита препарат применяется в дозе 2000 мг на курс (две инфузии по 1000 мг, каждая с промежутком в 2 нед). Ритуксимаб вводится внутривенно медленно, рекомендуется проведение инфузии в условиях стационара с возможностью точного контроля за скоростью введения. Для профилактики инфузионных реакций целесообразно предварительное введение метилпреднизолона 100 мг. При необходимости возможно проведение повторного курса инфузий ритуксимаба через 6–12 мес.
Согласно европейским клиническим рекомендациям, ритуксимаб целесообразно назначать в случаях неэффективности или невозможности проведения терапии инфликсимабом. Возможность применения ритуксимаба в качестве первого биологического препарата служит в настоящее время предметом исследований.
Глюкокортикостероиды. Глюкокортикостероиды обладают многогранным противовоспалительным действием, обусловленным блокадой синтеза провоспалительных цитокинов и простагландинов, а также торможением пролиферации за счет воздействия на генетический аппарат клеток. Глюкокортикостероиды оказывают быстрый и ярко выраженный дозозависимый эффект в отношении клинических и лабораторных проявлений воспаления. Применение глюкокортикостероидов чревато развитием нежелательных реакций, частота которых также повышается с увеличением дозы препарата (стероидный остеопороз, медикаментозный синдром Иценко–Кушинга, поражение слизистой ЖКТ). Эти препараты сами по себе в большинстве случаев не могут обеспечить полноценного контроля над течением ревматоидного артрита и должны назначаться вместе с БПВП.
Глюкокортикостероиды при данном заболевании применяются системно и локально. Для системного применения показан основной метод лечения — назначение низких доз внутрь (преднизолон — до 10 мг/сут, метилпреднизолон — до 8 мг/сут) на длительный период при высокой воспалительной активности, полиартикулярном поражении, недостаточной эффективности БПВП.
Средние и высокие дозы глюкокортикостероидов внутрь (15 мг/сут и более, обычно 30–40 мг/сут в пересчете на преднизолон), а также пульс-терапия глюкокортикостероидами — внутривенное введение высоких доз метилпреднизолона (250–1000 мг) или дексаметазона (40–120 мг) могут применяться для лечения тяжелых системных проявлений ревматоидного артрита (выпотной серозит, гемолитическая анемия, кожный васкулит, лихорадка и др.), а также некоторых особых форм болезни. Продолжительность лечения определяется временем, необходимым для купирования симптоматики, и составляет обычно 4–6 нед, после чего осуществляется постепенное ступенчатое снижение дозы с переходом на лечение низкими дозами глюкокортикостероидов.
Глюкокортикостероиды в средних и высоких дозах, пульс-терапия, по-видимому, не обладают самостоятельным влиянием на течение ревматоидного артрита и развитие эрозивного процесса в суставах.
Для локальной терапии применяются препараты в микрокристаллической форме, назначающиеся в виде внутрисуставных и периартикулярных инъекций: бетаметазон, триамсинолон, метилпреднизолон, гидрокортизон.
Глюкокортикостероиды для локального применения обладают ярко выраженным противовоспалительным действием, преимущественно в месте введения, а в ряде случаев — и системным действием. Рекомендуемые суточные дозы составляют: 7 мг — для бетаметазона, 40 мг — для триамсинолона и метилпреднизолона, 125 мг — для гидрокортизона. Эта доза (суммарно) может использоваться для внутрисуставного введения в один крупный (коленный) сустав, два сустава среднего размера (локтевые, голеностопные и др.), 4–5 мелких суставов (пястно-фаланговые и др.), либо для периартикулярного введения препарата в 3–4 точки.
Эффект после однократного введения обычно наступает на протяжении 1–3 дней и сохраняется в течение 2–4 нед при хорошей переносимости.
В связи с этим повторные инъекции глюкокортикостероидов в один сустав нецелесообразно назначать ранее чем через 3–4 недели. Проведение курса из нескольких внутрисуставных инъекций в один и тот же сустав не имеет терапевтического смысла и чревато осложнениями (локальный остеопороз, усиление деструкции хряща, остеонекроз, нагноение). В связи с повышенным риском развития остеонекроза внутрисуставное введение глюкокортикостероидов в тазобедренный сустав в целом не рекомендуется.
Глюкокортикостероиды для локального применения назначаются в качестве дополнительного метода купирования обострений ревматоидного артрита и не могут служить заменой системной терапии.
НПВП. Значение НПВП в лечении ревматоидного артрита за последние годы существенно снизилось в связи с появлением новых эффективных схем патогенетической терапии. Противовоспалительное действие НПВП достигается с помощью подавления активности ЦОГ, или избирательно ЦОГ-2, и тем самым снижается синтез простагландинов. Таким образом НПВП действуют на конечное звено ревматоидного воспаления.
Действие НПВП при ревматоидном артрите — уменьшение выраженности симптомов болезни (боль, скованность, припухлость суставов). НПВП обладают обезболивающим, противовоспалительным, жаропонижающим эффектом, но мало влияют на лабораторные показатели воспаления. В подавляющем большинстве случаев НПВП не способны как-либо заметно изменить течение заболевания. Их назначение в качестве единственного противоревматического средства при достоверном диагнозе ревматоидный артрит в настоящее время считается ошибкой. Тем не менее НПВП являются основным средством симптоматической терапии при данном заболевании и в большинстве случаев назначаются в сочетании с БПВП.
Наряду с лечебным эффектом, все НПВП, включая селективные (ингибиторы ЦОГ-2), способны вызывать эрозивно-язвенное поражение ЖКТ (в первую очередь верхних его отделов — «НПВП-гастропатия») с возможными осложнениями (кровотечения, перфорации и пр.), а также нефротоксические и другие нежелательные реакции.
Основные характерные черты, которые необходимо учитывать при назначении НПВП, следующие.
Существует индивидуальная чувствительность к различным НПВП как в отношении эффективности, так и переносимости лечения. Дозы НПВП при ревматоидном артрите соответствуют стандартным. Продолжительность лечения НПВП определяется индивидуально и зависит от потребности больного в симптоматической терапии. При хорошем ответе на терапию БПВП препарат из группы НПВП может быть отменен.
К наиболее часто применяющимся при ревматоидном артрите НПВП относятся:
Селективные НПВП, по эффективности достоверно не отличаясь от неселективных, реже вызывают НПВП-гастропатии и серьезные нежелательные реакции со стороны ЖКТ, хотя и не исключают развитие этих осложнений. Ряд клинических исследований продемонстрировал повышенную вероятность развития тяжелой сосудистой патологии (инфаркт миокарда, инсульт) у пациентов, получавших препараты из группы коксибов, в связи с чем возможность лечения целекоксибом должна обсуждаться с особой осторожностью у больных с ИБС и другими серьезными кардиоваскулярными патологиями.
Дополнительные медикаментозные методы лечения. В качестве симптоматического анальгетика (или дополнительного анальгетика при недостаточной эффективности НПВП) может использоваться парацетамол (ацетаминофен) в дозе 500–1500 мг/сут, который обладает относительно невысокой токсичностью. Для локальной симптоматической терапии используются НПВП в виде гелей и мазей, а также диметилсульфоксид в виде 30–50% водного раствора в форме аппликаций. При наличии остеопороза показано соответствующее лечение препаратами кальция, витамина Д3, бифосфонатами, кальцитонином.
Общие принципы ведения больных РА
Больному с установленным диагнозом ревматоидный артрит должен быть назначен препарат из группы БПВП, который при хорошем клиническом эффекте может применяться как единственный метод терапии [9]. Другие лечебные средства используются по мере необходимости.
Больной должен быть информирован о характере своего заболевания, течении, прогнозе, необходимости длительного сложного лечения, а также о возможных нежелательных реакциях и схеме контроля за лечением, неблагоприятных сочетаниях с другими препаратами (в частности, алкоголем), возможной активации очагов хронической инфекции на фоне лечения, целесообразности временной отмены иммуносупрессивных препаратов при возникновении острых инфекционных заболеваний, о необходимости контрацепции на фоне лечения.
Терапия ревматоидного артрита должна назначаться врачом-ревматологом и проводиться под его наблюдением. Лечение биологическими препаратами может проводиться только под контролем ревматолога, имеющего достаточные знания и опыт для его проведения. Терапия является длительной и подразумевает периодический контроль активности болезни и оценку ответа на терапию. Упрощенный алгоритм представлен на рисунке 2.
Мониторинг активности болезни и ответа на терапию включает оценку показателей суставного статуса (число болезненных и припухших суставов и др.), острофазовых показателей крови (СОЭ, СРБ), оценку боли и активности болезни по визуальной аналоговой шкале, оценку функциональной активности больного в повседневной деятельности с помощью русского варианта опросника состояния здоровья (HAQ). Существуют признанные международным сообществом ревматологов методики количественной оценки ответа на лечение с помощью рекомендованного Европейской лигой по борьбе с ревматизмом (EULAR) индекса DAS (Disease Activity Score) и критериев Американской коллегии ревматологов (ACR) [1]. Кроме того, должен осуществляться мониторинг безопасности проводимой пациенту терапии (в соответствии и формуляром и существующими клиническими рекомендациями). В связи с тем, что эрозивный процесс может развиваться даже при низкой воспалительной активности, помимо оценки активности болезни и ответа на терапию обязательно применяется рентгенография суставов. Прогрессирование деструктивных изменений в суставах оценивают путем стандартной рентгенографии кистей и стоп с использованием рентгенологической классификации стадий ревматоидного артрита, количественных методик по индексам Sharp и Larsen. С целью мониторинга состояния больного обследование рекомендуется проводить с определенной периодичностью (табл. 2).
Лечение резистентного к терапии РА
Резистентным к лечению целесообразно считать пациента с неэффективностью (отсутствием 20% улучшения по основным показателям) как минимум двух стандартных БПВП в достаточно высоких дозах (метотрексат — 15–20 мг/нед, сульфасалазин — 2000 мг/сут, лефлуномид — 20 мг/сут). Неэффективность может быть первичной и вторичной (возникающей после периода удовлетворительного ответа на терапию либо при повторном назначении препарата). Существуют следующие пути преодоления резистентности к терапии:
С точки зрения отдаленных результатов в отношении функциональных нарушений, качества жизни и ее продолжительности оптимальной стратегией терапии ревматоидного артрита является многолетнее лечение БПВП с планомерной сменой схемы их применения по мере необходимости [11].
Литература
Д. Е. Каратеев, доктор медицинских наук
Институт ревматологии РАМН, Москва