Чем можно осушить хлороводород
Галогены
♠ Техника безопасности
Опыты с галогенами следует проводить под тягой (в вытяжном шкафу). Необходимо работать в очках или маске. Все работы с галогенами, особенно бромом, можно проводить только с разрешения преподавателя.
Хлор – ядовитый зеленовато-желтый газ. Вдыхание небольших количеств его вызывает кашель, при вдыхании больших количеств возможны тяжелые последствия, в том числе воспаление и отек легких.
При тяжелом отравлении хлором до прибытия врача необходим покой, вдыхание кислорода. Пострадавшему дают молоко, согревают конечности. При несильном отравлении дают молоко, выводят на свежий воздух до исчезновения симптомов отравления.
Остатки MnO2 или KMnO4 (после получения хлора) выливайте не в раковину, а в «банки для слива» (под тягой). После того как основная масса из колбы перенесена в «банку для слива», следует заполнить колбу водой доверху, затем вылить эту воду в раковину под тягой. Лишь после этого можно вынести колбу из-под тяги.
Бром – тяжелая жидкость, образующая темно-красные пары, способные вызвать отравление, слезотечение, удушье и поражение дыхательных путей. На коже образуются трудно заживающие язвы. Наливать бром в пробирки и капельные воронки следует осторожно, через химическую воронку, только в резиновых перчатках.
При попадании брома на кожу следует быстро промыть пораженные места спиртом, большим количеством воды, а затем многократно 2% раствором гидрокарбоната натрия NaHCO3. При случайном вдыхании паров брома необходим покой, вдыхание паров разбавленного раствора аммиака, затем вдыхание кислорода.
Пары иода темно-фиолетового цвета, имеющие неприятный запах, похожий на запах хлора, разъедают слизистые оболочки. При отравлении парами иода следует вдыхать водяные пары с примесью аммиака, глаза промыть 1% раствором тиосульфата натрия Na2S2O3.
Занятия 3-4. Демонстрационный эксперимент
♣ 1: Очистка газов
Если в узле для получения газа используется соляная кислота, сразу после него ставят промывалку с водой. * Зачем? Воду заливают через отвод а (рис. 13) так, чтобы она закрыла шарик б (или, при отсутствии шарика, была на 0,5 см выше дырочек). Трубку в присоединяют к узлу для получения газа.
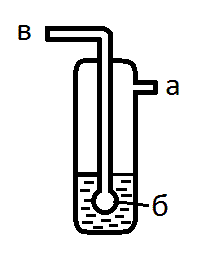

Рис. 13. Осушитель в промывалке
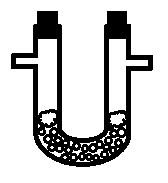
Осушка. Жидкий осушитель помещают в промывалку, твердый – в U-образную трубку. Насыпать твердый осушитель надо так, чтобы нижняя часть трубки была целиком им заполнена, а отводы – свободны (рис. 14); с обеих сторон осушитель ограничивается кусочками ваты. Жидкий осушитель заливают в промывалку при помощи специальной воронки с оттянутым концом (воронка Мюнке).
Рис. 14. Осушитель в U-образной трубке
Воздух, хлор, хлороводород обычно осушают конц. H2SO4 или безводным CaCl2. Сероводород и углекислый газ – безводным CaCl2. Сернистый газ – конц. H2SO4. Аммиак сушат твердыми щелочами или оксидами кальция, бария. Для осушки NO, NO2 используют P2O5, нанесенный на стекловату.
* Почему сероводород не осушают серной кислотой? Почему аммиак не осушают серной кислотой? Почему NO2 не осушают щелочами? Чем осушают водород?
Защита от аэрозолей. При получении газа в колбе или пробирке Вюрца прикапыванием жидкости к порошкообразному веществу легко образуются микроскопические твердые частицы или капельки, проносимые потоком газа через весь прибор – аэрозоли. Чтобы избежать загрязнения ими, вставьте в отвод колбы Вюрца (или на входе в промывалку, U-образную трубку) кусочек ваты.
♣ 2: «Фонтан»
Опыт «фонтан» проделывают с сухими газами, хорошо растворимыми в воде. Его можно использовать как одно из доказательств получения данного газа.
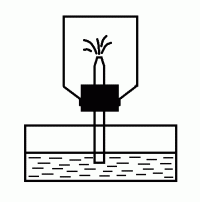
Выделяющимся газом наполняют сухую толстостенную банку, закрывают ее пробкой с трубкой, обращенной оттянутым концом внутрь (рис. 15). Открытый конец трубки помещают в кристаллизатор с водой (можно подкрасить воду индикатором). Закрывают трубку пальцем и встряхивают банку так, чтобы внутрь попала капля воды. Затем снова помещают трубку в воду и убирают палец. * Чем объясняется «фонтанирование» воды внутрь банки?
Рис. 15. Опыт «фонтан»
♥ Опыты
1. Получение хлора и хлорной воды
В колбу или пробирку Вюрца насыпать растертый в ступке и слегка смоченный водой (* для чего?) KMnO4, а через капельную воронку налить конц. HCl. Пропустить выделяющийся хлор через промывалку с дистиллированной водой (* для чего?) и через осушитель (* какой и в каком узле?).
* Как доказать, что выделяется хлор?
Пропустить хлор в пробирку с водой, охлаждаемой снегом.
Поднести к выделяющемуся хлору фильтровальную бумагу, смоченную раствором KI. Фиксировать происходящие изменения.
Наполнить хлором несколько банок (* сколько? – см. опыт 2) и закрыть их стеклянными пластинками. * Как определить окончание заполнения банки?
После окончания выделения хлора проверить, что находится в колбе Вюрца. * Как это сделать?
* Какими еще способами можно получить хлор в лаборатории?
** Какой процесс лежит в основе этих способов получения хлора?
2. Свойства хлора и хлорной воды
А) Поместить на листок бумаги немного порошка сурьмы и медленно высыпать ее в банку с хлором.
Фото В.В. Загорского:
Б) Поместить на листок бумаги немного порошка алюминия и медленно высыпать его в банку с хлором.
В) Положить в ложечку для сжигания немного красного фосфора, поджечь его и внести в банку с хлором. * Чем отличается характер и продукты горения фосфора на воздухе и в хлоре?
Г) 1 каплей хлорной воды (* где она образовалась? – см. опыт 1) смочить лакмусовую бумажку. * Каков состав хлорной воды?
** Какие химические свойства характерны для хлора? Какие химические свойства проявляет хлорная вода? А какие свойства проявляет хлор при образовании хлорной воды?
3. Свойства брома и бромной воды
А) Налить в термостойкую пробирку немного брома, закрепить ее вертикально в лапке штатива над песчаной баней и бросить в пробирку несколько зачищенных наждачной бумагой кусочков алюминия. * Сразу или нет начинается реакция? Почему?
Б) Поместить в пробирку немного сухого красного фосфора. Капнуть с помощью пипетки 1-2 капли жидкого брома. * Как отличается состав продуктов по высоте пробирки?


В) Капнуть 1 каплю жидкого брома в пробирку с водой.
Отлить 2-3 мл полученного раствора в другую пробирку и добавить по каплям 1 М раствор NaOH. Добавить к полученному раствору несколько капель 1 М раствора H2SO4. * Каков состав бромной воды? Какое влияние оказывают щелочь и кислота на смещение равновесия в бромной воде и почему?
** Какие химические свойства характерны для брома? Сравните взаимодействие алюминия и фосфора с хлором и бромом. Объясните различие.
4. Плавление и сублимация иода
А) Поместить несколько кристалликов иода в широкий стакан. Закрыть часовым стеклом. Осторожно нагреть.

Б) Насыпать в узкую пробирку иод (слой 1,5-2 см в высоту), заткнуть кусочком ваты. Нагреть горелкой дно пробирки, покачать и, наклонив, дать остыть.
** Чем обусловлено различие протекающих процессов в опытах А и Б?
5. Растворимость галогенов
А) Налить в пробирки по 2-3 мл хлорной, бромной и иодной воды (* какова растворимость галогенов в воде?) и прилить около 0,5 мл неполярного растворителя (* приведите 2 примера таковых). Закрыть пробирки пробками, встряхнуть, дать отстояться. * Вспомните, что такое экстракция.
Б) По одному кристаллику иода растворить в 1 мл CCl4, гексана, бензола, этилового спирта. * Объясните различие в окраске растворов. Иод в спирте, гексане, бензоле:
В) По одному кристаллику иода растворить в 1 мл растворов KI, KBr, KCl. * За счет чего происходит растворение иода в этих растворах? Иод в растворе KCl, KBr, KI:
** В каких растворителях лучше растворяются галогены – полярных или неполярных, – и почему?
6. Сравнение окислительных свойств галогенов
В пробирку с раствором KBr прилить 0,5 мл неполярного растворителя (* зачем?) и постепенно, при взбалтывании, добавлять хлорную воду из опыта 1. Повторить с раствором KI.
Сl2 + мало KI (иод на стенках):
В пробирку с раствором KCl постепенно добавлять бромную воду.
** Как изменяются окислительные свойства галогенов в группе?
7. Взаимодействие галогенидов с концентрированной серной кислотой
В одну пробирку поместить немного сухого KCl, в другую – KBr, в третью – KI. Смочить соли 1-2 каплями конц. серной кислоты. К отверстию каждой пробирки поднести поочередно лакмусовой бумажку; бумажку, смоченную раствором KMnO4; и бумажку, смоченную раствором нитрата или ацетата свинца. * Для чего?


** Какие свойства галогенидов можно сравнить на основании этого опыта?
8. Получение и свойства хлороводорода
А) В колбу Вюрца насыпать 5-10 г NaCl так, чтобы поверхность соли была скошена (* зачем?). На выходе поставить U-образную трубку. * Какой осушитель в нее поместить? Через капельную воронку прилить в колбу конц. H2SO4. Осторожно нагреть колбу через асбестовую сетку. Наполнить хлороводородом сухую толстостенную банку. * Как это сделать? Как определить окончание ее заполнения?
Б) Проделать опыт «фонтан». * Какими индикаторами можно подкрасить воду – лакмусом, метилоранжем, фенолфталеином?
** О каких свойствах хлороводорода говорит опыт Б? Можно ли использовать опыт А для получения бромоводорода, иодоводорода?
9. Качественные реакции на галогенид-ионы
А) Подействовать на растворы хлорида, бромида и иодида калия раствором нитрата серебра. Проверить растворимость осадков в 1 М растворе аммиака.


Б) Подействовать на растворы хлорида, бромида и иодида калия раствором нитрата или ацетата свинца.
** Как различить хлорид и бромид? Бромид и иодид?
Хлорная вода: состав, получение, химическая формула, использование хлора для очистки
С помощью этого элемента повсеместно очищают питье, что позволяет решить многочисленные проблемы с ее качеством. Он помогает избавиться практически ото всех известных вирусов и бактерий, оказывающих пагубное влияние на человеческий организм. На сегодняшний день не существует другого средства, способствующего столь эффективной дезинфекции. Поэтому в нашей статье мы поговорим о хлорной воде: что это такое, состав, химическая формула, применение.
Что собой представляет
По сути, это растворенный в H2O хлор. В растворе, помимо молекул Cl, содержатся также хлорноватистая и хлороводородная кислоты.
Почти во всех водопроводных системах жидкость, предназначенная для питья, подлежит хлорированию. Объясняется это присутствием большого количества вредоносных микроорганизмов, способных спровоцировать возникновение тяжелейших заболеваний. Уничтожить опасные для человека примеси можно еще тремя способами: облучением, окислением или кипячением. Однако кипятить и облучать довольно нерационально, а окислять — опасно.
Существует и четвертая методика очистки — озонирование, но и в этом случае возникающие проблемы не позволяют эффективно применять ее на практике. Озон почти мгновенно улетучивается. Поэтому в момент, когда чистое питье достигнет водопроводных кранов в квартирах и домах, результат обработки окажется ничтожным.
Характеристики хлоридсодержащих жидкостей
В природной среде элемент находится в связанной форме (хлорид). Его присутствие зафиксировано в ряде минералов, к ним относятся: галит, карналлит и сильвит. Соединение вода плюс хлор возникает там, где подземные потоки проходят через пласты хлорсодержащих отложений. Также образование возможно в морях и некоторых озерах.
Большая часть веществ без проблем растворяется при контакте с H2O. Так образуются свободные подвижные ионы, благодаря которым солевые растворы обладают гораздо большей электропроводностью по сравнению с продуктом дистилляции.
Проводя анализ качественного состава в каком-либо водоеме, в первую очередь учитывают концентрацию хлоридных объединений. Так, в регионах с холодными климатическими условиями количество хлоридов в наземных и подземных потоках может равняться 10 мг/л. В южных зонах показатель способен достигать 100 мг/л. Большую угрозу экологии и здоровью человека представляют несанкционированно организованные или оборудованные ненадлежащим образом свалки. При сгорании хлорсоединения выделяют не меньше вредных соединений, чем при растворении.
Использование хлора для очистки воды сейчас повсеместное явление. Его избыток не лучшим образом сказывается на вкусовых качествах питья. Но использовать для бытовых и хозяйственных нужд такую жидкость можно. А вот задействовать ее в сельском хозяйстве — неверное решение.
Формулы
Являясь сильнейшим окислителем, она способна растворять даже золото. Представить ее наглядно можно по-разному.
Химическая
Вариант формулы требует указания всех составляющих.
Cl2 + H2O = HCl + HClO.
Структурная
Графическая вариация упрощает понимание, каким образом происходит слияние. Связь атомов в теле молекулы становится более наглядной. Так как хлорная вода содержит несколько соединений, следует рассмотреть их все.
1,5 м3/ч Для технической воды
1,5 м3/ч Для технической воды
MBFT-75 Мембрана на 75GPD
Ионная
Хлорная и хлороводородная кислоты представляют собой электролиты. Поэтому они способны распадаться на ионы в жидкостном растворе. Течение реакций можно проследить по формулам:
Электронная
Эта версия демонстрирует размещение электронов в атоме, расположенных на энергетических подуровнях:
Это подтверждает то, что Cl причисляется к р-семейству элементов и показывает количество валентных электронов.
На рисунке ниже укажем формулу хлороводородной кислоты:
Нормы примесей
При растворении хлора в воде она обогащается ионами кальция и магния, что объясняет ее чрезмерную жесткость. Хлоридионы появляются в процессе образования раствора жидкость + вещество, являющегося сильнейшим электролитом MgCl2. В природе на их возникновение влияют естественные факторы, такие как вымывание хлорсодержащих пород. В водопроводной жидкости, которую мы используем для повседневных нужд, наполнения бассейнов, в качестве питья ионы возникают благодаря хлорированию. Этот процесс осуществляется с целью дезинфекции.
При этом очень важно, чтобы концентрация элемента не превышала установленную норму. Так, для употребления подходит H2O, в которой содержится не более 350 мг/л хлора. Для технического использования показатель может быть и 700 мг/л. Избавиться от лишней хлорки в воде чаще всего удается с помощью простого метода — отстаивания.
Обеззараживание
Оптимальное количество окислителя приблизительно 0,5 мг/л. Смешивание с реагентом производится с особой тщательностью. Употреблять питьевой раствор после реакции можно не ранее, чем через 30 минут.
SF-mix Clack до 0,8 м3/ч
SF-mix Runxin до 0,8 м3/ч
SF-mix ручной до 0,8 м3/ч
Гипохлорид натрия выступает самым надежным средством для дезинфекции. Благодаря своим свойствам он эффективно устраняет вредоносные бактерии, а также является вполне безопасным по части взрывоопасности. Этот элемент более активный и не отличается токсичностью.
Вред повышенного содержания хлора в воде для здоровья человека
Мы уже разобрались, что это соединение используют для обеззараживания. В отношении человеческого организма это, конечно, не самая полезная добавка. Здесь важно осознавать степень его вреда и полезности.
В виде газа он без труда растворяется, в том числе и в дыхательных органах человека, а также на слизистых его носа и глаз. В процессе растворения элемента происходит образование соляной кислоты. Именно оказывает столь пагубное воздействие на телесную оболочку. Хлорные пары поражают сердце и легкие, заставляют задыхаться. Нарушается функционирование абсолютно всех тканей в организме.
Растворимость хлора (хлорки) в воде позволяет ему беспрепятственно проникать в тело живых существ. Организм ощущает его присутствие как сильный болевой синдром. Дополнительную опасность представляет атомарный кислород. Высокая активность дает ему возможность оказывать разрушительное воздействие не только на слизистые, но и на БЖУ систему. При контакте с кожей такая «живительная влага» высушивает ее, повреждая жировую подкожную прослойку. Особо тяжких последствий при этом не будет, но масса неприятных ощущений — гарантирована.
Глаза отличаются особой чувствительностью. При попадании паров Cl появляется непрекращающееся жжение и раздражение, словно при глазной болезни. Оказавшись в такой ситуации, нужно помнить, что влияние атомарного кислорода на них невозможно предвидеть. Ухудшение самочувствия может наступить внезапно. К сожалению, слишком часто происходят такие неприятные и небезопасные для человека случаи.
Воды без хлора в системе водоснабжения практически не бывает. Набирая ванну, вы даже не замечаете, что она вместе с ним испаряется и попадает в легкие, на слизистые. Впоследствии вещество оседает на внутренних органах и выводит их из строя, также, как при употреблении такого питья.
Поэтому несмотря на выраженные обеззараживающие свойства, элемент имеет перечень противопоказаний для:
Избыточное количество Cl способно спровоцировать:
Чем избыток хлорной воды вреден для бытового оборудования
Это вещество в больших количествах оказывает разрушительное воздействие не только на человеческий организм. Немалый вред оно наносит и технике. Слишком жесткая жидкость провоцирует выпадение характерного осадка, который скапливается на нагревательных элементах. Из-за этого в несколько раз возрастает вероятность поломки стиральных машин, посудомоечных аппаратов, котлов для подогрева H2O.
Воздействие на коммуникации
Коррозии вследствие избытка хлора, к сожалению, подвержены многие металлы. В системах водоснабжении хлорка выступает одной из ведущих причин возникновения разрывов и трещин в трубах, что зачастую приводит к масштабным протечкам.
Способы получения хлорной воды
Выбор методики во многом зависит от предназначения процесса и качества очищаемой среды. Большое значение имеет количество вредоносных примесей и их активность.
Аэрационная установка AS-1054 VO-90
Диспенсер магистральный настольный AquaPro 919H/RO (горячая и холодная вода)
Известь с Cl
Довольно распространенный метод обеззараживания систем водоснабжения. Это вещество перевозят и хранят в емкостях из дерева или железобетона. Изнутри их в обязательном порядке отделывают кислотоупорным материалом (специальной плиткой) или цементом. Хлорирование известью производится с задействованием 2% раствора из расчета 5 кг/100 л. Существенным минусом такого способа выступают производственные затраты на изготовление очищающего средства и его большой расход.
Диоксид хлора
Он отличается рядом серьезных преимуществ:
При этом хлорная вода, ее цвет, вкус и запах соответствуют всем нормам. Однако, есть у представленного способа и свои недостатки. Он отличается дороговизной и довольно взрывоопасен, что немаловажно.
Дехлорирование
Когда концентрация превышает установленные нормы, проводят очищение от избытка элемента. Делают это посредством добавления в уже хлорсодержащую жидкость веществ, связывающих излишки и удаляющих их из состава. К таковым помощникам относятся: сульфит, гипосульфит натрия, сернистый газ.
Оптимальный вариант решения проблемы — использование угольного фильтра. Приобрести подходящее очистное средство сейчас совсем несложно. Рынок наводнен многочисленными экземплярами, с помощью которых можно эффективно избавиться от всех нежелательных примесей. Так, компания «Вода Отчества» уже много лет осуществляет успешную разработку и производство водоочистного оборудования для бытовых и промышленных нужд потребителей. Остановить свой выбор на их продукции — по-настоящему правильное решение. Ведь забота о здоровье наших родных и близких — первостепенная задача каждого.
Угольные элементы в приборе фильтрации устраняют неприятный запах, вкус, избавляют от излишков Cl, а также нежелательной органики. В процессе дехлорирования углем происходит реакция окисления. Продолжительность очистки варьируется от 2 до 8 минут. Наибольшей эффективности удастся достичь путем обратной промывки.
Вышеперечисленные методы удаления излишков хлорида можно применять как в домах, так и для очистки колодцев. Проводя обработку, следует строго соблюдать необходимые меры предосторожности.
Использование хлорной жидкости и хлорноватистой кислоты
Использовать вещества, содержащие активный Cl, начали очень давно, еще несколько столетий назад. Элемент был обозначен в далеком 1774 году химиком Бертолле. Он обнаружил, что вода, в состав которой входит хлор, способна отбеливать хлопковые и льняные ткани, удаляя с них въевшиеся желтоватые пятна. Тогда же этот выдающийся человек открыл собственное предприятие по отбеливанию материи и бумаги. Первым и единственным работником на фабрике в тот момент был только его сын.
При растворении хлора в воде появляется хлорноватистая кислота, которая не отличается высокой устойчивостью. В растворе ее обычно не больше 30%. Медленное течение реакции обеспечивает, как правило, кислая среда и температурный режим, приближенный к комнатному. Наличие соляной кислоты позволяет установиться равновесию. А при повышенных температурах в слабокислой основе процесс значительно ускоряется.
В XIX веке по результатам многочисленных исследований подтвердили дезинфицирующие свойства хлорки. В то время уже стало ясно, что аналогов, способных сравниться с данным веществом по части устранения различного рода загрязнений, не существует. Очередное же полезное качество сделало хлор еще более популярным.
Впервые с целью дезинфекции его стали задействовать в венской больнице в 1846 году. Доктора омывали им ладони перед контактом с пациентами и после. Проходивший в то время в Вене конгресс подтвердил, что подавляющее большинство болезней, характеризующихся как эпидемии, активно распространяются в водоемах. Cl в одночасье был признан одним из лучших средств для устранения заражающих бактерий из водной среды. Оказался он как нельзя кстати и при сооружении первых систем водоснабжения. На сегодняшний день продолжает занимать ведущее место среди современных средств дезинфекции.
Пожалуй, ни у кого теперь не осталось вопросов: растворим ли хлор в воде, чем опасен его избыток и как избежать связанных с ним проблем. Надеемся, что наша статья оказалась для вас действительно полезной.