Что общего у всех элементов vii группы главной подгруппы периодической системы
Общая характеристика подгруппы
35Br [Ar] 3d 10 4s 2 4p 5
53I [Kr] 4d 10 5s 2 5p 5
85At [Xe] 4f 14 5d 10 6s 2 6p 5
5 элементов главной подгруппы VII группы имеют общее групповое название «галогены»
(Hal), что означает «солерождающие».
Свойства элементов подгруппы галогенов
1. Порядковый номер
2. Валентные электроны
3. Энергия ионизации атома, эВ
4. Относительная электроотрицательность
5. Степень окисления в соединениях
Однако атомы галогенов, кроме фтора, могут проявлять и положительные степени окисления : +1, +3, +5, +7. Возможные значения степеней окисления объясняются электронным строением, которое у атомов фтора можно представить схемой
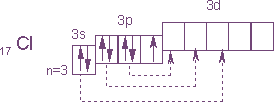
Электронное строение атома хлора выражается схемой:
Одинаковое строение внешнего электронного слоя (ns 2 np 5 ) обусловливает большое сходство элементов.
При образовании ковалентных связей галогены чаще всего используют один неспаренный р-электрон, имеющийся в невозбужденном атоме, проявляя при этом
Валентные состояния атомов CI, Br, I.
Образуя связи с атомами более электроотрицательных элементов, атомы хлора, брома и йода могут переходить из основного валентного состояния в возбужденные, что сопровождается переходом электронов на вакантные орбитали d-подуровня. При этом число неспаренных электронов увеличивается, вследствие чего атомы CI, Br, I могут образовывать большее число ковалентных связей:
Общая характеристика элементов VII группы
Элементы, входящие в VII группу периодической системы, делятся на две подгруппы: главную — подгруппу галогенов — и побочную — подгруппу марганца. В эту же группу помещают и водород, хотя его атом имеет на внешнем, валентном, уровне единственный электрон и его следовало бы поместить в I группу. Однако водород имеет очень мало общего как с элементами основой подгруппы — щелочными металлами, так и с элементами побочной подгруппы — медью, серебром и золотом. В то же время он, как и галогены, присоединяя в реакциях с активными металлами электрон, образует гидриды, имеющие некоторое сходство с галогенидами.
Частные аналитические реакции ионов Mn 2+
1.5.5. Окисление висмутатом натрия NaBiO3, протекает по уравнению:
Реакция идет на холоду.Выполнение реакции: к 1-2 каплям раствора соли марганца прибавляют 3-4 капли 6 М раствора HNO3 и 5-6 капель H2O, после чего вносят лопаточкой немного порошка NaBiO3. перемешав содержимое пробирки, дают постоять 1-2 минуты, центрифугируют для отделения избытка висмутата натрия. В присутствии Mn 2+ раствор становится фиолетовым в результате образования марганцевой кислоты, которая является одним из наиболее сильных окислителей.
1.5.6. Окисление двуокисью свинца PbО2 в азотнокислой среде при нагревании:
Содержание рутения и осмия в земной коре оценивается на уровне 2·10 −11 %.
Рутений является единственным платиновым металлом, который обнаруживается в составе живых организмов. (По некоторым данным — ещё и платина). Концентрируется в основном в мышечной ткани. Высший оксид рутения крайне ядовит и, будучи сильным окислителем, может вызвать возгорание пожароопасных веществ.
VII группа главная подгруппа периодический таблицы Менделеева (галогены)
К элементам главной подгруппы VII группы периодической таблицы Менделеева относятся элементы с общим названием «галогены»:
Общая характеристика галогенов
От F к At (сверху вниз в периодической таблице)
Увеличивается
Уменьшается
Электронные конфигурации у данных элементов схожи, они содержат 7 электронов на внешнем слое ns 2 np 5 :
Br – 3d 10 4s 2 4p 5 ;
I — 4d 10 5s 2 5p 5 ;
At – 4f 14 5d 10 6s 2 6p 5
Электронная конфигурация фтора и хлора
Электронная конфигурация брома и йода
Нахождение в природе галогенов
Галогены являются химически активными веществами, в связи с чем, в природе они встречаются только в виде соединений. Их распространённость в земной коре снижается при увеличении атомного радиуса (от фтора к иоду). Например, содержание астата в земной коре исчисляется граммами.
Наиболее распространённые соединения фтора — флюорит CaF2, криолит Na3AlF6 и др., хлора — каменная соль (галит) NaCl, сильвин KCl и сильвинит KCl⋅NaCl.
Бром и иод не образуют индивидуальных минералов, но их соединения содержатся в морской воде и могут накапливаться водорослями.
Способы получения фтора
Фтор получают методом электролиза расплава гидрофторида калия (смеси HF и KF):
Физические свойства фтора
Фтор при обычной температуре — зеленовато-жёлтый ядовитый газ, с резким запахом, очень реакционноспособный, хорошо растворим в жидких водороде и кислороде.
Химические свойства фтора
Фтор является самым сильным окислителем из всех простых веществ. Непосредственно он не взаимодействует только с N2, Не, Ne, Аr, а при нормальных условиях также и с O2.
Взаимодействие с простыми веществами
С кислородом
С галогенами (Cl, Br, I)
Фтор вступает в реакции с другими галогенами:
Например, Cl2 + F2 → 2ClF
С водородом
Взаимодействует с водородом со взрывом даже в темноте:
С серой
Реакция с серой протекает легко даже при сильном охлажлении:
С углеродом
Реакция окисления порошкообразного углерода сопровождается самовоспламенением последнего:
С азотом
При нагревании фтор реагирует и с азотом:
С фосфором
Фтор взаимодействует с P энергично (со взрывом) на свету и в темноте, даже при охлаждении жидким N2:
С кремнием
Взаимодействует с кремнием с образованием фторида кремния
C инертными газами
Окисляет ксенон, образуя фторид ксенона:
С металлами
При взаимодействии с металлами образуются фториды:
Взаимодействие со сложными веществами
С водой
Фтор активно разлагает воду с образованием таких соединений, как фториды кислорода OF2, O2F2; пероксид водорода Н2O2; кислород, озон, фтороводород:
С кислотами
С щелочами и аммиаком
Фтор окисляет щелочи:
Реагирует с газообразным аммиаком:
С солями
Не взаимодействует
Взаимодействие фтора с водными растворами солей невозможны, т.к. он ступает в реакцию с водой.
С оксидами
Реагирует с оксидом кремния, который загорается в атмосфере F2:
Способы получения хлора
Промышленный способ
Электролиз расплавов или водных растворов хлоридов, чаще – NaCl.
A(+): 2Cl − ̶ 2e → Cl2 0
2Na + + 2Cl − → 2Na º + Cl2º
Таким образом, получаем:
A(+): 2Cl − ̶ 2e → Cl2 0
Таким образом, получаем:
Лабораторный способ
Окисление концентрированной HCI сильными окислителями:
Физические свойства хлора
Хлор Cl2 при обычной температуре – тяжелый, желто-зеленый газ с резким удушающим запахом.
Cl2 в 2,5 раза тяжелее воздуха, малорастворим в воде (
6,5 г/л); хорошо растворим в неполярных органических растворителях. В свободном состоянии встречается только в вулканических газах.
Химические свойства хлора
Хлор — очень сильный окислитель. Окисляет металлы, неметаллы и сложные вещества, с образованием в устойчивые хлорид-ионы:
Взаимодействие с простыми веществами
С кислородом
Непосредственно не взаимодействует
С галогенами
Хлор взаимодействует с другими галогенами – более активные галогены окисляют менее активные. В зависимости от условий могут получиться различные соединения:
С водородом
Реакция с водородом при обычных условиях не протекает. Однако, при нагревании, УФ — освещении или электрическом разряде реакция протекает со взрывом:
Непосредственно не взаимодействует
С фосфором
Непосредственно не взаимодействует
С кремнием
2Cl2 + Si = SiCl4 (при нагревании)
С металлами
Взаимодействие со сложными веществами
Окисляет сложные вещества:
2Cl2 + 2H2O → 4HCl + O2 (на свету или кипячении)
С водой
При растворении хлора в воде вступает в реакцию диспропорционирования (самоокисления-самовосстановления), с образованием хлорноватистой кислоты:
С водными растворами щелочей
При взаимодействии с щелочами хлор диспропорционирует с образованием солей, состав которых зависит от условий проведения реакции:
Эти реакции имеют важное практическое значение, приводят к получению гипохлоритов — КClO3 и Са(ClO)2; хлората калия (бертолетова соль) — КClO3
С солями
Более активные галогены вытесняют менее активные галогены из солей и галогеноводородов:
HC ≡ CH + 2Cl2 → Cl2HC — CHCl2 1,1,2,2-тетрахлорэтан
Способы получения брома
Промышленный способ
Бром втесняют при помощи хлора:
Далее бром отгоняют из раствора водяным паром или воздухом.
Лабораторный способ
Физические свойства брома
В обычных условиях бром – красно-бурая жидкость с резким зловонным запахом. При Т=-7,2°C жидкий бром застывает, образуя красно-коричневые игольчатые кристаллы.
Пары брома жёлто-бурого цвета, Ткип = 58,78°C.
В воде бром растворяется лучше других галогенов (3,58 г брома в 100 г H2O при 20°C). Хорошо растворим во многих органических растворителях.
Бромная вода имеет желто-бурую окраску, быстро исчезающую, при взаимодействии растворенного Br2 с каким-либо веществом. «Обесцвечивание бромной воды» — широко используется в качестве теста на обнаружение в растворе многих неорганических и органических веществ.
Химические свойства брома
Химические свойства брома сходны с хлором. Различаются только условия протекания реакций.
Взаимодействие с простыми веществами
С металлами
Жидкий бром сильный окислитель. Например, железо и алюминий самовозгораются при соприкосновении с бромом даже при обычной температуре.
С водородом
Взаимодействие брома с водородом происходит лишь при повышенной температуре. Реакция эндотермической и обратимой.
С азотом, углеродом, кислородом и благородными газами
Непосредственно не взаимодействует
С галогенами
Бром окисляется более активными галогенами:
Взаимодействие со сложными веществами
Обесцвечивание бромной воды
Обесцвечивание бромной воды – качественная реакция на многие неорганические и органические соединения:
Способы получения йода
Промышленный способ
Лабораторный способ
2 FеC3 + 2 НI = 2 FeCl2 + I2 + 2 НСl
Физические свойства йода
Свободный йод I2 при обычной температуре — черно-серое с фиолетовым оттенком кристаллическое вещество с металлическим блеском. Легко возгоняется. Пары йода имеют своеобразный запах и очень ядовиты.
Среди галогенов I2 обладает самой меньшей растворимостью в воде, однако он хорошо растворим в спирте и других органических растворителях.
Химические свойства йода
Химическая активность йода – наименьшая по сравнению с другими галогенами. Со многими элементами йод непосредственно не взаимодействует, а с некоторыми реагирует только при повышенных температурах (водород, кремний, многие металлы).
Йод-крахмальная реакция
Обнаружить I2 даже в самой минимальной концентрации можно с помощью раствора крахмала, который при наличии I2 окрашивается в грязно-синий цвет.
Йод-крахмальная реакция используется при качественном обнаружении йода, а также его количественного анализа
Взаимодействие с простыми веществами
С водородом
Реакция обратима и возможна только при высокой температуре:
С металлами
При добавлении капли воды в качестве катализатора цинк, железо и алюминий в смеси с порошком йода горят, образуя йодиды:
С азотом, углеродом, кислородом
Непосредственно не взаимодействует
Взаимодействие со сложными веществами
С водой
Частично реагирует с водой (реакция диспропорционирования):
С щелочью
Диспропорционирует в водном растворе щелочи:
C аммиаком
C аммиаком образует аддукт нитрид трииодида:
С иодидами щелочных металлов
Молекулы галогенов присоединяются к иодидам щелочных металлов с образованием полииодидов (периодидов):
С окислителями
Йод проявляет восстановительные свойства в реакциях с сильными окислителями:
C восстановителями
Иод менее сильный окислитель, чем фтор, хлор и бром. Восстановители, такие как H2S, Na2S2O3 и др. восстанавливают его до иона I − :
Общая характеристика элементов VII группы
Элементы, входящие в VII группу периодической системы, делятся на две подгруппы: главную — подгруппу галогенов — и побочную — подгруппу марганца. В эту же группу помещают и водород, хотя его атом имеет на внешнем, валентном, уровне единственный электрон и его следовало бы поместить в I группу. Однако водород имеет очень мало общего как с элементами основой подгруппы — щелочными металлами, так и с элементами побочной подгруппы — медью, серебром и золотом. В то же время он, как и галогены, присоединяя в реакциях с активными металлами электрон, образует гидриды, имеющие некоторое сходство с галогенидами.
К подгруппе галогенов относятся фтор, хлор, бром, иод и астат. Первые четыре элемента встречаются в природе, последний получен искусственно и поэтому изучен значительно меньше остальных галогенов. Слово галоген означает солеобразующий. Это название элементы подгруппы получили благодаря легкости, с которой они реагируют со многими металлами, образуя соли.
К подгруппе марганца принадлежат марганец, технеций и рений. В отличи и от галогенов элементы подгруппы марганца имеют на внешнем электронном уровне всего два электрона и поэтому не проявляют способности присоединять электроны, образуя отрицательно заряженные ионы.
Марганец распространен в природе и широко используется в промышленности.
Хлор был открыт шведским химиком К. В. Шееле в 1774 г.
Нахождение в природе. Из-за высокой активности хлор в свободном состоянии в природе не встречается. Широко известны его природные соединения — хлориды щелочных и щелочноземельных металлов, наиболее распространенными из которых являются каменная (поваренная) соль NаС1, сильвинит — смесь хлоридов калия и натрия — и карналлит КС1 · МgC12 · 6Н2О. Как примеси к названным минералам встречаются хлориды других металлов. Значительное количество хлоридов различиях металлов содержится в морской воде.
В отсутствие влаги хлор довольно инертен, но в присутствии даже следов влаги активность его резко возрастает. 0н хорошо взаимодействует с металлами:
2 Fе + 3 С12 = 2 FеС13 (хлорид железа (III)
Cu + С12 = СuС12 (хлорид меди (II)
и многими неметаллами:
Н2 + С12 = 2 НСl (хлороводород)
Si + 2 С12 = SiС14 (хлорид кремния. (IV))
2 Р + 5 С12 = 2 РС15 (хлорид фосфора (V))
С кислородом, углеродом и азотом хлор в непосредственное взаимодействие не вступает.
При взаимодействии хлора с холодными растворами щелочей образуются соответствующие соли этих кислот:
С12 + 2 NaOН = NaС1 + NaClО + Н2О
3 С12 + 6 NаОН = 5 NаСl + NаС1O3 + 3 Н2О
3 С12 + 6 КОН = 5 КСl + КС1O3 + 3 Н2О
Образовавшийся хлорат калия называется бертолетовой солью.
Хлор — сильный окислитель, поэтому легко взаимодействует со сложными веществами, в состав которых входят элементы, способные окисляться до более высокого валентного состояния.
Получение. В лабораторных условиях хлор получают действием концентрированной соляной кислоты на различные окислители, например диоксид марганца (при нагревании), перманганат калия или бертолетову соль:
2 КМпО4 + 16 НСl = 2 КС1 + 2 МnС12 + 5 С12 + 8 Н2О
В промышленности хлор получают электролизом растворов, или расплавов хлоридов щелочных металлов. При электролизе расплава хлорида щелочного металла на катоде выделяется щелочной металл, а на аноде — хлор:
В растворе хлорид щелочного металла диссоциирует на ионы:
Вода как слабый электролит также диссоциирует на ионы:
Применение. Ежегодное мировое потребление хлора превышает 1 млн. т. Он используется для отбеливания бумаги и тканей, обеззараживания питьевой воды, производства различных. ядохимикатов, соляной кислоты, хлорорганических веществ и растворителей, а также в лабораторной практике.
Сухой хлороводород довольно инертный и не реагирует даже с активными металлами, а в присутствии следов влаги такая реакция протекает довольно энергично.
Хлороводород может присоединяться к непредельным углеводородам по месту двойной или тройной связи, образуя хлорорганические соединения.
В лабораторных условиях хлороводород получают действием концентрированной серной кислоты на сухой хлорид натрия:
Первая из этих реакций протекает при слабом нагревании, а вторая — при более высокой температуре. Поэтому получать хлороводород в лаборатории лучше по первому уравнению и серной кислоты следует брать столько, сколько требуется для образования гидросульфата натрия.
В промышленности хлороводород получают действием концентрированной серной кислоты на сухой хлорид натрия при высокой температуре (по второму уравнению), а также сжиганием водород в атмосфере хлора:
Хлороводород образуется в значительных количествах как побочный продукт при хлорировании насыщениях и ароматических углеводородов.
Кроме свойств, присущих сильным кислотам, эта кислота характеризуется также восстановительными свойствами: концентрированная соляная кислота реагирует с различными сильными окислителями с образованием свободного хлора.
Соляную кислоту хранят и транспортируют в стальных цистернах, покрытых изнутри кислотоупорной резиной, или в стеклянных баллонах.
Из солей соляной кислоты наибольшее применение находит:
хлорид калия КС1. Применяется как калийное удобрение, а также как сырье для получения других солей калия и едкого кали;
хлорид бария ВаС12. Применяется как ядохимикат в сельском хозяйстве;
Хлорноватистая кислота НСlO образуется при взаимодействии хлора с водой, а также ее солей с сильными минеральными кислотами. Она относится к слабым кислотам, очень неустойчива. Состав продуктов реакции ее разложения зависит от условий. При сильном освещении хлорноватистой кислоты, наличии в растворе восстановителя, а также длительном стоянии она разлагается с выделением атомарного кислорода:
В присутствии водоотнимающих веществ образуется оксид хлора (I):
Cl2О можно считать ангидридом хлорноватистой кислоты. При нагревании хлорноватистая кислота разлагается с образованием двух кислот — соляной и хлорноватой:
3 НСlO = 2 НСl + НСlO3
Поэтому при взаимодействии хлора с горячим раствором щелочи образуется соли не соляной и хлорноватистой, а соляной и хлорноватой кислот:
6 NаОН + 3 Сl2 = 5 NаСl + NаСlО3 + 3 Н2О
Соли хлорноватистой кислоты — г и п о х л о р и т ы — очень сильные окислители. Они образуются при взаимодействии хлора со щелочами на холоду. Одновременно образуются соли соляной кислоты. Из таких смесей наибольшее распространение получили хлорная известь и жавелевая вода.
Хлорная, или белильная, известь СаОСl2, или СаСl ( СlO ), образуется при взаимодействии хлора с порошкообразным гидроксидом кальция — пушенкой :
Под действием углекислого газа, содержащегося в воздухе, она разлагается с выделением хлора:
Хлорная известь применяется как отбеливающее и дезинфицирующее
Хлористая кислота НСlO2 образуется при действии концентрированной серной кислоты на хлориты щелочных металлов, которые получаются как промежуточные продукты при электролизе растворов хлоридов щелочных металлов в отсутствие диафрагмы между катодным и анодным пространствами. Это слабая, неустойчивая кислота, очень сильный окислитель в кислой среде. При взаимодействии ее с соляной кислотой выделяется хлор:
Хлориты натрия используются для получения диоксида хлора, при обеззараживании воды, а также как отбеливаюший агент.
Хлорноватая кислота НСlO3 образуется при действии на ее соли —
х л о р а т ы — серной кислоты. Это очень неустойчивая кислота, очень сильный окислитель. Может существовать только в разбавленных растворах. При упаривании раствора НСlO3 при низкой температуре в вакууме можно получить вязкий раствор, содержащий около 40 % хлорной кислоты. При более высоком содержании кислоты раствор разлагается со взрывом. Разложение со взрывом происходит и при меньшей концентрации в присутствии восстановителей. В разбавленных растворах хлорная кислота проявляет окислительные свойства, причем реакции протекают вполне спокойно:
Соли хлорноватой кислоты — хлораты — образуются при электролизе растворов хлоридов в отсутствие диафрагмы между катодным и анодным пространствами, а также при растворении хлора в горячем растворе щелочей, как показано выше. Образующийся при электролизе хлорат калия (бертолетова соль) слабо растворяется в воде и в виде белого осадка легко отделяется от других солей. Как и кислота, хлораты — довольно сильные окислители:
Хлораты применяются для производства взрывчатых веществ, а также получения кислорода в лабораторных условиях и солей хпорной —кислоты — п е р х л о р а т о в. При нагревании бертолетовой соли в присутствии диоксида марганца МпО2, играющего роль катализатора, выделяется кислород. Если же нагревать хлорат калия без катализатора, то он разлагается с образованием калиевых солей хлороводородной и хлорной кислот:
При обработке перхлоратов концентрированной серной кислотой можно получить хлорную кислоту :
Это самая сильная кислота. Она наиболее устойчива из всех кислород содержащих кислот хлора, однако безводная кислота при нагревании, встряхивании или контакте с восстановителями может разлагаться со взрывом. Разбавленные растворы хлорной кислоты вполне устойчивы и безопасны в работе. Хлораты калия, рубидия, цезия, аммония и большинства органических оснований плохо растворяются в воде.
В промышленности перхлорат калия получают электролитическим окислением бертолетовой соли:
В органических растворителях бром растворяется значительно лучше.
Подобно хлору бром взаимодействует с металлами и неметаллами:
2 Al + 3 Вr2 = 2 AlBr3 (бромид алюминия)
Н2 + Вr2 = 2 НВr ( бромоводород )
2 Р + 3 Br2 = 2 РВr3 (бромид фосфора (III))
Все реакции брома протекают менее энергично, чем хлора. Менее энергично реагирует бром и с водой. При растворении в воде реагирует только часть брома, образуя бромоводородную и бромноватистую кислоты:
При растворении брома в растворе щелочи на холоду образуются соли
Вr2 + 2 NаОН = NaBr + NаВrО + Н2О
С предельными и непредельными углеводородами бром также реагирует менее энергично, чем хлор:
Бром, как и хлор, является окислителем. Так, он легко окисляет сернистую кислоту до серной:
Если к раствору сероводорода прибавить бромную воду, то красно-бурая окраска исчезает и раствор мутнеет вследствие выделения серы:
2 КМnO4 + 16 НВr = 2 КВr + 2 МnВr2 + 5 Вr2 + 8 Н2О
В промышленности бром получают действием хлора на различные бромиды:
Химические свойства бромводорода и его водного раствора — бромоводородной кислоты — аналогичны свойствам хлороводорода и соляной кислоты с той лишь разницей, что бромоводородная кислота является более сильной кислотой, а бромоводород — более сильным восстановителем.
Бромводород легко присоединяется по месту двойной или тройной связи непредельных углеводородов, образуя бромпроизводные соответствующих органических соединений:
Из-за легкой окисляемости бромводорода его нельзя получить действием концентрированной серной кислоты на бромиды щелочных металлов при нагревании, так как серная кислота окисляет бромиды
до свободного брома:
Свободный от брома бромоводород получают взаимодействием трибромида фосфора с водой:
Бромоводородная кислота используется для получения бромидов различных металлов, особенно бромида серебра, который используется в производстве светочувствительных кинофотоматериалов.
Кислородные соединения брома аналогичны кислородным соединениям хлора, но кислоты являются более слабыми электролитами и более слабыми окислителями. Кроме бромата калия КВrО3, который применяется в аналитической химии и лабораторной практике, они практического значения не имеют.
Иод был открыт французским химиком-селитроваром Б. Куртуа в 1811 г.
При нагревании иод взаимодействует c фосфором:
2 Р+ 3I2 = 2 РI3 ( иодид фосфора (III))
В присутствии воды, играющей роль катализатора, иод интенсивно, почти со взрывом, реагирует с алюминием:
2 Аl + 3I2 = 2 АlI3 ( иодид алюминия)
С водой иод почти не реагирует, а со щелочью реагирует аналогично
При взаимодействии иода с тиосульфатом образуется не сульфат, как
в случае с хлором или бромом, а тетратионат :
2 FеC3 + 2 НI = 2 FeCl2 + I2 + 2 НСl
В промышленности иод получают действием хлора на иодиды :
Иодоводородная кислота — очень сильный восстановитель, поэтому окисляется даже кислородом воздуха, вследствие чего раствор ее окрашивается в бурый цвет:
На свету окисление проходит более энергично, чем в темноте, поэтому растворы иодоводородной кислоты хранят в темной стеклянной посуде.
Большинство солей иодоводородной кислоты — и о д и д о в —хорошо растворимо в воде. Нерастворимыми солями иодоводородной
Иодоводород получают действием воды на фосфортрииодид :
Получить Иодоводород действием серной кислоты на иодиды щелочных металлов невозможно, так как почти весь иодид окисляется концентрированной серной кислотой до свободного иода :
Иодоводородная кислота применяется только в лабораторной практике.
Кислородные соединения иода аналогичны кислородным соединениям брома. Слабые кислоты НIO, НIO3 и НIO4 являются также слабыми окислителями. Они находят применение только в лабораторной практике.
В свободном состоянии фтор впервые получен французским химиком А. Муассаном в 1886 г.
Неметаллы в порошкообразном состоянии реагируют со фтором очень энергично, а в компактном — значительно труднее. Углерод в виде сажи сгорает в атмосфере фтора мгновенно, а графит реагирует со фтором только при высокой температуре. С кислородом и азотом фтор непосредственно не взаимодействует.
Так как в состав стекла входит значительное количество диоксида кремния, плавиковая кислота разъедает стекло, поэтому хранить ее можно в посуде, изготовленной из полимерных материалов (полиэтилена, фторопласта или эбонита), или в стеклянной, покрытой изнутри слоем парафина.
Фтороводород применяется для получения фторорганических соединений, в производстве фторопластов, металлургии редких металлов, а также как травильный агент при обработке поверхности некоторых металлов.
Получают фтороводород действием концентрированной серной кислоты на плавиковый шпат СаF2:
Фтороводород образуется также как побочный продукт при переработке апатитов,
Кислородсодержащих кислот фтор не образует, хотя соединения фтора с кислородом известны.
Марганец впервые получили К. В. Шееле и Ю. Ган в 1774 г.
При взаимодействии металлического марганца а различными неметаллами образуются соединения марганца (II):
Мn + С2 = МпСl2 (хлорид марганца (II))
Мn + S = МnS ( cулъфид марганца 3 Мn + 2 Р = Мn3Р2 (фосфид марганца (II)) 2 Мn + N2 = Мn2Si (силицид марганца (II)) Марганец легко растворяется в кислотах-неокислителях с выделением водорода: Он растворяется также в воде в присутствии соединений, дающих при гидролизе кислую реакцию: Растворение марганца в кислотах-окислителях сопровождается выделением продуктов восстановления этих кислот: Марганец может восстанавливать многие оксиды металлов и по этому используется в металлургии: 5 Мn + Nb2О5 = 5 MnО + 2 Nb 3 Мn + Fе2О3 = 3 МnО + 2 Fе Для получения ферромарганца, используемого в металлургии, смесь железной руды и пиролюзита восстанавливают коксом в электропечах: Монооксид марганца МnО — это порошок зеленовато-серого цвета, обладающий основными свойствами и поэтому реагируюший с кислотами и кислотными оксидами: В воде монооксид марганца практически нерастворим. Гидроксид марганца (II) Мn (ОН)2 — белое вещество, которое легко окисляется на воздухе до бурого гидроксида марганца (IV): Образуется гидроксид марганца (II) при взаимодействии его солей со щелочами: Гидроксид марганца (II) обладает основными свойствами. Он реагирует с кислотами и кислотными оксидами: Гидроксид марганца (II) обладает восстановительными свойствами. В присутствии сильных окислителей он может окисляться до перманганата: 2 Мп (ОН)2 + 5 КВгО + 2 КОН = 2 КМnO4 + 5 КВг + 3 Н2О При недостаточном количестве окислителя образуется диоксид марганца: Большинство солей марганца (II) хорошо растворимо в воде. В сухом виде их кристаллогидраты окрашены в слабо-розовый цвет. Нерастворимыми солями марганца (II) являются карбонат МnСО3, сульфид МnS и фосфат Мn3(РО4)2. При действии сильных окислителей в кислой среде марганец (II) в зависимости от количества окислителя может переходить в МnО2, или перманганат: При более высокой температуре разложение диоксида сопровождается образованием оксида Мn3O4. Соединения марганца (III) практического значения не имеют, Диоксид марганца МnО2 или оксид марганца (IV), вещество темно — серого цвета. При нагревании на воздухе до 530 ‘С диоксид марганца разлагается, выделяя кислород, как показано выше. В вакууме или в присутствии восстановителя эта реакция протекает значительно интенсивнее. При кипячении диоксида марганца с концентрированной азотной кислотой образуется соль марганца (II) и выделяется кислород: Диоксид марганца в кислой среде проявляет окислительные свойства: При сплавили оксида марганца (IV) со щелочами без доступа воздуха образуется манганит, или манганат (IV): В присутствии кислорода воздуха, игравшего роль окислителя, при сплавлении образуется соль манганата (VI): Манганат калия К2МnO4 самопроизвольно разлагается на перманганат калия и диоксид марганца: Перманганат калия КМnO4 широко применяется в лабораторной практике, промышленности, медицине и быту. Он является очень сильным окислителем. В зависимости от среды марганец в присутствии восстановителя может восстанавливаться до различной степени окисления. В кислой среде он всегда восстанавливается до Мn (II): Аналогично ведут себя манганат калия К2МnО4 и диоксид марганца. В щелочной среде перманганат калия восстанавливается до манганата : В нейтральной или слабощелочной среде перманганат калия восстанавливается до диоксида марганца: Последняя реакция используется в аналитической химии при количественном определении марганца. Раньше перманганат калия получали окислением либо диоксида марганца, либо манганата калия. Диоксид марганца окисляли селитрой при сплавлении со щелочью: Образовавшийся манганат калия в растворе самопроизвольно распадался на перманганат калия и диоксид марганца: По второму способу манганат калия окисляли хлором: В настоящее время перманганат калия получают электролитическим окислением манганата : Перманганат калия широко применяется как в промышленности, так и в лабораторной практике. Его используют для отбелки хлопка, шерсти, прядильных волокон, осветления масел и окисления различных органических веществ. В лабораторной практике он применяется для получения хлора и кислорода: 2 КМnO4 + 16 НСl = 2 КСl + 2 МnСl2 + 5 Cl2 + 8 Н2О