Что означает в кардиологии мпп
Пролапс клапанов сердца
Пролапс клапанов сердца – это заболевание, сопровождающееся нарушением работы клапана, находящегося между желудочком и левым предсердием и являющееся распространённой и относительно неопасной аномалией, во время которой при сокращении сердца проявляется неестественное выпячивание створок клапана.
Клапаном сердца называют состоящие из отдельных элементов подвижные заслонки, перекрывающие отверстия для циркуляции крови из одного отдела сердца в другой. Работа клапанов состоит в том, чтобы управлять кровяными потоками. В сердце размещены четыре клапана – митральный, трёхстворчатый, аортальный и лёгочный, которые пропускают кровь в одном направлении и не дают ей возможность возвращаться обратно. При сокращении сердечной мышцы создаётся давление, и кровь выбрасывается из сердца, а клапаны, регулирующие в этом направлении движение крови в момент сокращения мышцы – раскрываются. После сокращения мышцы давление в сердце падает, клапан закрывается, и кровь не может вернуться в сердце. Среди прочих видов пролапса чаще всего встречается пролапс митрального клапана, причиной которого является врождённая слабость соединительной ткани, из которой состоят сердечные клапаны.
Чем опасен пролапс клапана и его виды
В основном пролапс клапанов сердца не выражается никакими симптомами, и выявляется случайно, при обследовании по другим поводам. Но некоторые пациенты могут ощущать в области сердца боли с вегетативными проявлениями (особенно женщины), головокружение, обмороки и предобморочное состояние, повышенную утомляемость, учащённое сердцебиение и перебои в работе сердца, чувство неполного вздоха и одышку, необоснованное чувство тревоги, частые кровотечения из носа, а также незначительное повышение температуры тела. Причиной этим проявлениям является плохое свёртывания крови, которое вызвано нарушением строения волокон соединительной ткани.
Пролапс клапанов сердца обычно имеет благоприятное течение и имеющий эту патологию человек, как правило, не нуждается в специальном лечении. Но всё же не следует относиться к пролапсу клапана сердца как к безобидному заболеванию. В некоторых случаях грубые формы пролапса могут вызвать серьёзные осложнения в работе сердца – повышенную аритмию (способную стать причиной внезапной смерти), тромбоэмболию и инфекционный эндокардит. При возникновении перечисленных осложнений необходимо срочное медикаментозное лечение или хирургическое вмешательство.
Пролапс клапанов сердца различают двух видов – первичный и вторичный.
Первичный пролапс является врождённым и нередко передаётся по наследству. Он обусловлен генетическим дефектом строения соединительной ткани створок клапана и сухожильных хорд и называется миксоматозной дегенерацией. У людей с патологией врождённого пролапса зачастую проявляются такие признаки: длинное худое лицо, при высоком росте длинные руки и ноги, тонкая и эластичная кожа, гипермобильность (слишком подвижные суставы), косоглазие при плохом зрении. Но тем не менее, врождённый пролапс не вызывает значительного нарушения циркуляции крови и лечения по этому поводу не требуется.
Вторичный пролапс клапанов сердца носит приобретённый характер. Он возникает при инфаркте миокарда, ревматизме, в результате травмы грудной клетки и других причинах. Во вторичном пролапсе провисания створок клапана может вызвать разрыв сухожильных хорд или воспаление.
Ограничения после операции по пролапсу клапана сердца
Послеоперационный период проходит от двух до трёх дней в отделении интенсивной терапии. Затем, в зависимости от состояния здоровья пациента до операции, больной может провести в стационаре от двух недель до нескольких месяцев. После выписки он должен некоторое время находиться под диспансерным наблюдением кардиолога, пройти иммуномодулирующую и антибактериальную терапию, а также курсы седативной и общеукрепляющей терапии. Лечащий врач назначает пациенту программу физических упражнений и специальное питание, так как послеоперационный период включает в себя некоторые ограничения в еде. Например, нежелательно употреблять продукты, увеличивающие нагрузку на сердце – острую, солёную и жирную пищу, напитки, содержащие кофеин, а также следует избегать запоров, которые негативно влияют на работу сердечной мышцы. В этом помогут сырые фрукты, овощи, и продукты, насыщенные клетчаткой (творог, сметана, сыр, хлеб из муки грубого помола). В крайнем случае, можно воспользоваться глицериновыми свечами или другими соответствующими препаратами.
Очень важно выполнять рекомендации доктора, так как они способствуют скорейшему выздоровлению и возврату к привычной деятельности – работе, домашним хлопотам, вождению автомобиля и другим обязанностям.
Дефект межпредсердной перегородки
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «18» апреля 2019 года
Протокол №62
Дефект межпредсердной перегородки – сообщение (отверстие в межпредсердной перегородке) между левым и правым предсердиями, допускающее патологическое шунтирование крови между этими двумя камерами сердца.
Название протокола: Дефект межпредсердной перегородки
Код (-ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| Q21.1 | Врожденный дефект предсердной перегородки |
Дата разработки/пересмотра протокола: 2013 год (пересмотр 2018 г.)
Сокращения, используемые в протоколе:
| АлТ | – | аланинаминотрансфераза |
| АсТ | – | аспартатаминотрансфераза |
| ВПС | – | врожденные пороки сердца |
| ДКХО | – | детское кардиохирургическое отделение |
| ДМПП | – | дефект межпредсердной перегородки |
| ИК | – | искусственное кровообращение |
| ИФА | – | иммуноферментный анализ |
| КоА | – | коарктация аорты |
| КТ | – | компьютерная томография |
| НРС | — | нарушение ритма сердца |
| ОАП | – | открытый артериальный проток |
| РЧА | – | радиочастотная аблация |
| СМЭКГ | – | суточное мониторирование электрокардиограммы |
| ССС | – | сердечно-сосудистая система |
| ТАДЛВ | – | тотальный аномальный дренаж легочных вен |
| ЦМВ | – | цитомегаловирус |
| ЭКГ | – | электрокардиограмма |
| ЭКС | электрокардиостимулятор | |
| ЭхоКГ | – | эхокардиография |
Пользователи протокола: кардиохирурги, кардиологи, детские кардиологи, интервенционные кардиологи, неонатологи, педиатры.
Категория пациентов: дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортных или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты, которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
| Классы рекомендаций | Определение | Предлагаемая формулировка |
| Класс I | Данные и/или всеобщее согласие, что конкретный метод лечения или вмешательство полезны, эффективны, имеют преимущества. | Рекомендуется / показан |
| Класс II | Противоречивые данные и/или расхождение мнений о пользе/эффективности конкретного метода лечения или процедуры. | |
| Класс IIa | Большинство данных/мнений говорит о пользе/ эффективности. | Целесообразно применять |
| Класс IIb | Данные/мнения не столь убедительно говорят о пользе/эффективности. | Можно применять |
| Класс III | Данные и/или всеобщее согласие, что конкретный метод лечения или вмешательство не являются полезной или эффективной, а в некоторых случаях могут приносить вред. | Не рекомендуется |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез: может протекать бессимптомно, утомляемость, симптомы сердечной недостаточности, одышка при физической нагрузке, частые респираторные заболевания.
Физикальное обследование:
Внешний осмотр: Усиленный правожелудочковый сердечный толчок.
Аускультация: Постоянное расщепление II тона во II м.р. слева от грудины независимо от фаз дыхания. Слабый или средней интенсивности систолический шум относительного стеноза клапана ЛА во II м.р. слева от грудины. Нежный мезодиастолический шум относительного стеноза трехстворчатого клапана вдоль левого края грудины в нижней трети (при значительном по объему лево-правом сбросе).
Диагностический алгоритм
Перечень основных диагностических мероприятий при госпитализации (пациент):
Лабораторные исследования:
Что означает в кардиологии мпп
АМПП — аневризма межпредсердной перегородки
ДИ — доверительный интервал
ЛП — левое предсердие
МПП — межпредсердная перегородка
ООО — открытое овальное окно
ПП — правое предсердие
ТТ ЭхоКГ — трансторакальная эхокардиография
ЧП ЭхоКГ — чреспищеводная эхокардиография
Аневризма межпредсердной перегородки (АМПП) — первичная аномалия развития межпредсердной перегородки (МПП) с вовлечением в аневризматическое выпячивание части или всей МПП вследствие избытка ткани. Наиболее часто АМПП формируется в «слабых» местах МПП — в области овального окна или в проекции спонтанного закрытия дефекта МПП [1, 2]. В качестве фактора, провоцирующего формирование АМПП, рассматривается разница в межпредсердном давлении. Вторичная АММП этиологически обусловлена заболеваниями, вызывающими повышение давления в правом предсердии (ПП) или левом предсердии (ЛП).
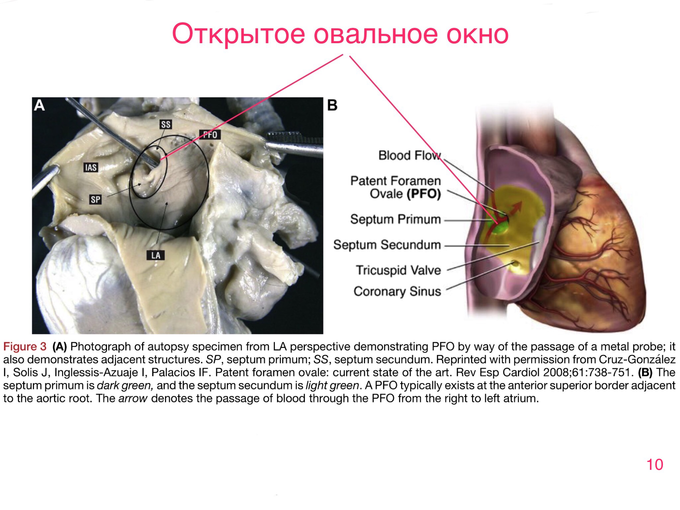
В антенатальном периоде МПП формируется по мере развития плода из 3 разных структур: 1) первичной перегородки (septum primum), локализующейся в нижней части предсердия и формирующей клапан для отверстия в области овальной ямки; 2) вторичной перегородки (septum secundum), располагающейся в верхней части предсердия; 3) остатков правого рога венозного синуса (зона от верхней до нижней полой вены). Гистологическое строение МПП неоднородно: в верхней части она представлена преимущественно миокардом, который ближе к краю овального окна сменяется фиброзной тканью [3]. Нижний край и клапан овального окна представлены тонкой тканью с отдельными волокнами кардиомиоцитов, слоями коллагена и эластических волокон. В отсутствие патологии соединительной ткани такое строение позволяет МПП сохранять контрактильность и способность сопротивляться растяжению [4, 5].
Сведения о распространенности АМПП значительно варьируют в зависимости от группы выборки и метода обследования. В общей популяции при аутопсии АМПП встречается в 1% случаев, возрастая при скрининговой трансторакальной (ТТ ЭхоКГ) и чреспищеводной (ЧП ЭхоКГ) эхокардиографии до 4,9% и даже 10% [6—8].
Один из дискутабельных вопросов, влияющих на мнение о распространенности и клиническом значении АМПП, — в каком качестве рассматривать варианты АМПП с одним или несколькими небольшими дефектами, которые не соответствуют принципам эмбрионального развития овального окна и сопровождаются шунтированием крови [9]. Частота выявления таких вариантов достигает 70% всех случаев АМПП. С анатомических позиций определение АМПП и дефекта МПП диаметрально противоположные. АМПП ассоциирована с избытком ткани, а дефект — с недостатком. Наиболее адаптированным представляется мнение, согласно которому к истинной АМПП следует относить только те случаи, которые не сопровождаются фенестрацией. Остальные варианты рассматривают как сочетание АМПП с малыми дефектами МПП, так как в этой ситуации клиническое значение АМПП, как и при изолированном дефекте МПП, функционирующем овальном окне, определяется не только ее размерами, но и объемом сброса через фенестрации, а также гемодинамическими нарушениями, которые вызывают этот сброс.
Существенный вклад в разброс данных о распространенности АМПП внесла эволюция взглядов на количественные критерии межпредсердной аневризмы, представления о которых формировались на протяжении десятилетий. Отсутствие единого подхода привело к широкой вариабельности мнений с уменьшением специфичности диагностики АМПП при использовании более «мягких» количественных критериев, характеризующих экскурсию аневризмы и величину ее основания.
До последнего времени наиболее часто применялись предложенные M. Silver и J. Dorsey (1978 г.) [1] критерии, которые долгое время считались «золотым стандартом» диагностики АМПП — максимальная экскурсия аневризматического выпячивания в ПП или ЛП, или суммарная экскурсия — более 10 мм, длина основания — более 15 мм [10—13]. На рисунке представлена схема измерения количественных характеристик АМПП при ЭхоКГ.

В последующих работах основные параметры АМПП варьировали как в сторону увеличения, так и уменьшения [13—16]. В одном из последних проспективных исследований [17], в котором использовались приведенные выше критерии, экскурсия АМПП варьировала от 10 до 40 мм (среднее значение 14 мм), основания — от 15 до 30 мм (среднее 20 мм). АМПП диагностирована у 370 (2,42%) из 15 232 обследованных.
В рекомендациях 2015 г. по эхокардиографической диагностике дефекта МПП и открытого овального окна (ООО) [18] диаметр основания аневризмы не упоминается в качестве критерия. Диагностировать АМПП предложено при максимальной экскурсии части или всей МПП в сторону ЛП или ПП более 10 мм или суммарно (общий размер экскурсии в ПП и ЛП) более 15 мм. В случаях с меньшей экскурсии применяют термин «мобильная МПП» [19].
Направление и глубина движения аневризмы в периоды кардиоцикла легли в основу классификации АМПП. Первые классификации включали 3 типа межпредсердных аневризм [20]. В 1989 г. R. Roudant и соавт. [21] определили первый тип аневризмы при локализации аневризматического выпячивания только в области овальной ямки, второй — в области овальной ямки с вовлечением задней части МПП, третий — с вовлечением всей МПП. Первый и второй типы ассоциированы с выбуханием аневризмы только в ПП, третий — только в ЛП. В 1991 г. А. Pearson и соавт. [10] описали дополнительный тип — 1С. В четырех случаях ТТ ЭхоКГ наблюдали преимущественное движение АМПП в ПП, но с экскурсией в ЛП в период ранней систолы или при выполнении пробы Вальсальвы. В классификации, которую широко используют в настоящее время, выделено 5 типов АМПП (табл. 1) [22].

В зависимости от частичного или полного вовлечения в аневризматическое выпячивание МПП предлагают также выделять локальный и генерализованный типы АМПП соответственно [17].
Визуализация АМПП хорошо обеспечивается при выполнении стандартной ЭхоКГ. Эхокардиографические сечения для визуализации АМПП при ТТ ЭхоКГ аналогичны тем, которые используют для оценки МПП: левая парастернальная позиция по короткой оси, апикальная и субкостальная четырехкамерные позиции. ЧП ЭхоКГ обладает большей чувствительностью в распознавании АМПП, а также позволяет выявить состояния, которые часто сочетаются с АМПП и не всегда хорошо визуализируются при ТТ ЭхоКГ (ООО, вторичный дефект МПП). Вместе с тем при ЧП ЭхоКГ увеличивается риск получения ложноположительных результатов диагностики АМПП, как при ТТ ЭхоКГ — ложноотрицательных.
В стандартный протокол эхокардиографического исследования целесообразно включать параметры, указанные в табл. 2.

АМПП может выступать в качестве изолированной внутрипредсердной аномалии и в сочетании с другими структурными аномалиями сердца. Наиболее часто АМПП встречается с внутри- и межпредсердными морфологическими аномалиями — ООО, сеть Киари, удлиненный евстахиев клапан [23—25]. При использовании только ТТ-ЭхоКГ частота выявления сочетания АМПП и ООО снижается ввиду гиподиагностики ООО при ТТ ЭхоКГ без выполнения ЧП ЭхоКГ [26].
В литературе имеются многочисленные данные о взаимосвязи АМПП и ПМК [27—31]. Однако во Фрамингемском исследовании при использовании современных критериев ПМК эта взаимосвязь не подтверждена [32]. Тем не менее для определенных подгрупп, в частности молодых пациентов, перенесших инсульт при нормальных коронарных артериях, указанная зависимость оказалась значимой [16]. В исследовании РЕПЛИКА, в котором группу обследования также составили лица молодого возраста, получены аналогичные результаты для сочетания аневризматичной или мобильной МПП с ПМК, базальными и/или множественными ложными хордами [26].
Значение фенестрации АМПП обсуждено выше. Следует еще раз подчеркнуть, что при малых шунтирующих сбросах только ЧП ЭхоКГ с контрастированием и пробой Вальсальвы является достаточно информативной.
В большинстве случаев клинически АМПП протекает благоприятно, без гемодинамических изменений и клинической манифестации. При аускультации АМПП может быть предположена по наличию щелчков вдоль левого края грудины, аналогичных таковым при пролапсе митрального клапана. Имеются данные о связи АМПП с предсердными нарушениями ритма, изменениями зубца Р на ЭКГ [15]. Блокада правой ножки пучка Гиса встречается в 21,9% случаев [33]. У детей с АМПП имеется предрасположенность к развитию наджелудочковых аритмий, синдрома слабости синусного узла [2].
Активно исследуется роль АМПП в развитии криптогенного инсульта [12, 34]. Связь АМПП с первичными криптогенными инсультами продемонстрировал метаанализ исследований J. Overell и соавт. [35]. Доказано существенное повышение риска развития инсультов при наличии АМПП и ООО. Причем соотношение рисков в подгрупповом анализе для лиц моложе 55 лет даже больше при изолированной АМПП — 6,14 (при 95% доверительном интервале — ДИ от 2,47 до 15,22), чем при изолированном ООО — 3,1 (при 95% ДИ от 2,29 до 4,21), увеличиваясь при сочетании АМПП и ООО до 15,59 (при 95% ДИ от 2,83 до 85,87).
По данным исследования European/PFO-ASA, включившем 581 пациента, перенесшего криптогенный инсульт, вероятность повторного инсульта при ООО составила 2,3%, при сочетании АМПП и ООО — 15,2%, несмотря на прием 300 мг аспирина [36]. В целом АМПП наряду с мобильной МПП и размерами ООО явились, по данным многофакторного анализа J. Lee и соавт. [37], независимыми предикторами повторного инсульта при ООО.
Взаимосвязь АМПП с ООО и риском развития инсульта может быть обусловлена несколькими факторами. Прежде всего при значительных размерах аневризмы и избыточных ее амплитудных характеристиках создаются предпосылки для тромбоэмболических осложнений [16]. Наличие патологически подвижной МПП также является существенным фактором риска развития ООО и парадоксальной эмболии [33]. В частности, подвижная аневризма МПП может способствовать более широкому открытию ООО и тем самым парадоксальной эмболии. Кроме того, мобильная АМПП может вести к ухудшению систолической функции ЛП и к обусловленному этим замедлению кровотока спонтанным контрастированием, что повышает риск тромбообразования в ЛП [38]. Однако чаще мобильная МПП не имеет самостоятельного значения и описывается как ассоциированное состояние при прогрессивном повышении давления в полости ЛП или ПП, при наличии сброса через нее, предсердных аритмиях.
В целом АМПП, как и ООО, может быть отнесена к факторам низкого, а при определенных условиях, к средней степени риска развития мозгового инсульта/кардиоэмболии головного мозга [39].
Связь АМПП с мигренью рассматривается только в контексте ее ассоциированности с функционирующим ООО в силу патогенетических особенностей возникновения мигрени с аурой при праволевом шунтировании (потенциальной возможностью попадания вазоактивных субстанций через межпредсердную коммуникацию в мозговой кровоток) [40].
Медикаментозная (атиагрегантная) терапия пациентам с изолированной АМПП без наличия ООО не показана. При транскатетерном закрытии ООО, сочетающегося с АМПП, отмечено значительное снижение амплитуды ее колебаний и снижение вероятности повторных эмболических эпизодов [41]. Вместе с тем АМПП ассоциирована с большей частотой резидуальных шунтов после чрескожного закрытия ООО, даже при использовании окклюдеров максимального диаметра [42].
Заключение
Аневризма МПП является первичной аномалией развития МПП, а при наличии фенестраций может рассматриваться как вариант межпредсердных коммуникаций наряду с ООО и ДМПП.
Инструментальная диагностика АМПП должна включать стандартную ТТ ЭхоКГ, дополненную при необходимости ЧП-ЭхоКГ. В диагностике и при определении типа аневризмы следует придерживаться современных рекомендаций, что позволит унифицировать результаты научных исследований в этой области.
Выявление АМПП подразумевает обязательный поиск прочих внутрипредсердных структурных аномалий с учетом данных о существенном повышении риска развития инсульта при сочетание АМПП с ООО. У пациентов, перенесших криптогенный инсульт, требуется целенаправленный поиск АМПП, особенно при развитии инсульта в молодом возрасте.
Последующие научные изыскания должны быть направлены на дальнейшее уточнение стратификации риска при АМПП и при ее сочетании с прочими вариантами внутрисердечных структурных аномалий, целесообразности первичной и вторичной профилактики кардиоэмболического инсульта.
Авторы заявляют об отсутствии конфликта интересов.
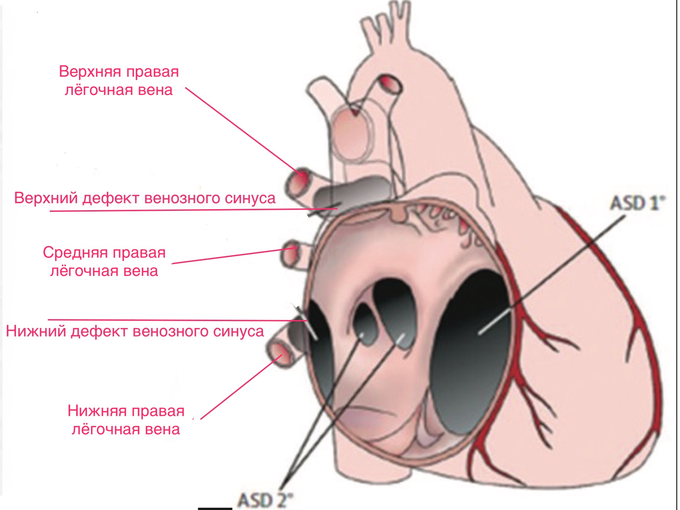
Дефекты межпредсердной перегородки.
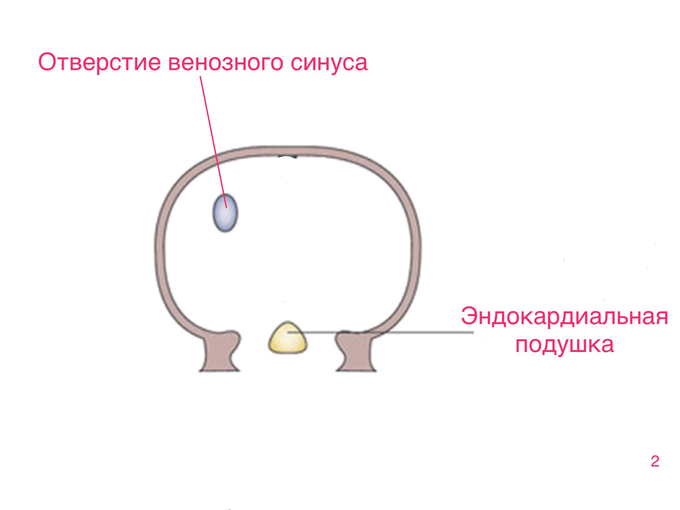
До 5-й недели эмбрионального развития, предсердия представляют собой одну общую камеру (скриншот 2)
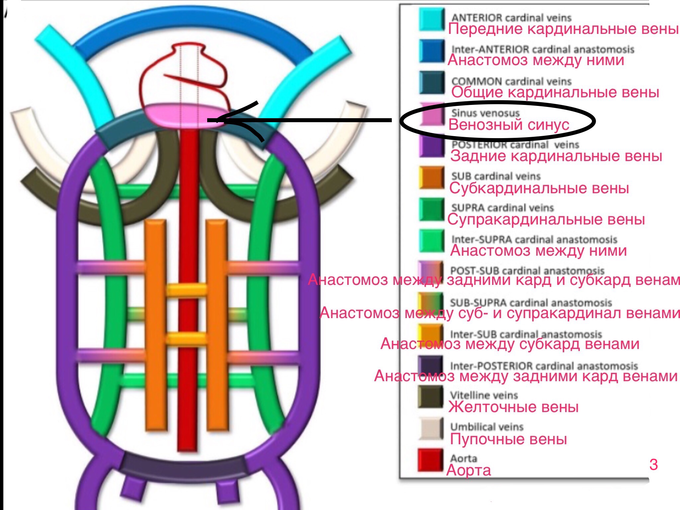
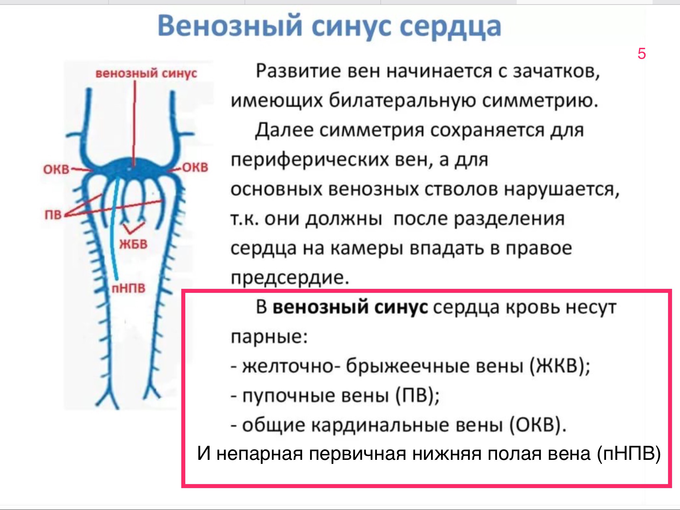
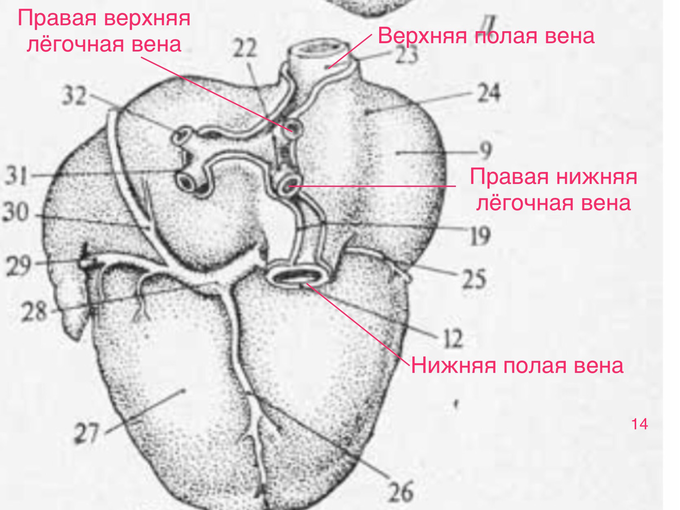
Венозный синус мы уже видели в предыдущих шпаргалках (скриншот 3)
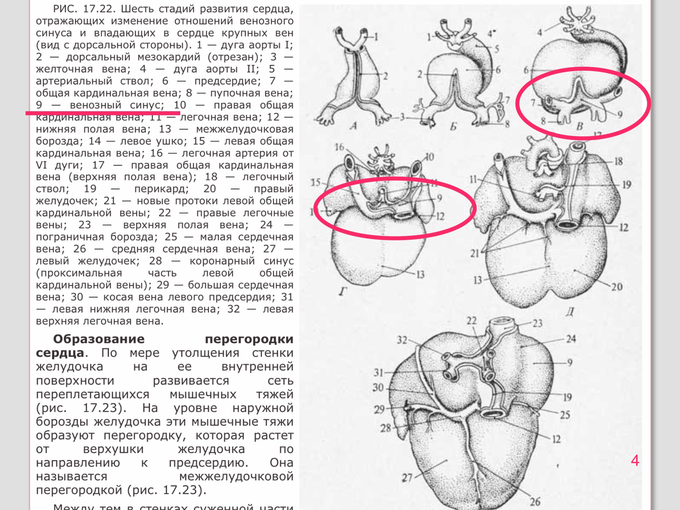
Посмотрим ещё раз (скриншот 4)
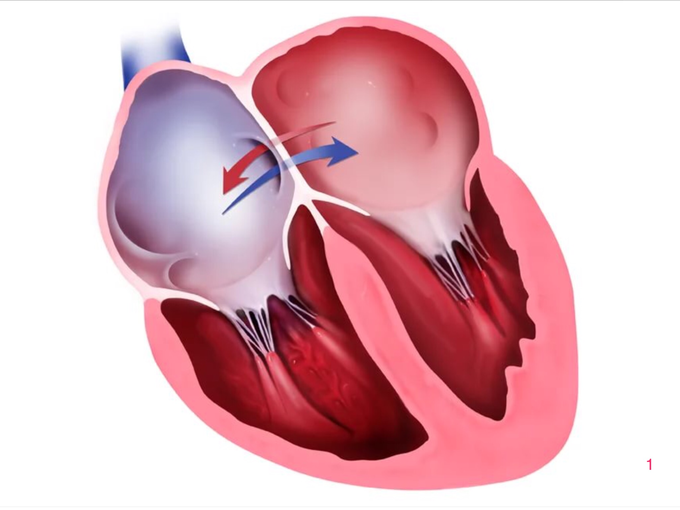
В дальнейшем, венозный синус абсорбируется (включается) в стенку правого предсердия, и вены, ранее впадавшие в него, теперь открываются непосредственно в правое предсердие. (Венозный синус нам ещё пригодится, при изучении некоторых аномалий сердца).
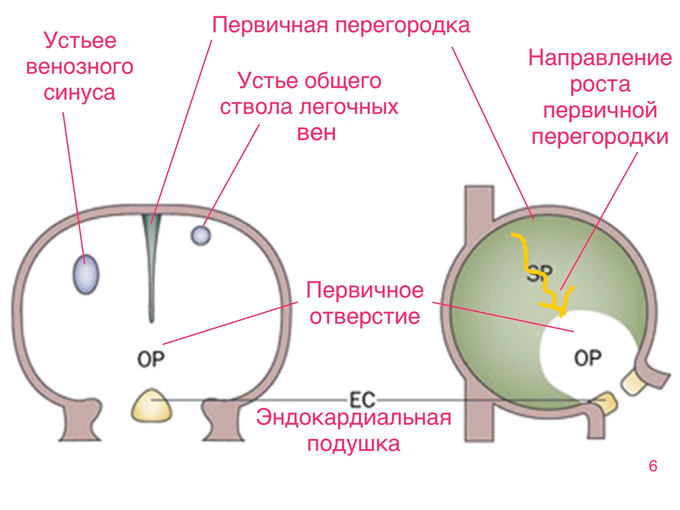
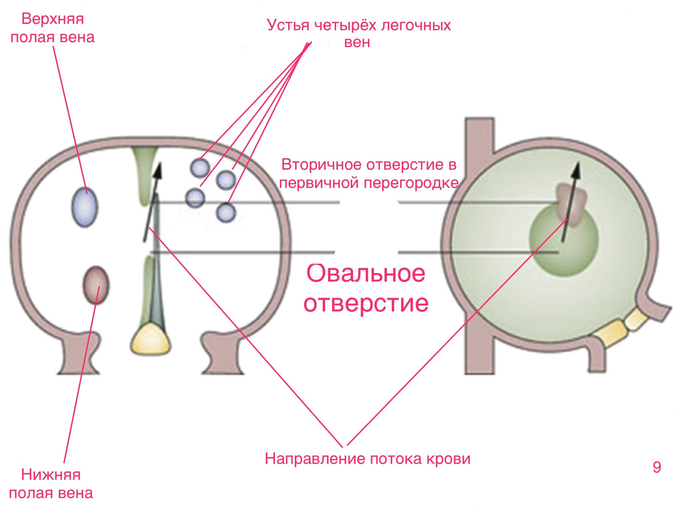
Начиная с 5-й недели, от краниальной стенки предсердной полости, в сторону эндокардиальных подушек, начинает расти первичная межпредсердная перегородка (скриншот 6)
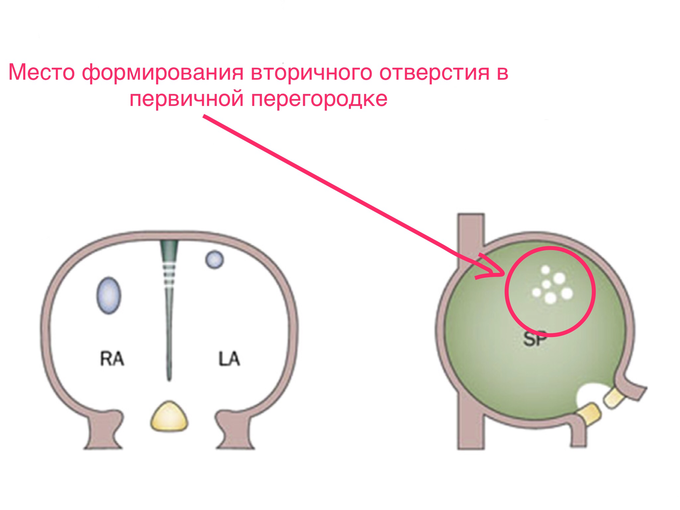
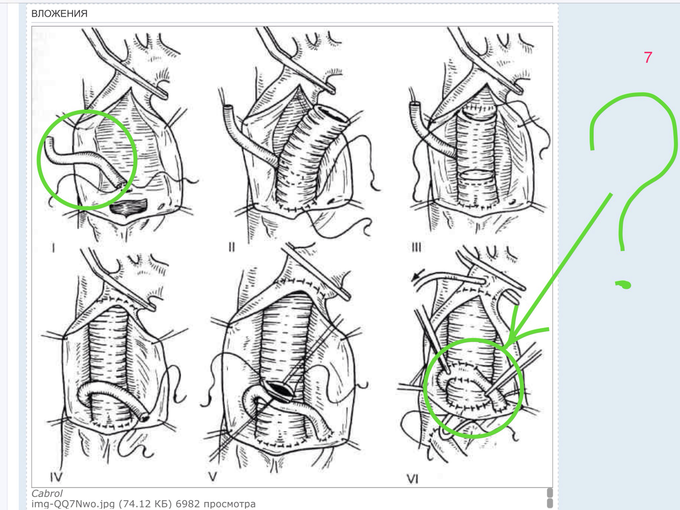
Непосредственно перед слиянием первичной перегородки с эндокардиальными подушками, в ней образуется новое отверстие. Это отверстие появляется сначала в виде множества мелких отверстий, возникающих в результате гибели клеток в этой области (скриншот 7)
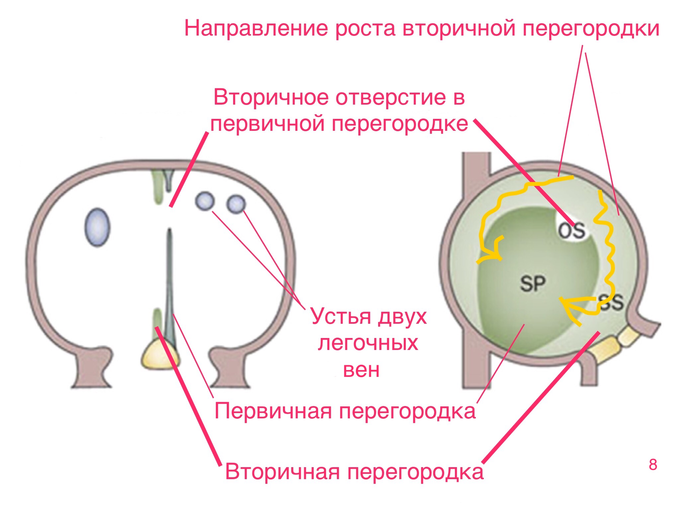
Мелкие отверстия быстро расширяются и, объединившись, образуют единое отверстие, известное как вторичное межпредсердное отверстие, которое становится единственным связующим проходом между предсердиями. После образования вторичного отверстия в первичной межпредсердной перегородке, рядом с ней появляется вторичная межпредсердная перегородка, которая имеет полулунную форму и растёт от периферии к центру (скриншот 8)
В процессе роста, края вторичной перегородки концентрически сближаются, но не срастаются полностью, а образуют овальное отверстие (скриншот 9)
Остатки первичной перегородки, прилегающие к овальному отверстию, служат клапаном, который пропускает кровь из правого предсердия в левое, но препятствует её обратному забросу.
В динамике, процесс образования овального отверстия выглядит так (скриншот 11)
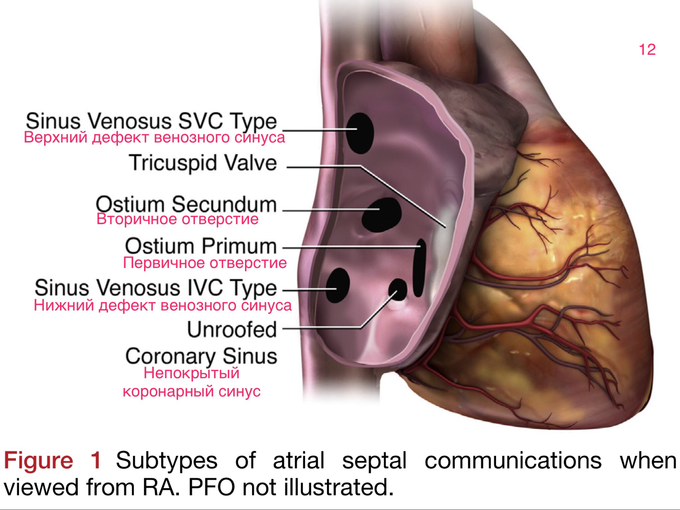
При нарушении этого алгоритма развития возникают дефекты межпредсердной перегородки. Их немного. Они представлены на рисунке (скриншот 12)
и в классификации (скриншот 13)
На УЗИ, дефект межпредсердной перегородки выглядит так ( скриншот 16)
Или так (скриншот 17)
Или так (скриншот 18)
Или так (скриншот 21)
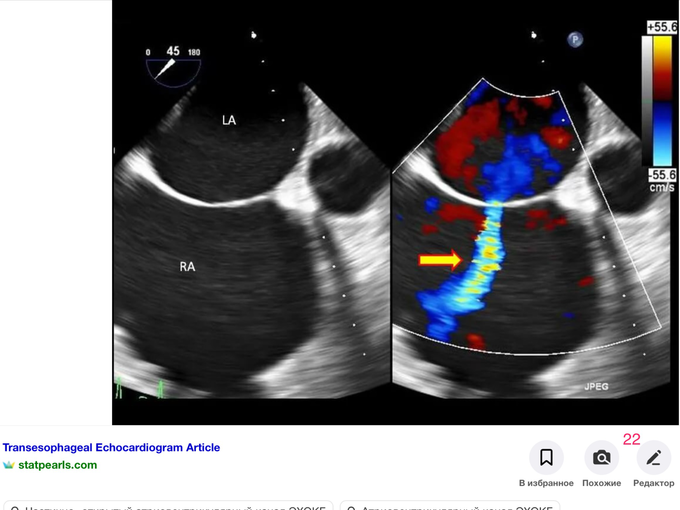
Или так (скриншот 22)
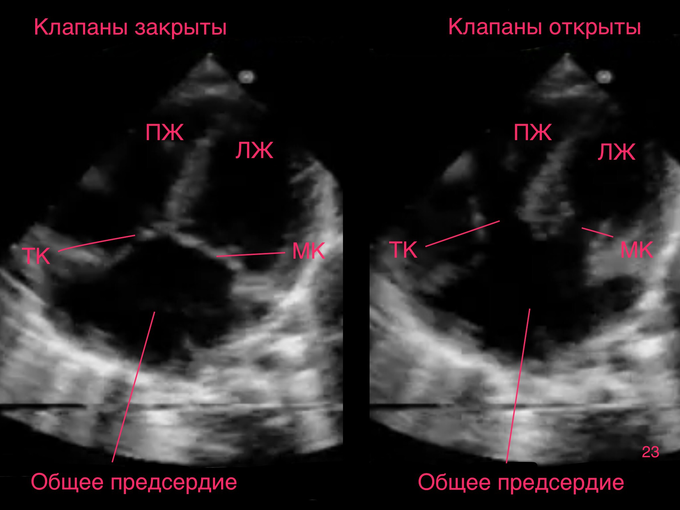
Общее предсердие (это когда межпредсердная перегородка совсем отсутствует) выглядит так (скриншот 23)
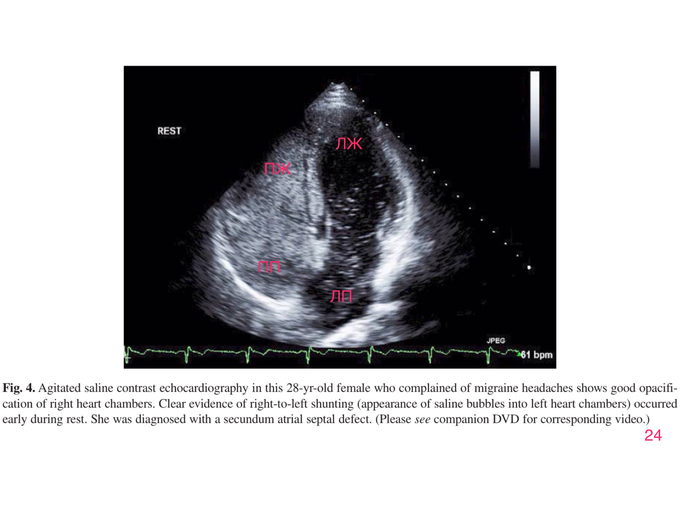
Диагностировать ДМПП помогает контрастная ЭхоКГ ажитированным (взболтанным) физраствором. Если пузыри появляются в левом предсердии, значит, в МПП есть отверстие. (Скриншот 24)
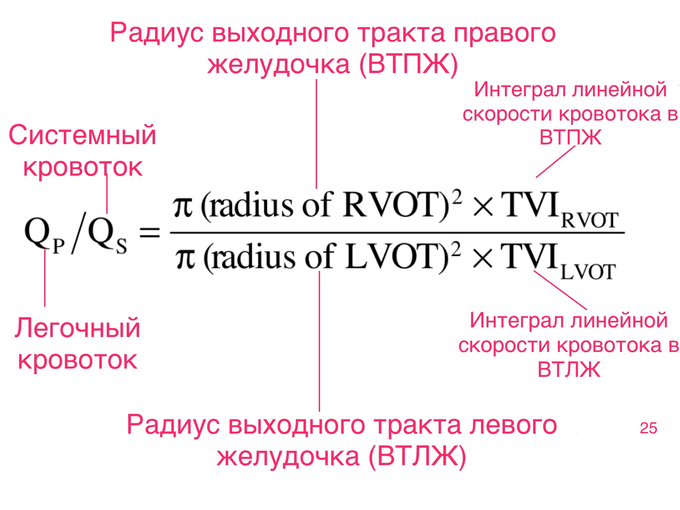
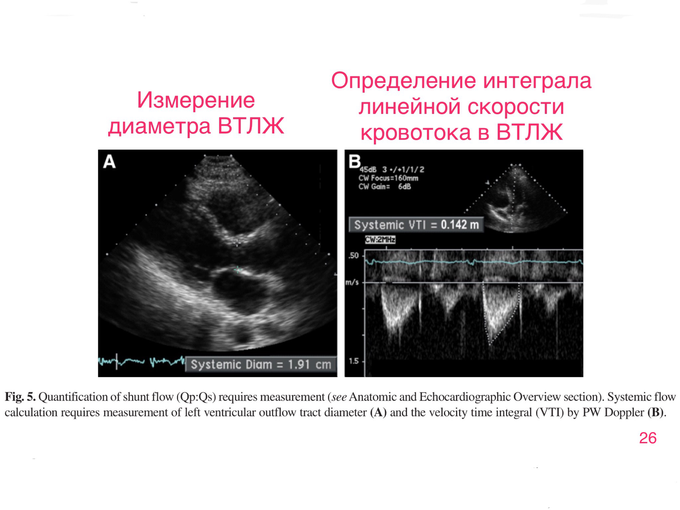
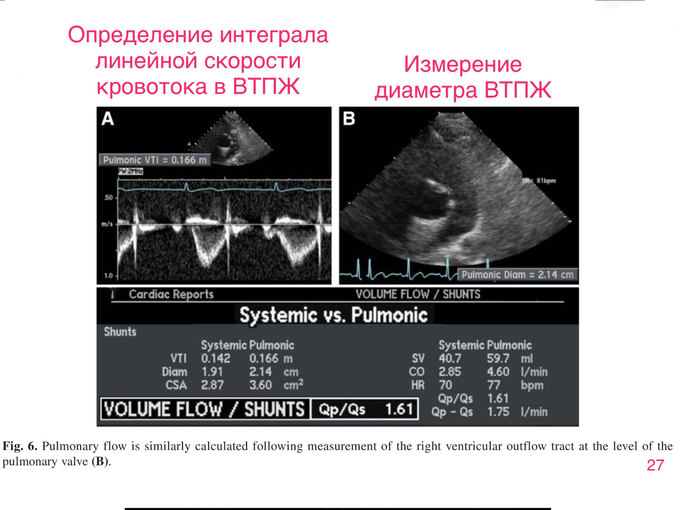
С практической точки зрения, важно иметь представление о гемодинамической значимости ДМПП. Величину сброса крови через дефект МПП можно определить по соотношению объемных скоростей кровотока в малом и большом кругах кровообращения. Это соотношение можно вычислить по формуле (скриншот 25)
Интеграл линейной скорости кровотока машина считает автоматически, в режиме импульсного допплера (если, конечно, такая функция имеется в её опциях).
Напоминаю, что в тексте могут самопроизвольно возникать искажения, а иллюстрации, из разных постов, могут самопроизвольно меняться местами. Модераторы объясняют это техническим несовершенством сайта. В любом случае, я буду стараться исправлять искажения, по мере их выявления.