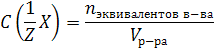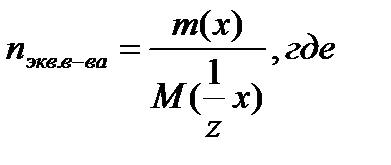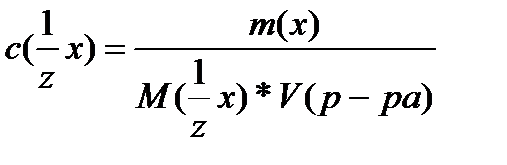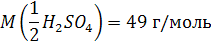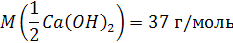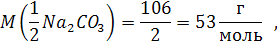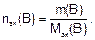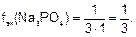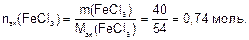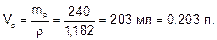Что показывает молярная концентрация эквивалента
Молярная концентрация эквивалента (нормальная концентрация)
Молярная концентрация эквивалента C(1/Z Х) (или н-нормальность) – это число молей эквивалентов растворенного вещества, содержащееся в 1 л раствора:
m(x) – масса растворенного вещества, г;
M(1/z x) – молярная масса эквивалента вещества, г/моль;
n экв. в-ва – количество вещества эквивалентов, моль.
Молярную концентрацию эквивалента вещества можно рассчитать по формуле:
Раствор называется однонормальным или нормальным, если в 1 л его содержится 1 моль эквивалентов растворенного вещества.
При определении количества вещества, необходимого для приготовления раствора той или иной нормальности, необходимо знать правила определения эквивалентов.
Молярная массам эквивалента кислоты равна ее молярной массе, деленной на основнойсть кислоты.
Так для соляной кислоты масса эквивалента равна ее молярной массе. Для двухосновной серной кислоты масса эквивалента равна 49 г (98 : 2)
Молярная масса эквивалента основания равна его молярной массе, деленной на кислотность основания (валентность металла или число гидроксидных групп).
Например, молярная масса эквивалента гидроксида калия равна его молярной массе, а масса эквивалента гидроксида кальция Ca(OH)2 будет равна 74:2 = 37 г.
Для солей масса эквивалента равна молярной массе соли, деленной на произведение степени окисления металла и числа его атомов в молекуле соли.
Так масса эквивалента карбоната натрия равна 106 : (1 * 2) = 53 г.
а масса эквивалента Al2(SO4)3 равна 342 : 6(3 * 2) = 57 г/моль
Молярная концентрация эквивалента(нормальная или эквивалентная концентрация)
Молярная концентрация эквивалента (нормальность) показывает, какое количество моль эквивалентов растворенного вещества содержится в 1 л раствора.
Молярную концентрацию эквивалента Сэк(В) находят как отношение количества эквивалентов вещества nэк(В) к объему раствора Vp
Размерность молярной концентрации эквивалента: моль•л. Сокращенная форма записи единицы молярной концентрации эквивалента – н. моль•л. Например, 2н. означает, что в 1 л раствора содержится 2 моль эквивалента растворенного вещества.
Зная массу растворенного вещества m(B) и его молярную массу эквивалента Мэк(В), можно найти количество эквивалента вещества:
Молярная масса эквивалента вещества равна произведению фактора эквивалентности fэк(В) на молярную массу вещества М(В)
Эквивалент – это реальная или условная частица вещества, соответствующая в реакциях обмена одному атому или иону водорода (Н или Н+), а в окислительно-восстановительных реакциях – одному электрону.
Фактор эквивалентности – число, показывающее, какую часть от реальной частицы (молекулы, атома, иона и т.д.) вещества составляет эквивалент этого вещества.
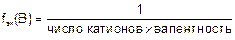
Например, для Na3PO4 заряд катиона Na+ равен 1, число катионов – 3, тогда
Пример. Вычислите молярную концентрацию эквивалента хлорида железа (III) в растворе, полученном при растворении 40 г FeCl3 в 200 мл воды. Плотность раствора 1,182 г/мл.
Молярная масса хлорида железа (III):
Фактор эквивалентности fэк = 1/3.
Молярная масса эквивалента
Mэк(FeCl3) = fэк(FeCl3)•M(FeCl3) = 162 • (1/3) = 54 г/моль.
Количество эквивалента вещества, содержащегося в 40 г хлорида железа (III), составляет:
r(H2O) = 1 г/мл; m(H2O) = 200 • 1 = 200 г;
mp = 40 + 200 = 240 г.
Объем раствора:
Находим молярную концентрацию эквивалента раствора хлорида железа (III):
Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Молярная концентрация эквивалента



Эквивалент – есть 1/z часть частицы (молекулы, атома).
У окислителей и восстановителей Z будет равно числу принятых или отданных электронов. Например, для процесса: Mn +7 + 5e à Mn +2 Z * = 5. От молекулы КMnO4 только 1/5 часть будет эквивалентной одному электрону.
Обратная величина числу эквивалентов (Z) – это фактор эквивалентности – f. Он и показывает, какая часть от реальной частицы эквивалентна иону или атому водорода, или одному электрону (в ОВР).
Он принимает дробные значения: 1/2, 1/3, 1/4 и т.д.
Для оснований и амфотерных гидроксидов в форме оснований число эквивалентов Z равно числу гидроксид-анионов. Например, Z(KOH) = 1;
Z (Са(OH)2) = 2 (без учета протекания реакций или до средних или до основных солей)
Для кислот Z равно числу атомов водорода, то есть, основности кислоты. Например, Z (HCl) = 1. Z (H3PO4 ) = 3
У солей Z равно произведению валентности (степени окисления) металла на число атомов металла. Например, Z(CaCl2) = (+2) · 1 = 2; Z (Al2(SO4)3) = 3·2 = 6.
У окислителей и восстановителей Z будет равно числу принятых или отданных электронов.
Например:
и наоборот:
Рассмотрим значения Z и f для многоосновных кислот и многокислотных оснований не в процессе окислительно-восстановительных реакций, а в процессе протекания реакций обмена:
Таким образом, f (Н2SO4,) = ½ в данном уравнении. Заметим, что по рассуждениям соответствия NaOH и H OH f (NaOH) всегда будет равен 1 (как и KOH, HCl, LiOH, HNO3, т.е. однокислотных оснований и одноосновных кислот). В аналитической химии говорят, что растворы KOH, HCl, LiOH, HNO3, NaOH готовят с учетом реальных частиц (Z = 1 и f =1), т.е. 1 моль (или одной молекулы), а не какой – то части.
Рассмотрим другой случай:
Расчет фактора эквивалентности в уравнениях реакций через коэффициент стехиометричности смотри в приложении.
II. Величины более мелких частиц («дробленых»), выраженные как количество вещества называются количеством вещества эквивалента:
где: ν – обычное количество вещества Х
Z – число эквивалентов вещества Х
ν1/Z (Х) – количество вещества эквивалентов для вещества (Х)
Дано 6 моль серной кислоты: 6 H2SO4 (это обычное количество вещества.) При Z =2 и f = ½ в каждом моль кислоты содержится уже 2 дробленых частицы, т.е., количества вещества эквивалентных частиц = 2. В 6 моль эквивалентных будет 12, в 2 раза больше.
Вывод: количество вещества эквивалента всегда больше обычного количества вещества в Z раз.
III. Молярная масса эквивалента. (M1/z).
Из данных формул видно, что вместо обычной молярной массы в них входит величина M1/z – молярная масса эквивалента (дробленой части одного моль) и, конечно, она будет меньше молярной массы в Z раз:
M1/z = или M1/z = М · f à M = M1/z · Z или M = Z f
Например: Если Z (H2SO4 ) = 2 или f = ½; М= 98 г/моль
Или M1/z = М · f = 98 г/моль · ½ = 49 г/моль
Этот расчет можно оформить в виде задачи:
Задача 13: Рассчитать молярную массу эквивалента H2SO4:
Решение:
Задача 14: Рассчитать количество вещества эквивалента для 2-х моль KMnO4
Дано: Решение:
ν (KMnO4) = 2 моль ν 1/Z = Z ·ν = 5 ·2 моль = 10 моль (-экв)
в) Молярная масса эквивалента: M 1/Z = (г/моль, кг/ моль) Z * x
IV. Молярная концентрация эквивалента. (С1/z).
Вспомним формулы обычной молярной концентрации:
Вывод: для одной и той же массы вещества или объема вещества молярная концентрация эквивалента (эквивалентных частиц) больше, чем молярная концентрация в Z раз.
Математически: это частное от деления количества вещества, содержащегося в системе к объему системы.
Задача16: В растворе объемом 7 литров содержится KMnO4 31,6 г. Рассчитать молярную концентрацию раствора и молярную концентрацию эквивалента.
1) Находим молярную концентрацию р-ра
2) Находим молярную концентрацию эквивалента:
Задача 17: В растворе объемом 5 л содержится серная кислота массой 98 г, молярная масса 98 г/моль Вычислить молярную концентрацию и молярную концентрацию эквивалента.
1 способ:
m (H2SO4) = 98 г 1) С = 0,2 моль/л
M = 98 г\моль M V 98г/моль·5 л Z = 2
2) С1/Z = С · Z = 0,2 моль\л. 2 = 0,4 моль /л
М 98 г/моль M1/z = 49 г/моль
Тогда
С1/z 0,4 моль/л С = 0.2 моль/л
Задача18: Рассчитать массу карбоната натрия для приготовления раствора объемом 50 мл с молярной концентрацией эквивалента 0,15 моль/л.
Массу обычно рассчитывают до 4-го знака после запятой.
Задача 19: Какой объем хлороводородной кислоты с массовой долей 38 % и плотностью 1,19 г\мл надо взять для приготовления раствора объемом 500 мл и молярной концентрацией эквивалента 2 моль\л
Для решения задачи разберем условие и увидим, что речь идет о двух растворах. Берут раствор кислоты с процентной концентрацией (массовой долей), неизвестного в задаче объема и из этого раствора готовят раствор с молярной концентрацией эквивалента. В задаче не говорят, как готовят раствор: добавлением воды или выпариванием определенного количества воды. Да нас это и не должно волновать. Главное мы должны увидеть, что связкой между растворами является неизменная масса чистого вещества хлороводорода. Массу чистого вещества хлороводорода можно вычислить из данных того раствора, которых достаточно для подстановки в формулу.
Для записи условия необходимо правильно и четко поставить индексы 1 и 2 для каждого из двух растворов:
Дано: Решение
W, % (HCl)1 = 38 % 1) Найдем массу HCl чист., содержащегося в
V ( HCl) р-ра2 = 500 мл 500 мл раствора HCl c молярной конц.
С1\Z ( HCl) р-ра2 = 2 моль/л эквивалента 2 моль/л, так как для этого
М HCl = 36,5 г/моль есть все данные
2 ) Рассчитаем, какова масса 38 % 1р-ра HCl, если масса HСlчист = 36,5г
1) Найдем объем 38%-го раствора HCl c массой 96,05 г
Выводы и указания для решения такого типа задач:
1. Помните что в формуле с использованием молярной концентрации или молярной концентрации эквивалента подразумевается объем с использованием размерности – литр [л]
2. В формуле перевода массы раствора в объем раствора через плотность используется размерность г/мл и в результате объем получаем в миллилитрах [мл].
3. Порядок логических рассуждений и прием запоминания:
а) Неизвестное ищем для раствора с W (массовой долей), поэтому сначала работаем с концентрацией «С1/z»; (ищем массу чистого вещества)
б) Затем работаем с формулой, включающей W (ищем массу необходимого раствора)
в) Переводим массу раствора в плотность по формуле с использованием «треугольника»:
— буква «С» находится по алфавиту раньше, чем W – работаем с формулой
— буква «W» находится в алфавите после «С» и затем работаем с ней;
— работаем с «треугольником».
Всего выполняем 3 действия в такой задаче. Однако, если необходимо, то переводим М в М1/z
V. Закон эквивалентов
Вещества взаимодействуют между собой в эквивалентных количествах:
Как следствие закона эквивалентов: концентрации реагирующих веществ обратно пропорциональны их объемам.
Задача 20: Определите молярную концентрацию эквивалента серной кислоты, 16 мл которой вступило в реакцию нейтрализации с 50 мл гидроксида натрия, молярная концентрация эквивалента которого 0,2 моль/л.
Задача 21: Сколько мл раствора гидроксида калия с концентрацией 0,2 моль/л потребуется для нейтрализации 20 мл раствора серной кислоты с концентрацией 0,1 моль/л.
2. В задачах 20 и 21 не нужно размерность «мл» переводить в «л».
Если в задаче такого типа используется одноосновная кислота, например, азотная или соляная, то С1/z = С.
Титр.
Титр – это масса растворенного вещества, содержащегося в 1 мл раствора.
Размерность такая же, как у плотности.
Если указано, что титр кислоты HCl с молярной концентрацией эквивалента 0,1 моль/л равен 0,00365 г/мл, то это означает, что в 1 мл данного раствора содержится 0,00365 г HCl титр вычисляют до 4-х значащих цифр после нулей. Зная титр, можно вычислить массу вещества в любом объеме раствора:
Титр можно вычислять: Т = (формула 2)
Так как m = С·М·V, то, подставив это значение в формулу 1 получим:
И далее, чтобы перевести «л» в «мл» необходимо дробь разделить на 1000.
Для записи значения титра сохраняются 4 значащих цифры.
Примеры записи:
Т = 0, 012801 = 0,01280 (после всех нулей – 4 значащих цифры)
Способы выражения концентрации
Существует множество способов измерить концентрацию раствора. Это так называемые способы выражения концентрации раствора.
Концентрация раствора — это количество вещества, находящегося в единице объема или массы раствора.
Что такое раствор
Среди окружающих нас веществ, лишь немногие представляют собой чистые вещества. Большинство являются смесями, состоящими из нескольких компонентов, которые могут находиться в одном или различных фазовых состояниях.
Смеси, имеющие однородный состав являются гомогенными, неоднородный состав – гетерогенными.
Иначе, гомогенные смеси, называют растворами, в которых одно вещество полностью растворяется в другом (растворителе). Растворитель – это тот компонент раствора, который при образовании раствора сохраняет свое фазовое состояние. Он обычно находится в наибольшем количестве.
Существуют растворы газовые, жидкие и твердые. Но более всего распространены жидкие растворы, поэтому, в данном разделе, именно на них мы сосредоточим свое внимание.
Концентрацию раствора можно охарактеризовать как:
Качественная концентрация характеризуется такими понятиями, как разбавленный и концентрированный раствор.
С этой точки зрения растворы можно классифицировать на:
Количественная концентрация выражается через молярную, нормальную (молярную концентрацию эквивалента), процентную, моляльную концентрации, титр и мольную долю.
Способы выражения концентрации растворов
Молярная концентрация растворов (молярность)
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным — растворено 0,01 моля вещества, миллимолярным — растворено 0,001 моля вещества.
Термин «молярная концентрация» распространяется на любой вид частиц.
Вместо обозначения единицы измерения — моль/л, возможно такое ее обозначение – М, например, 0,2 М HCl.
Молярная концентрация эквивалента или нормальная концентрация растворов (нормальность).
Понятие эквивалентности мы уже вводили. Напомним, что эквивалент – это условная частица, которая равноценна по химическому действию одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Например, эквивалент KMnO4 в окислительно – восстановительной реакции в кислой среде равен 1/5 (KMnO4).
Еще одно необходимое понятие — фактор эквивалентности – это число, обозначающее, какая доля условной частицы реагирует с 1 ионом водорода в данной кислотоно-основной реакции или с одним электроном в данной окислительно – восстановительной реакции.
Он может быть равен 1 или быть меньше 1. Фактор эквивалентности, например, для KMnO4 в окислительно – восстановительной реакции в кислой среде составляет fэкв(KMnO4) = 1/5.
Следующее понятие – молярная масса эквивалента вещества х. Это масса 1 моля эквивалента этого вещества, равная произведению фактора эквивалентности на молярную массу вещества х:
Молярная концентрация эквивалента (нормальность) определяется числом молярных масс эквивалентов на 1 литр раствора.
Для обозначения нормальной концентрации допускается сокращение «н» вместо «моль/л».
Процентная концентрация раствора или массовая доля
Массовая концентрация показывает сколько единиц массы растворенного вещества содержится в 100 единицах массы раствора.
Это отношение массы m(х) вещества x к общей массе m раствора или смеси веществ:
Массовую долю выражают в долях от единицы или процентах.
Моляльная концентрация раствора
Моляльная концентрация раствора b(x) показывает количество молей n растворенного вещества х в 1 кг. растворителя m. Единица измерения моляльной концентрации — моль/кг :
Титр раствора
Титр раствора показывает массу растворенного вещества х, содержащуюся в 1 мл. раствора. Единица измерения титра — г/мл:
Мольная или молярная доля
Мольная или молярная доля α(х) вещества х в растворе равна отношению количества данного вещества n(х) к общему количеству всех веществ, содержащихся в растворе Σn:
Между приведенными способами выражения концентраций существует взаимосвязь, которая позволяет, зная одну единицу измерения концентрации найти (пересчитать) ее в другие единицы. Существуют формулы, позволяющие провести такой пересчет, которые, в случае необходимости, вы сможете найти в сети. В разделе задач показано, как произвести такой пересчет, не зная формул.
Пример перевода процентной концентрации в молярную, нормальную концентрацию, моляльность, титр
Решение.
1. Рассчитать молярную массу FeSO4:
M (FeSO4) = 56+32+16·4 = 152 г/моль
2. Рассчитать молярную массу эквивалента:
Мэ = fэкв· М(FeSO4) = 1/2·152 = 76 г/моль
3. Найдем m раствора объемом 2 л
4. Найдем массу 2 % раствора по формуле:
m(FeSO4) = 0,02·2,06 = 0,0412 кг = 41,2 г
5. Найдем молярность, которая определяется как количество молей растворенного вещества в одном литре раствора:
n = m/М
n = 41,2/152 = 0,27 моль
См = n/V
См = 0,27/2 = 0,135 моль/л
6. Найдем нормальность:
nэ = 41,2/76 = 0,54 моль
Сн = 0,54/2 = 0,27 моль/л
7. Найдем моляльность раствора. Моляльная концентрация равна:
b (x) = n(x)/m
Масса растворителя, т.е. воды в растворе равна:
mH2O = 2,06-0,0412 = 2,02 кг
b (FeSO4) = n(FeSO4)/m = 0,27/2,02 = 0,13 моль/кг
8. Найдем титр раствора, который показывает какая масса вещества содержится в 1 мл раствора:
Т(х) = m (х)/V
Т(FeSO4) = m (FeSO4)/V = 41,2/2000 = 0,0021 г/мл