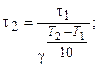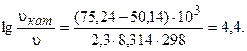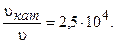Что показывает температурный коэффициент в химии
Правило Вант-Гоффа. Температурный коэффициент скорости реакции
Зависимость скорости реакции от температуры приближенно определяется эмпирическим правилом Вант-Гоффа: при изменении температуры на каждые 10 градусов скорость большинства реакций изменяется в 2-4 раза.
Математически правило Вант-Гоффа выражается так:
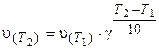
где v(T2) и v(T1) — скорости реакций, соответственно при температурах Т2 и T1 (T2> T1);
γ-температурный коэффициент скорости реакции.
Значение γ для эндотермической реакции выше, чем для экзотермической. Для многих реакций γ лежит в пределах 2-4.
Физический смысл величины γ заключается в том, что он показывает, во сколько раз изменяется скорость реакции при изменении температуры на каждые 10 градусов.
Поскольку скорость реакции и константа скорости химической реакции прямопропорциональны, то выражение (3.6) часто записывают в следующем виде:
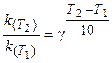
где k(T2), k(T1)- константы скорости реакции соответственно
при температурах T2 и T1;
Пример 8. На сколько градусов надо повысить температуру, что бы скорость реакции возросла в 27 раз? Температурный коэффициент реакции равен 3.
Решение. Используем выражение (3.6):
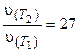
Получаем: 27 = 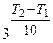
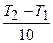
Ответ: на 30 градусов.
Скорость реакции и время, за которое она протекает, связаны обратно пропорциональной зависимостью: чем больше v, тем
меньше t. Математически это выражается соотношением

Пример 9. При температуре 293 К реакция протекает за 2 мин. За какое время будет протекать эта реакция при температуре 273 К, если γ = 2.
Решение. Из уравнения (3.8) следует:
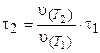
Используем уравнение (3.6), поскольку 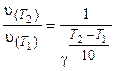
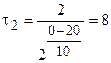
Правило Вант-Гоффа применимо для ограниченного числа химических реакций. Влияние температуры на скорость процес-сов чаще определяют по уравнению Аррениуса.
Уравнение Аррениуса. В 1889 г. шведский ученый С. Арре-1иус на основании экспериментов вывел уравнение, которое на-звано его именем

где k — константа скорости реакции;
k0 — предэксноненциальный множитель;
е — основание натурального логарифма;
Ea — постоянная, называемая энергией активации, определяемая природой реагентов:
R-универсальная газовая постоянная, равная 8,314 Дж/моль×К.
Значения Еa для химических реакций лежат в пределах 4 — 400 кДж/моль.
Многие реакции характеризуются определенным энергети-ческим барьером. Для его преодоления необходима энергия актации — некоторая избыточная энергия (по сравнению со вредней энергией молекул при данной температуре), которой должны обладать молекулы для того, чтобы их столкновение было эффективным, т. е. привело бы к образованию нового ве-щества. С ростом температуры число активных молекул быстро увеличивается, что и приводит к резкому возрастанию скорости реакции.
В общем случае, если температура реакции изменяется от Т1 до Т2, уравнение (3.9) после логарифмирования примет вид:
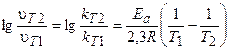
Это уравнение позволяет рассчитывать энергию активации реакции при изменении температуры от Т1 до Т2.
Скорость химических реакций возрастает в присутствии катализатора. Действие катализатора заключается в том, что он образует с реагентами неустойчивые промежуточные соединения (активированные комплексы), распад которых приводит к. образованию продуктов реакции. При этом энергия активации, понижается, и активными становятся молекулы, энергия которых была недостаточна для осуществления реакции в отсутствие, катализатора. В результате возрастает общее число активных£ молекул и увеличивается скорость реакции.
Изменение скорости реакции в присутствии катализатора выражается следующим уравнением:
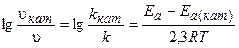
где vкат, и Ea(кат) — скорость и энергия активации химической реакции в присутствии катализатора;
v и Еа — скорость и энергия активации химической реакции без катализатора.
Пример 10. Энергия активации некоторой реакции в отсутствие катализатора равна 75,24 кДж/моль, с катализатором — 50,14 кДж/моль. Во сколько раз возрастает скорость реакции в присутствии катализатора, если реакция протекает при температуре 298 К? Решение. Воспользуемся уравнением (3.11). Подставляя в уравнение данные
Еа = 75,24 кДж / моль = 75,24 ×103 Дж / моль и
Еа(кат)=- 50,14 кД/моль= 50,14 ×103 Дж /моль, получим
Окончательно находим:
Таким образом, снижение энергии активации на 25,1 кДж/моль привело к увеличению скорости реакции в 25 000 раз.
Что показывает температурный коэффициент в химии
Ключевые слова конспекта: Скорость химической реакции. Факторы, влияющие на скорость реакции: природа реагирующих веществ, площадь их соприкосновения, температура, концентрация, катализатор. Катализ. Ферменты. Ингибиторы.
Скорость — это отношение изменения какой-либо величины к промежутку времени, за которое это изменение произошло. Химические реакции протекают с разными скоростями. Одни практически мгновенно, например смесь водорода с кислородом (гремучая смесь) взрывается за доли секунды. Быстро протекает реакция нейтрализации, т. е. взаимодействие растворов кислоты со щёлочью (основанием):
Другие реакции протекают значительно медленнее, например брожение глюкозы или коррозия металлов:
Что же понимается под скоростью химической реакции? Предположим, некоторое взаимодействие протекает по схеме А + В = АВ. В ходе реакции вещества А и В расходуются, превращаясь в новое вещество АВ. Изменение количества веществ, участвующих в химической реакции, характеризует такая величина, как концентрация.
| Концентрация — количество вещества в единице объёма; её измеряют в моль/л. |
В ходе реакции концентрация исходных веществ (реагентов) уменьшается, а концентрация продукта реакции увеличивается. Изменение концентраций во времени и характеризует скорость химической реакции.
| Скорость химической реакции — отношение изменения концентрации реагента ко времени, за которое это изменение произошло. |
Математически эту закономерность можно выразить следующей формулой:
Если в приведённой формуле С1 и С2 — это начальная и конечная концентрации одного из реагентов, то разность С2 – С1 имеет отрицательное значение, ведь С2 0.
Размерность скорости реакции легко определить: концентрация измеряется в моль/л, время — в секундах, следовательно, единицей скорости реакции является 1 моль/(л • с).
Управление скоростью химической реакции имеет большое значение. Увеличение скорости реакции позволяет получить больше продуктов реакций: стали, пластмасс, химических удобрений, лекарств, топлива и др. Замедление скорости реакции позволяет уменьшать потери металла от коррозии, дольше сохранять продукты питания и т. д.
Рассмотрим, какие факторы влияют на скорость химической реакции.
✅ 1. Природа (состав и строение) реагирующих веществ. Реакции между органическими веществами протекают медленнее подобных реакций между неорганическими веществами. По-разному взаимодействуют галогены с водородом: фтор — со взрывом, хлор — со взрывом лишь при нагревании, бром — без взрыва, а реакция водорода с йодом является эндотермической и протекает медленно. Интенсивность взаимодействия щелочных металлов с водой зависит от их восстановительных свойств, которые усиливаются с увеличением радиуса атома.
✅ 2. Температура. Зависимость скорости химической реакции от температуры была установлена в конце 1884 г. голландским учёным Якобом Хендриком Вант-Гоффом.
Математическое выражение правила Вант-Гоффа записывают следующим образом:
где υ2 — скорость реакции при температуре t2;
υ1 — скорость реакции при температуре t1;
t2 — конечная температура реакции;
t1 — начальная температура реакции,
γ (греческая буква «гамма») — температурный коэффициент реакции, который соответствует изменению скорости химической реакции (увеличивает или уменьшает её) при изменении температуры на 10 градусов.
Например, температурный коэффициент какой–либо реакции близок к 3. Это означает, что при повышении температуры на 20 °С скорость реакции возрастёт в 9 раз:
✅ 3. Площадь соприкосновения реагирующих веществ. Этот фактор учитывается для гетерогенных реакций. Напомним, что гетерогенными (от греч. heteros — другой) называются реакции, идущие между веществами разного агрегатного состояния, т. е. имеющими поверхность раздела. Например, на поверхности соприкосновения жидкости или газа с твёрдым веществом и т. д.
Понятно, что, чем больше площадь соприкосновения реагирующих веществ, тем выше скорость химической реакции. Чтобы увеличить её, в промышленности используют особый метод, который называется «кипящий слой». Твёрдое вещество измельчают до очень мелких частиц, через которые затем пропускают снизу второй реагент, как правило, в газообразном состоянии. При прохождении этого реагента через слой измельчённого вещества наблюдается эффект, напоминающий кипение. Метод «кипящего слоя» используется при производстве серной кислоты для обжига серного колчедана, при каталитическом крекинге нефтепродуктов.
✅ 4. Концентрация реагирующих веществ. Зависимость была установлена норвежскими учёными Като Максимилианом Гульдбергом и Петером Вааге в 1867 г. и получила название закона действующих масс.
| Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных их коэффициентам в уравнении реакции. |
Математическое выражение закона действующих масс для реакции aА + bВ = dD выглядит так:
где υ — скорость химической реакции, СА и СB — концентрации реагентов А и В, а и b — коэффициенты в уравнении реакции, k — коэффициент пропорциональности — константа скорости реакции, которая показывает скорость химической реакции при концентрации реагирующих веществ, равных 1 моль/л.
Например, для второй стадии производства азотной кислоты, которая описывается уравнением 2NO + O2 = 2NO2↑, закон действующих масс отражает формула υ = k • C 2 (NO) • С(O2)
Если в гетерогенной реакции принимает участие твёрдое вещество, его концентрация не входит в уравнение закона. Например, для реакции между раскалённым оксидом меди(II) и водородом СuО + Н2 = Сu + Н2O справедливо следующее выражение: υ = k • С(Н2)
Это означает, что внесение дополнительного количества твёрдого вещества (оксида меди(II)) не оказывает влияния на скорость реакции.
✅ 5. Катализатор. Напомним, что катализаторами (от греч. katalysis — разрушение) называются вещества, изменяющие скорость химической реакции и не входящие в состав продуктов реакции.
Современную химическую промышленность невозможно представить без использования катализаторов. С их помощью ускоряют химические процессы, чтобы быстрее получить нужные вещества и уничтожить вредные (например, химические отходы). Производство минеральных кислот, аммиака и метанола, уксусной кислоты и полимеров, нефтепереработка и производство лекарственных препаратов — около 90 % всех химических производств основано на применении катализаторов.
С помощью катализаторов удаётся повысить производительность химических процессов и уменьшить себестоимость продукции. Катализаторы также позволяют сделать производство экологически более безопасным, т. е. уменьшить загрязнение окружающей среды вредными выбросами.
Катализаторы вошли в жизнь человека, когда он стал использовать процессы брожения для получения уксуса из виноградного сока, варить сыр и выпекать хлеб. Ведь все эти процессы протекают в присутствии биологических катализаторов, или ферментов (от лат. fermentum — закваска). Их также называют энзимами.
Ферменты содержатся во всех живых клетках. Они направляют, регулируют и многократно ускоряют биологические процессы, играя тем самым важную роль в обмене веществ и энергии.
Область применения биологических катализаторов шире, чем неорганических: ежегодный рост их производства в мире составляет 15%, а неорганических — всего 3%. Ферменты «трудятся» в медицине, сельском хозяйстве, пищевой промышленности, защищают окружающую среду, помогают в быту. Например, использование стирального порошка с ферментами — залог успешной стирки. Зная, что ферменты имеют белковую природу и под действием высокой температуры способны денатурировать, вы понимаете, насколько важно следовать инструкции по применению таких порошков.
Обратное влияние на скорость химической реакции оказывают ингибиторы (от лат. inhibere — сдерживать, останавливать) — вещества, подавляющие или задерживающие течение физиологических и физико-химических (главным образом, ферментативных) процессов. Такие вещества важны, как и катализаторы: ингибиторы коррозии, например, помогают сохранить металлы от разрушения.
Конспект урока по химии «Скорость химических реакций». В учебных целях использованы цитаты из пособия «Химия. 11 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
Что показывает температурный коэффициент в химии
Температурный коэффициент сопротивления
Как вы могли заметить, значения удельных электрических сопротивлений в таблице из предыдущей статьи даны при температуре 20 ° Цельсия. Если вы предположили, что они могут измениться при изменении температуры, то оказались правы.
Зависимость сопротивления проводов от температуры, отличной от стандартной (составляющей обычно 20 градусов Цельсия), можно выразить через следующую формулу:
| Проводник | α, на градус Цельсия |
| Никель | 0,005866 |
| Железо | 0,005671 |
| Молибден | 0,004579 |
| Вольфрам | 0,004403 |
| Алюминий | 0,004308 |
| Медь | 0,004041 |
| Серебро | 0,003819 |
| Платина | 0,003729 |
| Золото | 0,003715 |
| Цинк | 0,003847 |
| Сталь (сплав) | 0,003 |
| Нихром (сплав) | 0,00017 |
| Нихром V (сплав) | 0,00013 |
| Манганин (сплав) | 0,000015 |
| Константан (сплав) | 0,000074 |
Давайте на примере нижеприведенной схемы посмотрим, как температура может повлиять на сопротивление проводов и ее функционирование в целом:
Общее сопротивление проводов этой схемы (провод 1 + провод 2) при стандартной температуре 20 ° С составляет 30 Ом. Проанализируем схему с помощью таблицы напряжений токов и сопротивлений:
При 20 ° С мы получаем 12,5 В на нагрузке, и в общей сложности 1,5 В (0,75 + 0,75) падения напряжения на сопротивлении проводов. Если температуру поднять до 35 ° С, то при помощи вышеприведенной формулы мы легко сможем рассчитать изменение сопротивления на каждом из проводов. Для медных проводов (α = 0,004041) это изменение составит:
Пересчитав значения таблицы, мы можем увидеть к каким последствиям привело изменение температуры:
Сравнив эти таблицы можно прийти к выводу, что напряжение на нагрузке при увеличении температуры снизилось (с 12,5 до 12,42 вольт), а падение напряжения на проводах увеличилось (с 0,75 до 0,79 вольт). Изменения на первый взгляд незначительны, но они могут быть существенны для протяженных линий электропередач, связывающих электростанции и подстанции, подстанции и потребителей.
Температурный коэффициент
содержание
Основы
20 ° C часто выбирают в качестве эталонной температуры.
В общем, любую температурную характеристику можно описать рядом Тейлора :
Аппроксимация получается полиномом Тейлора n-й степени:
Следует отметить, что температурные коэффициенты зависят от эталонной температуры.
Пример: температурные коэффициенты для идеального газа
При идеализирующих предположениях изменение давления и изменение объема линейны.
Пример: температурный коэффициент электрического сопротивления
Имеющиеся в продаже маломощные резисторы, значение сопротивления которых должно быть как можно более постоянным во всем диапазоне рабочих температур, обычно имеют температурные коэффициенты в диапазоне от 100 ppm на Кельвин до 200 ppm на Кельвин, прецизионные резисторы доступны в диапазон от 50 ppm на Кельвин до 1 ppm на Кельвин. В этом случае линейный температурный коэффициент указывается с префиксом TK (на английском языке с префиксом «TC» для температурного коэффициента ), например TK100 для сопротивления с 100 ppm на Кельвин.
Дальнейшие примеры
Помимо уже упомянутых общеизвестных температурных коэффициентов электрического сопротивления или объема или давления для идеальных газов, существует множество других температурных коэффициентов. Для определенного объекта температурная зависимость определенного размера обычно технически актуальна, поэтому этот объект или его использование просто упоминается как «один» (один) температурный коэффициент, и поэтому ясно, какой размер изменяется, примеры включают: