Что понимают под атомно кристаллической структурой
Атомно-кристаллическая структура металлов



Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Кристалл состоит из атомов (ионов), расположенных в определенном порядке, который периодически повторяется в трех измерениях.
В кристаллах существует не только ближний, но и дальний порядок размещения атомов, т. е. упорядоченное расположение частиц в кристалле сохраняется на больших участках кристаллов.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узлах которой располагаются атомы (ионы), образующие металл (твердое кристаллическое тело).
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической ячейки. 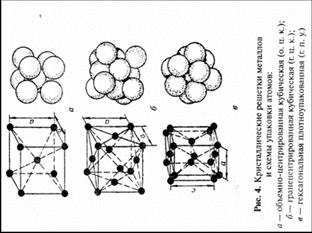
Подавляющее число технически важных металлов образуют одну из следующих решеток: кубическую объемно-центрированную, кубическую гранецентрированную и гексагональную (рис. 4).
В кубической объемно-центрированной решетке атомы расположены в узлах ячейки и один атом — в центре объема куба (рис. 4, а). Кубическую объемно-центрированную решетку имеют металлы: ое-железо, хром, ниобий, вольфрам, ванадий и др.
В кубической гранецентрированной решетке атомы расположены в углах куба и в центре каждой грани (рис. 4, б). Этот тип решетки имеют металлы: железо, никель, медь, золото и др.
В гексагональной решетке (рис. 4, в) атомы расположены в углах и центре шестигранных оснований призмы и три атома в средней плоскости призмы. Эту упаковку атомов имеют металлы: магний, цинк и др.
Некоторые металлы имеют тетрагональную решетку.
Размеры кристаллической решетки характеризуются величинами периодов, под которыми понимают расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку (рис. 4). Период решетки измеряется в ангстремах (А) (1А=1—8 см).
Период решетки металлов находится в пределах от 1 до 7 А.
Что понимают под атомно кристаллической структурой
Под атомно-кристаллической структурой понимают взаимное расположение атомов (ионов), существующее в реальном кристалле.
В твердом состоянии металл представляет собой постройку, состоящую из положительно заряженных ионов, омываемых «газом» из свободных коллективизированных электронов. Связь в металле осуществляется электростатическими силами. Между ионами и коллективизированными электронами проводимости возникают электростатические силы притяжения, которые стягивают ионы. Такая связь называется металлической.
Силы связи в металлах определяются силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстоянии один от другого, при котором энергия взаимодействия минимальна. Как видно из рис. 4, этому положению соответствует равновесное расстояние 


Рис. 4. Схема энергии взаимодействия двух атомов в зависимости от межатомного расстояния
Рис. 5. Схема кристаллической решетки
Поэтому в металле атомы располагаются закономерно, образуя правильную кристаллическую решетку, что соответствует минимальной энергии взаимодействия атомов.
Кристаллическая решетка (рис. 5) состоит из воображаемых линий и плоскостей, проходящих через точки расположения ионов в пространстве. Жирными линиями выведен наименьший параллелепипед, последовательным перемещением которого вдоль трех своих осей может быть построен весь кристалл.
Этот наименьший объем кристалла, дающий представление об атомной структуре металла в любом объеме, получил название элементарной кристаллической ячейки.
Для однозначной ее характеристики необходимо знать следующие величины: три ребра (а, b и с) и три угла между осями а, Р и у (см. рис. 5).
Большинство металлов образует одну из следующих высокосимметричных решеток с плотной упаковкой атомов: кубическую объемно центрированную, кубическую гранецентрированную и гексагональную (рис. 6).
Как видно из рис. 6, а, в кубической объемно центрированной решетке (ОЦК) атомы расположены в вершинах куба и один атом в центре объема куба. Кубическую объемно центрированную решетку имеют металлы: 
В кубической гранецентрированной решетке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани (рис. 6, б). Решетку такого типа имеют металлы: 
В гексагональной решетке (рис. 6, в) атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома — в средней плоскости призмы. Такую упаковку атомов имеют металлы: 
Расстояния 

Периоды решетки для большинства металлов находятся в пределах 
На одну элементарную ячейку объемно центрированной решетки приходятся два атома: один в центре куба и другой вносят атомы, располагающиеся в вершинах куба (каждый атом в вершине куба одновременно принадлежит восьми сопряженным элементарным ячейкам и на данную ячейку приходится лишь 1/8 массы этого атома, а на всю ячейку 1/8 X 8 = 1 атом).
На элементарную ячейку гранецентрированной кубической решетки приходятся четыре атома; из них один (по такому же
Рис. 7. Схема, показывающая число атомов, находящихся на равном и наименьшем расстоянии от данного атома А в разных кристаллических решетках (С. С. Штейнберг): а
расчету, как и для объемно центрированной кубической решетки) вносят атомы в вершинах куба, а три суммарно 
На элементарную ячейку гексагональной плотноупакованной решетки приходятся шесть атомов
Плотность кристаллической решетки — объема, занятого атомами, которые условно можно рассматривать как жесткие шары (см. рис. 6, а), характеризуется координационным числом, под которым понимают число атомов, находящихся на равном и наименьшем расстоянии от данного атома. Чем выше координационное число, тем больше плотность упаковки атомов.
В элементарной ячейке объемно центрированной кубической решетки наименьшее расстояние между атомами соответствует 

Для гранецентрированной кубической решетки координационное число равно 






Рис. 8. Индексы кристаллографических плоскостей (а-в) и направлений (г) в ОЦК решетке
от 1,633 (например, для цинка и кадмия), то координационное число гексагональной решетки соответствует 6.
Гранецентрированная кубическая и гексагональная плотно-упакованная 
При уменьшении координационного числа в гексагональной решетке с 12 до 6 коэффициент компактности составляет около 50 %, а при координационном числе 4 — всего около 25 %.
Половину наименьшего расстояния между атомами в их кристаллической решетке называют атомным радиусом. Атомный радиус возрастает при уменьшении координационного числа, так как при этом увеличивается пространство между атомами. Поэтому атомные радиусы разных металлов обычно приводятся к
Кристаллографические обозначения атомных плоскостей. Для определения положения атомных плоскостей (проходящих через атомы) в кристаллических пространственных решетках пользуются индексами 
Приведем примеры обозначения плоскостей. Установим первоначально индексы для плоскости куба. Каждая плоскость
куба (рис. 8, а) пересекает только одну ось, при этом отсекаемые отрезки будут равны 


В кубической решетке кроме плоскостей куба (рис. 8, а) различают плоскость октаэдра (111) (рис. 8, в) и плоскость ромбического додекаэдра (110) (рис. 8, б).
Следует иметь в виду, что индексы характеризуют не одну какую-либо плоскость, а целую группу параллельных плоскостей, и тогда их заключают в фигурные скобки.
Индексы направлений. Для определения индексов направлений расположения рядов атомов в кристаллической решетке необходимо из семейства параллельных плоскостей выбрать направление плоскостей, проходящих через начало координат. Далее, приняв за единицу длину ребра элементарной ячейки (или период решетки), определяют координаты любой точки этого направления. Полученные значения координат точки приводят к отношению трех наименьших чисел. Зги числа, заключенные в квадратные скобки 





Анизотропия свойств металлов. Нетрудно видеть, что плотность расположения атомов по различным плоскостям (так называемая ретикулярная плотность) неодинакова. Так, плоскости (100) в ОЦК решетке принадлежит лишь один атом 


Вследствие неодинаковой плотности атомов в различных плоскостях и направлениях решетки свойства (химические, физические, механические) каждого монокристалла зависят от направления вырезки образца по отношению к направлениям в решетке. Подобная неодинаковость свойств монокристалла в разных
кристаллографических направлениях называется анизотропией.
Кристалл — тело анизотропное в отличие от аморфных тел (стекло, пластмассы и др.), свойства которых не зависят от направления.
Технические металлы являются поликристаллами, т. е. состоят из большого числа анизотропных кристаллитов. В большинстве случаев кристаллиты статистически неупорядоченно ориентированы по отношению друг к другу; поэтому во всех направлениях свойства более или менее одинаковы, т. е. поликристаллическое тело является псевдоизотропным. Такая мнимая изотропность металла не будет наблюдаться, если кристаллиты имеют одинаковую преимущественную ориентацию в каких-то направлениях. Эта ориентированность, или текстура, создается в известной степени, но не полностью (например, в результате значительной холодной деформации); в этом случае поликристаллический металл приобретает анизотропию свойств.
Лекция по дисциплине Металловедение на тему «Атомно-кристаллическое строение металлов»
Министерство образования и науки Украины
Донбасский государственный технический университет
по дисциплине Металловедение
«Атомно-кристаллическое строение металлов»
«Атомно-кристаллическое строение металлов»
1. Строение металлов в твердом состоянии
Все металлы и металлические сплавы – тела кристаллические, атомы (ионы) расположены в металле закономерно в отличие от аморфных тел, в которых атомы расположены хаотично.
Металлическое состояние возникает в комплексе атомов, когда при их сближении внешние электроны теряют связь с отдельными атомами, становятся общими, т. е. коллективизируются и свободно перемещаются между положительно заряженными и периодически расположенными ионами.
Устойчивость металла определяется электрическим притяжением между положительно заряженными ионами и обобщенными электронами (такое взаимодействие получило название металлической связи).
Сила связи в металлах определяется силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстоянии друг от друга, чтобы энергия взаимодействия была минимальной (рис. 1)
Рисунок 1. Энергетические условия взаимодействия атомов в кристаллической решетке вещества
Величина а соответствует расстояние между атомами в кристаллической решетке, а а0 соответствует равновесному расстоянию между атомами. В связи с этим в металле атомы располагаются закономерно, образуя правильную кристаллическую решетку, что соответствует минимальной энергии взаимодействия атомов.
Металлические состояния характеризуются высокой энергией связи между атомами. Мерой ее служит теплота сублимации (сумма энергии необходимой для перехода твердого металла к парообразному состоянию, для металла – от 20 до 200 ккал/(г·атом)).
2. Атомно-кристаллическое строение металлов
Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Атомы в кристалле расположены в определенном порядке, который периодически повторяется в трех измерениях.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узле которой располагаются атомы (ионы), образующие металл.
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической ячейки (решетки).
Для характеристики элементарной ячейки задают шесть величин: три ребра ячейки a, b, c и три угла между ними б, в, г. Эти величины называют параметрами кристаллической решетки.
Кристаллические решетки бывают простыми (атомы только в вершинах решетки) и сложными.
Металлы образуют одну из следующих высокосимметричных сложных решеток с плотной упаковкой атомов: кубическую объемноцентрированную (ОЦК), кубическую гранецентрированную (ГЦК) и гексагональную (ГПУ) (рис. 2).
ОЦК: Rb, K, Na, Li, Tiв, Tlв, Zrв, Ta, W, V, Feб, Cr, Nb, Ba, и др.
ГЦК: Cu, Al, Pt, Pb, Ni, Ag, Au, Pd, Rh, Ir, Feг, Coб, Caб, Ce, Srб, Th, Sc и др.
ГПУ: Mg, Cd, Re, Os, Ru, Zn, Be, Coв, Caб, Zrб, Laб, Tiб и др.
Рисунок 2. Кристаллические решетки металлов и схемы упаковки атомов
Расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку, называют периодом решетки, измеряется в нанометрах (1нм = 10-9см = Е= 10-8см).
Периоды решетки металлов находятся в пределах 0,2 – 0,7 нм.
Для ОЦК: a, b, c; a = b = c.
Для ГЦК: a, b, c; a = b = c.
Для ГПУ: а, с; с/а = 1,633 (к Zn не относится)
Число атомов в каждой элементарной ячейке (плотность упаковки – равняется числу атомов, приходящихся на одну элементарную ячейку):
ОЦК: ПУ (плотноупакованная) = 
ГЦК: ПУ = 
ГПУ: ПУ = 
Координационное число – под ним понимают число атомов, находящихся на равном и наименьшем расстоянии от данного атома. Чем выше координационное число, тем больше плотность упаковки атомов:
ГЦК: 
Коэффициент заполнения ячейки (плотность укладки) – определяется как отношение объема, занятого атомами к объему ячейки:
Для характеристики величины атома служит атомный радиус, под которым понимается половина расстояния между ближайшими соседними атомами. Атомный радиус возрастает при уменьшении координационного числа.
3. Полиморфные (аллотропические) превращения
Атомы металла – исходя из геометрических соображений, могут образовать любую кристаллическую решетку.
Однако устойчивым, а, следовательно, реально существующим типом является решетка, обладающая наиболее низким запасом свободной энергии.
Многие металлы в зависимости от температуры могут существовать в разных кристаллических формах (т. н. полиморфных (аллотропических) модификациях). В результате полиморфного превращения атомы кристаллического тела, имеющего решетку одного типа, перестраиваются таким образом, что образуется кристаллическая решетка другого типа.
Полиморфную модификацию, устойчивую при более низкой температуре, для большинства металлов принято обозначать буквой б, при более высокой температуре в, затем г и т. д.
Полиморфное превращение протекает при постоянной температуре (например, при нагреве идет поглощение теплоты).
Известные полиморфные превращения: Feб ↔ Feв; Coб ↔ Coв; Tiб ↔ Tiв; Mnб ↔ Mnв ↔ Mnг ↔ Mnд; Snб ↔ Snв, а также для Ca, Li, N, Cs, Sr, Te, Zr, V и др.
Металл с данной кристаллической решеткой должен обладать меньшим запасом свободной энергии.
Рисунок 3. Полиморфизм железа и его связь со свободной энергией системы
Полиморфизм железа. Из рис. 3, видно, что в интервале температур 911 – 1392°С устойчивым является г-железо (К 12) (имеет min свободную энергию), а при температурах ниже 911°С и выше 1392°С устойчиво б-железо (К 8).
В твердом металле полиморфные превращения происходят в результате зарождения и роста кристаллов аналогично кристаллизации из жидкого состояния. Зародыши новой модификации наиболее часто возникают на границах зерна исходных кристаллов.
В результате полиморфного превращения образуется новые кристаллические зерна, имеющие другой размер и форму, поэтому превращение также называют перекристаллизацией.
Полиморфное превращение сопровождается скачкообразным изменением всех свойств металлов и сплавов: удельного объема, теплоемкости, теплопроводности, электропроводности, магнитных свойств, механических и химических свойств и т. д.
Высокотемпературная модификация имеет высокую пластичность.
В таблице № 1 показан интервал температур существования различных аллотропических форм некоторых, имеющих практическое значение металлов, у которых обнаружена температурная аллотропия.
4. Анизотропия свойств металлов
Из атомно-кристаллического строения металлов видно, что плотность расположения атомов по различным плоскостям в кристаллических решетках неодинакова (рис. 4).
Вследствие неодинаковой плотности атомов в различных плоскостях и направлениях решетки многие свойства (химические, физические, механические) каждого кристалла зависят от направления решетки. Подобная неодинаковость свойств монокристалла в разных кристаллографических направлениях называется анизотропией.
Рисунок 4. Расположение атомов в различных плоскостях и направлениях в кубической решетке (ОЦК)
Кристалл – тело анизотропное в отличие от аморфных тел (стекло, пластмассы и т. д.), свойства которых не зависят от направления.
Технические металлы являются поликристаллами, т. е. состоят из большого числа анизотропных кристаллов. В большинстве случаев, как уже указывалось выше, кристаллы статистически неупорядоченно ориентированы один по отношению к другому, поэтому во всех направлениях свойства более или менее одинаковы, т. е. поликристаллическое тело является изотропным (вернее – квазиизотропным (ложная изотропия)). Такая мнимая изотропность не будет наблюдаться, если кристаллы имеют одинаковую преимущественную ориентировку в каких-то направлениях. Эта ориентированность, или текстура, создается в известной степени, но не полностью в результате значительной холодной деформации; в этом случае поликристаллический металл приобретает анизотропию свойств.


















