Что принимать при альцгеймере
Болезнь Альцгеймера: линии терапии

Активация холинергической системы – первая ступень в терапии болезни Альцгеймера. Ингибитор холинэстеразы донепезил обладает высокой биодоступностью и эффективен для профилактики прогрессирования деменции и поддержания когнитивных функций пациента.
В 2018-ом году немецкое издание InTouch сделало сенсационное заявление: наследник английского престола, принц Чарльз, никогда не станет королём, поскольку у него диагностирована болезнь Альцгеймера (БА). Информацию, якобы, подтвердили и инсайдеры: по их словам, Чарльз постоянно забывает, что происходило пять минут назад и плохо ориентируется.
Что ж, перспектива получения монаршей короны — не панацея от дебюта БА, как и любых других неизлечимых заболеваний. Возможности нейропротективной терапии болезни Альцгеймера остаются на сегодняшний день весьма ограниченными [1]. Единственное, чем современная медицина может помочь пациентам (а их сегодня, по подсчетам ВОЗ, в мире не менее 25 млн [2]) — фармакотерапия и реабилитация. Результативное лечение легкой (мягкой) и умеренной деменции очень важно, поскольку именно на этом этапе отмечается наибольший темп прогрессирования когнитивных нарушений, психотических и асоциальных расстройств.
«Золотым стандартом» лечения БА, согласно консенсусу FDA, мнению регуляторов ЕС, а также одобрению МЗ РФ, является ступенчатая терапия. Её первый этап — применение ингибиторов холинэстеразы [3,4] оптимизирующих синаптическую передачу, например, донепезила (Алзепил®).
Алгоритм патогенетической терапии БА* [5]
Мягкая деменция
Цель: поддержание когнитивного и повседневного функционирования пациента, профилактика прогрессирования.
Препараты (уровень доказательности 1++, А): донепезил и др. ингибиторы АХЭ
Критерии эффективности: стабилизация когнитивных расстройств и нарушений..
Умеренная деменция
Цель: Стабилизация состояния когнитивных функций и возможности самообслуживания.
Препараты (уровень доказательности 1++, А): донепезил и др. ингибиторы АХЭ, акатинол, мемантин.
Критерии эффективности: улучшение функционирования в быту, замедление прогрессирования деменции.
Умеренно-тяжелая и тяжелая деменция
Цель: поддержание возможности минимального самообслуживания, облегчение ухода.
Препараты (уровень доказательности 1+ и 1++, А): комбинация донепезил+мемантин или мемантин в режиме монотерапии
Критерии эффективности: стабилизация состояния, поддерживание гигиенических навыков.
* С симптоматической целью при развитии депрессии или поведенческих расстройств при БА применяются антидепрессанты и нейролептики.
Алзепил® способствует активации холинергической системы — «центрального игрока» в работе памяти и способности к обучению. Препарат обладает высокой биодоступностью. Пациенты с нарушением функции почек не нуждаются в изменении схемы лечения, т.к. это состояние не влияет на клиренс донепезила. В связи с возможным увеличением экспозиции при легком или умеренном нарушении функции печени повышение дозы следует выполнять с учетом индивидуальной переносимости. [5]
Схема титрации [6]
Один из недавних метаанализов 30 исследований (8257 участника) подтвердил, что приём донепезила в дозе 10 мг/сут на протяжении 6 месяцев приводил к лучшему сохранению когнитивных функций в сравнении с плацебо при минимуме НЯ [7].
Литература
Материал предназначен для медицинских работников.
Что такое болезнь Альцгеймера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Полякова Т. А., невролога со стажем в 12 лет.
Определение болезни. Причины заболевания
Болезнь Альцгеймера — это хроническое нейродегенеративное заболевание, с медленным началом и значительным ухудшением с течением времени. В 70 % случаев болезнь Альцгеймера приводит к деменции.
Этиология. Факторы риска
Заболевание на данный момент изучено плохо. Предполагается, что в 70% случаев болезнь Альцгеймера объясняется генетическими причинами, среди других факторов риска — черепно-мозговые травмы, депрессия, эндокринные заболевания в анамнезе (гипотиреоз), эстрогенная недостаточность у женщин.
Сопутствующие заболевания
Статистические данные
Распространённость и факторы риска
Заболевание более распространено среди женщин. Предположительно, это связано со следующими факторами:
Симптомы болезни Альцгеймера
Признаки болезни Альцгеймера на ранней стадии часто ошибочно принимаются за нормальные признаки старения.
Кратковременная потеря памяти — наиболее распространенный ранний симптом болезни Альцгеймера, который выражается в том, что больному трудно запоминать последние события. В трети случаев заболевание можно распознать по изменениям поведения.
По мере усугубления болезни возникают следующие симптомы:
Важный признак болезни Альцгеймера — нарушение способности справляться с повседневностью. При заболевании возникают проблемы с самообслуживанием и поведенческие расстройства.
Признаки болезни Альцгеймера у мужчин и женщин
Признаки болезни Альцгеймера у женщин и мужчин схожи, однако у женщин она чаще сопровождается депрессией.
Патогенез болезни Альцгеймера
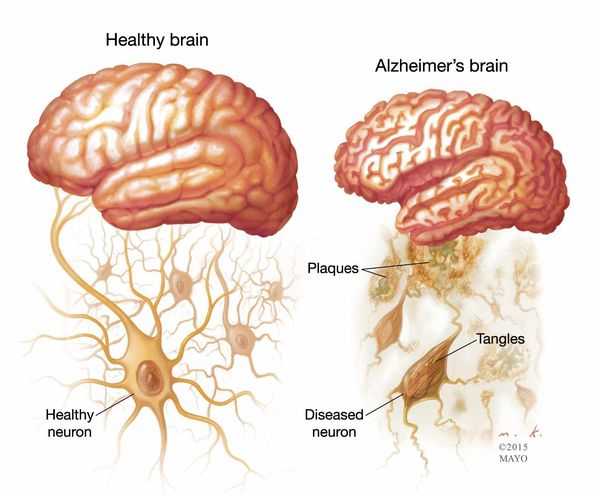
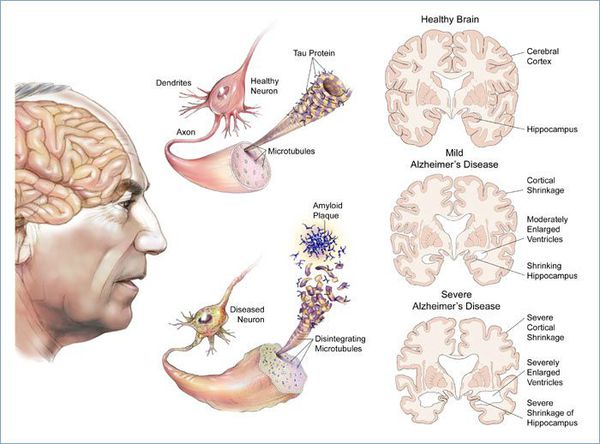
Существуют отличительные патоморфологические признаки болезни Альцгеймера: амилоидные (сенильные) бляшки — это внеклеточные отложения в виде скопления фрагмента белка, называемые бета-амилоидом; нейрофибриллярные клубочки — скрученные микроскопические нити тау-белка внутриклеточной локализации. Происходит потеря связи между клетками мозга, ответственными за память, обучение и общение. Эти соединения, или синапсы, передают информацию из клетки в клетку. Важная роль в патогенезе принадлежит воспалительному процессу, связанному с активацией микроглии, которая инициируется накоплением амилоида. [1]
Патофизиология болезни Альцгеймера:
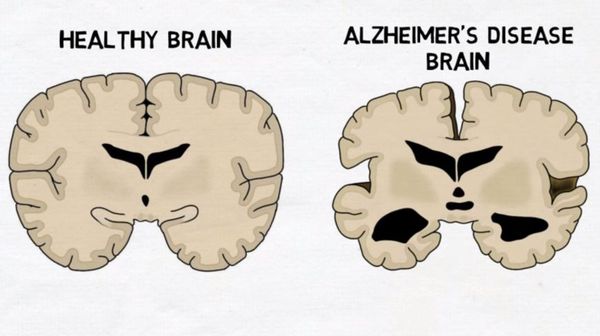
Макроскопически выявляется диффузная атрофия головного мозга с уменьшением объёма извилин и расширением боковых борозд, наиболее выраженная в височно-теменной области.
У значительной части больных цереброваскулярная патология может инициировать или усиливать дегенеративный процесс, связанный с отложением амилоида или другими характерными для заболевания изменениями.
Классификация и стадии развития болезни Альцгеймера
Типичный фенотип болезни Альцгеймера — сочетание выраженных мнестических нарушений гиппокампального типа с акустико-мнестической афазией, зрительно-пространственными нарушениями и апраксией. [3]
Три атипичных фенотипа болезни Альцгеймера (неамнестических):
Заболевание также подразделяется на формы с ранним началом, зачастую с положительным семейным анамнезом (до 65 лет) и поздним началом (старше 65 лет). Они отличаются патогенезом, генетическими факторами и разной скоростью прогрессирования.
Три стадии болезни Альцгеймера:
Первая (предеменция, ранняя деменция): больные обслуживают себя сами, но им нужна помощь для решения финансовых вопросов, приготовления пищи и т. д.
Вторая (умеренная деменция): зависимость от посторонней помощи растет — больные не способны самостоятельно одеться, осуществить гигиенические процедуры, долго оставаться дома без присмотра.
Третья (тяжёлая деменция): больные не могут выполнить ни одно из привычных повседневных действий без помощи других людей.
Переход от одной стадии к другой коррелирует со снижением оценки по MMSE (Краткая шкала психического статуса), которая является надежным инструментом для отслеживания динамики заболевания.
Осложнения болезни Альцгеймера
Продолжительность жизни людей с болезнью Альцгеймера после установления диагноза обычно колеблется от трех до десяти лет. Более четырнадцати лет после установления диагноза живут менее 3% больных. Уменьшение выживаемости связано с тяжелыми когнитивными нарушениями, снижением уровня физической активности, частыми падениями и нарушениями в неврологическом статусе. Сопутствующие соматические заболевания также влияют на продолжительность и качество жизни при болезни Альцгеймера. Пневмония и обезвоживание — наиболее частые непосредственные причины смерти, вызванной болезнью Альцгеймера. Кроме того, чем старше возраст, тем выше общий возраст выживаемости. У мужчин прогноз менее благоприятен по сравнению с женщинами.
Диагностика болезни Альцгеймера
Трудности ранней диагностики болезни Альцгеймера во многом объясняются «маскированным» характером заболевания в этот период, когда отсутствуют явные внешние признаки деменции. Для постановки диагноза, определения тактики ведения пациента необходимо выявить характер и выраженность когнитивных нарушений.
Нейропсихологический тест
Основной метод оценки когнитивных функций — нейропсихологическое обследование, которое проводит врач, обученный данным методам исследования. В некоторых странах практикуется обследование больных их родственниками с помощью шкал для оценки когнитивных функций: монреальской когнитивной шкалы, Адденбрукской, шкала краткого исследования психических функций MMSE.
Биомаркеры болезни Альцгеймера
Молекулярная диагностика на ранней стадии заболевания также создаёт перспективы для раннего назначения лечения болезни Альцгеймера. Определение биомаркеров в плазме является менее инвазивной альтернативой для диагностики болезни Альцгеймера. Биомаркеры классифицируются на биомаркеры накопления амилоида и биомаркеры нейродегенерации. Основные биомаркеры отражают патологию амилоида (внеклеточное накопление Aβ1-40/1-42) или внутриклеточные включения нейрофибриллярных клубочков (гиперфосфорилированного тау). [4] [5]
Согласно рекомендациям 4-го Канадского консенсуса по диагностике и лечению деменции и рациональному использованию биомаркеров для диагностики болезни Альцгеймера и других деменций (CCCDTD4, 2011): [6]
1. Определение биомаркеров цереброспинальной жидкости не рекомендуются для диагностики болезни Альцгеймера с типичной клинической картиной (2А уровень).
2. Исследование биомаркеров не рекомендуется для скрининга здоровых людей с целью оценки риска развития болезни Альцгеймера в будущем (уровень 1В).
3.Биомаркеры цереброспинальной жидкости можно рассматривать в особых случаях, когда есть атипичные признаки или диагностические трудности при дифференциальной диагностике лобного варианта болезни Альцгеймера от лобно-височной деменции, а также случаи первично прогрессирующей афазии как следствие болезни Альцгеймера или лобно-височной дегенерации (уровень 2В).
МРТ и КТ головного мозга
Современные методы нейровизуализации — магнито-резонансная томография и компьютерная томография головного мозга — позволяют расширить диагностические возможности прижизненной диагностики болезни Альцгеймера.
МРТ и КТ проводят для выявления поддающихся лечению причин деменции и нарушений, которые могут усугубить симптомы. Структурные изменения по данным магнитно-резонансной томографии являются более прогностически значимыми для дальнейших изменений в когнитивной сфере, чем биомаркеры цереброспинальной жидкости. По данным магнитно-резонансной томографии, признаки цереброваскулярного заболевания, такие как лейкоареоз и множественные подкорковые лакунарные инфаркты, чаще наблюдаются у пациентов с болезнью Альцгеймера, чем в контрольной группе. [7] Асимметричная атрофия медиальных отделов височной доли также не исключает сосудистую деменцию.
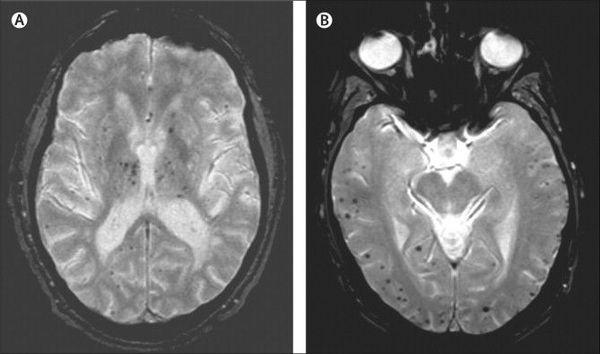
Описана смешанная модель патогенеза болезни Альцгеймера, которая предполагает взаимодействие церебральной амилоидной ангиопатии с сосудистыми факторами на ранних стадиях патологического процесса. Предполагается, что синергия между накоплением амилоида и цереброваскулярной патологией может инициировать дальнейшую дисфункцию нейронов и нейродегенерацию. [8] В этом отношении церебральные микрокровоизлияния, выявляемые в режиме Т2 градиентного эхо на магнитно-резонансной томографии, являются дополнительным и доступным диагностическим маркером, повышающим диагностическую значимость лейкоареоза и свидетельствующим в пользу церебральной амилоидной ангиопатии или гипертонической микроангиопатиии, особенно в случаях смешанной патологии и тяжелого когнитивного дефицита.
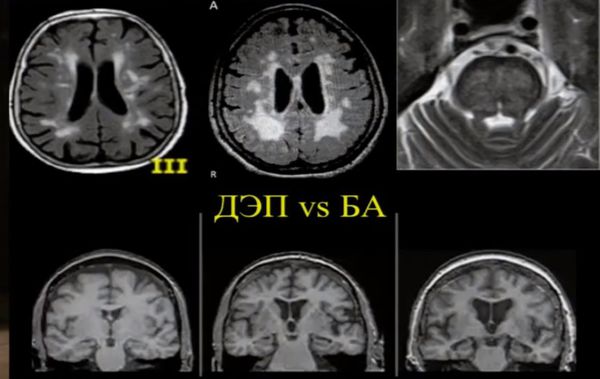
Локализация церебральных микрокровоизлияний является дифференциально-диагностическим признаком ведущего патологического процесса. В случае болезни Альцгеймера наблюдается корковая локализация микрокровоизлияний, в случае дисциркуляторной энцефалопатии или сосудистой деменции будут визуализироваться микрокровоизлияния в глубинных отделах мозга. [9] [10]
Одним из наиболее перспективных методов диагностики болезни Альцгеймера является позитронно-эмиссионная томография с лигандом, который связывается с амилоидом (PiB), однако накопление амилоида и захват соответствующего лиганда нарастают на стадии умеренных когнитивных нарушений, но после конверсии в деменцию дальнейшего накопления не происходит. [11]
Лечение болезни Альцгеймера
Болезнь Альцгеймера пока не поддается лечению. Но благодаря группе новых препаратов и симптоматическому лечению Альцгеймера можно сделать так, что снижение интеллекта больных будет более постепенным.
Лекарства
В России зарегистрированы все современные антидементные препараты. Более того, они вошли в список жизненно важных лекарственных средств. Их всего четыре, и они прежде всего от болезни Альцгеймера, но нередко применяются и при деменциях другого происхождения.
К таким средствам относятся:
Облегчение расстройств психики и поведения, сопровождающих болезнь Альцгеймера
С целью лечения сопутствующих расстройств психики и поведения используются также антидепрессанты и нейролептики.
Поддерживающие методы
Существуют и нелекарственные методы воздействия — тренировки интеллектуальных функций. Нейропсихологическая реабилитация позволяет стимулировать к развитию новых нейронный сетей, обучая рабочие нервные клетки.
Специальная диета при болезни Альцгеймера не требуется: питание не влияет на развитие заболевания.
Прекращение лечения
Причиной для прекращения приёма антидементных препаратов может стать выраженная брадикардия, но это осложнение возникает крайне редко.
Рекомендации для ухаживающих за близкими с болезнью Альцгеймера
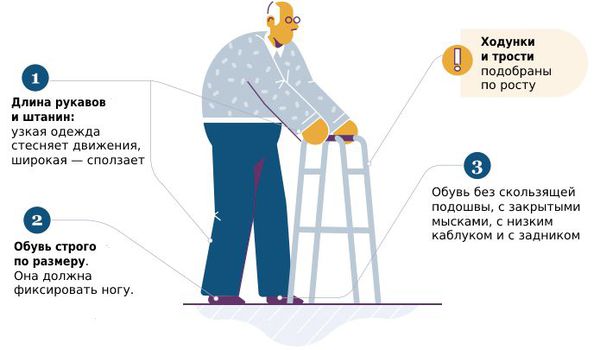
При уходе за больным человеком важно организовать для него безопасное и удобное пространство.
Также важно внимательно выбирать обувь и одежду.
С развитием деменции постепенно сужается круг практических задач, с которыми может справиться пожилой человек. Очень важно помочь больному найти увлечение по душе.
Такими занятиями могут быть:
Ухаживая за больным, не следует игнорировать своё здоровье. Пациенту нужно обеспечить нормальное питание, режим, активный образ жизни — это в полной мере относится и к близким больного человека.
Где обеспечивают уход при болезни Альцгеймера
Государственных специализированных пансионатов по уходу за людьми с болезнью Альцгеймера в нашей стране пока нет.
Прогноз. Профилактика
С увеличением осведомлённости общества о деменции будет расти и потребность в помощи по уходу, понадобятся значительные затраты для её организации. Пока же преобладает в основном неформальная помощь в семьях. Усилия по улучшению качества и доступности помощи потребуют вложений в меры первичной профилактики, и возможно, это позволит контролировать «эпидемии» деменций в разных регионах мира. В качестве основных мишеней первичной профилактики рассматриваются улучшение образования и устранение сосудистых факторов риска.
Профилактика
На сегодняшний день одной из основных целей профилактики является создание различных новых форм внебольничной помощи пациентам пожилого и старческого возраста с целью улучшения диагностики когнитивных нарушений разной степени тяжести, более раннее выявление заболеваний. С такой целью в развитых странах созданы клиники памяти, Альцгеймеровские центры. [2]
В России также работают кабинеты памяти, научно-исследовательские центры по изучению расстройств памяти, запущены социальные интернет-проекты, например, memini.ru. Большое значение имеют «школы для родственников», так как родственники остаются один на один с этой болезнью и часто не знают, что надо делать.
Человек с деменцией обращен в прошлое. Больных надо аккуратно «тормошить» и в интеллектуальном плане, и в двигательном. Неподвижность плохо влияет на мозг. Лучший способ сохранить разум, это, как ни странно, даже не интеллектуальная деятельность, а двигательная активность. Именно в этом случае в мозге создаются условия, которые способствуют образованию новых связей между нейронами и укреплению мозгового резерва, что впоследствии противодействует развитию деменции.
Продолжительность жизни
Юридические вопросы
Требования для признания гражданина недееспособным раскрываются в статье 29 Гражданского кодекса РФ. Потеря дееспособности компенсируется больному человеку установлением опёки. Опекун «восполняет» утраченные возможности гражданина, признанного недееспособным, и действует в его интересах.
Процедура признания гражданина недееспособным описана в 31 главе Гражданского процессуального кодекса РФ, в статьях 281–285.
Современные подходы к лечению болезни Альцгеймера

В лекции рассмотрены этиологическая структура и критерии диагностики деменции, а также особенности клинической картины и алгоритмы базисной терапии болезни Альцгеймера – наиболее распространенной причины деменции.
Олег Семенович Левин, д.м.н., профессор, заведующий кафедрой неврологии с курсом рефлексологии и мануальной терапии ФГБОУ ДПО РМАНПО
Сегодня в мире живет от 30 до 50 млн. пациентов с деменцией – каждый пятый пациент старше 85 лет и каждый десятый в возрасте от 80 до 84 лет. В 2008 году в России проживало более 3 млн. пациентов с умеренными когнитивными расстройствами и практически 2 млн. пациентов с деменцией, которая более чем в половине случаев была связана с болезнью Альцгеймера (БА).
Несмотря на широкую распространенность когнитивных нарушений у пациентов пожилого возраста и использование стандартных диагностических критериев, официально регистрируются не более 10% случаев деменции и только 5% пациентов получают терапию. Первичная деменция – БА, лобно-височная дегенерация и TDP43-энцефалопатия – развивается на фоне прогрессирующей нейродегенерации в результате нарушения метаболизма белков в нейронах. В основе патогенеза вторичной деменции лежат коморбидные состояния, вызывающие поражение структур мозга – цереброваскулярная патология (сосудистая деменция), демиелинизирующие процессы, нормотензивная гидроцефалия, посттравматическая или метаболическая/токсическая энцефалопатия. На фоне мультисистемных дегенеративных процессов развивается деменция с тельцами Леви, кортикобазальная дегенерация, прогрессирующий надъядерный паралич или гепатолентикулярная дегенерация. При коморбидном течении БА и цереброваскулярных заболеваний устанавливают деменцию смешанного типа. От 25% до 50% всех случаев деменции составляет БА. На смешанную и сосудистую формы приходится 15-30% и 10-25%, соответственно. Деменция с тельцами Леви и алкогольная деменция составляют от 3 до 10% всех случаев деменции.
Диагностика деменции основана на оценке клинических симптомов, ассоциированных с тремя психофунциональными аспектами заболевания – аффективными и поведенческими нарушениями, функциональным и когнитивным дефицитом. В частности, на наличие деменции указывают множественный (≥2 нарушений) когнитивный дефицит – нарушение внимания, памяти, праксиса, гнозиса и т.д., – прогрессирующее снижение когнитивных функций по сравнению с предшествующим уровнем, органическое поражение головного мозга (в т.ч. метаболическое или аутоиммунно-воспалительное), нарушение социальной, трудовой или бытовой адаптации и автономии и стойкий дефицит, не связанный с острым расстройством сознания или психиатрическим заболеванием.
Для количественной оценки тяжести деменции традиционно используют клиническую шкалу краткого исследования психического статуса (Mini-Mental State Examination, MMSE), предложенную в 1975 году M. Froistein. Шкала включает шесть субтестов, позволяющих выявлять нарушения ключевых когнитивных функций: ориентации во времени и пространстве, памяти, внимания и счета, отсроченного воспроизведения, речи и моторных функций (конструктивный праксис). О.С. Левин с соавт. предлагают использовать адаптированную форму шкалы MMSE для проведения скринингового нейропсихологического исследования (3-КТ), которое, помимо тестов на оценку конструктивного праксиса, семантического аспекта речи и отсроченного воспроизведения, включает субтесты для оценки фонетической активности и опосредованного воспроизведения (узнавание).
«Отправной точкой» для назначения нейропсихологического скрининга являются жалобы или изменение поведения пациента. После исключения псевдодеменции (напр., депрессии) и потенциально обратимой деменции с помощью лабораторных и инструментальных (КТ/МРТ) методов исключают наличие эндокринных и метаболических нарушений (гипотиреоз, дефицит витамина B12) и органической патологии мозга (опухоли, гидроцефалия). Установление типа деменции проводят по результатам оценки присутствия сосудистых факторов риска, признаков цереброваскулярной патологии или инфаркта/лейкоареоза на КТ/МРТ и определения характера структурных повреждений мозга: при подкорково-лобных и корково-подкорковых поражениях устанавливают сосудистую и смешанную деменцию, соответственно; БА и TDP43-энцефалопатии соответствует задняя корковая деменция, а для лобно-височной дегенерации и деменции с тельцами Леви характерны передняя корковая и подкорково-корковая дисфункция, соответственно.
Более половины всех случаев деменции связаны с БА. Характерным морфологическим признаком и «пусковым» механизмом нейродегенеративных процессов при БА является повышенная аккумуляция нерастворимых агрегатов гиперфосфорилированного тау-белка (pTau), образующего нейрофибриллярные клубочки в телах нейронов, и бета-амилоидного пептида (Aβ), формирующего сенильные бляшки в межклеточном пространстве. Накопление этих белков вызывает повреждения тел и отростков нейронов и дегенерацию синапсов, что, в свою очередь, приводит к атрофии височных и теменных отделов коры головного мозга и гиппокампа. Помимо основных клинических проявлений БА выделяют дополнительные, «малые» признаки заболевания – феномен поворота головы («направление» заданного пациенту вопроса сопровождающему родственнику), эйфорию, застенчивую (само)критичность, аккуратность в одежде, «маскировочные» приемы (проблема поиска слов), потирание руками и книжные парафазии.
Ключевой особенностью клинической картины БА является строгий временной характер прогрессирования когнитивных нарушений. Так, в результате повреждения нейронов гиппокампа и конвекситальных отделов височной коры одними из первых манифестируют снижение памяти и изменение речи по типу акустико-мнестической афазии (неспособность назвать предмет), соответственно, за которыми следуют зрительно-пространственные расстройства, ассоциированные с атрофией гиппокампа и теменной коры, и апраксия (агнозия, акалькулия) на фоне относительной сохранности поведенческих стереотипов и двигательных функций; дисбазия и паркинсонизм развиваются на поздних стадиях БА.
На первой стадии болезни (19-24 балла по шкале MMSE) больные способны обслуживать себя, но нуждаются в помощи при решении финансовых и бытовых вопросов; на второй стадии заболевания (10-18 баллов по шкале MMSE) пациенты утрачивают способность к полноценной реализации базовых моторных навыков, например, не могут самостоятельно одеться или принять ванну; на третьей стадии (0-9 баллов по шкале MMSE) больные полностью теряют способность к самостоятельному выполнению повседневных действий, в том числе принятие пищи. Помимо этого, течение БА различается у больных с ранним (≤65 лет) и поздним (≥65 лет) дебютом заболевания. Для ранней БА (средний возраст дебюта – 61 год) характерна более высокая скорость прогрессирования с фокальным вовлечением задних отделов теменной коры, раннее развитие афазии и других корковых дисфункций, относительно гомогенная клиническая картина на развернутом этапе деменции (афато-апракто-агностический синдром), длительная сохранность реакции на болезнь и личностных особенностей, более выраженная атрофия структур мозга на КТ/МРТ по сравнению с возрастной нормой и чаще отрицательный семейный анамнез, в то время как при поздней форме (средний возраст дебюта – 72 года) наблюдается полиморфная клиническая картина: первостепенно отмечается атрофия гиппокампа и, как следствие, преобладание нарушений памяти и зрительно-пространственных функций на ранней стадии и прогрессирование афазии, апраксии, нарушений внимания и мышления, а также выраженные изменения личности и утрата критики на более позднем этапе заболевания; среди структурных особенностей на КТ/МРТ отмечается наличие лейкоареоза и сосудистых очагов на КТ/МРТ.
Важной отличительной особенностью фокальных форм БА является прогрессирование задней корковой атрофии – ассиметричной атрофии затылочных и теменных долей с расширением задних рогов боковых желудочков, которая приводит к нарушению зрительно-пространственных функций – развитию синдрома Балинга и Герстмана, алексии, апраксии и зрительной агнозии, нарушению моторного воспроизведения и оценки расстояния до объектов, а также искажению цветовосприятия и ощущению движения статичных объектов. При повреждении лобных или височных отделов развиваются амнестические и неамнестические формы БА.
Согласно положениям МКБ11, нозологические формы деменции – БА, дисциркуляторная энцефалопатия, болезнь Паркинсона и болезнь диффузных телец Леви – сосредоточены в классе нервных болезней (G), в то время как деменция на фоне БА и болезни Паркинсона, а также сосудистая деменция и деменция с тельцами Леви относятся к классу психических заболеваний (F).
Главными целями базисной терапии БА, помимо снижения скорости прогрессирования когнитивных нарушений, являются поддержание бытовой независимости, снижение нагрузки по уходу за больным для родственников и социальных служб, а также скорости развития поздних поведенческих нарушений и риска госпитализации в психиатрические учреждения. Согласно положениям клиническим рекомендаций Европейской федерации неврологических сообществ (European Federation of Neurologic Societies, EFNS) 2010 года, доказанной эффективностью обладают ингибиторы холинэстеразы (ИХЭ), антиглутаматергические средства и препараты моноклональных антител (адуканумаб и зумаб), которые позволяют выводить агрегаты бета-амилоида из ткани мозга, тем самым стабилизируя когнитивные функции пациентам. Клиническая эффективность препаратов других классов – нейротрофических, антиамилоидных (иммунотерапия и ингибиторы секретаз), противовоспалительных и ноотропных препаратов (напр., пирацетам и нисерголин), митохондриотропных средств и антиоксидантов, статинов, селегилина, пентоксифиллина – на сегодняшний день остается недоказанной. Данные об эффективности Ginkgo biloba (EGb) и церебролизина противоречивы, что дает основание применять эти средства при невозможности прохождения базисного лечения. При БА легкой и умеренной степени тяжести могут быть использованы методы когнитивной стимуляции и реабилитации.
.png)
.png)
.png)