Что принимать вместе с денолом при гастрите
Схема лечения хеликобактер пилори: все современные методы эрадикационной терапии
Для выявления Хеликобактер пилори используется дыхательный уреазный тест, не требующий много времени, безвредный и не вызывающий никаких неприятных ощущений и представляющий собой золотой стандарт диагностики инфекции. Симптомы и лечение Хеликобактер пилори индивидуальны. Факт присутствия возбудителя в организме далеко не всегда сопровождается патологическими процессами и требует приема лекарственных препаратов.
Для выяснения и согласования лучших подходов к выявлению и лечению хеликобактерной инфекции в Европе была сформирована группа из ведущих специалистов гастроэнтерологов. Периодически на основании проводимых конференций и совещаний они публикуют протоколы – Маастрихтские консенсусы, по названию города, где проходили первые встречи.
Всего их на данный момент существует пять:
По результатам консенсуса «Маастрихт 2» было установлено, что, к сожалению, ни одна из проводимых схем эрадикации, несмотря на одновременное применение нескольких препаратов, не гарантирует полное уничтожение инфекции. В связи с этим было рекомендовано лечить пациентов сначала по схеме «первой линии», а затем при отсутствии терапевтического эффекта – по схеме «второй линии».
Необходимость проведения повторных курсов антихеликобактерной терапии объясняется повышением резистентности H. pylori к назначаемым антибиотикам, что является главной проблемой современной гастроэнтерологии при лечении ассоциированных с возбудителем заболеваний.
Применяемые сегодня, чтобы вылечить хеликобактерную инфекцию, эрадикационные схемы были утверждены на «Маастрихт 4».
Основными требованиями для них являются:
Интересно: Исторически первой успешно апробированной схемой эрадикации Хеликобактер пилори было применение субсалицилата висмута и Метронидазола. Испытал ее на себе ученый Барри Маршалл, обнаруживший совместно с коллегой Helicobacter pylori в слизистой желудка. В 1984 гг. он преднамеренно выпил содержимое чашки Петри с культурой бактерий, а затем вскоре после появления характерных симптомов спровоцированного гастрита провел указанное лечение. После 14 дней терапии по результатам биопсии возбудителя в желудке обнаружено не было.
Препараты I линии
Задачей эрадикационной терапии первой линии является уничтожение H. pylori у максимально возможного числа пациентов.
Согласно рекомендациям Маастрихт 3, назначают так называемую трехкомпонентную схему (тройная терапия), которая включает следующие препараты и дозировки в день:
Как ИПП, снижающие секрецию желудочного сока и выделение соляной кислоты, больных лечат следующими препаратами в указанных дозировках на один прием:
Минимальная продолжительность курса лечения составляет 7 дней. По ряду проведенных клинических исследований оказывается, что более эффективно принимать указанные препараты 10 или 14 дней. Чтобы была достигнута максимальная эрадикация Хеликобактер пилори и исключена вероятность рецидивов, тройную терапию при отсутствии противопоказаний и других ограничений нужно назначать в полном объеме и по дозировкам, и по срокам лечения.
Трехкомпонентную схему можно применять как первую линию терапии в странах, где частота устойчивых к действию кларитромицина штаммов H. pylori составляет менее 15–20%. Развитие устойчивости возбудителя к Кларитромицину объясняется частым назначением антибиотиков из группы макролидов при бактериальных осложнениях ОРВИ и респираторных заболеваниях у детей и взрослых. Если резистентность к Кларитромицину обнаруживается в среднем у 10% населения, то для Метронидазола этот показатель гораздо выше и составляет от 20 до 40%, что значительно ограничивает возможность применения этого антибактериального средства.
Как альтернатива трехкомпонентной эрадикационной терапии может использоваться четырехкомпонентная схема, дополнительно включающая висмута трикалия дицитрат (препарат Де-Нол) по 120 мг 4 раза в день. Если у больного с диагностированной хеликобактерной инфекцией имеется атрофия слизистой желудка, сопровождающаяся отсутствием продукции соляной кислоты, то назначать ИПП в данном случае не надо, поэтому их исключают, оставляя висмута трикалия дицитрат.
Для пациентов пожилого возраста, у которых ввиду высокого риска осложнений при назначении сразу двух антибиотиков, проведение полноценной антихеликобактерной терапии первой линии невозможно, рекомендуется следующая сокращенная схема лечения на 14 дней:
При наличии показаний у пожилых пациентов антибиотик может быть вообще отменен. При этом прием препаратов висмута назначают на 28 дней, при болевых ощущениях дополнительно выписывают короткий курс ИПП.
Лечение обострений хронических заболеваний органов пищеварения
Создание ряда высокоэффективных фармакопрепаратов обеспечило существенное повышение эффективности лечения больных с патологий органов системы пищеварения. Среди этих лекарственных средств заслуживают внимание блокаторы Н2-рецепторов гистамина (ранитидин,
П. Я. Григорьев, доктор медицинских наук, профессор
Э. П. Яковенко, доктор медицинских наук, профессор
А. П. Яковенко, кандидат медицинских наук
Н. А. Агафонова, А. С. Прянишников, П. В. Гуляев, Е. В. Таланова, С. Б. Кальнова
Создание ряда высокоэффективных фармакопрепаратов обеспечило существенное повышение эффективности лечения больных с патологий органов системы пищеварения. Среди этих лекарственных средств заслуживают внимание блокаторы Н2-рецепторов гистамина (ранитидин, фамотидин и др.), ингибиторы протонной помпы (омепразол, лансопразол, пантопразол, рабипразол), прокинетики (цизаприд, домперидон, прукелоприд и др.), полиферментные препараты (креон, панцитрат, мезим-форте, ликреаза и др.), противовирусные (интерфероны, рибавирин, ламивудин и др.), а также антибактериальные и противопаразитарные средства. При оптимальном их использовании быстро и надежно достигается ремиссия гастроэзофагеальной рефлюксной болезни, язвенной болезни желудка и двенадцатиперстной кишки, предупреждается развитие осложнений язвенной болезни и геморрагического гастродуоденита. Нередко удается ингибировать репликацию вирусов, купировать активность и прогрессирование хронических вирусных гепатитов В и С и предупредить трансформацию хронического гепатита в цирроз и цирроз-рак печени.
В настоящее время в патогенезе острого и хронического гастрита, дуоденита, язвенной болезни желудка (ЯБЖ), язвенной болезни двенадцатиперстной кишки (ЯБДПК), MALT-лимфомы желудка и даже рака желудка доказана роль Helicobacter pylori (Нр). Обсуждается роль Нр-инфекции в патогенезе ряда экстрагастральных заболеваний: ишемической болезни сердца, мигрени, цирроза печени и др.
Разработка и внедрение в практику комбинированной антигеликобактерной лекарственной терапии ЯБЖ и ЯБДПК радикально изменили прогноз этих и некоторых других заболеваний желудка и двенадцатиперстной кишки.
Оптимальными вариантами эрадикационной терапии при ЯБЖ, ЯБДПК и эрозивных гастритах (гастродуоденитах), ассоциированных с Нр, признаны семидневные трех- или четырехкомпонентные схемы. Трехкомпонентная схема включает омепразол 20 мг, или лансопразол 30 мг, или пантопразол 40 мг, или пилорид (ранитидин висмут цитрат) 400 мг, которые принимаются с интервалом в 12 часов + кларитромицин 250 мг 2 раза в день или амоксициллин 500 мг 4 раза в день или 1000 мг 2 раза в день, или тетрациклин 500 мг 4 раза в день или 1000 мг 2 раза в день + метронидазол 400 мг 2 раза в день или фуразолидон 0,2 г 2 раза в день. Четырехкомпонентная 7-10-дневная эрадикационная терапия используется, если предыдущий вариант оказался неэффективным, и включает омепразол 20 мг 2 раза в день, или лансопразол 30 мг 2 раза в день, или пантопразол 40 мг 2 раза в день + препараты висмута (вентрисол или де-нол 120 мг 4 раза в день или бисмофальк 2 табл. 3 раза в день) + тетрациклина гидрохлорид 500 мг 4 раза в день, или амоксициллин 500 мг 4 раза в день + метронидазол 250 мг 4 раза в день или фуразолидон 0,1 г 4 раза в день. При этом все антибактериальные препараты необходимо принимать во время еды. В четырехкомпонентной схеме целесообразно использовать комбинированный препарат гастростат, в состав которого входят эти же ингредиенты. Другие комбинации использовать не рекомендуется в силу их малой эффективности.
После окончания 7-10-дневной эрадикационной терапии необходимо продолжить лечение при ЯБЖ в течение семи недель, при ЯБДПК — пяти недель, при эрозивном гастродуодените — трех недель одним из следующих антисекреторных препаратов: ранитидин 300 мг в сутки, фамотидин 40 мг в сутки, омепразол 20 мг в сутки, лансопразол 30 мг в сутки, пантопразол 40 мг в сутки. В качестве симптоматических средств дополнительно могут использоваться антациды (маалокс и др.) и цитопротекторы (вентер и др.).
Вышеуказанная терапия более чем в 90% случаев приводит к эрадикации Нр. В результате этого купируется активное воспаление в слизистой оболочке (СО) желудка и двенадцатиперстной кишки, обеспечивается заживление эрозий и язв, предупреждается развитие обострений и осложнений (кровотечение, прободение, стенозирование), лимфомы и, возможно, рака желудка.
Отечественные ученые обращают внимание практических врачей на то, что нередко имеет место гипердиагностика язвенной болезни и гастрита (гастродуоденита), не раскрываются причины возникновения болезней, не учитывается, что эрозивно-язвенный процесс в гастродуоденальной СО носит гетерогенный характер и не всегда связан с ЯБ. Так, например, при остром гастрите также могут появляться эрозии, локальные участки кровоизлияний в СО и кровотечения. При гистологическом исследовании у таких больных в СО выявляются умеренные признаки воспаления. Наиболее частыми причинами такого острого гастрита (гастродуоденита) являются: химические повреждения СО (алкоголь, нестероидные противовоспалительные средства, агрессивные щелочные жидкости), вирусы (цитомегаловирус, вирусы герпеса), бактерии (гемолитические стрептококки и др.), уремия, радиационные облучения. Изредка некоторые микробы вызывают даже острый флегмонозный гастрит. Ученым удалось установить причины стрессового гастрита, факторами риска развития которого являются: гипоксия, заболевания печени и почек, тяжелые операции, ожоги, сепсис, травмы ЦНС. Нередко в течение 24 часов после воздействия стрессовых факторов в СОЖ возникают острые эрозии и язвы. При этом приблизительно у 30% больных наблюдаются желудочно-кишечные кровотечения, причем у части из них они бывают массивными, угрожающими жизни. У пострадавших с ожогами часто диагностируются повреждения СО верхних отделов пищеварительного тракта, которые получили название «язвы Курлинга», при которых, особенно локализующихся в ДПК, существует большой риск не только развития кровотечений, но и перфораций. У больных с травмой головы и инсультом нередко в гастродуоденальной СО обнаруживаются острые язвы (язвы Кушинга). При этих язвах, особенно дуоденальной локализации, также существует большой риск развития кровотечений и перфораций. Поэтому необычайно важно выделять людей с высоким риском возникновения стрессовых повреждений ЖКТ и как можно раньше начинать лечение антисекреторными препаратами для профилактики развития кровотечения и перфорации.
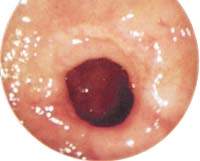 |
| Поверхностная язва привратника |
Отечественными учеными проведено немало исследований с целью установления связи между приемом нестероидных противовоспалительных средств (НПВС) и повреждениями ЖКТ. У больных, принимающих данные препараты по поводу ревматоидного артрита, остеоартроза и других болезней, язвообразование отмечается в 15-20% случаев, часто возникают осложнения (кровотечения и перфорации), особенно у лиц, имеющих в анамнезе ЯБ. Суммарный риск поражения ЖКТ у принимающих НПВС приблизительно в три раза выше, чем у не принимающих эти препараты. У пожилых пациентов (старше 65 лет) такой риск возрастает в пять раз. Врачи, назначающие данные препараты, обязаны предусмотреть решение трех задач: предупреждение развития НПВС-индуцированных язв (особенно при наличии факторов риска), их лечение (часто в условиях, когда требуется продолжение приема НПВС), а также профилактика повреждений СО тонкой и толстой кишки, возникающих при длительном их приеме. Несмотря на то что в лечебную практику начинает внедряться новый класс НПВС (селективные ингибиторы циклооксигеназы-2), которые не должны оказывать повреждающего эффекта на СО ЖКТ, их безопасность требует клинического подтверждения, и данные исследования к настоящему времени еще не завершены.
Главная задача профилактики стрессового гастрита и в известной мере НПВС-ассоциированных повреждений гастродуоденальной СО — увеличение рН внутрижелудочного содержимого до 4 и выше, так как при данном уровне рН происходит инактивация протеолитического фермента пепсина и повышение коагуляции крови. На сегодняшний день с этой целью целесообразно воспользоваться блокаторами Н2-рецепторов гистамина (ранитидин, фамотидин и др.) или ингибиторами протонной помпы (омепразол, лансопразол, пантопразол).
Отечественные и зарубежные ученые большое внимание уделили также изучению различных форм хронического гастрита (ХГ). Наряду с ХГ, связанным с Нр, и ХГ типа А, выделяются эозинофильный, лимфоцитарный и гранулематозный (болезнь Крона, туберкулез, гистоплазмоз, сифилис, саркоидоз и др.) гастриты, а также гипертрофические гастропатии (болезнь Менетрие, псевдолимфома желудка, синдром Золлингера — Эллисона), застойная гастропатия при портальной гипертензии (не является истинным гастритом), щелочной (желчный) рефлюкс-гастрит. При некоторых формах ХГ развивается гипо- и ахлоргидрия и недостаточность витамина В12. По мнению отечественных ученых, клиническая значимость ХГ состоит в том, что он может считаться ранним предраковым заболеванием, развитие которого происходит от атрофии СО к кишечной метаплазии и далее к раку желудка. Диагноз ХГ должен всегда основываться только на результатах квалифицированного гистологического исследования прицельно взятых биоптатов СОЖ, на что имеются указания в упомянутых выше государственных стандартах.
Одним из наиболее распространенных кислотозависимых заболеваний является гастроэзофагеальная рефлюксная болезнь (ГЭРБ), для лечения которой разработаны рекомендации и определены обязанности больного и врача.
Больному рекомендуется: спать на кровати с приподнятым не менее чем на 15 см головным концом; снизить массу тела, если имеется патологическое ожирение; не ложиться после еды в течение 1,5 часа; не принимать пищу перед сном, ограничить прием жира; прекратить курить и употреблять алкоголь; избегать тесной одежды, тугих поясов, а также работы в наклонном положении тела; по возможности ограничить прием лекарственных средств, оказывающих отрицательное влияние на моторику пищевода и тонус нижнего пищеводного сфинктера (пролонгированные нитраты, антагонисты кальция, теофиллин, миогенные спазмолитики, а также препараты, повреждающие СО пищевода (аспирин и другие аналоги).
Медикаментозное лечение назначается дифференцированно в зависимости от выраженности клинических, функциональных и морфологических изменений в верхних отделах пищеварительного тракта. При гастроэзофагеальном рефлюксе без эзофагита (есть симптомы, но нет видимых изменений СО пищевода) используются два варианта терапии. В случаях если ГЭРБ сочетается с замедлением эвакуации из желудка, снижением тонуса нижнего пищеводного сфинктера, гипомоторной дискинезией кишечника, целесообразно назначать внутрь прокинетики — мотилиум (домперидон) 10 мг или координакс (цизаприд, перистил и другие аналоги) 5-10 мг 4 раза в день в сочетании с буферными антацидами (маалокс или аналоги) по одной дозе через час после еды и одну дозу непосредственно перед сном. После достижения клинической ремиссии продолжается «терапия по требованию», то есть прерывистое симптоматическое лечение (при изжоге — мотилиум + антацид или быстрорастворимый зантак — 150 мг). При наличии выраженной недостаточности нижнего пищеводного сфинктера и/или высокого уровня интрагастральной кислотности целесообразно использовать блокаторы Н2-рецепторов гистамина (ранитидин 150 мг 2 раза в сутки или фамотидин 20 мг 2 раза в сутки), а при их неэффективности — ингибиторы протонной помпы (омепразол 20 мг в сутки или ланзопразол 30 мг в сутки) до достижения клинической ремиссии. В дальнейшем назначается «терапия по требованию», предусматривающая при появлении симптомов ГЭРБ прием антисекреторных препаратов в половинной суточной дозе или антацидов.
При рефлюкс-эзофагите I степени в течение 6 недель используются блокаторы Н2-рецепторов гистамина — ранитидин 150 мг, или фамотидин 20 мг 2 раза в день с интервалом в 12 часов, или ингибиторы протонной помпы — омепразол 20 мг в сутки или ланзопразол 30 мг в сутки. При наступлении ремиссии (в среднем через 6 недель) больного переводят на терапию «по требованию» с использованием антацидов, или Н2-блокаторов, или ингибиторов протонной помпы.
При рефлюкс-эзофагите III-1V степени на 4 недели назначается ингибитор протонной помпы омепразол 20 мг или лансопразол 30 мг 2 раза в день с интервалом в 12 часов. Далее, при купировании симптомов ГЭРБ продолжается прием омепразола 20 мг в сутки или лансопразола 30 мг в сутки до 8 недель с последующим переходом на постоянную поддерживающую терапию с использованием вышеуказанных препаратов в половинной суточной дозе в течение года. При недостаточной эффективности данной терапии возможно сочетание антисекреторных средств с прокинетиками-мотилиумом или координаксом в обычных суточных дозах. К дополнительным средствам терапии рефрактерных форм ГЭРБ относят сукральфат (вентер, сукрат-гель) 1,0 г 4 раза в день за 30 минут до еды в течение одного месяца.
Практический врач часто встречает больных с синдромом избыточного бактериального роста (СИБР) и изменением состава микрофлоры в кишечнике, называемым дисбактериозом. К возникновению этого синдрома могут приводить разные причины: болезни органов пищеварения, сопровождающиеся секреторно — моторными нарушениями, особенно при наличии очагов воспаления; перенесенные острые кишечные инфекции (бактериальная дизентерия, иерсиниозный энтероколит и др.); длительный прием лекарственных средств, влияющих на секрецию пищеварительных желез, регенерацию эпителия и моторно-эвакуаторную функцию пищеварительного тракта; длительный, а иногда и нерациональный прием антибактериальных препаратов; неполноценное питание; алкоголизм. Клинические проявления синдрома избыточного бактериального роста в кишечнике связаны с гиперизбыточной продукцией органических кислот и преждевременной деконъюгацией желчных кислот, выделением бактериальных токсинов, разрушением пищеварительных ферментов, развитием моторных расстройств.
Для СИБР характерно наличие абдоминальных болей или дискомфорта в животе, нарушение стула (изменение формы и нарушение пассажа), вздутие и чувство распирания живота, потеря массы тела, слабость, повышенная утомляемость, раздражительность. Лечение СИБР наряду с соответствующей диетой включает один-два семидневных курса антибактериальной терапии, назначение ферментных препаратов, лекарственных средств, регулирующих моторно-эвакуаторную функцию кишечника и интракишечный уровень рН, устраняющих дефицит витаминов, минеральных элементов и др., то есть проводится комбинированное лечение. Показаниями для назначения антибактериальной терапии являются: 1) избыточный бактериальный рост в тонкой кишке; 2) наличие воспалительных изменений в слизистой оболочке кишечника; 3) выявление условнопатогенной микрофлоры в посевах кишечного содержимого.
При СИБР в тонкой кишке в основном используется один из следующих антибактериальных препаратов: тетрациклина гидрохлорид 250 мг 4 раза в сутки, ципрофлоксацин 250 мг 2 раза в сутки, бисептол 960 мг 2 раза в сутки, метронидазол 500 мг 2 раза в сутки, фуразолидон 100 мг 3-4 раза в сутки, эрсефурил 200 мг 4 раза в сутки, интетрикс 1 капс. 4 раза в сутки, цефалексин 250 мг 4 раза в сутки. В ряде случаев можно применить энтерол 2-4 капсулы или пакета в сутки. При СИБР в толстой кишке предпочтение отдается одному из нижеперечисленных препаратов: фталазол или сульгин 1,0 г в сутки, эрсефурил 800 мг в сутки, интетрикс 4 капсулы в сутки, метронидазол 1,0 г в сутки, бактисубтил 4-6 капсул в сутки.
После окончания курса антибактериальной терапии назначаются пробиотики — препараты, содержащие нормальные штаммы кишечной флоры и пребиотики — средства, обеспечивающие их рост и функциональную активность. Для восстановления микрофлоры тонкой кишки используются пробиотики, содержащие аэробные штаммы (бифиформ 2-4 капсулы в сутки или лактобактерин 5-10 доз в сутки), толстой кишки — пробиотики, включающие анаэробные штаммы (бифидумбактерин 5-10 доз в сутки или колибактерин 5-10 доз в сутки,), толстой и тонкой кишки — комбинированные препараты (бифиформ 2-4 капсулы в сутки или бификол 5-10 доз в сутки). Продолжительность их приема составляет 2-4 недели.
Бифиформ — пробиотик, одна капсула которого содержит бифидумбактерин и энтерококки в объеме не менее 10 в седьмой степени каждого вида бактерий. Капсулы препарата покрыты энтеросолюбильной оболочкой, благодаря чему бактерии доходят до кишечника в неизмененном виде. Наличие в препарате анаэробной флоры делает его универсальным для восстановления микробиоценоза тонкой и толстой кишки. Кроме того, каждая капсула содержит особую питательную среду, необходимую для роста и размножения молочнокислых бактерий, что позволяет выживать и быть метаболически активной микрофлоре, содержащейся в препарате бифиформ.
В проведенном нами исследовании участвовали 119 больных, из них 68 женщин и 51 мужчина в возрасте от 21 до 76 лет (средний возраст 39,7 лет).
Для разработки эффективных подходов к назначению бифиформа нами апробированы три схемы терапии. Первая схема, при которой бифиформ назначался без предшествующей терапии, направленной на деконтаминацию кишечника, была использована у 37 больных. Вторая схема, предусматривающая прием бифиформа после предшествующей деконтаминации кишечника, назначалась 28 больным. Третью схему, при которой лечение бифиформом проводилось в виде монотерапии, получали 24 больных. Больные контрольной группы получали терапию, аналогичную второй схеме, но они не получали бифиформ или другие пробиотики.
Бифиформ назначался по 1 капсуле два раза в день в течение 15 дней. Однако если к седьмому дню лечения тяжесть клинических проявлений уменьшалась менее чем на одну степень, дозу препарата увеличивали до 2 капсул два раза в день и терапия продолжалась еще две недели. Для деконтаминации кишечника и снятия воспалительных явлений у больных с хроническими заболеваниями органов пищеварения проводились от одного до трех курсов противомикробной терапии продолжительностью от пяти до семи дней со сменой препаратов в очередном курсе.
Прием бифиформа оказал положительный эффект на состав кишечной микрофлоры. К концу лечения у 35 (76,1%) больных отмечено восстановление нормальной кишечной микрофлоры, и лишь у 11 (23,9%) состав ее оставался измененным. У большинства больных нормализовалось общее количество кишечной флоры, отмечено увеличение количества кишечной палочки, бифидобактерий, нормализация содержания энтерококков и исчезновение условно-патогенных энтеробактерий (лактозонегативных, гемолизирующих штаммов кишечной флоры, представителей родов Klebsiella, Enterobacter, Proteus, Pseudomonas, Citrobacter и др.). Следует отметить, что у значительной части больных, у которых оставались изменения в составе кишечной флоры, имели место и клинические симптомы (боли в животе, метеоризм, нарушения стула), что подтверждает их патогенетическую связь.
Бифиформ как в комплексном лечении, так и в виде монотерапии показал свою эффективность в купировании клинических проявлений диспепсии, в нормализации процессов пищеварения и восстановлении нормального состава кишечной флоры при широком спектре заболеваний органов пищеварения. Доза бифиформа по 1-2 капсулы два раза в день в течение двух недель является достаточно эффективной в ведении больных с хроническими заболеваниями органов пищеварения.
Отсутствие эффекта от проводимого лечения может быть связано с диетическими нарушениями, психоэмоциональными расстройствами, употреблением алкоголя, но чаще — неполным восстановлением нормальной кишечной микрофлоры в результате неадекватной терапии лекарственными средствами. Успех лечения в известной степени зависит не только от лекарственной терапии, предписываемой врачом, но и от пациента, которому необходимо избавиться от вредных привычек, изменить стиль жизни, пунктуально принимать лекарства и т. д.
Все материалы, поступающие в редакцию, рецензируются независимыми рецензентами и при необходимости редактируются. Редакция не несет ответственности за пропажу рукописи.
Направление в редакцию работ, ранее опубликованных или представленных для публикации в другие издания, не допускается.
Не забывайте указать точный почтовый адрес и телефон для контакта.
Лечение заболеваний, ассоциированных с инфекцией Helicobacter pylori
Необходимость установления единого подхода к диагностике и терапии инфекции Helicobacter pylori (HP-инфекции), основанного на опыте лучших европейских исследователей, привела к созыву в г. Маастрихт (Нидерланды) в феврале 1996 г. конференции, организованн
Необходимость установления единого подхода к диагностике и терапии инфекции Helicobacter pylori (HP-инфекции), основанного на опыте лучших европейских исследователей, привела к созыву в г. Маастрихт (Нидерланды) в феврале 1996 г. конференции, организованной Европейской группой по изучению H. pylori. На конференции был обсужден и принят документ под названием «Current European Concepts in the Management of Helicobacter pylori Infection — The Maastricht Consensus Report» (Маастрихт-1). В этом первом соглашении были установлены основные показания к эрадикации и рекомендованы оптимальные схемы лечения. Второй Консенсус (Маастрихт-2) был принят в 2000 г., показания были подразделены на обязательные и целесообразные (табл. 1А и табл.1Б).
В 2005 г. во Флоренции был принят последний, третий Консенсус (Маастрихт-3) по ведению HP-инфекции. Целью его была выработка глобального подхода и анализ ключевых вопросов, в частности, показаний к эрадикации, стратегии и тактики ведения пациентов. Учитывая высокий уровень доказательности необходимости эрадикации Н. pylori в первой группе показаний (обязательных), принятых Консенсусом Маастрихт-2, они не подвергались повторному пересмотру. При выработке последнего Консенсуса Маастрихт-3 участники вернулись к обсуждению и принятию только тех показаний, которые значились как целесообразные (ГЭРБ, функциональная диспепсия, прием НПВС). На основании анализа последних научных данных была признана необходимость проведения эрадикации Н. pilory при функциональной диспепсии, поскольку морфологически при наличии НР-инфекции практически в 100% обнаруживается хронический гастрит, который является прогрессирующим заболеванием с определенным риском последующего язвообразования и малигнизации.
Проведенные рандомизированные исследования показали, что после эрадикации Н. pylori улучшение состояния больных наблюдается в 50%, а полное исчезновение симптомов — у 30%. В то же время при персистировании инфекции улучшение отмечается лишь у 38%, а исчезновение — у 18% [1]. Показания к эрадикации Н. pylori при ГЭРБ были обоснованы тем, что НР-инфекция сопровождается гиперхлоргидрией у большинства пациентов, а после эрадикации секреторная функция нормализуется. Эрадикация Н. pylori не повышает риск развития ГЭРБ в сравнении с терапией ингибиторами протонной помпы (ИПП). Напротив, монотерапия ИПП, снижая желудочную секрецию, способствует распространению Н. pylori и заселению им тела желудка, что сопровождается развитием фундального гастрита с более высоким риском атрофии. Целесообразность эрадикации Н. pylori при необходимости приема НПВС была аргументирована повышением риска язвообразования при сочетании двух ульцерогенных факторов (Н. pylori и НПВС). Так, по данным C. O’Morein [2], эрозивно-язвенное поражение гастродуоденальной зоны при наличии этих двух факторов выявляются у 55% больных, при отмене НПВС уменьшаются в два раза, а при эрадикации Н. pylori — в пять раз. Таким образом, повторный пересмотр целесообразных рекомендаций подтвердил необходимость проведения эрадикации Н. pylori при функциональной диспепсии, ГЭРБ и приеме НПВС.
Консенсус Маастрихт-3 впервые включил показания к эрадикации Н. pylori при двух внежелудочных состояниях: железодефицитной анемии (ЖДА) и идиопатической тромбоцитопенической пурпуре (ИТП). Роль Н. pylori в развитии ЖДА была доказана на основании выявления дефицита железа вследствие потребления его микроорганизмом, а также восстановлением показателей после эрадикации Н. pylori. Целесообразность эрадикационной терапии при ИТП была доказана снижением уровня антитромбоцитарных антител у больных после эрадикации Н. pylori.
Таким образом, в соответствии с рекомендациями Консенсуса Маастрихт-3, показаниями к эрадикации Н. pylori являются:
Педиатрические аспекты инфекции Н. pylori впервые обсуждались в 1997 г. в г. Эшторил (Португалия) по инициативе Европейской группы по изучению Н. pylori, затем обсуждение было продолжено на состоявшихся в Будапеште второй (1998 г.) и в Хельсинки третьей (1999 г.) встречах педиатров-экспертов [3, 4]. Итогом работы явилось формирование рабочего алгоритма обследования и лечения детей, включающего следующие этапы:
Принятые в Риме в 1999 г. рекомендации ESPGHAN по ведению инфекции Н. pylori предусматривают простой алгоритм показаний к эрадикации:
Педиатрические аспекты инфекции Н. pylori обсуждались и при принятии Консенсуса Маастрихт-3, в частности, были подчеркнуты следующие положения:
Важные требования к эрадикационной терапии HР-инфекции были опубликованы в «Рекомендациях по диагностике и лечению инфекции Н. pylori у взрослых при язвенной болезни желудка и двенадцатиперстной кишки» Российской гастроэнтерологической ассоциации и Российской группы по изучению Н. pylori [5]:
В отличие от других микроорганизмов Н. pylori in vitro чувствителен к большинству антимикробных препаратов. Еще в 1988 г. в исследованиях McNulty C. A. M. и Dent J. C. [6] показали его чувствительность к 21 антибактериальному агенту.
Н. pylori чувствителен к подавляющему большинству антибиотиков пенициллинового ряда и большинству цефалоспоринов (цефуроксиму, цефокситину, цефалексину), причем их минимальная подавляющая концентрация для 90% бактерий (МПК-90) не превышает 0,5 мг/л. Макролиды и фторхинолоны in vitro также проявляют достаточно высокую активность в отношении Н. pylori, их МПК-90 ниже 0,5 мг/л. Весьма эффективны и антибиотики других групп (нитрофураны, гентамицин, тетрациклин, рифампицин). Метронидазол обладает активностью средней степени. Н. pylori устойчив к ванкомицину, цефсулодину, триметоприму и сульфаниламидам, поэтому эти антибактериальные средства используют при его культивировании для подавления конкурентной флоры. Среди противоязвенных средств ни одно не обладает существенной активностью против H. pylori in vitro, кроме солей висмута: трикалия дицитрата (Де-нола), субсалицилата, субгаллата.
Несмотря на активность in vitro, при назначении in vivo вышеперечисленные антибактериальные препараты отнюдь не отличаются столь же высокой эффективностью. Одной из причин этого является снижение их активности в кислой среде желудка. Исследования, проведенные МсNulty C. A. M. [7], показали, что активность пенициллина и ампициллина в условиях кислой среды снижается более чем в 10 раз, цефалексина — в 16 раз, ципрофлоксацина — в 10 раз, а эритромицина — более чем в 100 раз. Макролиды последнего поколения (кларитромицин, Вильпрафен® Солютаб), в отличие от эритромицина, гораздо более устойчивы в кислой среде [8]. Незначительное изменение активности наблюдается у тетрациклина и фуразолидона. Активность же метронидазола и Де-нола не изменяется при кислых значениях рН [9], поэтому они успешно применяются в лечении НР-инфекции.
Другой причиной снижения эффективности антибактериальных препаратов in vivo является неспособность некоторых их них накапливаться в слизи, покрывающей желудочный эпителий. Неионизированные молекулы эритромицина и ципрофлоксацина из слизистой оболочки быстро диффундируют в просвет желудка. При меньших значениях рН возможен их переход в ионизированную форму и задержка в слизистом слое, но снижение рН само по себе приводит к их почти полному разрушению. Поэтому эритромицин практически не эффективен при лечении НР-инфекции. В отличие от эритромицина, кларитромицин и рокситромицин отличаются хорошим проникновением в ткани и слизистый слой [10]. Ципрофлоксацин и другие фторхинолоны не применяются в терапии Н. pylori еще и потому, что при их назначении очень быстро формируются резистентные штаммы ко всей группе хиноловых препаратов [11].
Амоксициллин (Флемоксин Солютаб®) — один из наиболее эффективных антибиотиков, применяемых при лечении Н. pylori-ассоциированных заболеваний. Препарат относится к группе бета-лактамных антибиотиков, подгруппе аминопенициллинов. При низких значениях рН амоксициллин сохраняет высокую активность. Максимальную активность проявляет при нейтральных значениях рН [12]. Является амфотерным соединением и при рН 3–6 проникает в ткани несколько хуже, тогда как в слизь, которая на 90% состоит из воды, способен проникать в большей степени [13], что позволяет добиться высокой его концентрации в слизистой желудка (вплоть до собственной пластинки слизистой оболочки) и в желудочном содержимом.
Солютаб — это особая технология производства препарата, при которой каждая таблетка состоит из отдельных микросфер, заключенных в наполнитель. Под воздействием любой жидкости таблетка начинает распадаться на микросферы, которая становится проницаемой только при воздействии бикарбонатов в кишечнике. Таким образом, действующее вещество высвобождается в зоне максимального всасывания. Это в свою очередь обеспечивает более равномерное и максимально полное всасывание активных компонентов препаратов, произведенных по указанной технологии, по сравнению с аналогами. Форма Солютаб также обеспечивает минимальную остаточную концентрацию действующего вещества в кишечнике, что гарантирует как предсказуемую эффективность, так и благоприятный профиль безопасности вследствие минимального влияния препарата на микрофлору кишечника и минимального раздражающего действия.
Таблетки Солютаб можно как проглотить целиком, так и растворить в воде с образованием сиропа или суспензии с приятным вкусом, который с удовольствием пьют как дети, так и взрослые.
Механизм воздействия амоксициллина на Н. pylori заключается в ингибировании процессов синтеза в мембране бактериальной клетки пенициллин-связывающих белков (ПСБ) — ферментов, осуществляющих завершающие стадии биосинтеза основного компонента клеточной стенки микроорганизма — пептидогликана [14]. Это приводит к нарушению синтеза клеточных оболочек и лишает микробную клетку способности противостоять осмотическому градиенту, в результате чего стенки набухают и разрушаются. Таким образом, амоксициллин оказывает бактерицидное действие, тогда как подавляющее большинство других бета-лактамов являются бактериостатиками. Данное обстоятельство объясняет нецелесообразность применения для лечения Н. pylori других антибиотиков данной группы (в том числе и родственного ампициллина).
Побочными эффектами, характерными для амоксициллина, являются: диарея, аллергическая реакция и псевдомембранозный колит. При проведении антихеликобактерной терапии детям рекомендуется суточная доза 60 мг/кг в сутки дважды в день во время или после еды. При приеме амоксициллина до еды его местное антибактериальное действие усиливается.
Н. pylori весьма чувствителен к тетрациклину, который ингибирует бактериальный синтез белка и подобно амоксициллину проявляет интралюминальную активность, причем даже при низких значениях рН [15]. В литературе нет сообщений о резистентности Н. pylori к тетрациклину, но этот препарат дает довольно большое количество побочных реакций: гепатотоксическое действие, тошноту, а также стойкое повреждение растущих зубов, вследствие чего не рекомендуется для использования в педиатрической практике.
Эффективность другой группы антибиотиков — макролидов в отношении Н. pylori была доказана во многих исследованиях [16]. Основу химической структуры макролидов составляет макроциклическое лактонное кольцо. Все они обладают противовоспалительным и иммуномодулирующим действием, накапливаясь в клетках организма (в том числе и в полиморфно-ядерных лейкоцитах) и влияя на миграцию нейтрофилов, окислительные реакции в фагоцитах и продукцию многих цитокинов. Механизм действия макролидов состоит в торможении синтеза белка в микробных клетках при их размножении путем связывания с каталитическим пептидилтрансферазным центром рибосомальной 50S-субъединицы. Это приводит к торможению реакции транслокации и транспептидации и нарушению процесса формирования и наращивания (элонгации) пептидной цепи. Обладают преимущественно бактериостатическим действием. Поскольку макролиды являются слабыми основаниями, их активность возрастает при рН 5,5–8,5.
Наиболее активным в отношении Н. pylori является кларитромицин. В отличие от других макролидов, которые в кислой среде подвергаются усиленному гидролизу, кларитромицин устойчив в кислоте желудочного сока. По данным Miki и соавторов (2003) [17], монотерапия кларитромицином приводит к уничтожению Н. pylori в 54% случаев, а согласно исследованиям Gisbert — в 15% случаев, что, тем не менее, является впечатляющим результатом.
Другие представители макролидов, в частности, джозамицин и рокситромицин мало уступают кларитромицину в клинической эффективности, но в меньшей степени вступают во взаимодействие с другими лекарственными препаратами, реже вызывают побочные эффекты и поэтому могут являться альтернативой кларитромицину [18].
Одним из основных препаратов, входящих в схемы антихеликобактерной терапии, является трикалия дицитрат висмута (ТДВ, Де-нол). При рН менее 5 ТДВ образует преципитаты в виде двух солей висмута — оксихлорида и цитрата, оптимум рН составляет 3,5 [19]. В области дна язвы препарат создает защитную пленку, образуя агрегаты с белками плазмы [20]. Он также способен образовывать кристаллы различной формы в зависимости от рН среды, которые, в частности, могут адгезироваться в местах некроза эпителиальных клеток [21].
ТДВ оказывает влияние на плотность и проницаемость слоя желудочной слизи, образуя комплекс висмут–протеогликан и замедляя диффузию Н+, но не влияя на диффузию других ионов [22]. ТДВ обладает также антипепсиновой активностью — вероятно, за счет связывания пепсина [23], а при кислых значениях рН способен связывать желчные кислоты [24]. ТДВ достоверно увеличивает секрецию простагландинов [25] и бикарбонатов [26] в желудке и двенадцатиперстной кишке.
Одним из основных свойств ТДВ является его бактерицидное действие на Н. pylori. Оно незначительно превосходит аналогичное действие других солей висмута in vitro, но многократно — in vivo. Это объясняется наибольшей растворимостью ТДВ в желудочном соке и слизи в самом широком диапазоне рН, что позволяет препарату легко проникать в слизистый слой и желудочные ямки. ТДВ препятствует адгезии Н. pylori к желудочному эпителию, приводит к повреждению и фрагментации мембраны бактериальной клетки, вакуолизации ее [27]. Он ингибирует ферменты Н. pylori: уреазу, каталазу, фосфолипазу и его протеолитическую активность [28]. В результате всего комплекса воздействий ТДВ наступает лизис бактериальной клетки в непосредственной близости от эпителия желудка. Очень важно, что препарат способен воздействовать как на вегетативные, так и на кокковые формы Н. pylori. Несмотря на различные механизмы действия, он обладает синергизмом с антибиотиками, поэтому может быть эффективно использован в сочетании с ними. К препарату не развивается резистентность. Более того, согласно данным Williamson R., Pipkin G. A. [29], ТДВ предотвращает развитие первичной и вторичной резистентности к антибиотикам.
Многочисленные исследования оценки эффективности терапии Де-нолом НР-инфекции показали, что после курса монотерапии у большинства больных удается добиться подавления инфекции и стойкого клинического улучшения [30], однако в дальнейшем восстанавливается прежняя степень обсемененности слизистой оболочки. То есть Де-нол в качестве монотерапии не в состоянии стойко подавить Н. pylori, поэтому используется комбинированная терапия. ТДВ, а также некоторые другие соли висмута: субсалицилат и, реже, субгаллат, в сочетании с антибиотиками широко используются в комплексной терапии НР-инфекции [31].
Хотя действие этих препаратов реализуется местно, все же незначительные концентрации висмута обнаруживаются в крови и моче в процессе лечения и достигают стабильных значений спустя четыре недели от его начала [32]. В экспериментах на животных было показано, что высокие дозы висмута могут вызвать побочные реакции со стороны ЦНС (т. н. «висмутовая энцефалопатия»). Пороговыми концентрациями висмута в крови у человека считаются 50–100 мг/л, однако в реальных условиях при назначении обычных доз Де-нола (8 мг/кг у детей, 480 мг/сут у взрослых) такие концентрации никогда не регистрируются и никаких побочных реакций со стороны ЦНС не возникает [33]. Исследование П. Л. Щербакова [34], проведенное у детей, показало, что на фоне стандартной антихеликобактерной терапии, включавшей обычные дозы Де-нола, концентрация висмута в крови у детей не превышала 55 мг/л, что соответствует нижней границе нормы пороговых значений и 10-кратно ниже концентраций, наблюдаемых при висмутовой энцефалопатии.
То есть Де-нол является безопасным и эффективным антихеликобактерным препаратом и может быть без опасений назначен детям. Однако, поскольку висмут медленно выводится из организма, его не рекомендуют назначать пациентам с почечной недостаточностью [35]. Кроме вышеописанных, из побочных действий препаратов висмута обычно наблюдается почернение стула вследствие образования в кишечнике сульфида висмута, в литературе имеется несколько сообщений о возникновении диареи, описаны редкие случаи аллергии на препарат в виде кожных сыпей [36]. В желудке препарат может связываться с пищей и антацидными препаратами, терапевтическое его действие в этом случае становится невозможным. Поэтому препарат рекомендуют принимать за 30 мин до еды и на ночь, не ранее чем через 2 часа после последнего приема пищи, и не сочетают с приемом антацидов. В детской практике рекомендуется назначать Де-нол детям старше 5 лет в дозе 8 мг/кг/с в 2 приема за 30 мин до еды.
В соответствии с рекомендациями ESPGHAN и NASPGHAN (2000 г.), оптимальными схемами для эрадикационной терапии хеликобактериоза являются следующие [37]:
В соответствии с рекомендациями ESPGHAN и NASPGHAN [77], оптимальными дозами препаратов, входящих в стандартные схемы, являются следующие: омепразол — 1 мг/кг до 20 мг 2 раза, амоксициллин 50 мг/кг до 1 г 2 раза, кларитромицин, джозамицин, рокситромицин 15 мг/кг до 500 мг 2 раза, метронидазол 20 мг/кг до 500 мг 2 раза, тетрациклин (с 12 лет) 50 мг/кг до 1 г 2 раза, трикалия дицитрат висмута (КСВ) 120 мг 3–4 раза.
В соответствии с этими рекомендациями и Консенсусом Маастрихт-2, в качестве 7-дневных схем эрадикации первой линии рекомендована схема, включающая ИПП, кларитромицин (джозамицин или другой представитель макролидов) и амоксициллин (ИКА), и в меньшей степени — схема, в которой вместо амоксициллина применяется метронидазол (ИКМ) [38]. Поскольку компоненты первой схемы были наиболее удачно сбалансированы по эффективности и минимальны по побочным действиям, она получила название «стандартной тройной терапии». Уровень эрадикации при использовании этой комбинации препаратов составил 78–91% [39]. По результатам G. M. Buzas, J. Jozan (2004) [40] эффективность схемы, включающей кларитромицин и амоксициллин, составила 79,6%, кларитромицин и нитроимидазол — 84,1%, амоксициллин с нитроимидазолом — 72,5%. В аналогичном исследовании, проведенном в Южной Корее и включавшем 352 пациента с дуоденальной язвой и неязвенной диспепсией, сравнивали комбинацию омепразола (20 мг 2 раза в сутки), кларитромицина (500 мг 2 раза в сутки) и амоксициллина (1,0 г 2 раза в сутки) или тинидазола (500 мг 2 раза в сутки), эффективность оказалась одинаковой (65,7% и 64,8%) [41]. К важному выводу о целесообразности включения в режим эрадикации кларитромицина пришли исследователи, которые сравнивали комбинацию лансопразола (30 г 2 раза в сутки), амоксициллина (1,0 г 2 раза в сутки) и метронидазола (400 мг 3 раза в сутки) с режимом, включавшим лансопразол и амоксициллин в той же дозе, но с заменой метронидазола на кларитромицин (500 мг 2 раза в сутки). Эффективность последнего варианта оказалась значительно более высокой (91% и 78%) [42].
В 1999–2002 гг. в Европе было проведено проспективное мультицентровое исследование, включавшее 16 педиатрических центров в 14 странах. Всего было обследовано 1233 пациента, 41% которых были родом из Африки и Ближнего Востока. Исследовалась как первичная (до лечения), так и вторичная (при неудачном лечении) резистентность. Первичная резистентность к кларитромицину была выявлена у 20% детей, вторичная — у 42%. Первичная резистентность к кларитромицину была достоверно выше у детей до 6 лет, чем у подростков старше 12 лет, и преобладала у жителей Южной Европы по сравнению с Северной. Эти различия легко объяснимы более частым назначением макролидов для лечения внежелудочных (в основном, респираторных) заболеваний у детей раннего возраста и существованием определенных ограничений в назначении препаратов этой группы в североевропейских странах. В Восточной Европе отдельные исследования также показали высокую резистентность к кларитромицину у детей. Так, в Болгарии она составила 12,4%, а в Польше — 23,5% [43].
Основной причиной роста резистентности Н. pylori к кларитромицину является не столько предшествующая неэффективная эрадикационная терапия, сколько широкое использование макролидов при лечении других заболеваний. Поскольку дети чаще получают препараты этой группы, то и распространенность устойчивых штаммов Н. pylori среди них существенно выше, чем у взрослых. Так, исследование, проведенное в японских семьях, показало, что хотя члены одной семьи обычно заражены идентичными штаммами Н. pylori, резистентность к кларитромицину выше у детей [44]. В целом резистентность Н. pylori к кларитромицину возрастает пропорционально его потреблению в данном регионе [45].
В странах Восточной Европы с невысоким уровнем жизни (в том числе и в странах СНГ) первично-резистентные к нитроимидазолу штаммы Н. pylori составляют 20–40%; в России в 1998 году резистентность к метронидазолу составила почти 30%, в Москве — 36% [46]. В странах Западной Европы, по данным Европейского многоцентрового исследования, средний уровень первичной резистентности Н. pylori к метронидазолу составляет 25,6% [47].
В 1997 г. впервые сообщалось о появлении резистентных к амоксициллину штаммов Н. pylori, составивших 1,4–7% в развитых странах [48]. Устойчивость Н. pylori к бета-лактамам определяется модификацией ПСБ микроорганизмов. Описаны модификации (результат мутаций) в ПСБ-1а и ПСБ-4; поскольку гены ПСБ локализованы в бактериальной хромосоме, устойчивость в популяции Н. pylori происходит, вероятно, по клональному типу. Если за период с 1985 по 1996 год в Японии не было выявлено ни одного резистентного штамма, то в 1997 г. их доля составила 1,1%, а в 2003 г. — 1,5% [49].
В 2005 году F. Megraud [50] представил данные о резистентности Н. pylori к антибактериальным препаратам, определившие последующий выбор тех или иных схем эрадикации. Так, показатели резистентности штаммов микроорганизма к метронидазолу находятся в пределах 19–42% в странах Европы и 33–37% — в США, 9–12% — в Японии, 53% — в Бразилии и 77% — в Мексике. В отношении кларитромицина эти показатели составляют в США и Японии около 13%. В европейских странах они колеблются в широких пределах: сравнительно низки в странах Северной (4,4%) и Центральной (8,7%) Европы и, напротив, очень высокие (24%) — в странах Южной Европы. В нашей стране к 2003 г. количество штаммов Н. pylori, резистентных к метронидазолу, достигло 55,5%. Опасной можно назвать тенденцию к росту доли полирезистентных штаммов — 11,1% [50].
Исследование эффективности схемы, рекомендованной в качестве стандартной Консенсусом Маастрихт-3 в Европе (эзомепразол + кларитромицин + метронидазол) в рекомендуемых дозах продолжительностью 10 дней, проведенное нами у 20 детей с Н. pylori-ассоциированными гастродуоденальными заболеваниями, показало низкую эффективность — 14,3%. Столь низкий результат объясняется высоким уровнем резистентности Н. pylori как к кларитромицину, так и к метронидазолу. В связи с полученными неутешительными результатами, мы не можем рекомендовать эту стандартную схему к использованию в России.
С учетом локальных особенностей штаммов Н. pylori, Консенсус Маастрихт-3 внес одну очень важную поправку: если устойчивость Н. pylori к кларитромицину в популяции конкретного региона превышает 15–20%, а к метронидазолу выше 40%, эти антибактериальные препараты не должны применяться в схемах эрадикации.
При высокой эффективности квадротерапии, не является ли целесообразным ее назначение в качестве терапии первой линии, особенно в условиях высокой антибиотикорезистентности? На этот вопрос позволяет ответить метаанализ 102 исследований эрадикации, включающий 398 вариантов и 25 644 пациента, не выявивший преимуществ квадротерапии по сравнению с тройной (эффективность 80,4% и 81,1% соответственно). Аналогичные результаты были получены в североамериканском исследовании, включавшем 275 пациентов. В данном исследовании сравнивали тройную терапию: омепразол (20 мг 2 раза в сутки) + кларитромицин (500 мг 2 раза в сутки) + амоксициллин (1,0 г 2 раза в сутки), с квадротерапией: омепразол (20 мг 2 раза в сутки) + висмута бискальцитрат (120 мг 4 раза в сутки) + метронидазол (375 мг 4 раза в сутки) + тетрациклин (375 мг 4 раза в сутки). Эффективность этих схем оказалась практически одинаковой (83,2% и 87,7% соответственно). Тройные (омепразол + амоксициллин + кларитромицин) и квадротерапия (омепразол + висмут + тетрациклин + метронидазол), используемые в качестве терапии первой линии, оказались эффективными в равной степени (87% vs 86%).
Согласно нашим данным, эффективность тройной терапии с амоксициллином (омепразол + амоксициллин + метронидазол) составляет 73%, а сходной квадротерапии (омепразол + амоксициллин + метронидазол + Де-нол) — 76%. Однако совсем другие результаты были получены при использовании схем с кларитромицином. Эффективность стандартной схемы, рекомендованной Консенсусом Маастрихт-3 (эзомепразол + кларитромицин + метронидазол), составила всего 14,3%, дополнение этой же схемы Де-нолом повысило эффективность до 65%. Полученные нами данные согласуются с результатами европейского исследования, проведенного Williamson R., Pipkin G. A. [32], по мнению которых Де-нол способен преодолевать как первичную, так и вторичную антибиотикорезистентность Н. pylori. Это позволяет рекомендовать Де-нол в схемах эрадикации Н. pylori и делает целесообразным назначение этого препарата уже в ходе первой линии терапии.
В случае неэффективности схем эрадикации первой и второй линии Консенсус Маастрихт-3 предлагает практическому врачу несколько приемлемых вариантов дальнейшей терапии. Поскольку к амоксициллину в процессе его применения не вырабатывается устойчивость штаммов Н. pylori, возможно назначение его высоких доз (0,75 г 4 раза в сутки в течение 14 дней) в комбинации с высокими (4-кратными) дозами ИПП в виде двойной терапии, однако, по нашему мнению, мегадозы этих препаратов могут обернуться значительным увеличением числа побочных реакций. Другим вариантом может быть замена метронидазола в схеме квадротерапии на нитрофураны. Согласно последним российским исследованиям, наиболее приемлемы нифурател (Макмирор 15 мг/кг/сут) или нифуроксазид (Энтерофурил 200 мг 2 раза в день). Альтернативой служит применение комбинации ИПП с амоксициллином и рифабутином (300 мг в сутки) или левофлоксацином (500 мг в сутки). Попытки замены кларитромицина на другие макролидные антибиотики также предпринималась. В исследовании, проведенном в США, сравнивалась эффективность квадротерапии, включающей ИПП (лансопразол), препараты висмута, амоксициллин и кларитромицин/азитромицин. В первом случае частота эрадикации равнялась 84,6%, во втором — 55,5%. То есть по эффективности азитромицин уступает кларитромицину.
Таким образом, в России, в условиях высокой резистентности Н. pylori к кларитромицину и метронидазолу, в качестве эрадикационной терапии первой линии могут быть рекомендованы следующие схемы:
Контроль эффективности терапии (достижение эрадикации) следует проводить через 4–6 недель после окончания лечения. Для контроля целесообразно использовать неинвазивные методы, прежде всего, дыхательные (С13-углеродный тест или Хелик-тест). При отрицательном результате теста (эрадикации Н. pylori) дальнейшего лечения не требуется. При положительном результате повторная терапия проводится по другой схеме с использованием других антибиотиков, в частности, может быть назначена классическая схема второй линии — квадротерапия, включающая ИПП + Де-нол + тетрациклин (с 12 лет) + метронидазол. Если при проведении терапии первой линии не использовались нитрофураны, то вместо метронидазола оптимально назначение нифуратела или нифуроксазида.
Эрадикационную терапию как первой, так и второй линии следует дополнять назначением современных пробиотиков. Исследования, проведенные как в России, так и за рубежом, показали повышение эффективности лечения и уменьшение побочных реакций при параллельном назначении пробиотиков. В работе П. Л. Щербакова с соавт. было показано повышение процента эрадикации Н. pylori с 84% при назначении стандартной тройной схемы до 92% при параллельном приеме Линекса. Нами были изучены показатели местного и общего иммунного статуса и результативность стандартной тройной терапии (ИПП + амоксициллин + метронидазол) при параллельном назначении Бифиформа. Исследование показало повышение эффективности лечения с 73% до 84%, уменьшение побочных реакций и дисбиотических отклонений в кале. Лечение пробиотиком сопровождалось повышением уровня секреторного IgA, фагоцитарной активности, а также снижением уровня IgE в крови. В литературе имеются данные об антихеликобактерной эффективности Saccharomyces boulardii и некоторых штаммов лактобацилл На основании этого с целью профилактики хеликобактериоза можно рекомендовать йогурты с лактобациллами определенных штаммов.
Литература
За остальным списком литературы обращайтесь в редакцию.
П. Л. Щербаков*, доктор медицинских наук, профессор
В. С. Кашников**, кандидат медицинских наук
Е. А. Корниенко***, доктор медицинских наук, профессор
*Центральный НИИ гастроэнтерологии, Москва
**Ставропольская детская клиническая больница, Ставрополь
***СПбГПМА, Санкт-Петербург
Контактная информация об авторах для переписки: petersh@su29.ru.