Что принимать вместе с нимесилом для защиты желудка
Сравнительная оценка влияния нимесулида на верхние отделы желудочно-кишечного тракта
Показано, что нимесулид оказывает значительно меньшее негативное влияние на верхние отделы желудочно-кишечного тракта, чем другие неселективные нестероидные противовоспалительные препараты (диклофенак, кетопрофен и индометацин).
Nimesulide has significantly less negative impact on the upper gastrointestinal tract than other non-selective non-steroidal anti-inflammatory drugs (diclofenac, ketoprofen and indomethacin).
Нимесулид — один из наиболее популярных в России представителей группы нестероидных противовоспалительных препаратов (НПВП). Это лекарство имеет в нашей стране репутацию эффективного и достаточно безопасного анальгетика и широко используется в различных отраслях медицины (прежде всего, в ревматологии, неврологии и травматологии), в которых имеется необходимость борьбы с острой или хронической болью [1–3].
Одной из главных особенностей российского опыта применения нимесулида является нередкое использование его продолжительными курсами. В большинстве стран мира нимесулид рассматривается прежде всего как ургентное обезболивающее средство; учитывая ограничения контролирующих органов, он назначается лишь на короткое время, обычно менее двух недель [4]. В нашей стране, напротив, нимесулид часто рекомендуют больным с хроническими заболеваниями, такими как остеоартроз (ОА), ревматоидный артрит (РА) и анкилозирующий спондилоартрит (АС). При этой патологии суммарный срок приема нимесулида у российских пациентов может достигать многих месяцев и даже лет.
Такая практика дает большой материал для оценки достоинств и недостатков лекарства, прежде всего, его безопасности.
Как известно, главной проблемой НПВП является риск развития побочных эффектов со стороны желудочно-кишечного тракта (ЖКТ) и сердечно-сосудистой системы [5, 6]. При этом основным достоинством нимесулида считается хорошая гастроинтестинальная переносимость, что, собственно, определяет основное преимущество этого препарата в сравнении со многими другими НПВП [1–4, 7].
Однако четких доказательств, подтверждающих низкий риск серьезных ЖКТ-осложнений (таких как кровотечения и клинически выраженные язвы) при использовании нимесулида, относительно немного. Имеются лишь немногочисленные работы, в которых специально изучалась частота таких опасных побочных эффектов, и отдельные исследования, организованные в соответствии с жесткими современными критериями «доказательной медицины», — двойные слепые, рандомизированные и контролируемые [7–9].
В этом случае большое значение приобретает анализ частоты осложнений, которые отмечаются в реальной клинической практике. Так, в клинику ФГБУ НИИР им. В. А. Насоновой РАМН ежегодно поступает для стационарного лечения большое число пациентов с различными ревматическими заболеваниями (РЗ) — ревматоидным артритом (РА), остеоартрозом (ОА), серонегативными спондилоартритами (ССА) и др., которые в течение длительного времени принимают НПВП, в т. ч. нимесулид. В данном учреждении функционирует собственный эндоскопический кабинет, основным направлением работы которого является выявление патологии верхних отделов ЖКТ. Результаты обследования больных РЗ, которые находятся в архиве кабинета эндоскопии, позволяют получить достаточно большой материал для оценки частоты патологии верхних отделов ЖКТ, возникающей на фоне приема НПВП.
Целью настоящего исследования было оценить сравнительную частоту и характер изменений верхних отделов ЖКТ у больных РЗ, регулярно принимавших нимесулид.
Материал и методы исследования
Мы провели ретроспективный анализ результатов всех эндоскопических исследований верхних отделов ЖКТ (эзофагогастродуоденоскопия (ЭГДС)), выполненных за период 2011–2013 гг. в клинике ФГБУ НИИР им. В. А. Насоновой РАМН больным РЗ, которые не менее 1 месяца до проведения данной процедуры получали нимесулид. В качестве контроля были использованы результаты ЭГДС, проведенных в тот же период всем больным, не менее месяца получавшим другие неселективные НПВП.
Все пациенты были направлены на эндоскопическое исследование лечащими врачами в связи с наличием определенных показаний: для исключения патологии верхних отделов ЖКТ из-за наличия симптомов гастроэзофагеального рефлюкса, гастралгии или диспепсии, наличия в анамнезе язвы желудка или двенадцатиперстной кишки (ДПК), для поиска источника анемии, для проведения онкопоиска, при необходимости взятия биопсии слизистой оболочки ДПК на амилоид и др.
Критериями отбора больных для проведения анализа являлся возраст старше 18 лет и зафиксированный в медицинской документации факт регулярного использования НПВП в течение не менее 1 месяца до момента до проведения ЭГДС.
В анализ не включались данные эндоскопического исследования у больных системными РЗ, при которых поражение ЖКТ может быть проявлением висцеральной патологии: системной склеродермией, поли/дерматомиозитом, системной красной волчанкой, болезнью Бехчета и системными васкулитами. В контрольную группу также не были включены пациенты, использовавшие мелоксикам, целекоксиб и эторикоксиб; принимавшие участие (на момент проведения ЭГДС) в клинических исследованиях, в которых изучалась безопасность НПВП; направленные на ЭГДС для контроля результатов курсового лечения язвы желудка, и/или ДПК, или эрозивного эзофагита.
Суммарно за три года ЭГДС была выполнена 1048 больным, соответствующим критериям отбора и принимавшим нимесулид, а также 816 больным, использовавшим другие неселективные НПВП. Этими препаратами были в основном диклофенак, кетопрофен, индометацин, ацеклофенак и ибупрофен; лишь единичные больные регулярно принимали пироксикам, теноксикам, кеторолак или метамизол.
Клиническая характеристика больных в исследуемых группах представлена в таблице.
Как видно, большинство пациентов были женщины среднего возраста, страдавшие ревматоидным артритом. В целом исследуемые группы были сопоставимы — правда, в контрольной группе было достоверно больше пациентов, страдающих ССА (преимущественно анкилозирующим спондилоартритом). Этот факт объясняет более высокую долю лиц мужского пола в контрольной группе. Следует отметить, что больные, принимавшие нимесулид, чаще имели язвенный анамнез, чаще принимали глюкокортикоиды (ГК) и достоверно реже — ингибиторы протонной помпы (ИПП).
При анализе результатов ЭГДС мы учитывали выявление эрозий, под которыми подразумевался поверхностный дефект слизистой, не имеющий видимой глубины, и язв — локального повреждения стенки ≥ 5 мм, имеющего видимую глубину. При обнаружении менее 10 эрозий они описывались как «единичные», а при выявлении ≥ 10 — как «множественные».
Электронная база данных была создана с помощью программы Microsoft Office Excel 2007, статистический анализ проводился с помощью программы SPSS 10.0. Приведенные в статье цифровые значения представлены в виде M ± m. Для оценки значимости отличия количественных параметров использован t-тест Стьюдента, для качественных параметров — χ 2 или точный тест Фишера.
Результаты
Общее число больных с эрозиями или язвами в группе 1 составило 244 (23,3%), в группе 2 — 272 (33,3%), р 65 лет) на частоту язв желудка и/или ДПК.
Оказалось, что язвы значительно чаще выявлялись у лиц, имевших язвенный анамнез. Так, в группе 1 у больных с этим фактором риска суммарная частота язв желудка и/или ДПК оказалась 11,5%, без — 3,1% (р 65 лет, принимавших нимесулид, частота язв составила 9,9%, более молодого возраста — 3,5% (р 65 лет) частота язв была намного ниже, чем в целом по группе. Тем не менее, язвы существенно чаще выявлялись в группе 2. Так, в группе 1 у 752 больных без факторов риска язвы были выявлены лишь у 16 (2,1%), а в контрольной группе — у 48 из 568 (8,5%), р 65 лет). Так, применение ИПП было отмечено у 16,2% больных из группы 1, имевших вышеуказанные факторы риска, и лишь у 5,3% не имевших; аналогично, в группе 2 эти препараты получали 26,2% и 5,6%.
Отдельным объектом нашего анализа стала оценка частоты патологии пищевода. Эрозивный эзофагит был выявлен лишь у небольшого числа больных (в сравнении с патологией желудка и ДПК). Тем не менее, эрозивный эзофагит достоверно реже выявлялся у пациентов в группе 1 — у 15 (1,4%), в сравнении с 26 (3,1%) в группе 2, р = 0,03.
Такие факторы риска, как пожилой возраст и ГК, не ассоциировались с более высокой частотой патологии пищевода ни в группе 1, ни в группе 2. В то же время эрозивный эзофагит достоверно чаще выявлялся у пациентов в группе 2, получавших НДА (но не в группе 1). Прием бисфосфонатов оказался однозначно важным фактором риска — и в группе 1, и группе 2, при использовании этих препаратов эрозивный эзофагит определялся достоверно чаще (p
А. Е. Каратеев, доктор медицинских наук, профессор
ФГБУ НИИР им. В. А. Насоновой РАМН, Москва
Профилактика НПВС-гастропатий у больных с факторами риска желудочно-кишечных повреждений
Нестероидные противовоспалительные средства (НПВС) представляют собой одну из наиболее востребованных групп препаратов. По данным Американской ассоциации ревматологов, более 5% населения планеты используют НПВС. Однако частота повреждений верхних отделов
Нестероидные противовоспалительные средства (НПВС) представляют собой одну из наиболее востребованных групп препаратов. По данным Американской ассоциации ревматологов, более 5% населения планеты используют НПВС. Однако частота повреждений верхних отделов желудочно-кишечного тракта (ЖКТ) — эрозивно-язвенные поражения, перфорации, кровотечения — при регулярном применении этих препаратов может достигать 40% [1]. Серьезную проблему представляет применение НПВС у больных с факторами риска повреждения верхних отделов ЖКТ. Обострение язвенной болезни, эрозивный гастродуоденит или рефлюкс-эзофагит, а также указания на них в анамнезе являются противопоказаниями к применению НПВС. Однако выраженность болевого синдрома нередко заставляет проводить противовоспалительную терапию и у таких больных.
К факторам риска относят наличие эрозивно-язвенных поражений желудка и двенадцатиперстной кишки и кровотечений из верхних отделов ЖКТ в анамнезе, возраст старше 65 лет, тяжелый ревматоидный артрит, использование больших доз или одновременный прием разных НПВС, комбинацию НПВС с глюкокортикоидами, сопутствующую антикоагулянтную терапию, женский пол, наличие Нelicobacter pylori, курение [2, 3].
При наличии факторов риска предлагаются различные подходы для определения тактики ведения больных.
При наличии двух и более факторов риска частота осложнений терапии НПВС возрастает, что оправдывает выбор двух профилактических тактик одновременно, например применение селективных ингибиторов ЦОГ-2 и ИПП. Количество больных с патологией верхнего отдела ЖКТ, нуждающихся в терапии НПВС, достаточно велико, что и явилось причиной для проведения настоящего исследования.
Целью работы явилась оценка эффективности, переносимости и безопасности применения препарата найз (нимесулид) в дозировке 100 мг 2 раза в день в течение 4 нед для лечения заболеваний суставов и позвоночника (остеоартрита, остеоартроза и остеохондроза) у больных с сопутствующими эрозивно-язвенными поражениями верхних отделов ЖКТ в стадии ремиссии/умеренного обострения на фоне профилактической терапии препаратом омез (омепразол) в дозировке 20 мг 2 раза в сутки.
Задачи исследования сводились к следующему:
Критериями включения в исследование служили:
В исследование не включались пациенты:
Найз (таблетки по 100 мг) назначался в дозе 100 мг 2 раза в день. Продолжительность лечения составляла 28–35 дней — в зависимости от выраженности обострения патологии суставов. В период исследования не допускался прием других НПВС, анальгетиков и глюкокортикостероидов. Одновременно с найзом назначался омез в дозе 20 мг 2 раза в день на весь период приема препарата.
Перед назначением комбинированной терапии диагноз неврологической, ревматологической патологии был верифицирован невропатологом, ревматологом с применением достаточных диагностических процедур. С учетом гастроэнтерологического анамнеза, проводили эзофагогастродуоденоскопию (ЭГДС) до и после курса лечения. До и после окончания терапии проводилось изучение общего и биохимического (билирубин, аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), гамма-глютаматтранспептидаза (гамма-ГТ), щелочная фосфатаза) анализов крови.
Субъективная оценка эффективности лечения состояла в выборе пациентом одного из следующих показателей: значительное улучшение; улучшение; отсутствие эффекта; ухудшение.
Субъективная оценка переносимости — выбор одного из следующих показателей: хорошая, удовлетворительная, плохая.
Объективная оценка проводилась врачом на основании динамики клинических, лабораторных и инструментальных показателей. Позитивная динамика двух-трех показателей считалась значительным улучшением, одного-двух — улучшением. Неэффективным лечение признавалось при отсутствии динамики показателей. Преобладание отрицательной динамики расценивалось как ухудшение.
Оценка безопасности применения основывалась на сопоставлении результатов: общего и биохимического анализов крови до и после лечения; ЭГДС до и после лечения. Появление эрозивно-язвенных повреждений слизистой или ухудшение исходного состояния слизистой расценивались как побочный эффект, связанный с приемом найза.
Всего в исследовании приняли участие 30 больных (14 мужчин, 16 женщин) в возрасте от 22 до 70 лет (средний возраст составил 53,7 ± 3,0 года). Болевой синдром был вызван остеохондрозом различных отделов позвоночника у 18 из них, остеоартрозом различных суставов — у 10, ревматоидным полиартритом — у 2 пациентов.
Для оценки симптоматики заболеваний суставов и позвоночника использовался ряд показателей, частота и характеристики которых представлены в таблице 1.
Что касается функциональной недостаточности, у 4 пациентов отмечена нулевая степень, у 13 — I степень, у 11 — II степень, у 2 — III степень.
Все пациенты имели отягощенный гастроэнтерологический анамнез.
В связи с необходимостью назначения противовоспалительной терапии всем больным до лечения проводилась ЭГДС.
Cреди пациентов с язвенной болезнью двенадцатиперстной кишки в анамнезе (9 больных) к моменту начала противовоспалительной терапии более 2/3 имели эрозивно-язвенные поражения. У 4 больных с обострением язвенной болезни двенадцатиперстной кишки и 1 больного с обострением язвенной болезни желудка лечение найзом было начато на фоне рубцующихся язвенных дефектов. При эрозивных гастритах и бульбитах, в связи с болями в позвоночнике или суставах, терапию найзом проводили, не дожидаясь заживления эрозий. Кроме того, у 5 больных при эндоскопическом исследовании был обнаружен рефлюкс-эзофагит (у 4 — катаральный, у 1 — эрозивный I степени).
Результаты исследования
Динамика клинических проявлений. Основной причиной назначения противовоспалительной терапии являлся болевой синдром, связанный с патологией позвоночника и суставов. Динамика основной симптоматики под влиянием терапии найзом представлена в таблице 2.
Функциональная недостаточность на фоне проводимой терапии характеризовалась следующим образом: 0 степень отмечалась до лечения у 4 пациентов, после лечения — у 19; I степень — у 13 до лечения и у 9 — после терапии; II степень — у 11 до и у 2 — после, III степень — у 2 до и ни у одного — после лечения.
Таким образом, курсовое лечение найзом приводило к достоверному уменьшению интенсивности болей при движении и пальпации, сокращению длительности утренней скованности и степени функциональной недостаточности.
Динамика лабораторных данных. В рамках оценки безопасности применения лекарственного средства проводилось исследование общего и биохимического анализов крови до и после лечения. Результаты представлены в таблице 3.
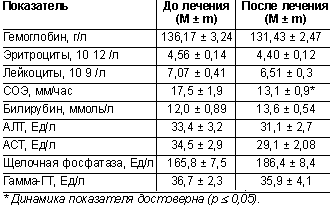 |
| Таблица 3. Результаты изучения лабораторных данных до и после лечения |
Приведенные данные демонстрируют отсутствие динамики лабораторных показателей, что свидетельствует о безопасности применения найза в использованных дозах в течение 28 дней. Достоверное снижение СОЭ отражает уменьшение воспалительной реакции после терапии.
Динамика эндоскопической картины. Из 4 пациентов с язвенной болезнью двенадцатиперстной кишки, принятых в исследование с остаточными язвами, заживление наблюдалось у 3 человек. В одном случае появилась острая язва луковицы двенадцатиперстной кишки и эрозивный эзофагит III степени. У 3 пациентов с язвенной болезнью двенадцатиперстной кишки в анамнезе, исходно имевших эрозивный бульбит и эрозивный гастрит, отмечалось заживление эрозий на фоне лечения. У 1 из 2 больных, к началу исследования имевшего рубцово-язвенную деформацию луковицы двенадцатиперстной кишки и поверхностный гастрит, появился эрозивный эзофагит II степени, состояние слизистой оболочки желудка и двенадцатиперстной кишки не изменилось. Обращает на себя внимание тот факт, что появление эрозивного эзофагита манифестировало появлением изжоги и отмечалось у больных в возрасте 70 лет.
У пациентов с язвенной болезнью желудка в анамнезе наблюдали заживление остаточного язвенного дефекта (1 больной) и эрозивного гастрита (1 больной).
В группе больных с эрозивным антральным гастритом в анамнезе, заживление эрозий наблюдали у 8 из 10 человек, однако у одного из них на фоне заживления эрозий возник эрозивный эзофагит I степени. У оставшихся 2 пациентов ухудшения состояния слизистой оболочки желудка отмечено не было. Ни у одного из 7 больных с эрозивным антральным гастритом в анамнезе, имевших на момент включения в исследование очаговый антральный гастрит, ухудшения состоянии слизистой оболочки не отмечено.
У 2 больных с резекцией 2/3 желудка (по поводу язвенной болезни двенадцатиперстной кишки) повреждений слизистой оболочки верхних отделов ЖКТ после терапии найзом обнаружено не было, более того, у пациентки с исходным эрозивным эзофагитом I степени при контрольном исследовании отмечена эпителизация эрозии пищевода.
Таким образом, отрицательная эндоскопическая динамика при использовании комбинированной терапии наблюдалась у 3 больных (10%) в виде эрозивного эзофагита I–III степени, и в одном случае сочеталась с появлением острых язв луковицы двенадцатиперстной кишки. При этом все эти пациенты отметили появление изжоги.
Оценка эффективности, безопасности и переносимости терапии. Субъективная оценка эффективности состояла в выборе пациентом одного из следующих показателей: значительное улучшение, улучшение, отсутствие эффекта, ухудшение. Субъективная оценка переносимости предполагала выбор больным одного из следующих показателей: хорошая, удовлетворительная, плохая. Значительное улучшение отметили 8 больных, улучшение — 22; хорошая переносимость наблюдалась у 26 пациентов, удовлетворительная — у 4.
Эффективность комбинированной терапии получила высокую оценку: улучшение отметили 73,3% больных, значительное улучшение — 26,7%. Переносимость была охарактеризована пациентами как хорошая в 86,6% и как удовлетворительная в 13,3% случаев. Удовлетворительную оценку лечению дали 3 человека в связи с появлением рефлюкс-эзофагита, которые отметили появление изжоги и тошноты, у одного пациента отмечались сухость во рту и тошнота. Следует отметить, что наблюдаемые побочные эффекты были выражены слабо, возникали на 2–4-й день лечения и не привели к отмене препарата.
Объективная оценка результатов лечения проводилась врачом на основании динамики клинических, лабораторных и инструментальных показателей. Позитивная динамика двух-трех показателей считалась значительным улучшением, одного-двух — улучшением. Неэффективным лечение признавалось при отсутствии динамики показателей. Преобладание отрицательной динамики расценивалось как ухудшение. Значительное улучшение отмечено у 8 больных, улучшение — у 22.
Врачебная оценка эффективности противовоспалительного действия найза совпадала с оценкой эффективности по данным пациентов.
Оценка безопасности применения основывалась на сопоставлении результатов общего и биохимического анализов крови до и после лечения; ЭГДС до и после лечения. Появление эрозивно-язвенных повреждений или ухудшение исходного состояния слизистой оболочки желудка и двенадцатиперстной кишки расценивалось как побочный эффект, связанный с приемом найза.
Динамика общего и биохимического анализов крови у всех пациентов отсутствовала. Исключение составило уменьшение СОЭ после лечения, что свидетельствовало о снижении воспаления.
Появление эрозивных повреждений слизистой оболочки пищевода наблюдали у 3 больных, в одном случае — в сочетании с появлением острой язвы двенадцатиперстной кишки. Таким образом, применение комбинированной терапии для лечения заболеваний суставов и позвоночника (остеоартрита, остеоартроза и остеохондроза) у больных с сопутствующими эрозивно-язвенными поражениями верхних отделов ЖКТ было безопасным в 90% случаев.
Основным повреждающим фактором НПВС является снижение локального синтеза простагландинов. Последние клинические и экспериментальные данные указывают на то, что традиционные НПВС замедляют заживление пептических язв, влияя на действие ростовых факторов, снижая пролиферацию эпителиальных клеток и ангиогенез в крае язвы, замедляя созревание грануляционной ткани [10]. Применение селективных ингибиторов ЦОГ-2 также приводит к замедлению заживления желудочных язв, сравнимому с таковым при использовании традиционных НПВС [10]. Появляются сообщения о гастроинтестинальных кровотечениях, об эзофагитах, возникших при использовании селективных ингибиторов ЦОГ-2 [5, 6].
По результатам наших собственных исследований были выявлены три случая появления эрозивного эзофагита I–III степени, и в одном случае он развивался в сочетании с острыми язвами двенадцатиперстной кишки. Причины неэффективности препарата омез у этих больных могут быть следующими: больные резистентны к действию омеза, т. е. являются non-responders; подавление кислотной продукции было адекватным, но сопровождалось нарушениями моторики верхних отделов ЖКТ, как при гастроэзофагеальной рефлюксной болезни, видимо, с рефлюксом желчи в пищевод и развитием эрозивного эзофагита. Вторая причина представляется более вероятной у 2 больных в возрасте 70 лет, первая причина — у пациента 53 лет.
При появлении жалоб на изжогу, тошноту необходимо провести эндоскопическое исследование верхних отделов ЖКТ и суточной рН-метрии на фоне терапии омезом. Сохранение кислотной продукции в этой ситуации должно привести к пересмотру кислотосупрессивной терапии. При адекватном подавлении желудочной секреции будет оправданным добавление к терапии прокинетиков, сукральфата или магалфила в обычных дозах.
В заключение хотелось бы отметить, что лечение найзом в сочетании с омезом у больных с поражением опорно-двигательного аппарата и сопутствующей патологией желудка и двенадцатиперстной кишки в стадии обострения приводило к улучшению основной (в 100% случаев) и сопутствующей (в 90% случаев) патологии ЖКТ. 10% больных имели осложнения (эрозивный эзофагит, острая язва луковицы двенадцатиперстной кишки).
При появлении или усугублении изжоги, боли в эпигастральной области, тошноты больным, принимающим НПВС, показана ЭГДС для решения вопроса о дальнейшей тактике ведения пациента, возможности дальнейшей терапии НПВС. Следует также учитывать, что соответствия между клиническими проявлениями НПВС-гастропатии и эндоскопическими «находками» не существует, поэтому эндоскопический контроль, особенно в ранние сроки лечения (первые 1–2 мес), является обязательным и адекватным методом профилактики тяжелых осложнений.
Использование комбинированной терапии найз + омез для лечения заболеваний суставов и позвоночника (остеоартрита, остеоартроза и остеохондроза) возможно у больных с сопутствующими эрозивно-язвенными поражениями верхних отделов ЖКТ и множественными факторами риска развития гастроинтестинальных побочных эффектов НПВС. При этом НПВС-гастропатия развивается в 3 раза реже, чем при использовании неселективных НПВС.
По вопросам литературы обращайтесь в редакцию.
О. Н. Минушкин, доктор медицинских наук, профессор
Л. В. Масловский, кандидат медицинских наук, доцент
В. М. Леонов
МЦ УД Президента РФ, Москва
Поражение органов пищеварения у пациентов, принимающих нестероидные противовоспалительные препараты: факторы риска, тактика ведения
Представлена сравнительная характеристика нестероидных противоспалительных препаратов (НПВП). Рассмотрены применение НПВП в клинической практике, побочные эффекты их применения, методы диагностики поражения верхних отделов желудочно-кишечного тракта и так
The comparative characteristic of non-steroid anti-flammation preparations (NPVP) are presented. The application of NPVP in the clinical practice, side effects of their application, methods of the upper divisions of gastrointestinal tract affection diagnostics and tactics of conducting patients, taking NPVP are examined.
Благодаря широкому спектру показаний нестероидные противовоспалительные препараты (НПВП) стали популярным классом лекарственных средств и на сегодняшний день являются лидерами по продажам в аптечной сети.
По данным проведенного в Европе опроса НПВП назначают 82% врачей общей практики и 84% ревматологов. В России в 2007 г. было продано 105,8 млн упаковок НПВП [1]. Самостоятельное потребление НПВП пациентами в 7 раз превышает объем врачебных назначений [1]. С учетом масштаба применения НПВП, вопросы их эффективного использования и безопасности данной терапии чрезвычайно актуальны.
Сравнительная характеристика нестероидных противоспалительных препаратов
Класс НПВП представлен примерно 20 различными по химической структуре препаратами: производными салициловой, индоловой, гетероарилуксусной, энолиоковой и других кислот, имеющими общие фармакологические эффекты. Основной механизм фармакологического действия всех НПВП заключается в блокаде фермента циклооксигеназы (ЦОГ), регулирующего биотрансформацию арахидоновой кислоты в простагландины (ПГ), простациклин (ПГI2) и тромбоксан А2 (ТхА2). Ингибиция ЦОГ-2 рассматривается как один из важных механизмов противоспалительной и анальгетической активности данного класса препаратов (рис.).
Применение НПВП в клинической практике
В клинической практике НПВП применяются в ряде ситуаций [1–3].
1. Ургентное обезболивание и купирование лихорадки при:
2. Комплексное анестезиологическое пособие.
3. Купирование боли при заболеваниях опорно-двигательной системы.
Перспективно использования НПВП в практике онкологов. Эффективность НПВП в профилактике развития и рецидивов злокачественных новообразований желудочно-кишечного тракта (ЖКТ) хорошо обоснована теоретически и подтверждена данными эпидемиологических и когортных наблюдательных исследований. Длительное применение НПВП (сулиндак, целекоксиб) позволяет снизить темпы прогрессирования заболевания при семейном аденоматозном полипозе и уменьшить риск рецидивов спорадических аденоматозных полипов толстой кишки. НПВП являются эффективным средством для купирования хронической боли у онкологических больных. Имеются данные, свидетельствующие об эффективности НПВП в качестве дополнительного компонента традиционной химиотерапии.
Побочные эффекты применения НПВП
Терапевтические эффекты, обусловленные ингибированием различного типа ЦОГ (табл. 1), сопряжены с развитием ряда побочных эффектов.
Подавление активности ЦОГ-1 ассоциируется с высокой частотой поражения ЖКТ. Подавление ЦОГ-2-зависимого синтеза ПГ I2-клетками сосудистого эндотелия при отсутствии влияния на контролируемый ЦОГ-1 синтез ТхА2-тромбоцитами на фоне применения селективных НПВП обусловливает высокий риск развития тромбоэмболических осложнений. Помимо этого регистрируются и другие класс-специфические побочные эффекты (табл. 2).
Патология органов пищеварения, ассоциированная с приемом НПВП
Прием НПВП, в первую очередь неселективных в отношении ЦОГ-1, ассоциируется с широким спектром поражения органов пищеварения, от функциональных нарушений до тяжелой органической патологии, способной привести к летальному исходу. Прием селективных НПВП, напротив, сопряжен с высоким риском тромбоэмболических осложнений. Возможно поражение любого отдела ЖКТ — от полости рта до прямой кишки. Различные желудочно-кишечные симптомы (изжога, тошнота, рвота, тяжесть в эпигастрии, гастралгии) испытывают от 10% до 40% больных, при эзофагогастродуоденоскопии (ЭГДС) гастропатии (эрозии, язвы) регистрируется у 15–30% обследованных, тяжелые осложнения в виде прободений, перфораций, кровотечений — у 0,5–3%, поражение тонкой, толстой кишки, печени отмечается у 1–5% пациентов, принимающих НПВП.
Особенностью НПВП-ассоциированных язв являются следующие характеристики:
Риск желудочно-кишечных кровотечений становится максимальным при приеме большинства НПВП к 84-му дню лечения, а для индометацина — в течение первых 7 дней (T. Lee, 2007).
Негативное влияние на ЖКТ не ограничивается только верхними отделами. В последние годы все большее внимание уделяется проблеме лекарственного поражения тонкой кишки, прежде всего т. н. НПВП-энтеропатии. Эта патология характеризуется нарушением проницаемости кишечной стенки с экссудацией белка и диапедезом эритроцитов, приводящей к железодефицитной анемии и гипоальбуминемии, а также повреждению слизистой оболочки с развитием эрозий, язв и их осложнений — кровотечения и перфорации, появлением циркулярных стриктур и нарушением проходимости ЖКТ.
Бессимптомное повышение трансаминаз отмечается у 1–5% больных, регулярно принимающих НПВП, серьезные гепатотоксические реакции отмечаются в 1 случае на 10 000 больных, регулярно принимающих НПВП (U. Boelsterli и соавт., 2002; A. Walker, 1997). Патогенез этой патологии неизвестен. Определенную роль могут играть: поражение митохондрий гепатоцитов, как результат блокады ферментных систем цикла Кребса и разобщения окислительного фосфорилирования, блокада фосфодиэстеразы, нарушение экскреции желчи вследствие образования комплексов с желчными кислотами и энтерогепатической рециркуляции НПВП, иммуногенетические нарушения и др. Поражение печени — редкая, но потенциально угрожающая жизни патология, связанная с приемом НПВП, имеющая характер метаболической или иммунологической идиосинкразии.
Методы лабораторной и инструментальной диагностики патологии ЖКТ
Основными методами диагностики поражения верхних отделов желудочно-кишечного тракта является ЭГДС, которую в группах риска необходимо провести в первый месяц от начала лечения. Вспомогательное значение может иметь исследование кала на скрытую кровь чувствительным методом.
Проведение диагностических мероприятий для выявления патологии тонкой кишки показано больным, регулярно принимающим НПВП, в случае наличия у них клинических симптомов (диарея, метеоризм, абдоминальная боль), признаков кишечного кровотечения или железодефицитной анемии, гипоальбуминемии. Для диагностики поражения слизистой тонкой кишки используют эндоскопические методы, позволяющие визуализировать тощую и подвздошную кишку — энтероскопию, для диагностики стриктур — энтерографию с контрастным веществом, для диагностики воспаления — кал на кальпротектин. Обязательным является исследование кала на скрытую кровь высокочувствительными методами (иммунохимический метод или тест на трансферрин и гемоглобин в кале).
С целью диагностики гетатотоксических реакций необходим мониторинг биохимических показателей печени (табл. 3).
Тактика ведения пациентов, получающих НПВП
При ведении пациентов, получающих НПВП, необходимо:
При наличии факторов риска необходимо проведение соответствующей профилактики. При риске ЖКТ-осложнений назначаются ингибиторы протонной помпы, при кардиоваскулярном риске — низкие дозы ацетилсалициловой кислоты.
Динамическое наблюдение за пациентами с различной степенью риска гастропатий [1]
1. Степень риска гастропатий отсутствует.
Если факторов риска нет, но длительность приема НПВП составляет более 4 недель, следует назначить селективные НПВП + ингибиторы протонной помпы (ИПП).
Контроль за нежелательными эффектами. Необходимые исследования: общий анализ крови (ОАК), определение уровней АЛТ, АСТ, креатинина; контроль артериального давления (АД) — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах; оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите. При появлении признаков патологии ЖКТ необходимо провести эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь чувствительным методом, кал на кальпротектин.
Лечебная тактика. Возможно назначение неселективных НПВП: ацеклофенак, диклофенак, ибупрофен, кетопрофен (2-я линия: индометацин, пироксикам, напроксен) или могут быть назначены селективные НПВП.
В группах риска применение ИПП должно продолжаться на протяжении всего курса лечения НПВП или низкими дозами Аспирина.
2. Риск умеренный.
Имеется 1 фактор риска (пожилой возраст без дополнительных факторов риска (нет тяжелой сопутствующей патологии), или прием кортикостероидов, или курение и прием алкоголя, или инфицированность Н. рylori, или диспепсия в анамнезе).
Контроль за нежелательными эффектами. Необходимые исследования: ОАК, определение уровней АЛТ, АСТ, креатинина; контроль АД — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах; оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите, при появлении признаков патологии ЖКТ необходимо эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь чувствительным методом, кал на кальпротектин; дополнительно ЭГДС через 1 месяц после начала приема НПВП, при появлении признаков НПВП-гастропатий определить наличие Н. рylori любым методом в соответствии со стандартами, общий анализ крови 1 раз в месяц.
Лечебная тактика. Может назначаться любой селективный НПВП или неселективный НПВП + ИПП (следует стремиться к назначению НПВП в малых дозах, коротким курсом).
3. Риск высокий.
Имеется 1 фактор риска (язвенный анамнез, или прием Аспирина, или тяжелая сопутствующая патология).
Контроль за нежелательными эффектами. Необходимые исследования: ОАК, определение уровней АЛТ, АСТ, креатинина; контроль АД — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах, оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите, при появлении признаков патологии ЖКТ — эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь чувствительным методом, кал на кальпротектин; дополнительно: ЭГДС через 1 месяц после начала приема НПВП, при появлении признаков НПВП-гастропатий определить наличие Н. рylori любым методом в соответствии со стандартами, общий анализ крови 1 раз в месяц.
Лечебная тактика. Назначить по выбору: селективный НПВП + ИПП (стремиться к назначению в малых дозах, коротким курсом).
4. Риск очень высокий.
У пациента есть язвы, осложненные кровотечением или перфорацией в анамнезе, или часто рецидивирующие язвы, или комбинация двух факторов риска и более.
Контроль за нежелательными эффектами. Необходимые исследования: ОАК, определение уровней АЛТ, АСТ, креатинина; контроль АД — перед лечением, через 3 недели от начала лечения, затем 1 раз в 3 месяца при непрерывном приеме в средних и высоких дозах, оценка субъективных жалоб (со стороны ЖКТ, отеки и т. д.) при каждом визите. При появлении признаков патологии ЖКТ необходимо эндоскопическое исследование (ЭГДС, колоноскопия, капсульная эндоскопия), кал на скрытую кровь, кал на кальпротектин; дополнительно: ЭГДС через 1 месяц после начала приема НПВП, при появлении признаков НПВП-гастропатий определить наличие Н. рylori любым методом в соответствии со стандартами, общий анализ крови 1 раз в месяц.
Лечебная тактика: назначить селективный НПВП + ИПП. У лиц с язвенным анамнезом и лиц, получающих препараты, влияющие на свертываемость крови, использование селективных НПВП без ИПП не является эффективным методом профилактики гастропатий и осложнений. В группах риска применение ИПП должно продолжаться на протяжении всего курса лечения НПВП или низкими дозами Аспирина.
При сочетании ЖКТ-факторов риска и кардиоваскулярных осложнений следует назначить селективный НПВП + ацетилсалициловую кислоту + ИПП.
Тактика ведения пациентов с различным сердечно-сосудистым риском в настоящей статье не рассматривается.
При приеме нимесулида контроль показателей, отражающих состояние печени (АЛТ, АСТ, щелочной фосфатазы), необходимо осуществлять 1 раз в месяц.
Лечение язв, ассоциированных с приемом НПВП [1, 4]
Прекращение приема НПВП само по себе не приводит к рубцеванию язв, но может повышать эффективность противоязвенной терапии.
Ингибиторы протонной помпы (40 мг в сутки омепразола (Омез®), или рабепразола, или 60 мг лансопразола) являются основным средством лечения гастродуоденальных язв и эрозий, превосходящими по лечебному действию Н2-гистаминоблокаторы и мизопростол (уровень доказательности рекомендаций А). Длительность курсовой терапии при локализации небольших язв в двенадцатиперстной кишке должна быть не менее 4–6 недель, а при больших размерах и локализации язв в желудке — 8–12 недель. Эффективность противоязвенной терапии может быть повышена комбинацией ИПП с препаратами висмута (уровень доказательности рекомендаций С).
С профилактической целью в группах риска используются ИПП (20 мг в сутки омепразола (Омез®) или рабепразола или 30 мг лансопразола) на протяжении всего приема любых НПВП, включая низкие дозы Аспирина.
Лечение НПВП-энтеропатий
Подходы к медикаментозному лечению НПВП-энтеропатии не разработаны. Применение ИПП не уменьшает риск развития НПВП-энтеропатии. Использование селективных НПВП снижает риск развития или рецидива патологии тонкой кишки. По сравнению с неселективными НПВП селективные НПВП существенно безопаснее в плане развития НПВП-энтеропатии. По некоторым данным, прием сульфасалазина и коллоидного субцитрата висмута способствовал уменьшению кровопотери при приеме НПВП. Одновременное назначение НПВП и сульфасалазина в дозе 2 г/сутки редуцировало увеличенную проницаемость кишечного эпителия, индуцированную приемом индометацина (J. Hayllar, 1994). Дополнительное назначение метронидазола в дозе 400 мг 2 раза в сутки 7 дней способствовало редукции изменений кишечной проницаемости, вызванной приемом индометацина (G. Davies, 1993).
Особенности применения нимесулида
Один из наиболее популярных в России селективных НПВП — нимесулид (Найз®). Эффективность нимесулида подтверждена длительным периодом (более 20 лет) клинического использования. Немаловажно, что генерики нимесулида в нашей стране по цене доступнее других представителей группы селективных НПВП.
Продемонстрировано преимущество нимесулида перед другими НПВП по быстроте действия и выраженности анальгетического эффекта. Благодаря своим биохимическим особенностям, нимесулид легко попадает в область воспаления (в частности, в пораженные суставы при артрите), накапливаясь в большей концентрации, чем в плазме крови. Через 30 мин после перорального приема концентрация препарата в крови достигает
50% от пиковой и отмечается отчетливый обезболивающий эффект. Через 1–3 ч наступает пик концентрации препарата и, соответственно, развивается максимальное анальгетическое и противовоспалительное действие.
Молекула нимесулида в отличие от многих других представителей лекарственной группы НПВП имеет свойства основания. Это затрудняет ее проникновение в слизистую верхних отделов ЖКТ, тем самым уменьшая возможность контактного раздражения слизистой желудка и развития диспепсии. Нимесулид в целом лучше переносится, чем неселективные НПВП. На сегодняшний день отсутствуют данные метаанализа о безопасности нимесулида, как и ряда других селективных НПВП, в отношении серьезных осложнений со стороны ЖКТ [5].
Все НПВП, включая селективные, способны вызывать эндоскопическое поражение ЖКТ, развитие тяжелых ЖКТ-осложнений.
При наличии факторов риска, к которым относится пожилой возраст, наличие соматической патологии и др. использование только селективных НПВП недостаточно профилактики гастропатий и ЖКТ-осложнений. Назначение ингибиторов протонной помпы требуется на весь период лечения НПВП.
В каждом случае выбор нимесулида, как препарата для длительного применения, должен сопровождаться тщательным анализом факторов риска и последующим активным контролем нежелательных эффектов.
Противопоказанием для назначения являются: наличие эрозивно-язвенных изменений слизистой оболочки желудка и двенадцатиперстной кишки, активное кровотечение, воспалительные заболевания кишечника, нарушения свертывания крови, печеночная почечная недостаточность, активное заболевание печени или сопутствующее применение любых потенциально гепатотоксичных средств.
У лиц с язвенным анамнезом и лиц, получающих препараты, влияющие на свертываемость крови, использование нимесулида необходимо на фоне сопутствующего приема ИПП. Применение нимесулида у больных с хроническими заболеваниями сердечно-сосудистой системы, как и других НПВП, возможно только на фоне их эффективной медикаментозной коррекции. В силу обсуждаемой проблемы гепатотоксических осложнений, нимесулид, как и все НПВП, не следует назначать больным с хроническими заболеваниями печени, сопровождающимися нарушением функции, или лицам, имеющим в анамнезе лекарственные гепатотоксические реакции.
Таким образом, во всех клинических ситуациях, даже если планируется кратковременное применение препаратов в низких дозах, выбор НПВП должен осуществляться индивидуально, исходя из фармакологических особенностей препарата, клинической ситуации и наличия факторов риска появления нежелательных эффектов. Врач должен осуществлять контроль за нежелательными эффектами. Пациенту также должна быть предоставлена необходимая информация о возможных нежелательных эффектах и методах самоконтроля в процессе лечения.
Литература
* ГБОУ ВПО ОмГМА МЗ РФ, Омск
** ГБОУ ВПО НГМУ МЗ РФ, Новосибирск
_575.gif)
.gif)
.gif)
_575.gif)
.gif)