Чем лечат кандидозный вульвовагинит
Что такое вульвовагинит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Долго-Сабурова Ю. В., гинеколога со стажем в 27 лет.
Определение болезни. Причины заболевания
Вульвовагинит (от лат. vulva — наружные половые органы и vagina — влагалище) — воспалительное заболевание слизистой оболочки наружных половых органов и влагалища. Это одна из самых частых акушерско-гинекологических патологий. В ряде случаев возникают изолированные поражения только слизистой оболочки наружных половых органов (вульвит) или влагалища (вагинит).
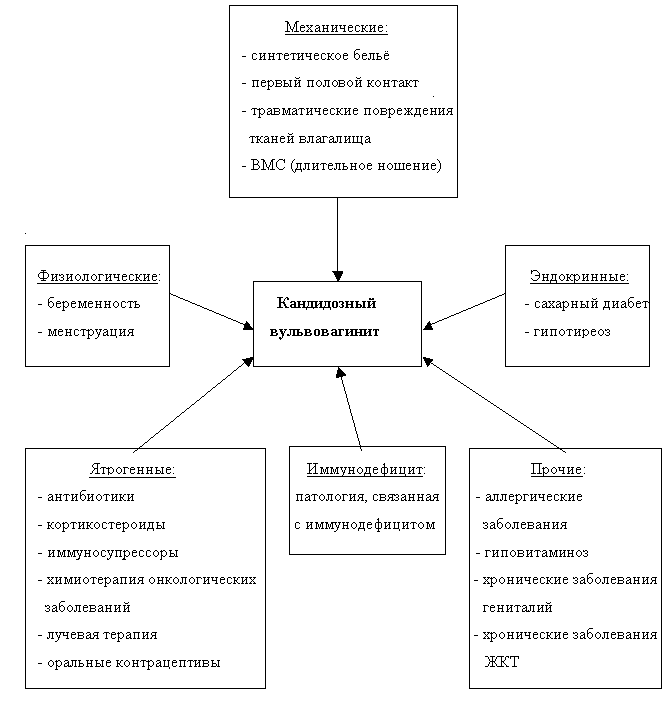
Причиной воспаления могут быть любые агрессивные факторы, которые способствуют повреждению эпителия слизистой оболочки:
Также можно выделить ряд факторов, которые способствуют нарушению внутренней среды организма, гормонального баланса и равновесия во взаимодействии иммунной системы и микробиоты человека. К ним относят:
На возникновение вульвовагинита оказывают влияние психосоматические нарушения и сексуальная неудовлетворённость. Частая смена половых партнёров достоверно увеличивает риск заболеваемости.
Также имеет значение и способ контрацепции: при использовании внутриматочных и химическых контрацептивов частота вульвовагинитов возрастает.
Ещё одним немаловажным фактором возникновения воспалительных заболеваний вульвы и влагалища является гигиеническая агрессия:
Также отрицательно влияет ношение тесной, многослойной одежды, синтетического нижнего белья, окрашенного дешёвыми красителями. [6] [7]
Симптомы вульвовагинита
Причины вульвовагинита многообразны, чего нельзя сказать о симптомах.
Клинические проявления нескольких случаев вульвовагинита, вызванных разными причинами, могут быть очень похожи. Они представляют собой пять признаков воспаления:
На практике женщины с вульвовагинитом обычно предъявляют жалобы на зуд, жжение, отёчность, покраснение, болезненность наружных половых органов.
Нарушение функции выражается в том, что болезненными или невозможными будут любые попытки пенетрации — половой контакт, осмотр врача, даже введение лекарств. Также повреждённые слизистые оболочки могут трескаться, на них могут появляться эрозии и язвочки.
Моча, попадающая на воспалённую слизистую оболочку вульварного кольца, может вызывать болезненные ощущения. [1] [9] [10]
Выделения из влагалища
Очень часто в первом ряду жалоб при вульвовагинитах упоминают влагалищные выделения. В среднем в 70% случаев визиты к гинекологам связаны с жалобами на выделения из половых путей. Но всегда ли вагинальные выделения являются признаком воспаления? Нет, далеко не всегда.
В норме слизистые оболочки влагалища и шейки матки половозрелой женщины могут продуцировать от 15 до 70 мл жидкости. Количество вагинально-цервикального секрета зависит от анатомических особенностей и гормонального фона женщины, её возраста, фазы цикла, характера питания, интенсивности физической нагрузки, сексуальной активности, метода контрацепции и многих других причин. Например, многие женщины замечают, что после окончания очередной менструации выделений совсем немного, а вот в середине цикла и ближе к менструации количество выделений может быть значительным.
Выделения в середине цикла, как правило, прозрачные, или чуть белесоватые, или желтоватые, густые, тягучие. Это – слизь из шейки матки, выработка которой сопровождает процесс овуляции. Иногда в этих выделениях можно заметить прожилки крови или даже наблюдать небольшие кровотечения. Это нормально. В этот период наиболее вероятно зачатие.
В последнюю неделю перед менструацией можно заметить бело-желтовато-сероватые густые выделения, похожие на мазь или хлопья (иногда возникают «творожистые» выделения). В таком случае многие женщины пугаются, подозревая, что у них возникла «молочница». Хотелось бы предостеречь от поспешных выводов. Нередко такие выделения возникают в связи с активным слущиванием (отслаиванием) поверхностных слоёв эпителия слизистой оболочки влагалища. Это происходит под воздействием определённого уровня эстрогена и прогестерона, характерных для секреторной (второй) фазы менструального цикла. Именно в этот момент необходимо «прислушаться» к своему организму, вспомнив про пять признаков воспаления: если вы ощущаете зуд, боль, жжение, припухлость, болезненность при половом контакте (т.е. любой дискомфорт), то вероятность того, что у вас вульвовагинит очень высока. В этом случае необходим осмотр гинеколога. Если же никаких симптомов воспаления нет, а есть только выделения, то с визитом к гинекологу можно и повременить, особенно в том случае, когда Вы были у врача пару месяцев назад.
Если возникли сомнения по поводу своего состояния, можно воспользоваться тестами для определения рН влагалища. Нормальные показатели рН 4,0-4,5 в сочетании с отсутствием дискомфортных ощущений говорят о том, что беспокоиться не о чем. [11] Понаблюдайте за собой, отметьте в календаре дни, когда у вас появляются и исчезают эти выделения. Это поможет лучше узнать своё тело.
Если появился дискомфорт (а выделений может, кстати, и не быть), то визит к врачу лучше не откладывать. Пока будете ожидать приёма, попытайтесь вспомнить, не было ли каких-нибудь событий, которые могли спровоцировать воспаление — половой контакт, использование нового гигиенического средства или белья, приём антибиотиков в ближайшие 2-3 месяца.
Патогенез вульвовагинита
Патогенез вульвовагинита основан на формировании локального воспаления в результате повреждения слизистой оболочки и гибели клеток эпителия.
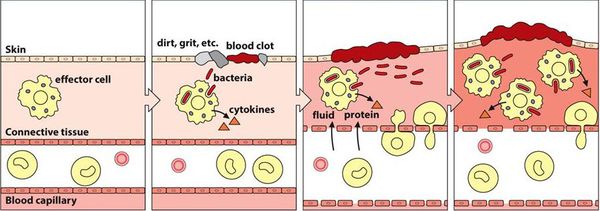
Воспалительная реакция — основа врождённой иммунологической защиты. Из повреждённых клеток в межклеточное пространство попадают различные ферменты и биологически активные вещества, которые способствуют усилению кровотока, расширению капилляров и увеличению их проницаемости. Из сосудов в очаг воспаления проникает жидкость. Таким образом, в месте повреждения возникает отёк, покраснение и повышение температуры.
Кроме жидкости из сосудов приходят лейкоциты, которые активируются за счёт тех же ферментов и биологически активных веществ. Они начинают выделять медиаторы воспаления и провоспалительные цитокины, которые действуют на сосуды и клетки иммунной системы и ещё больше усиливают воспаление.
Многие биологически активные вещества могут раздражать и повреждать нервные окончания и рецепторы, что вызывает различную гамму ощущений — от лёгкого жжения и покалывания до зуда и, наконец, сильной боли.
В самом начале статьи был приведён длинный список факторов, способствующих повреждению. Основной причиной повреждения являются различные инфекции. Но даже если изначально повреждение было неинфекционным (например, слизистая оболочка была подвергнута воздействию механического или химического фактора), микроорганизмы быстро активизируются и вызывают гораздо более бурное течение воспалительного процесса. Лейкоциты начинают фагоцитировать (пожирать) микроорганизмы, в результате чего активируется и привлекается ещё больше лейкоцитов. Далее всё будет зависеть от того, какая из противоборствующих сторон будет сильнее — повреждающие факторы или защитные.
Следует отметить, что особенности реакции воспаления очень индивидуальны и во многом генетически обусловлены. [8]
Классификация и стадии развития вульвовагинита
По причинному фактору вульвовагиниты подразделяют на две основные группы: первично-инфекционные и первично-неинфекционные.
Кандидозный вульвовагинит
В последние годы отмечается значительный рост и распространение вульвовагинального кандидоза. Распространение эндокринной патологии, растущая частота антибиотикотерапии, назначения цитостатиков в повседневной врачебной практике, широкое применение гормо
В последние годы отмечается значительный рост и распространение вульвовагинального кандидоза. Распространение эндокринной патологии, растущая частота антибиотикотерапии, назначения цитостатиков в повседневной врачебной практике, широкое применение гормональных методов контрацепции, использование вагинальных тампонов, гигиенических прокладок — все это предрасполагает к заболеваниям нижних отделов половой системы, обусловленных дрожжеподобными грибами рода Candida. 75–80% женщин переносят в течение жизни хотя бы один эпизод вульвовагинального кандидоза, а у 40–45% развивается по крайней мере один рецидив. 5% женщин во всем мире страдают рецидивирующим вульвовагинальным кандидозом, для которого характерно три или более эпизодов обострения инфекции в течение года. В связи с широкой рекламой в средствах массовой информации разнообразных антимикотических средств, их доступностью в аптечной сети в настоящее время весьма распространено самолечение, которое приводит к длительно текущим рецидивирующим формам вульвовагинального кандидоза из-за применения однократных коротких курсов терапии [1–8].
В 54–76% случаев возбудителем вульвовагинального кандидоза является Candida albicans, в других случаях обнаруживают C. glabrata, C. tropicalis, C. guillermondii, C. parapsilosis, C. kefir [1–8].
Выделим три основных фактора защиты макроорганизма, препятствующих развитию вульвовагинального кандидоза.
– фагоцитозом, осуществляемым макрофагами и нейтрофилами;
– Т-лимфоцитами разных популяций;
– антителами — иммуноглобулинами всех классов.
Основная роль антител в защите от инфекции заключается в блокировании Candida рецепторов и литических ферментов возбудителя.
К развитию вульвовагинального кандидоза может приводить изменение гормонального фона за счет: повышения содержания гликогена в эпителиоцитах; сдвигов рН; прямого стимулирующего действия эстрогенов на рост грибов, повышения авидности вагинального эпителия к грибам, что способствует их лучшей адгезии; угнетения механизмов иммунной защиты.
Так, во время беременности вульвовагинальный кандидоз развивается в 30–40% случаев, что обусловлено изменениями гормонального баланса во время беременности, накоплением гликогена в эпителиальных клетках в связи с увеличением количества эстрогенов, иммуносупрессивным действием высокого уровня прогестерона в сыворотке крови.
Другим примером может являться использование контрацептивов с большим количеством эстрогенов, которые повышают эффективность связывания дрожжеподобных грибов с эпителиальными клетками влагалища.
Одним из основных факторов риска является антибиотикотерапия, причем не только пероральное и парентеральное применение препаратов, но и местное их использование.
Различные состояния, приводящие к угнетению иммунной системы макроорганизма, например гиповитаминозы, хронические заболевания, травмы, операции, прием антибиотиков, цитостатиков, лучевая терапия, также могут способствовать развитию вульвовагинального кандидоза.
Некоторые работы предрасполагают к экзогенному заражению грибами: на заводах по переработке овощей, фруктов, производству антибиотиков, белково-витаминных препаратов и других биологически активных веществ [5].
В развитии кандидозной инфекции выделяются следующие этапы:
При вульвовагинальном кандидозе псевдомицелий проникает в глубь эпителия. На этом уровне инфекция может персистировать длительное время, так как устанавливается динамическое равновесие между грибами, которые не могут проникнуть в более глубокие слои слизистой оболочки, и макроорганизмом, который сдерживает такую возможность, но не способен полностью элиминировать возбудитель. Нарушение этого равновесия приводит либо к обострению заболевания, либо к выздоровлению, либо к ремиссии.
Выделяют три формы вульвовагинального кандидоза.
Кандиданосительство. Жалоб и выраженной клинической картины заболевания нет. При микробиологическом исследовании в отделяемом влагалища обнаруживают в небольшом количестве почкующиеся формы дрожжеподобных грибов при отсутствии в большинстве случаев псевдомицелия. Кандиданосительство может переходить в клинически выраженную форму.
Острая форма вульвовагинального кандидоза. Длительность заболевания не превышает 2 мес. В клинической картине преобладают выраженные признаки местного воспаления вульвы: гиперемия, отек, выделения, зуд и жжение.
Хроническая форма вульвовагинального кандидоза. Длительность заболевания составляет более 2 мес, при этом на слизистых оболочках вульвы и влагалища выражены инфильтрация, лихенизация, атрофия.
В зависимости от состояния вагинального микроценоза классифицируют три формы Candida-инфекции влагалища.
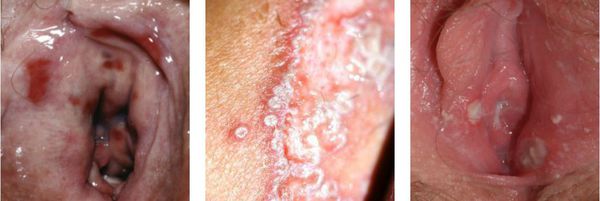
В клинике патогномоничным симптомом вульвовагинального кандидоза являются творожистые налеты серо-белого цвета, с кислым запахом, точечные или 5–7 мм в диаметре, иногда сливающиеся между собой. Очаги резко отграничены, округлых или овальных очертаний, как бы вкраплены в слизистую оболочку вульвы и влагалища, налеты содержат массы размножающихся грибов Candida.
В острой стадии заболевания творожистые пленки «сидят» плотно, снимаются с трудом, обнажая эрозированную поверхность, в дальнейшем — легко. За счет их отторжения появляются густые беловатые творожистые выделения. Слизистая оболочка в области поражения имеет выраженную склонность к кровоточивости, а по периферии очага интенсивно гиперемирована.
Зуд чаще беспокоит больных во время менструации, после физических нагрузок. В некоторых случаях могут отмечаться чувство жжения, некоторая болезненность при мочеиспускании.
Резкая боль, жжение, как правило, беспокоят пациенток при половых контактах, что может приводить к формированию невротического синдрома.
Микроскопическое исследование позволяет определить наличие гриба, его спор, мицелия, количество лейкоцитов [1–8].
Для видовой идентификации гриба обязательно культуральное исследование. В настоящее время продолжаются разработки методов полимеразной цепной реакции, которые также позволят устанавливать видовую принадлежность.
Лечение показано только при наличии клинической картины заболевания, подтвержденной микроскопически и культурально.
Существующие лекарственные формы современных антимикотиков предполагают два пути проникновения препаратов в кровь: пероральный, со всасыванием в кишечнике, и внутривенный. При вульвовагинальном кандидозе преимущественно используется первый путь.
На всасывание препарата и на распределение его в организме во многом оказывает влияние растворимость. Так, флуконазол является водорастворимым и поэтому быстро и почти полностью всасывается, а в крови существует преимущественно в свободной форме. Последнее обусловливает хорошее распределение в жидких средах организма: содержание препарата в ликворе приближается к плазменной концентрации. Флуконазол слабо метаболизируется печенью и выводится почками, в основном в неизмененном виде, поэтому при снижении клубочковой фильтрации его выведение замедляется, и доза препарата при этом должна быть снижена.
Другие системные антимикотики, используемые в терапии вульвовагинального кандидоза, являются липофильными, они не растворимы в воде. Лучше всех в кишечнике всасывается тербинафин. Итраконазол и кетоконазол хорошо всасываются в кислой среде, поэтому у больных с ахлоргидрией абсорбция может оказаться сниженной.
Липофильные препараты в крови находятся преимущественно в несвободной, связанной с белками плазмы форме. Поэтому их содержание в разных жидких средах незначительно.
Липофильные препараты хорошо накапливаются в тканях, особенно богатых липидами, в частности в печени, селезенке, жировой ткани, в кожном сале. Это свойство, а также кератофильность (способность связываться с кератином эпидермиса) используются в лечении. Жировая ткань служит депо для липофильных ферментов: в ней они концентрируются и из нее медленно высвобождаются в кровь.
Интенсивной биотрансформации подвергаются все липофильные препараты. Быстрый метаболизм кетоконазола, итраконазола и тербинафина с эффектом первого прохождения через печень может существенно снижать их концентрации. Как правило, образующиеся метаболиты неактивны. Биотрансформация, происходящая при участии микросомальных ферментов печени, ускоряется препаратами — индукторами этих ферментов (например, рифампицином, дифенином). Выведение липофильных препаратов происходит с калом (азолы) и мочой (тербинафин), в виде метаболитов и реже в неизмененной форме.
В последние годы наиболее часто предлагаются схемы лечения с использованием флуконазола. Это препарат азольного ряда, с широким спектром противогрибкового действия, являющийся синтетическим производным бис-триазола. Как и другие препараты группы азолов, флуконазол угнетает образование эргостерола, основного компонента мембраны грибов, действуя на фермент 14-α-деметилазу, входящий в систему цитохрома P450. Нарушение биосинтеза мембраны обусловливает фунгистатический эффект препарата, а в ходе перекисного окисления и других процессов приводят к гибели клетки гриба. В отличие от других азольных препаратов флуконазол обладает высокой специфичностью по отношению к зависимым от цитохрома Р450 ферментам грибов. Поэтому при использовании флуконазола не наблюдается побочное действие на синтез стероидов и другие метаболические процессы, связанные с Р450. Среди грибов рода Candida наиболее чувствительными к флуконазолу являются C. albicans, а также C. tropicalis, C. parapsilosis, чувствительными считают штаммы C. krusei, в меньшей степени C. glabrata.
При лечении кандидоза следует учитывать вид возбудителя. Как правило, определять чувствительность к препарату до начала лечения кандидоза не требуется, если заболевание вызвано C. albicans. Устойчивость штаммов C. albicans может развиваться при хронических формах заболевании, у ВИЧ-инфицированных. При кандидозе, вызванном другими видами Candida, следует определить чувствительность до лечения.
Флуконазол растворим в воде, быстро и полностью всасывается в желудочно-кишечном тракте. В кровь попадает более 90% от принятой внутрь дозы. Одновременный прием пищи, а также желудочная кислотность не влияют на абсорбцию препарата. Концентрации в плазме напрямую зависят от дозы. Пиковые концентрации достигаются в течение 1–2 ч. Механизм действия флуконазола связан с нарушением образования эргостерина из ланостерина. Флуконазол ингибирует цитохром Р450-зависимые ферменты грибковой клетки. В настоящее время выпускается флуконазол в таблетках (Микофлюкан), капсулах и в виде раствора для внутривенных инфузий (Флюкостат).
При вульвовагинальном кандидозе показано применение флуконазола по 150 мг перорально однократно. При рецидивирующей форме заболевания флуконазол назначают перорально 150 мг с повторным назначением через 3 дня, затем флуконазол назначают по 150 мг в неделю перорально в течение 6 мес.
У беременных оправдано применение натамицина (Пимафуцин). Натамицин — противогрибковый антибиотик из ряда полиенов-макролидов, продуцируемый актиномицетом Streptomyces natalensis. Механизм действия препарата сходен с таковыми у других полиеновых антибиотиков: натамицин связывается с эргостеролом, нарушая проницаемость мембраны. Вагинальные свечи Пимафуцин назначаются на ночь, в течение 3–6 сут. Исследования подтвердили высокую эффективность и надежность Пимафуцина при лечении беременных
При остром вульвовагинальном кандидозе могут быть использованы местные формы азоловых препаратов: клотримазол в виде вагинальных таблеток по 100 мг на ночь интравагинально глубоко в течение 6 дней; эконазол в виде суппозиториев интравагинально глубоко в течение 14 дней на ночь [4]; итраконазол — вагинальные таблетки 200 мг — интравагинально глубоко в течение 10 дней [3].
Ко многим из существующих местных препаратов для лечения вульвовагинального кандидоза в настоящее время нередко развивается резистентность [6–8].
Основные механизмы устойчивости грибов связаны с тем, что:
В исследованиях in vitro было показано, что существует синергизм между некоторыми антимикотическими препаратами, позволяющий преодолеть проблему перекрестной резистентности. В результате исследования этих взаимодействий стало возможным создание принципиально нового антимикотического препарата — сертаконазола. Сертаконазол — противогрибковый препарат нового поколения «двойных классов». Препарат содержит два синергичных класса в одной молекуле: азоловую и бензотиафеновую группу. Сертаконазол обладает фунгицидным, фунгистатическим действием, блокирует диморфную трансформацию грибов, обладает широким спектром действия, характеризуется высокой комплаентностью. При этом имидазоловая часть молекулы обеспечивает нарушение биосинтеза эргостерола, вмешательство на уровне цитохром Р450-зависимого фермента 14а, ингибирует рост грибов, обеспечивает фунгистатический механизм. Бензотиафеновая структура замещает триптофан в мембране гриба, что приводит к разрушению и гибели гриба, т. е. осуществляется фунгицидное действие. Местное использование сертаконазола (суппозитории Залаин) позволяет повысить эффективность терапии вульвовагинального кандидоза. Схема лечения предусматривает однократное назначение препарата.
При необходимости (выраженности субъективных ощущений, снижения дозы препарата из-за беременности или сопутствующего заболевания и т. п.) антимикотическая терапия кандидозного вульвовагинита может быть дополнена неспецифическими средствами. К ним относятся: 10–20% раствор буры в глицерине, растворы марганцовокислого калия 1 : 5000, нитрата серебра 1 : 2000. Эти препараты не обладают ни фунгицидным, ни фунгистатическим свойством, а лишь способствуют максимальному удалению мицелиальных форм гриба из крипт влагалища, а также нарушению прикрепления гриба к стенке влагалища и торможению его размножения.
Поскольку нередко наблюдается сочетанная инфекция, обусловленная дрожжеподобными грибами и различными бактериями, в последние годы применяют комплексные препараты, к которым относится, в частности, Макмирор комплех (1 вагинальный суппозиторий содержит 10 г нифуратела и 200 000 ЕД нистатина).
При вульвовагинальном кандидозе Макмирор назначают по 1 свече перед сном в течение 10 дней. При применении препарата возможны местные аллергические реакции. Макмирор противопоказан при беременности и лактации.
Обоснована комбинация антимикотических средств с метронидазолом. Метронидазол обладает антибактериальным, противопротозойным, трихомонацидным действием, воздействует на простейшие грамотрицательные анаэробные бактерии, грамположительные анаэробные палочки и кокки, подавляя в них синтез ДНК и РНК, вызывая их деградацию. Вагинальные суппозитории Нео-пенотран содержат (1 доза) 100 мг миконазола и 500 мг метронидазола. Вагинальные таблетки Клион Д 100 (1 доза) содержат 100 мг миконазола и 100 мг метронидазола.
Литература
И. В. Хамаганова, доктор медицинских наук, профессор
РГМУ, Москва
Кандидозный вульвовагинит (патогенез, клиника, диагностика, современные принципы терапии).
А.Л.Тихомиров, доктор медицинских наук, профессор, Ч.Г.Олейник
Кандидозный вульвовагинит – инфекционное поражение слизистой вульвы и влагалища, вызываемое дрожжеподобными грибами рода Candida. Поражает, как правило, женщин репродуктивного возраста, реже встречается у девушек и женщин в периоде пери- и постменопаузы.
Значительное учащение случаев кандидозного вульвовагинита обусловлено действием ряда предрасполагающих факторов.
При назначении антибиотиков широкого спектра действия необходимо учитывать, что они подавляют не только патогенные бактерии, но и находящиеся во влагалище лактобациллы, являющиеся физиологическими антагонистами дрожжеподобных грибов (лактобациллы подавляют прикрепление Candida к клеткам эпителия и их размножение). В результате рН влагалищного содержимого увеличивается (сдвигается в щёлочную сторону), процесс самоочищения влагалища нарушается. Кроме того, Candida обладают способностью использовать антибиотики в качестве источников питания. При этом создаются благоприятные условия для активного размножения Candida в половых органах женщины.
Хорошо известен и факт развития кандидозного вульвовагинита при беременности. Первый эпизод кандидозного вульвовагинита отмечается у многих женщин именно во время беременности. Частота кандидозного вульвовагинита у беременных достигает 40-46% (Horowitz B.J.,1991). Такая высокая частота обусловлена изменениями гормонального баланса во время беременности. Наиболее высокая степень колонизации отмечается в последнем триместре и у первородящих.
Кандидозный вульвовагинит – одна из болезней современной цивилизации. Развитию кандидозного вульвовагинита способствует ношение белья из синтетических тканей, плотно облегающего тело, в результате чего создаётся микроклимат с повышенной влажностью и температурой, что приводит к мацерации рогового слоя кожи, возникновению термостатных условий для развития местной микрофлоры, в том числе и кишечной, где среди грибов C.albicans составляет свыше 95% (Антоньев А.А., 1985). Вирулентность C.albicans увеличивается в условиях повышенной влажности (потливости). Поэтому ношение тесного синтетического нижнего белья, подмывание душем под напором, использование спреев, применение прокладок являются триггером развития реакции гиперчувствительности и предрасполагают к колонизации Candida.
Обычно кандидоз возникает эндогенно как следствие дисметаболических расстройств и дисфункции иммунной системы. Возможно также заражение половым путём, хотя эта точка зрения всё ещё остаётся дискутабельной (несмотря на то, что партнёры могут быть носителями одного и того же штамма возбудителя).
Патогенез кандидозного вульвовагинита сложен и недостаточно изучен. Учитывая тот факт, что штаммы C.albicans, выделенные у больных кандидозным вульвовагинитом и у носителей, существенно не различаются по ряду биохимических характеристик можно сделать заключение о ведущей роли состояния макроорганизма в развитии кандидозного вульвовагинита, а не свойств возбудителя. Триггером развития заболевания является не изменение свойств гриба, а снижение резистентности организма хозяина.
В развитии кандидозной инфекции различают следующие этапы:
В этой последовательности отражены все этапы развития тяжёлого кандидоза, однако в более лёгких случаях инфекция может стабилизироваться на одном из этих этапов.
При кандидозном вульвовагините инфекционный процесс затрагивает чаще только поверхностные слои эпителия влагалища. В силу существующего на этом уровне динамического равновесия между микроорганизмами (грибами), которые стремятся, но не могут проникнуть в более глубоко расположенные слои слизистой оболочки, и макрорганизмом, который пытается, но не способен полностью элиминировать возбудитель – инфекция может персистировать десятки лет. А сдвиги этого равновесия могут привести либо к обострению заболевания, либо к ремиссии или выздоровлению.
В настоящее время различают 3 клинические формы кандидозного вульвовагинита:
2) острая форма кандидозного вульвовагинита
3) хронический (рецидивирующий) кандидозный вульвовагинит.
Хронический кандидозный вульвовагинит характеризуется длительностью заболевания более 2 месяцев. А на коже и слизистых оболочках вульвы и влагалища преобладают вторичные элементы в виде инфильтрации, лихенизации и атрофичности тканей.
После завершения курса лечения, несмотря на отрицательные результаты культурального исследования, эрадикация микрорганизма может быть неполной. Это может привести к возникновению рецидивов, причём этиологическую роль в их развитии обычно играет тот же штамм. Рецидивирующий кандидозный вульвовагинит определяется как четыре или более обострения заболевания, доказанных микологически, в течение 12 месяцев. Развивается примерно у 5% пациенток с кандидозным вульвовагинитом. При этом у 50% женщин с рецидивирующим кандидозным вульвовагинитом симптомы заболевания появляются в интервале от нескольких дней до 3 мес. после успешного излечения острой формы.
Клинические проявления кандидоза разнообразны и зависят от характера предшествующих заболеваний, стадии патологического процесса, сопутствующей микробной флоры и т.д. Для генитального кандидоза характерны следующие клинические симптомы: обильные или умеренные творожистые выделения из влагалища, зуд и жжение в области наружных половых органов, усиление зуда во второй половине дня, во время сна, после водных процедур, полового акта, длительной ходьбы, во время менструации, неприятный запах, усиливающийся после половых контактов.
Существуют ситуации когда происходит инвазия паренхиматозных органов псевдогифами с развитием в них микроабсцессов. В этом случае наступает диссеминированный или генерализованный кандидоз, который отличается торпидностью течения и характеризуется выраженной реакцией со стороны всех систем организма вовлечённых в процесс.
Диагностика кандидозного вульвовагинита должна быть комплексной.
Ведущая роль в диагностике кандидозного вульвовагинита наряду с клиническими симптомами принадлежит микробиологическим методам исследования (микроскопия мазков вагинального отделяемого и культуральный метод исследования), диагностическая ценность которых достигает 95% (Анкирская А.С., 1995).
Микроскопическое исследование является одним из наиболее доступных и простых методов диагностики. Исследование проводят в нативных и окрашенных по Граму препаратах.
В последние годы применяют методы экспресс-диагностики, которые в минимально короткие сроки, с довольно высокой точностью позволяют выявить штаммы гриба, при помощи готовых тест-систем с благоприятными средами для роста грибов. Использование экспресс-диагностики является весьма перспективным, оно не требует много времени, не сложно в использовании, однако их результаты не позволяют судить о сопутствующей флоре.
При тяжёлых, рецидивирующих формах кандидозного вульвовагинита, сопровождающихся нарушениями в иммунной системе, возможно определение титров антител к грибам рода Candida в сыворотке крови. Но этот метод исследования практически не применяется из-за высокой частоты ложноотрицательных и ложноположительных результатов.
Кольпоскопический метод диагностики не является специфическим. Он выявляет изменения эпителия, характерные для воспалительного процесса, но не позволяет определить этиологию заболевания.
В зависимости от концентрации дрожжеподобных грибов рода Candida и характера сопутствующей микрофлоры в вагинальном биотопе выделяют 3 формы Candida-инфекции влагалища:
1) бессимптомное носительство
2) истинный кандидоз (высокая концентрация грибов сочетается с высокой концентрацией лактобацилл)
3) сочетанная форма бактериального вагиноза с кандидозным вульвовагинитом (грибы вегетируют при подавляющем преобладании облигатных анаэробов).
Такая нозологическая дифференциация целесообразна с точки зрения выбора рациональной этиотропной терапии.
Несмотря на бурное развитие фармакологической индустрии, огромный выбор антимикотических препаратов, проблема лечения кандидозного вульвовагинита не теряет свою актуальность. Учитывая высокую частоту заболевания, длительное течение, частое рецидивирование процесса можно предположить, что вероятнее всего в основе лежит необоснованный подход к диагностике и лечению данного заболевания. Таким образом, необходимость разработки новых схем терапии кандидозного вульвовагинита с привлечением уже известных антимикотических препаратов, адекватного спектра действия, с одновременным воздействием непосредственно на возбудитель и на все возможные системные резервуары дрожжеподобных грибов для исключения возможных рецидивов, является важной задачей.
Терапия кандидозного вульвовагинита зависит от клинической формы заболевания.
Основной целью лечения кандидозного вульвовагинита является прежде всего эрадикация возбудителя.
В соответствии с классификацией Страчунского Л.С. (1994) для лечения кандидозного вульвовагинита в настоящее время используются следующие основные противогрибковые препараты:
Обычно диагноз кандидозного вульвовагинита устанавливается достаточно легко, и большая часть пациенток излечивается местным применением противогрибковых препаратов. Но традиционное интравагинальное лечение нередко оказывается нерегулярным и сопряжено с такими побочными действиями как раздражение и чувство жжения во влагалище, учащённое мочеиспускание. Этим обусловлена плохая приверженность лечению. Женщины нередко прекращают лечение по мере исчезновения симптомов заболевания, тогда как эрадикация возбудителя не происходит. В то же время надо учитывать что в период развития клинических проявлений кандидозного вульвовагинита кандидная колонизация кишечника достоверно выше. Для эрадикации кишечного резервуара могут быть использованы неабсорбируемые пероральные антимикотики.
Общей рекомендацией по лечению осложнённых форм кандидозного вульвовагинита является удлинение терапевтической схемы (при использовании местных форм продолжительность лечения возрастает вдвое, при использовании препаратов для системного воздействия рекомендуется повторный приём той же дозы через неделю при однократном назначении и т.д.).
Таким образом, для уменьшения вероятности развития рецидивов врач должен всегда применять системный подход к диагностике и лечению заболевания с воздействием одновременно как на возбудитель, так и на все возможные резервуары дрожжеподобных грибов.
Учитывая, что беременность является главным предрасполагающим фактором развития кандидозного вульвовагинита, особой проблемой является его лечение при беременности. Главным требованием в этой ситуации является безопасность лечения. По данным различных авторов, при беременности не установлена необходимость в более продолжительных курсах лечения. Предпочтение следует отдавать местному лечению.
Из всего арсенала антимикотиков, существующих на сегодняшний день, широкое применение в лечении кандидозного вульвовагинита нашли препараты, относящиеся к новому классу триазольных соединений и содержащие в своём составе флуконазол, например микомакс.
Флуконазол [a-2,3-дифлуорофенил)- a-(1Н-1,2,4-триазол-1-илметил)-1Н-1,2,4-триазол-1-этанол], 150 миллиграмм. Флуконазол высокоактивен в отношении Candida albicans и лишь около 3-5% штаммов Candida albicans резистентны к флуконазолу или имеют промежуточную чувствительность. Candida krusei и отдельные штаммы Candida glabrata резистентны к флуконазолу. К флюконазолу могут быть устойчивы и Saccharomyces cerevisiae.
Следует отметить увеличение эффективности лечения кандидозного вульвовагинита примерно на 10-12% после двухкратного применения флуконазола (одна доза 150 мг 1 раз в 5-6 дней) по сравнению с однократным приёмом, эффективность достигает 94-95%.
Флуконазол оказывает хороший профилактический эффект при рецидивирующем кандидозе. Он хорошо переносится. Возможное осложнение – лёгкий, быстро проходящий желудочно-кишечный дискомфорт (менее 2%), ещё реже наблюдается головная боль и кожные высыпания.
Применение флуконазола у беременных и кормящих нецелесообразно для лечения кандидозного вульвовагинита, так как возможный риск для плода превышает показания.
Пимафуцин выпускается в различных лекарственных формах: кишечнорастворимые таблетки по 100 мг, влагалищные свечи по 100 мг, 2% крем.
К натамицину чувствительны большинство патогенных дрожжеподобных грибов, особенно C.albicans.
Натамицин связывает стеролы клеточных мембран, нарушая их целостность и функцию, что приводит к гибели микроорганизмов. Натамицин практически не абсорбируется из ЖКТ. Он не токсичен и не оказывает аллергизирующего действия. Натамицин в таблетках, благодаря кишечнорастворимой оболочке, действует только в кишечнике. Резистентности к натамицину в клинической практике не встречается.
Пимафуцин не оказывает тератогенного действия (при назначении его беременным в дозе 100 мг/сут), в связи с чем возможно его применение во время беременности (даже в I триместре) и в период лактации.
Для лечения кандидозного вульвовагинита или вульвовагинита смешанного генеза как небеременных, так и беременных и кормящих женщин можно рекомендовать комбинированный препарат для местного применения, с низкой системной абсорбцией – тержинан. В состав этого препарата входит: тернидазол – производное имидазола – действующий на анаэробный компонент микрофлоры влагалища; неомицин сульфат – антибиотик широкого спектра действия из группы аминогликозидов, действие которого направлено на грамположительные и грамотрицательные бактерии; нистатин – противогрибковый антибиотик из группы полиенов, высокоактивен в отношении грибов рода Candida; преднизолон – глюкокортикоид, оказывает выраженное противовоспалительное действие (позволяет быстро купировать в острой стадии признаки воспаления – гиперемию, боль, зуд и т.д.).
На сегодняшний день тержинан является одним из немногих местных препаратов, обладающих широким спектром действия за счёт удачно подобранной комбинации составных частей.
Учитывая особенности кандидозной инфекции, а также фармакодинамики и фармакокинетики вышеизложенных антимикотиков нами была разработана нижеприведенная схема лечения кандидозного вульвовагинита и оценена её клиническая эфективность. Проведено клинико-микробиологическое обследование 56 пациенток в возрасте от 18 до 49 лет с кандидозным вульвовагинитом, подтверждённый микроскопическим и культуральным методами исследования. Улучшение состояния большинство пациенток отметили уже на 3-4 день лечения. Микологическая санация и полное клиническое выздоровление были достигнуты у 53 (94,6%) пациенток.
Предлагаемая схема включает препараты с различными точками приложения, воздействуя одновременно на различные этапы жизнедеятельности и метаболизма возбудителя, а также на все возможные системные резервуары дрожжеподобных грибов.
Гино-Травоген – 1 вагинальный суппозиторий глубоко во влагалище на ночь 1-ый день
Пимафуцин (per os) по 100 мг 4 раза в день – 10 дней с 2-го дня лечения
Предложенная схема лечения кандидозного вульвовагинита имеет высокую эффективность, быстро купирует симптомы, уменьшает процент рецидива, способствует повышению эффективности терапии этого широко распространённого гинекологического заболевания. Частое рецидивирование заболевания после проведения антимикотического лечения различными препаратами позволяет рекомендовать данную комплексную терапию для лечения как острого, так и хронического рецидивирующего кандидозного вульвовагинита у небеременных и некормящих женщин.
Для лечения кандидозного вульвовагинита беременных женщин из выше упомянутых препаратов возможно применение:
При наличии у полового партнёра баланита, болезненности до и после коитуса, рекомендовано лечение препаратом мифунгар в виде крема, который наносится тонким слоем 2-3 раза в сутки.
Вопросы лечения генитального кандидоза представляют собой большие трудности и вследствие того, что чаще всего кандидоз – это не заболевание, передающееся половым путём, а маркер неблагополучия в организме (иммунодефицитные состояния, дисгормональные нарушения и др.). В связи с этим, паралельно с антимикотической терапией, необходимо проводить коррекцию состояний, приводящих к развитию кандидозного вульвовагинита.
Несмотря на предложенные схемы лечения кандидозного вульвовагинита выбор лекарственного средства, в каждом конкретном случае, должен зависеть от тяжести клинического течения заболевания, наличия микстинфекции и сопутствующих заболеваний. Только такой комплексный подход к данной проблеме позволит повысить эффективность лечения кандидозного вульвовагинита снижая частоту и процент рецидивирования данного заболевания.
Что такое вульвовагинит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Долго-Сабурова Ю. В., гинеколога со стажем в 27 лет.
Определение болезни. Причины заболевания
Вульвовагинит (от лат. vulva — наружные половые органы и vagina — влагалище) — воспалительное заболевание слизистой оболочки наружных половых органов и влагалища. Это одна из самых частых акушерско-гинекологических патологий. В ряде случаев возникают изолированные поражения только слизистой оболочки наружных половых органов (вульвит) или влагалища (вагинит).
Причиной воспаления могут быть любые агрессивные факторы, которые способствуют повреждению эпителия слизистой оболочки:
Также можно выделить ряд факторов, которые способствуют нарушению внутренней среды организма, гормонального баланса и равновесия во взаимодействии иммунной системы и микробиоты человека. К ним относят:
На возникновение вульвовагинита оказывают влияние психосоматические нарушения и сексуальная неудовлетворённость. Частая смена половых партнёров достоверно увеличивает риск заболеваемости.
Также имеет значение и способ контрацепции: при использовании внутриматочных и химическых контрацептивов частота вульвовагинитов возрастает.
Ещё одним немаловажным фактором возникновения воспалительных заболеваний вульвы и влагалища является гигиеническая агрессия:
Также отрицательно влияет ношение тесной, многослойной одежды, синтетического нижнего белья, окрашенного дешёвыми красителями. [6] [7]
Симптомы вульвовагинита
Причины вульвовагинита многообразны, чего нельзя сказать о симптомах.
Клинические проявления нескольких случаев вульвовагинита, вызванных разными причинами, могут быть очень похожи. Они представляют собой пять признаков воспаления:
На практике женщины с вульвовагинитом обычно предъявляют жалобы на зуд, жжение, отёчность, покраснение, болезненность наружных половых органов.
Нарушение функции выражается в том, что болезненными или невозможными будут любые попытки пенетрации — половой контакт, осмотр врача, даже введение лекарств. Также повреждённые слизистые оболочки могут трескаться, на них могут появляться эрозии и язвочки.
Моча, попадающая на воспалённую слизистую оболочку вульварного кольца, может вызывать болезненные ощущения. [1] [9] [10]
Выделения из влагалища
Очень часто в первом ряду жалоб при вульвовагинитах упоминают влагалищные выделения. В среднем в 70% случаев визиты к гинекологам связаны с жалобами на выделения из половых путей. Но всегда ли вагинальные выделения являются признаком воспаления? Нет, далеко не всегда.
В норме слизистые оболочки влагалища и шейки матки половозрелой женщины могут продуцировать от 15 до 70 мл жидкости. Количество вагинально-цервикального секрета зависит от анатомических особенностей и гормонального фона женщины, её возраста, фазы цикла, характера питания, интенсивности физической нагрузки, сексуальной активности, метода контрацепции и многих других причин. Например, многие женщины замечают, что после окончания очередной менструации выделений совсем немного, а вот в середине цикла и ближе к менструации количество выделений может быть значительным.
Выделения в середине цикла, как правило, прозрачные, или чуть белесоватые, или желтоватые, густые, тягучие. Это – слизь из шейки матки, выработка которой сопровождает процесс овуляции. Иногда в этих выделениях можно заметить прожилки крови или даже наблюдать небольшие кровотечения. Это нормально. В этот период наиболее вероятно зачатие.
В последнюю неделю перед менструацией можно заметить бело-желтовато-сероватые густые выделения, похожие на мазь или хлопья (иногда возникают «творожистые» выделения). В таком случае многие женщины пугаются, подозревая, что у них возникла «молочница». Хотелось бы предостеречь от поспешных выводов. Нередко такие выделения возникают в связи с активным слущиванием (отслаиванием) поверхностных слоёв эпителия слизистой оболочки влагалища. Это происходит под воздействием определённого уровня эстрогена и прогестерона, характерных для секреторной (второй) фазы менструального цикла. Именно в этот момент необходимо «прислушаться» к своему организму, вспомнив про пять признаков воспаления: если вы ощущаете зуд, боль, жжение, припухлость, болезненность при половом контакте (т.е. любой дискомфорт), то вероятность того, что у вас вульвовагинит очень высока. В этом случае необходим осмотр гинеколога. Если же никаких симптомов воспаления нет, а есть только выделения, то с визитом к гинекологу можно и повременить, особенно в том случае, когда Вы были у врача пару месяцев назад.
Если возникли сомнения по поводу своего состояния, можно воспользоваться тестами для определения рН влагалища. Нормальные показатели рН 4,0-4,5 в сочетании с отсутствием дискомфортных ощущений говорят о том, что беспокоиться не о чем. [11] Понаблюдайте за собой, отметьте в календаре дни, когда у вас появляются и исчезают эти выделения. Это поможет лучше узнать своё тело.
Если появился дискомфорт (а выделений может, кстати, и не быть), то визит к врачу лучше не откладывать. Пока будете ожидать приёма, попытайтесь вспомнить, не было ли каких-нибудь событий, которые могли спровоцировать воспаление — половой контакт, использование нового гигиенического средства или белья, приём антибиотиков в ближайшие 2-3 месяца.
Патогенез вульвовагинита
Патогенез вульвовагинита основан на формировании локального воспаления в результате повреждения слизистой оболочки и гибели клеток эпителия.
Воспалительная реакция — основа врождённой иммунологической защиты. Из повреждённых клеток в межклеточное пространство попадают различные ферменты и биологически активные вещества, которые способствуют усилению кровотока, расширению капилляров и увеличению их проницаемости. Из сосудов в очаг воспаления проникает жидкость. Таким образом, в месте повреждения возникает отёк, покраснение и повышение температуры.
Кроме жидкости из сосудов приходят лейкоциты, которые активируются за счёт тех же ферментов и биологически активных веществ. Они начинают выделять медиаторы воспаления и провоспалительные цитокины, которые действуют на сосуды и клетки иммунной системы и ещё больше усиливают воспаление.
Многие биологически активные вещества могут раздражать и повреждать нервные окончания и рецепторы, что вызывает различную гамму ощущений — от лёгкого жжения и покалывания до зуда и, наконец, сильной боли.
В самом начале статьи был приведён длинный список факторов, способствующих повреждению. Основной причиной повреждения являются различные инфекции. Но даже если изначально повреждение было неинфекционным (например, слизистая оболочка была подвергнута воздействию механического или химического фактора), микроорганизмы быстро активизируются и вызывают гораздо более бурное течение воспалительного процесса. Лейкоциты начинают фагоцитировать (пожирать) микроорганизмы, в результате чего активируется и привлекается ещё больше лейкоцитов. Далее всё будет зависеть от того, какая из противоборствующих сторон будет сильнее — повреждающие факторы или защитные.
Следует отметить, что особенности реакции воспаления очень индивидуальны и во многом генетически обусловлены. [8]
Классификация и стадии развития вульвовагинита
По причинному фактору вульвовагиниты подразделяют на две основные группы: первично-инфекционные и первично-неинфекционные.
Современные представления о лечении урогенитального кандидоза
Урогенитальный кандидоз — это грибковое заболевание слизистых оболочек и кожи мочеполовых органов, вызываемое дрожжеподобными грибами рода Candida. В настоящее время описано более 170 биологических видов дрожжеподобных грибов, из них возбудителями урог
Урогенитальный кандидоз — это грибковое заболевание слизистых оболочек и кожи мочеполовых органов, вызываемое дрожжеподобными грибами рода Candida.
В настоящее время описано более 170 биологических видов дрожжеподобных грибов, из них возбудителями урогенитального кандидоза являются: C. albicans — в 80% (за рубежом — в 45–70%), C. glabrata — в 15–30%, C. tropicalis, C. krusei, C. parapsilosis — в 4–7% случаев.
Заболевание поражает и мужчин и женщин, однако чаще встречается у женщин репродуктивного возраста. По распространенности кандидозный вульвовагинит стоит на втором месте среди всех вульвовагинальных инфекций. Пик заболеваемости отмечается в 20–45 лет.
Половой путь передачи инфекции встречается в 30–40% случаев. Чаще (60–70%) заболевание обусловлено эндогенной инфекцией. При беременности заболеваемость возрастает на 10–20%, риск передачи инфекции новорожденному в родах составляет примерно 70–85%.
К факторам риска обычно относят беременность, применение гормональной контрацепции и заместительной гормонотерапии (особенно гормональными препаратами первого поколения), длительное и бессистемное использование антибиотиков, иммунодепрессантов, цитостатиков и некоторых других препаратов. Однако необходимо отметить, что антибактериальные средства выступают как фактор риска только на фоне существующего кандидоносительства и их влияние кратковременно. Нарушения углеводного обмена, обусловленные сахарным диабетом, способствуют упорному течению урогенитального кандидоза с частыми рецидивами, плохо поддающимися терапии.
Иммунодефицитные состояния, системные заболевания, приводящие к иммунной недостаточности, также провоцируют возникновение и рецидивы урогенитального кандидоза. Особенно тяжело протекает кандидаинфекция у ВИЧ-инфицированных пациентов. Нередко в терминальной стадии СПИДа развивается генерализованная кандидаинфекция.
К основным патогенетическим факторам традиционно относят дисбаланс микрофлоры влагалища, повышение концентрации эстрогена и прогестинов в тканях, нарушение местного иммунитета половых путей.
Вульвовагинальный кандидоз — наиболее часто употребляемое название заболевания, поскольку его основными клиническими проявлениями являются вульвит и вагинит. Однако по локализации выделяют также кандидозный цервицит, кольпит, уретрит, бартолинит. По характеру течения заболевания различают:
Острый генитальный кандидоз характеризуется ярко выраженной воспалительной картиной. Основные жалобы и симптомы при кандидозном вульвовагините — зуд и жжение, постоянные или усиливающиеся во второй половине дня, вечером, ночью, после длительной ходьбы, а у пациентов с атопической предрасположенностью — под действием множества разных факторов. В области вульвы и половых губ зуд, как правило, интенсивный, сопровождается расчесами. Сильный, постоянный зуд нередко ведет к бессоннице, неврозам. Чувство зуда и жжения, боли, особенно в области расчесов, препятствует мочеиспусканию и может приводить к задержке мочи. Болезненность и чувство жжения во влагалище усиливаются во время коитуса и приводят к появлению страха перед половым сношением и расстройству половой жизни (диспареунии).
Следующий симптом — лейкорея. Бели не обильны, белого цвета, густые (сливкообразные) или хлопьевидные, творожистые, пленчатые, имеют нерезкий, кисловатый запах. Редко бывают водянистыми, с творожисто-крошковатыми вкраплениями. Могут отсутствовать полностью.
При поражении близлежащих кожных покровов отмечаются гиперемия, мацерация кожи, отдельные пустулезные элементы, зуд в области заднего прохода.
У пациентов, имеющих предрасположенность, кандидоз нередко рецидивирует, т. е. наблюдаются возвраты болезни после полного угасания клинических проявлений и восстановления нарушенных функций слизистой в процессе лечения. Если такие рецидивы наблюдаются не менее 4 раз в год, то заболевание классифицируется как хронический рецидивирующий вульвовагинальный кандидоз. Тактика лечения в этом случае отличается от таковой при спорадических эпизодах.
Другая форма течения хронической инфекции — персистирующий вульвовагинальный кандидоз, при котором клинические симптомы сохраняются постоянно и лишь несколько стихают после лечения. Рецидивы следует отличать от обострений, которые развиваются не после болезни, а на фоне сохраняющейся клинической симптоматики. Разумеется, и подход к лечению в этом случае несколько иной, чем при других формах.
Если ранее хронизацию и рецидивирование заболевания объясняли реинфицированием (либо эндо-, либо экзогенным), то в настоящее время причиной этих явлений считают состояние макроорганизма, так как постоянно выделяется один и тот же штамм гриба.
В зарубежной литературе нередко употребляют термины «осложненный» и «вторичный» вульвовагинальный кандидоз. К осложненному относят как хронические формы, так и нетипичную этиологию, выраженные клинические проявления, течение на фоне тяжелых предрасполагающих состояний (сахарный диабет, рак, болезни крови, иммунодефицит, в том числе ВИЧ-инфекция), т. е. случаи, плохо поддающиеся терапии.
К вторичному вульвовагинальному кандидозу обычно относят случаи возникновения инфекции на фоне существующего неинфекционного поражения половых органов при красном плоском лишае, болезни Бехчета, пемфигоиде.
Как правило, симптомы кандидоза развиваются быстро, за неделю до менструации и несколько стихают во время менструации. При хронической персистирующей форме нарастает их интенсивность.
В плане дифференциальной диагностики схожие симптомы имеют две другие наиболее частые инфекции влагалища — бактериальный вагиноз и трихомониаз.
Симптомы бактериального вагиноза, как правило, возникают в первую неделю менструального цикла и самостоятельно проходят в середине цикла. Рецидив бактериального вагиноза иногда следует за рецидивом вагинального кандидоза.
Для острого трихомониаза характерны зуд и более выраженное жжение. Выделения, как правило, более обильные, жидкие, пенистые.
Микроскопия нативного препарата или окрашенного мазка — наиболее простой и доступный метод выявления гриба, его мицелия и спор. Культуральная диагностика рекомендуется лишь в некоторых случаях:
Противокандидозные препараты включают:
Большинство случаев вульвовагинального кандидоза поддается терапии местными противогрибковыми средствами и антисептиками.
Преимуществом местных средств является безопасность, так как системная абсорбция практически невелика, в то же время создаются очень высокие концентрации антимикотика непосредственно в области поражения, т. е. на поверхности слизистой.
Вагинальные кремы рекомендуются для лечения вульвитов, таблетки и суппозитории — вагинитов.
При лечении беременных женщин местные антимикотики по показаниям можно назначать только во II и III триместрах. Системные антимикотики при беременности не рекомендуются.
Довольно часто при кандидозном вульвовагините отмечаются сопутствующие инфекции или нарушение влагалищного микробиоценоза. В таких случаях используются комбинированные препараты, которые отличаются высокой клинической эффективностью и могут с успехом применяться в терапии вульвовагинитов смешанной этиологии. Среди таких препаратов наибольшей популярностью пользуются:
Однако за рубежом комбинированные формы не рекомендуются к применению, так как, по мнению некоторых исследователей, они ухудшают фармакокинетику за счет конкуренции составляющих комбинированного препарата. В таких случаях предпочтение отдается сочетанию местного лечения с системным.
В терапии вульвовагинального кандидоза используются также местные антисептики:
При выраженном вульвите назначают теплые ванночки с содой и местные кортикостероидные кремы I и II классов. Отличных результатов в ходе терапии удается достигнуть, применяя при выраженном вульвите крем травокорт, который содержит антимикотик изоконазол в сочетании с кортикостероидом II класса дифлукортолона-21-валератом. Такое оптимальное сочетание позволяет быстро купировать симптомы у женщин и особенно у мужчин. Этот крем удобен в применении, так как назначается всего 1 раз в сутки (на ночь) у женщин и 2 раза (утром и вечером) — у мужчин. Травокорт не имеет запаха и не пачкает белье.
Высокоактивные кортикостероидные мази III и IV классов не рекомендуются, так как могут привести к обострению, усилению симптомов. Патогенетическая терапия включает также использование антигистаминных препаратов и кетотифена.
В упорных случаях и при диссеминированном кандидозе предпочтение отдается системной терапии, а в ряде случаев — сочетанию системного и местного лечения.
Препараты флуконазола являются «золотым стандартом» в лечении больных кандидозом. Для терапии данной патологии также применяются итраконазол и кетоконазол.
При беременности и лактации использовать системные препараты не рекомендуется, а существующие в некоторых работах ссылки на положительные результаты не доказаны достаточным количеством наблюдений и научных исследований.
Продолжительность системной терапии при неосложненном вульвовагинальном кандидозе минимальна (однократный прием, или прием пероральных препаратов не более 5 дней).
Общей рекомендацией по лечению осложненных форм является удлинение курса терапии (объем местной и системной терапии увеличивается вдвое).
На основании собственного опыта нами предложены схемы терапии неосложненного и осложненного вульвовагинального кандидоза (табл.).
Наши наблюдения свидетельствуют о том, что наиболее адекватными являются методы профилактики рецидивов при помощи как местных, так и системных препаратов.
Лечение хронического рецидивирующего вульвовагинального кандидоза
Лечение персистирующего вульвовагинального кандидоза
Начальный курс проводится такой же, как при хроническом рецидивирующем кандидозе. Поддерживающая терапия состоит в постоянном приеме противокандидозных препаратов: флуконазол (микофлюкан), таблетки по 150 мг,1–2 раза в месяц в течение 12–24 мес.
В лечении устойчивого к антимикотикам кандидоза, если терапия оказалась неэффективной, требуется повторно подтвердить диагноз, производя посев и выделение возбудителя с последующим определением его вида и чувствительности к противогрибковым препаратам. Выбор системного или местного антимикотика и его дозы далее осуществляется в соответствии с результатами исследования.
После повторного подтверждения диагноза возможен переход на местную терапию антимикотиками или антисептиками, назначаемыми в высоких дозах, часто и длительными курсами.
Целесообразно также использование витаминных комплексов, содержащих биотин.
Н. В. Кунгуров, доктор медицинских наук, профессор
Н. М. Герасимова, доктор биологических наук, профессор
И. Ф. Вишневская
Уральский НИИ дерматовенерологии и иммунопатологии Минздрава России, г. Екатеринбург
Что такое вагинальный кандидоз (молочница)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Соснина А. С., гинеколога со стажем в 14 лет.
Определение болезни. Причины заболевания
Краткое содержание статьи — в видео:
Candida — это условно-патогенные микроорганизмы, факультативные анаэробы (организмы, способные жить как в присутствии кислорода, так и без него). Они обладают тропизмом — направлением роста на клетки богатые гликогеном, в частности клетки слизистой оболочки влагалища. Самый распространённый вид возбудителя, который встречается в 70—90 % случаев, — Candida albicans.
В последние годы растёт заболеваемость кандидозом, вызванным другими представителями рода Candida. Наиболее часто выявляются:
Частота кандидозного вагинита среди инфекционных заболеваний влагалища и вульвы составляет 30—45 %. Патология занимает второе место среди всех инфекционных заболеваний влагалища и является крайне распространённым поводом для обращения женщин за медицинской помощью. По данным J. S. Bingham (1999):
Кандидозный вагинит редко наблюдается в постменопаузе, за исключением тех пациенток, которые получают гормональную заместительную терапию.
Предрасполагающими факторами заболевания являются:
Заболевание, как правило, не передаётся половым путём, но установлено, что оно связано с характером половых контактов: анально-вагинальным и орогенитальным. Также не исключается вероятность развития кандидозного баланопостита у половых партнёров пациенток с вагинальным кандидозом.
Симптомы вагинального кандидоза
Основные симптомы при вагинальном кандидозе:
В целом симптомы вагинального кандидоза нарастают перед менструацией. При беременности проявление болезни также усугубляется, это связано со снижением иммунитета у беременных женщин.
Объективные признаки вагинального кандидоза:
Патогенез вагинального кандидоза
Основные этапы патогенеза:
При вагинальном кандидозе воспаление происходит в верхних слоях эпителия влагалища. Причина состоит в том, что поддерживается динамическое равновесие между грибом, который не может проникнуть в более глубокие слои, и организмом, который сдерживает его распространение. Соответственно инфекция может долго развиваться в одном месте, проявляясь творожистыми выделениями из влагалища. Обострение заболевания происходит при сдвиге равновесия между развитием грибов и защитными силами организма.
Классификация и стадии развития вагинального кандидоза
По классификации, предложенной D.A. Eschenbach, вагинальный кандидоз подразделяют на два типа:
У женщин различают три формы заболевания:
Для острой формы вагинального кандидоза характерны выраженные симптомы: обильные выделения из влагалища, жжение и зуд во влагалище и наружных половых органах. На фоне таких симптомов нередко снижается трудоспособность пациентки и развиваются неврозы. Острая форма вагинального кандидоза встречается наиболее часто и формируется в результате увеличения количества грибов рода Candida во влагалище на фоне снижения иммунитета пациентки.
Неосложнённая форма заболевания предполагает впервые выявленный или возникающий менее четырёх раз в год вагинальный кандидоз с умеренными проявлениями вагинита у пациенток без сопутствующих факторов риска (сахарный диабет, приём глюкокортикоидов, цитостатиков и др.).
Осложнения вагинального кандидоза
К осложнениям вагинального кандидоза у женщин относятся:
Стеноз влагалища развивается при воспалении стенок влагалища. При этом просвет влагалища сужается, а стенки влагалища становятся плохо растяжимы. Пациентки испытывают боль при половом акте.
Уретрит — воспаление слизистой мочеиспускательного канала. Проявляется болезненным мочеиспусканием, чувством жжения в области уретры, выделением с мочой крови или гноя, дискомфортом при соприкосновении с бельём, слипанием краёв уретры, покраснением области вокруг мочеиспускательного канала.
Цистит — воспаление мочевого пузыря. Патология возникает при попадании возбудителя восходящим путём через уретру в мочевой пузырь. Симптомы цистита схожи с симптомами уретрита, однако есть некоторые отличия: частые позывы к мочеиспусканию при небольшом количестве мочи, чувство неполного опорожнения мочевого пузыря, боль, резь в конце мочеиспускания, помутнение мочи, повышение температуры тела, боли внизу живота.
На фоне вагинального кандидоза возрастает частота осложнений при беременности, а также увеличивается риск инфицирования плода.
Кандидоз плода может вызвать его внутриутробную гибель или приводить к преждевременным родам. После родов у женщин возможно развитие кандидозного эндометрита — воспалительного процесса в тканях, выстилающих внутреннюю полость матки.
Диагностика вагинального кандидоза
Диагностика вагинального кандидоза основывается на характерных жалобах пациентки, данных анамнеза, клинических проявлениях, выявленных при гинекологическом осмотре. В зеркалах видна гиперемия, отёк слизистой, белые налёты на стенках влагалища.
Независимо от этих признаков, подтверждение диагноза должно основываться на лабораторных данных:
Дифференциальную диагностику проводят со следующими заболеваниями:
Лечение вагинального кандидоза
Существуют различные группы препаратов для лечения вагинального кандидоза:
При лечении острых форм вагинального кандидоза назначают местное лечение. Препарат не всасывается в системный кровоток, а действует в области влагалища и слизистой. Примеры схем лечения:
При хроническом кандидозе наряду с местным лечением применяют системные антимикотики:
При рецидивирующей форме заболевания (более четырёх эпизодов в год) применяют схему:
Для купирования рецидивов препарат применяют в дозировке 150 мг один раз в неделю в течение шести месяцев.
В последние годы всё больше исследуется способность C. albicans формировать биоплёнки — вещества на поверхности колонии микроорганизмов, которые служат барьером для проникновения лекарственных средств и обеспечивают выживание. Основным полисахаридом, определяющим развитие резистентности к антибиотикам, является глюкан. Его рассматривают как одну из причин формирования резистентности к антимикотическим препаратам. Этим объясняется отсутствие эффекта при лечении у некоторых больных. Таким пациенткам можно порекомендовать препарат фентиконазол 600 мг в сутки с интервалом в три дня. Лекарство отличается от других способностью преодолевать биоплёнки, тем самым повышая эффективность лечения при резистентности к другим препаратам.
Прогноз. Профилактика
При своевременном обращении пациентки к врачу, лабораторном обследовании и отсутствии самолечения прогноз благоприятный. Самолечение опасно из-за риска рецидива заболевания, его хронизации и возникновения резистентности к препарату, неверно выбранному пациенткой или при неадекватной дозе.
Для профилактики кандидозного вагинита рекомендуется: