Чем лечить e coli гинекология
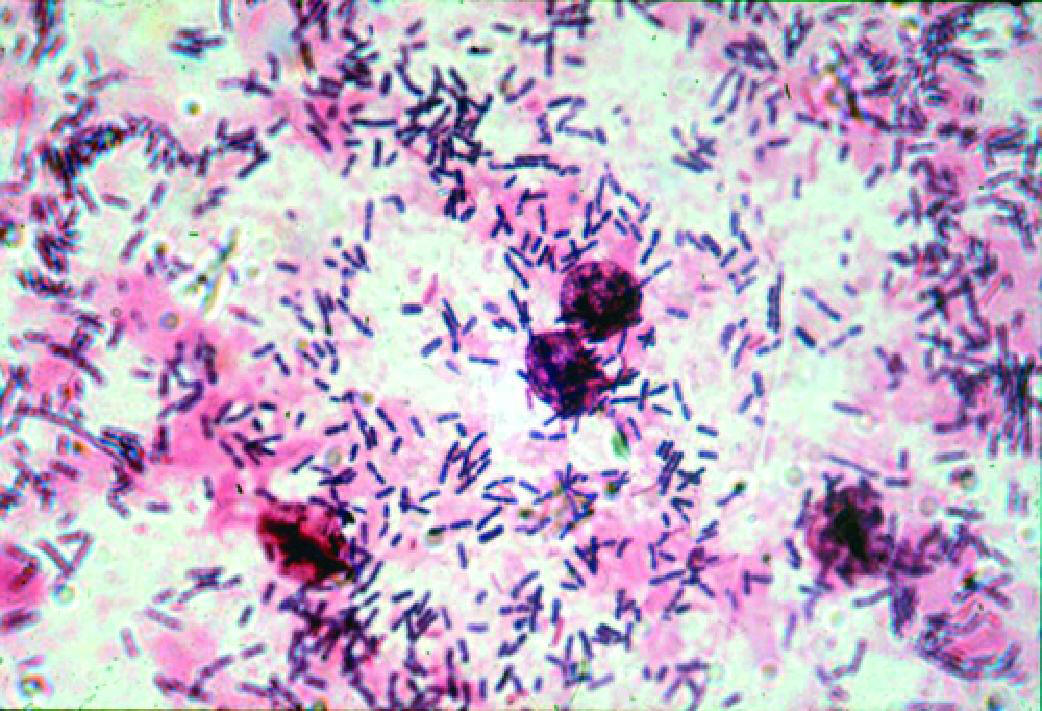
Кишечная палочка
Все слышали о таком понятии как микробиота человека (микробиом). Это огромное количество бактерий и других микроорганизмов, постоянно живущие в пищеварительном тракте и играющие важнейшую роль в поддержании жизни и здоровья человека. Количество бактерий в кишечнике близко к общему количеству клеток организма, а вес может достигать 1,5-3 кг!
Помимо поддержания полезной микрофлоры, кишечные палочки E. coli вырабатывают ряд необходимых для человека витаминов: В1, В2, В3, В5, В6, биотин, В9, B12, К, жирные кислоты (уксусную, муравьиную, а ряд штаммов также молочную, янтарную и другие), участвуют в обмене холестерина, билирубина, холина, желчных кислот, оказывают влияние на всасывание железа и кальция.
Существуют разные виды кишечных палочек: полезные выполняют те важные функции, о которых рассказано выше, и есть патогенные штаммы E.coli. Патогенная кишечная палочка вызывает разнообразные болезни под общим название эшерихиозы, или в просторечии эти болезни называют просто «кишечная палочка».
Полезные и патогенные кишечные палочки не отличаются по морфологическим признакам ( по форме, окрасу и т.п.), поэтому при анализе отличить их невозможно.
Вероятно, те палочки, которые живут в кишечнике в симбиозе у человека, не патогенны, т.е. организм к ним приспособлен. Болезнь вызывают попавшие извне E.coli.
Откуда берется патогенная кишечная палочка и какие симптомы она взывает? Как можно заразиться кишечной палочкой?
При потреблении зараженной пищи или заглатывании воды при купании, палочка проникает в организм и начинает активно размножаться в кишечнике, вытесняя полезные микроорганизмы и приводя к болезни.
Разновидности кишечной палочки и симптомы
Патогенные палочки бывают разных видов, и симптомы, ими вызываемые, могут отличаться.
Однако не только эти симптомы кишечной палочки опасны.
Кишечная палочка является самой частой причиной заболеваний мочеполовой сферы у женщин и у мужчин.
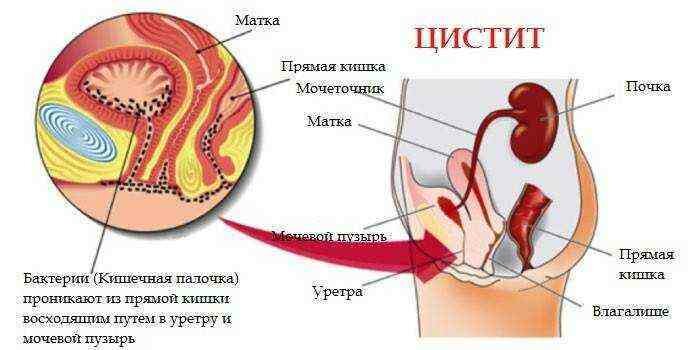
У женщин кишечная палочка вызывает циститы, пиелонефриты, и является причиной острого кольпита, вульвовагинита.
Как происходит заражение?
Инфицирование кишечными палочками (а также другими уропатогенными микробами, обитающими в кишечнике) мочеполовых органов, и у мужчин, и особенно у женщин, часто происходит непосредственно из желудочно-кишечного тракта при недостаточном соблюдении гигиены или применении специфических сексуальных практик.
У мужчин кишечные палочки являются причиной:
Именно поэтому задача адекватной терапии кишечной палочки приобретает особую остроту.
Как лечить кишечную палочку?
При более тяжелых состояниях, а также при инфицировании кишечной палочкой мочеполовых путей, назначают антибактериальную терапию. В этих случаях важно выбрать препарат, к которому отмечается наибольшая чувствительность возбудителя.
Макмирор является противомикробным средством, востребованным при заражении E.coli, сальмонеллами, шигеллами, амебами, хеликобактером и многими другими возбудителями.
Поскольку энтерит, вызываемый кишечной палочкой, часто встречается у детей, и он особенно опасен у детей до 1 года и чуть старше, при назначении лечения необходим препарат, который разрешен детям уже с самого раннего возраста. По инструкции, Макмирор может использоваться в лечении детей любого возраста. При этом грудному ребенку выписывать этот препарат обязательно должен врач, определяя нужную дозировку индивидуально. Также Макмирор разрешен к применению у беременных женщин.
Эти свойства препарата Макмирор делают его препаратом выбора в терапии кишечной палочки.
Лечение мочеполовых заболеваний, вызванных кишечной палочкой.
Лечение диареи у детей и диареи путешественников, вызванной кишечной палочкой, помимо антибактериальной терапии, включает:
При инфицировании кишечной палочкой мочевых путей, вместе с препаратом Макмирор, рекомендуется обильное питье для усиления диуреза, применение препаратов для коррекции гормонального статуса и иммунной системы, симптоматическая терапия (НПВС и т.п.).
Кишечная палочка в мазке
У некоторых женщин и мужчин определяется кишечная палочка в мазке.
Поговорим о том, насколько опасен этот микроорганизм, и что делать при его обнаружении.
Что такое эшерихия коли?
Эшерихия коли (кишечная палочка) – это бактерия из семейства энтеробактерий.
Она в норме обитает в организме человека, в основном в кишечнике.
Так как выход из него (анальное отверстие) находится совсем рядом с мочеполовыми органами, бактерии могут колонизировать их.
Обычно это не сопровождается симптомами.
Но иногда эшерихия коли способна вызывать воспалительные процессы:
При наличии эшерихий во влагалище или уретре они могут определяться в мазке.
Кишечная палочка в мазке: причины
Причиной обнаружения кишечной палочки в мазке является чрезмерное увеличение количества этого микроорганизма в структурах мочеполовой системы.
В норме их должно быть очень мало.
В малых концентрациях они в мазке не обнаруживаются.
Причины, по которой может определяться кишечная палочка в мазке у женщин:
Причины, по которой может определяться кишечная палочка в мазке у мужчин:
Кишечная палочка в мазке у женщин: симптомы
В большинстве случаев кишечная палочка в мазке симптомы не вызывает.
Она становится случайной находкой при плановом обследовании женщины.
Но при избыточном росте кишечной палочки могут воспаляться органы мочевыделительной или половой системы.
Эта бактерия – самый частый возбудитель цистита у женщин.
В таком случае она определяется в моче и уретре.
Симптомы острого цистита:
Во влагалище кишечная палочка может вызывать вагинит.
Он проявляется такими симптомами:
Может наблюдаться выделение крови из влагалища после полового акта.
Вследствие воспалительного процесса слизистая оболочка разрыхляется и легко травмируется.
Кишечная палочка может стать возбудителем неспецифических воспалительных процессов в малом тазу.
Эти заболевания проявляются:
В самых тяжелых случаях такие патологии сопровождаются гнойным процессом и требуют хирургического лечения.
Кроме того, кишечная палочка – это самый частый возбудитель пиелонефрита.
Пиелонефрит – это воспаление канальцевой системы почки.
Он несет угрозу для жизни женщины и иногда требует хирургического лечения.
Кишечная палочка в мазке у мужчин: симптомы
У мужчин кишечная палочка чаще всего вызывает уретрит.
У мужчин уретра имеют большую длину, чем у женщин.
Поэтому на мочевой пузырь инфекция обычно не распространяется.
Но в редких случаях это возможно.
Симптомы цистита у мужчин такие же, как у женщин.
Кишечная палочка в мазке рассказывает подполковник медицинской службы, врач Ленкин Сергей Геннадьевич
Содержание данной статьи проверено и подтверждено на соответствие медицинским
стандартам врачем дерматовенерологом, урологом, к.м.н.
Ленкиным Сергеем Геннадьевичем
| Наименование | Срок | Цена |
|---|---|---|
| Прием уролога | 900.00 руб. | |
| Посев на флору с определением чувствительности к основному спектру антибиотиков | 7 д. | 940.00 руб. |
Что делать, если нашли кишечную палочку в мазке?
Если обнаружена кишечная палочка в мазке, врач может назначить дополнительные исследования.
Это может быть ПЦР или бак посев мазка на кишечную палочку.
Данные методы диагностики позволяют определить концентрацию возбудителя в клиническом материале.
Если высеялась кишечная палочка в мазке, норма её составляет до 10 4 КОЕ/мл.
В зависимости от клинической ситуации, врач может назначить и другие исследования:
Кишечная палочка в мазке у женщин: лечение
При большой концентрации бактерий в мазке лечить кишечную палочку приходится антибактериальными препаратами.
Они также требуются в случае наличия клинической симптоматики воспалительного процесса, даже если концентрация микроорганизмов в пределах нормы.
Женщинам могут назначаться:
Антибиотики могут назначаться разные.
Препарат врач выбирает на основании антибиотикограммы.
Она составляется в процессе культуральной диагностики инфекции.
После бак посева определяется чувствительность кишечной палочки к разным антибиотикам.
Женщине назначаются препараты, к которым эшерихия наиболее чувствительна.
Обычно это цефалоспорины третьего поколения или защищенные полусинтетические пенициллины.
Могут применяться и фторхинолоны.
Они наиболее предпочтительны при поражении мочевыделительной системы (цистит, пиелонефрит).
Прием таблеток внутрь может дополняться использованием препаратов локального действия.
Им отдают предпочтение при вагините.
Часто воспалительный процесс в половых органах вызывают одновременно несколько возбудителей.
Поэтому весьма популярными лекарствами среди врачей и пациентов остаются свечи или вагинальные таблетки, которые содержат в составе одновременно:
Кроме антибактериальной терапии, лечение кишечной палочки в мазке может включать:
Кишечная палочка в мазке при беременности
Выявление кишечной палочке в мазке при беременности не всегда требует лечения.
Необходимость и целесообразность проведения терапии определяется врачом-гинекологом.
Если риск, который несет в себе кишечная палочка, превышает риск назначения антибиотиков, то лечение проводится.
Оно позволяет предотвратить осложнения (распространение инфекции) и инфицирование плода во время родов.
Выраженный воспалительный процесс непосредственно перед родоразрешением может стать показанием к проведению кесарева сечения.
Если у вас обнаружена кишечная палочка в мазке, обращайтесь в нашу клинику.
Опытный врач проведет расшифровку анализов и назначит лечение.
При выявлении кишечной палочки в мазке обращайтесь к автору этой статьи – венерологу в Москве с 15 летним опытом работы.
Эшерихиозы
Эшерихиозы ( ЮEscherichioses ) — коли-инфекция, коли-энтерит, диарея путешественников — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечных палочек, протекающих с симптомами общей интоксика
Эшерихиозы (ЮEscherichioses) — коли-инфекция, коли-энтерит, диарея путешественников — группа бактериальных антропонозных инфекционных болезней, вызываемых патогенными (диареегенными) штаммами кишечных палочек, протекающих с симптомами общей интоксикации и поражением желудочно-кишечного тракта (ЖКТ) с развитием гастроэнтерита или энтероколита, в редких случаях — как генерализованная форма болезни с внекишечными проявлениями.
Согласно Международной классификации болезней 10-го пересмотра (МКБ-10, 1997) регистрация эшерихиозов проводится под шифрами:
А04,0 — энтеропатогенный эшерихиоз;
А04,1 — энтеротоксигенный эшерихиоз;
А04,2 — энтероинвазивный эшерихиоз;
А04,3 — энтерогеморрагический эшерихиоз;
А04,4 — эшерихиоз других патогенных серогрупп.
История и распространение. Возбудитель открыт немецким педиатром T. Эшерихом в 1886 г. Он выделил его из кишечника детей и определил как Bacterium coli commune, предположив, что она может быть причиной поносов у детей. В его честь микроб назван Еscherichia coli.
Эшерихии — постоянные обитатели кишечника человека, но некоторые из них могут вызывать поражения ЖКТ, что доказано экспериментально Г. Н. Габричевским в 1894 г. и подтверждено клинически в 1922 г. А. Адамом. Различие по антигенной структуре патогенных и непатогенных кишечных палочек, выявленное Ф. Кауфманном в 1942–1945 гг., легло в основу классификации патогенных эшерихий. По рекомендации ВОЗ эшерихии, вызывающие поражение ЖКТ, называются диареегенными.
Эшерихиоз — повсеместно распространенное заболевание, чаще диагностируемое у детей до 1 года; у взрослых оно регистрируется как диарея путешественников. Групповые вспышки зарегистрированы в последние годы в Канаде, США, Японии, России и других странах. Показатель заболеваемости эшерихиозом остается высоким в Калининграде, Санкт-Петербурге, Ненецком автономном округе. Так, в Калининграде с 1999 по 2002 г. зарегистрировано более 1000 случаев заболевания на 100 тыс. населения. В Москве выявлено около 1000 случаев заболевания эшерихиозом на 100 тыс. населения за последние 10 лет; летальных исходов нет.
Этиология. Эшерихии — подвижные грамотрицательные палочки, аэробы, относящиеся к виду Еscherichia (Е.) coli, роду Escherichia, семейству Enterobacteriaceae. Растут на обычных питательных средах, выделяют бактерицидные вещества — колицины. Серовары не имеют морфологических отличий. Эшерихии содержат соматические антигены (О-Аг) 173 серотипов, капсульные (К-Аг) — 80 сероваров и жгутиковые (Н-Аг) — 56 серотипов. Диареегенные кишечные палочки подразделяются на пять типов: энтеротоксигенные (ЭТКП, ETEC), энтеропатогенные (ЭПКП, EPEC), энтероинвазивные (ЭИКП, EIEC), энтерогеморрагические (ЭГКП, EHEC), энтероадгезивные (ЭАКП, EAEC).
Фактор патогенности ЭТКП — пили (разновидность ворсинок), или фимбриальные факторы, которые определяют способность к адгезии и колонизации нижних отделов тонкого кишечника, а также к токсинообразованию. Термолабильный и термостабильный энтеротоксины ответственны за повышенную экскрецию жидкости в просвет кишки. ЭИКП, имеющие плазмиды, способны проникать в клетки кишечного эпителия и размножаться в них. Патогенность ЭПКП обусловлена способностью к адгезии. ЭГКП выделяют цитотоксин, шигоподобные токсины 1-го и 2-го типов, содержат плазмиды, которые облегчают адгезию к энтероцитам. Факторы патогенности энтероадгезивных кишечных палочек изучены недостаточно.
Эшерихии устойчивы в окружающей среде, могут месяцами сохраняться в воде, почве, испражнениях. Сохраняют жизнеспособность в молоке до 34 дней, в детских питательных смесях — до 92 дней, на игрушках — до 3–5 мес. Хорошо переносят высушивание, обладают способностью размножаться в пищевых продуктах, особенно в молоке. Быстро погибают при воздействии дезинфицирующих средств и при кипячении. У многих штаммов Е. соli отмечается резистентность к ряду антибиотиков (неомицин, ампициллин, цефалотин и др.). Устойчивость к антибиотикам выявлена у 13–35,1% штаммов патогенных эшерихий.
Эпидемиология. Основной источник эшерихиозов — больные со стертыми формами заболевания; меньшую роль играют реконвалесценты и носители. Значимость последних возрастает, если они работают на предприятиях по приготовлению и реализации пищевых продуктов. Однако, по мнению W. Robson et al. (1993), B. Bell et al. (1994), источник инфекции при энтерогеморрагических эшерихиозах (О157) — крупный рогатый скот. Инфицирование людей происходит при употреблении продуктов, которые были недостаточно термически обработаны. Зарегистрированы групповые вспышки заболеваний эшерихиозом О157 в США, Канаде, Японии — странах, где распространено употребление в пищу гамбургеров. Это и дало основание данным исследователям рассматривать эшерихиоз О157 как антропозоонозное заболевание. Механизм передачи — фекально-оральный, который реализуется пищевым путем, реже — водным и бытовым. По данным ВОЗ, пищевой путь характерен для энтеротоксигенных и энтероинвазивных эшерихий, бытовой — для энтеропатогенных.
Из пищевых продуктов фактором передачи чаще являются молочные изделия, готовые мясные продукты, напитки (квас, компот и др.).
В детских коллективах распространение инфекции может происходить через игрушки, загрязненные предметы обихода, через руки больных матерей и персонала. Реже регистрируется водный путь передачи эшерихиозов. Наиболее опасно загрязнение открытых водоемов, которое происходит в результате сброса необезвреженных хозяйственно-бытовых сточных вод, особенно из детских учреждений и инфекционных больниц.
Восприимчивость к эшерихиозам высокая, особенно среди новорожденных и ослабленных детей. Около 35% детей, которые общались с источником инфекции, становятся носителями. У взрослых восприимчивость повышается в связи с переездом в другую климатическую зону, изменением характера питания и т. д. (диарея путешественников).
Эпидемический процесс, вызванный разными возбудителями Е. соli, может различаться. Заболевания, вызванные эшерихиями ЕТЕС, чаще регистрируются в развивающихся странах тропических и субтропических зон в виде спорадических случаев, а групповые случаи — среди детей 1–3 лет. Эшерихиозы, вызванные ЕIЕС, хотя и регистрируются во всех климатических зонах, преобладают в развивающихся странах. Заболевания носят групповой характер среди детей 1–2 лет в летне-осенний период. ЕРЕС вызывает спорадическую заболеваемость во всех климатических зонах, чаще всего среди детей до 1 года, которые находились на искусственном вскармливании. Эшерихиозы, вызванные ЕНЕС и ЕАЕС, выявлены в странах Северной Америки и Европы среди взрослых и детей старше 1 года; для них характерна летне-осенняя сезонность. Вспышки среди взрослых чаще регистрировались в домах для престарелых.
Патоморфологические данные определяются локализацией патологического процесса и малохарактерны.
Патогенез. Эшерихии проникают через рот, минуя желудочный барьер, и, в зависимости от типовой принадлежности, оказывают свое патогенное действие.
Энтеротоксигенные штаммы способны к выработке энтеротоксинов и фактора колонизации, с помощью которого осуществляется прикрепление и колонизация тонкой кишки.
Энтеротоксины — это термолабильные или термостабильные вещества, воздействующие на биохимические функции эпителия крипт, не вызывая видимых морфологических изменений. Энтеротоксины усиливают активность аденилатциклазы и гуанилатциклазы. При их участии и под стимулирующим влиянием простагландинов увеличивается образование циклического аденозинмонофосфата. В результате в просвет кишки секретируется большое количество воды и электролитов, которые не успевают реабсорбироваться в толстой кишке, и развивается диарея с последующими нарушениями водно-электролитного баланса.
Заражающая доза ЭТКП составляет 108–1010 микробных клеток.
ЭИКП обладают способностью внедряться в клетки эпителия толстой кишки. Проникновение ЭИКП в слизистую оболочку приводит к развитию воспалительной реакции и образованию эрозий кишечной стенки. Повреждение эпителия способствует увеличению всасывания в кровь эндотоксинов. У больных в испражнениях появляются слизь, кровь и полиморфноядерные лейкоциты. Заражающая доза ЭИКП — 5х105 микробных клеток.
Механизм патогенности ЭПКП малоизучен. У штаммов 055, 086, 0111 и др. выявлен фактор адгезии к клеткам Нер-2, за счет которого обеспечивается колонизация тонкого кишечника. У других штаммов (018, 044, 0112 и др.) этот фактор не обнаружен. Видимо, они имеют иные факторы патогенности, которые пока неизвестны. Заражающая доза ЭПКП — 10х1010 микробных клеток.
ЭГКП выделяют цитотоксин SLT (Shiga-like toxin), который вызывает разрушение клеток эндотелия мелких кровеносных сосудов кишечной стенки проксимальных отделов толстой кишки. Сгустки крови и фибрин приводят к нарушению кровоснабжения кишки, появлению в кале крови. Происходит развитие ишемии кишечной стенки вплоть до некроза. У некоторых больных наблюдаются осложнения с развитием синдрома диссеменированного сосудистого свертывания, инфекционного токсического шока и острой почечной недостаточности (ОПН).
ЭАКП способны к колонизации эпителия тонкой кишки. Вызванные ими заболевания взрослых и детей протекают длительно, но легко. Это связано с тем, что бактерии прочно закрепляются на поверхности эпителиальных клеток.
После перенесенного заболевания формируется кратковременный непрочный типоспецифический иммунитет.
Клиника. Клинические проявления эшерихиозов зависят от типа возбудителя, возраста больного, иммунного статуса.
Принята следующая клиническая классификация эшерихиозов (Н. Д. Ющук, Ю. Я. Венгеров, 1999).
По этиологическим признакам:
По форме заболевания:
По тяжести течения:
При эшерихиозе, вызванном энтеротоксигенными штаммами, инкубационный период продолжается от 16 до 72 ч. Характерно холероподобное течение болезни, протекающее с поражением тонкой кишки без выраженного синдрома интоксикации (диарея путешественников).
Заболевание начинается остро; больных беспокоят слабость, головокружение, температура нормальная или субфебрильная. Появляются тошнота, повторная рвота, разлитые боли в животе схваткообразного характера, стул частый (до 10–15 раз в сутки), жидкий, обильный, водянистый, нередко напоминающий рисовый отвар. Живот вздут, при пальпации определяется урчание, небольшая разлитая болезненность.
Заболевание может иметь как легкое, так и тяжелое течение. Тяжесть течения определяется степенью дегидратации. Возможна молниеносная форма заболевания с быстрым развитием эксикоза. Длительность болезни — 5–10 дней.
Энтероинвазивные эшерихии вызывают дизентериеподобное заболевание, которое протекает с симптомами общей интоксикации и преимущественным поражением толстой кишки. Инкубационный период длится 6–48 ч. Начало острое, характеризуется повышением температуры до 38–39 °С, ознобом, слабостью, головной болью, болью в мышцах, снижением аппетита. У части больных температура нормальная или субфебрильная. Через несколько часов присоединяются симптомы поражения ЖКТ (боли схваткообразного характера, преимущественно в нижней части живота, ложные позывы на дефекацию, тенезмы, жидкий стул — обычно калового характера с примесью слизи и крови до 10 и более раз в сутки. При более тяжелом течении заболевания — стул в виде «ректального плевка». Сигмовидная кишка — спазмированная, уплотненная и болезненная. Печень и селезенка не увеличены. При ректороманоскопии — катаральный, реже — катарально-геморрагический или катарально-эрозивный проктосигмоидит.
Течение болезни доброкачественное. Лихорадка длится 1–2, реже — 3–4 дня; длительность заболевания — 5–7 дней. Через 1–2 дня стул нормализуется, спазм и болезненность толстой кишки сохраняются в течение 5–7 дней болезни. Восстановление слизистой оболочки толстой кишки наступает к 7–10-му дню болезни.
У детей энтеропатогенный эшерихиоз, вызываемый Е. соli 1-го класса, протекает в виде различной тяжести энтеритов, энтероколитов, а у новорожденных и недоношенных детей — в септической форме. Для кишечной формы у детей характерно острое начало болезни, температура — 38–39 °С, слабость, рвота, водянистая диарея, стул желтого или оранжевого цвета. Быстро развивается токсикоз и эксикоз, масса тела снижается. Септическая форма заболевания протекает с выраженными симптомами интоксикации (повышение температуры, анорексия, срыгивание, рвота). Возникают множественные гнойные очаги.
Энтеропатогенный эшерихиоз, вызываемый Е. соli 2-го класса, регистрируется у взрослых и детей. Инкубационный период — 1–5 дней. Характерно острое начало заболевания (температура — 38–38,5 °С, озноб, нечастая рвота, боли в животе, стул без патологических примесей, жидкий, до 5–8 раз в сутки), течение доброкачественное. У некоторых больных отмечаются гипотония, тахикардия.
При эшерихиозе, вызванном энтерогеморрагическими штаммами, заболевание характеризуется синдромом общей интоксикации и поражением проксимального отдела толстой кишки. Инкубационый период составляет 1–7 дней. Заболевание начинается остро с болей в животе, тошноты, рвоты. Температура субфебрильная или нормальная, стул жидкий, до 4–5 раз в день, без примеси крови. Состояние больных ухудшается на 2–4-й день болезни, когда стул учащается, появляются примесь крови, тенезмы. При эндоскопическом исследовании выявляется катарально-геморрагический или фибринозно-язвенный колит. Более выраженные патоморфологические изменения обнаруживаются в слепой кишке. Наиболее тяжело протекает заболевание, вызванное штаммом 0157.Н 7. У 3–5% больных через 6–8 дней от начала заболевания развивается гемолитико-уремический синдром (синдром Гассера), который проявляется гемолитической анемией, тромбоцитопенией и развитием ОПН и токсической энцефалопатии (судороги, парезы, сопор, кома). Летальность в этих случаях может составлять 3–7%. Синдром Гассера чаще регистрируется у детей до 5 лет.
Особенности эшерихиоза, вызванные энтероадгезивными штаммами, изучены мало. Заболевание регистрируется у пациентов с ослабленной иммунной системой. Чаще выявляются внекишечные формы — поражение мочевыводящих (пиелонефрит, цистит) и желчевыводящих (холецистит, холангит) путей. Возможны септические формы (коли-сепсис, менингит).
Чаще эшерихиозы протекают доброкачественно, но возможны осложнения — такие как инфекционный токсический шок, гиповолемический шок с дегидратацией 3–4-й степени, ОПН, сепсис, пневмония, пиелоцистит, пиелонефрит, холецистит, холангит, менингит, менингоэнцефалит.
Диагностика. Клиническая картина эшерихиозов сходна с другими кишечными инфекциями, поэтому основу подтверждения диагноза составляют бактериологические методы исследования. Материал (испражнения, рвотные массы, промывные воды желудка, кровь, мочу, ликвор, желчь) следует брать в первые дни болезни до назначения больным этиотропной терапии. Посевы производят на среды Эндо, Левина, Плоскирева, а также на среду обогащения Мюллера.
Применяются серологические методы исследования — реакция агглютинации, реакция непрямой гемагглютинации — в парных сыворотках, но они неубедительны, так как возможны ложно-положительные результаты из-за антигенного сходства с другими энтеробактериями, и используются для ретроспективной диагностики, особенно во время вспышки.
Перспективным методом диагностики является полимеразная цепная реакция (ПЦР). Инструментальные методы обследования (ректороманоскопия, колоноскопия) при эшерихиозах малоинформативны.
Дифференциальный диагноз эшерихиозов проводят с другими острыми диарейными инфекциями: холерой, шигеллезом, сальмонеллезом, кампилобактериозом, пищевыми токсикоинфекциями стафилококковой этиологии и вирусными диареями: ротавирусной, энтеровирусной, Норволк-вирусной инфекцией и др.
В отличие от эшерихиозов, холера характеризуется отсутствием интоксикации, лихорадки, болевого синдрома, наличием многократной рвоты, быстрым развитием дегидратации 3–4-й степени. Помогает в постановке диагноза эпидемиологический анамнез — пребывание в эндемичных регионах холеры.
Шигеллезу, в отличие от эшерихиозов, свойственна высокая лихорадка; боли локализуются в левой подвздошной области; пальпируется спазмированная, болезненная сигмовидная кишка; стул скудный, в виде «ректального плевка».
Сальмонеллез, в отличие от эшерихиозов, характеризуется более выраженной интоксикацией, разлитыми болями в животе, болезненностью при пальпации в эпигастральной и околопупочной областях, урчанием. Характерен зловонный стул зеленоватого цвета.
При проведении дифференциальной диагностики эшерихиозов с кампилобактериозом также выявляются определенные различия. Для кампилобактериоза более характерно начало заболевания с продромального периода (артралгий, слабости, озноба). Боли в животе, диарея присоединяются на 2–3-й день болезни. Боль в животе локализуется чаще в левой подвздошной области. Возможны сыпь, увеличение печени. Заражение чаще всего происходит при употреблении в пищу инфицированного мяса (свинины, говядины, мяса птиц).
Для пищевых токсикоинфекций стафилококковой этиологии, в отличие от эшерихиозов, характерно острое, бурное начало заболевания, короткий инкубационный период (30–60 мин). Более выражены симптомы интоксикации — рвота неукротимая, боли в животе режущего характера с локализацией в эпигастральной и околопупочной областях. Характерен групповой характер заболевания, связь заболевания с пищевым фактором, быстрый регресс болезни.
Для ротавирусного гастроэнтерита, в отличие от эшерихиозов, характерны катаральные явления, изменения слизистой ротоглотки (гиперемия, зернистость), слабость, адинамия. Боли в животе диффузные, стул жидкий, «пенистый», с резким кислым запахом, позывы на дефекацию носят императивный характер. При пальпации отмечается «крупнокалиберное» урчание в области слепой (реже — сигмовидной) кишки.
При проведении дифференциального диагноза эшерихиозов с энтеровирусной инфекцией также можно выявить определенные отличия. Для энтеровирусной инфекции характерны катаральные явления, субфебрильная температура (до недели), многократная мучительная рвота, продолжительность диареи до 2 нед, увеличение печени и селезенки.
Для Норволк-вирусной инфекции, в отличие от эшерихиозов, характерны короткий инкубационный период от 10 ч до 2 сут, ломота в мышцах, головокружение, боли в эпигастральной и околопупочной областях. Продолжительность заболевания короткая — от нескольких часов до 3 сут.
Лечение. Госпитализация больных с эшерихиозами проводится по клиническим и эпидемиологическим показаниям. Больные при среднетяжелом и тяжелом течении заболевания госпитализируются в инфекционные больницы. В легких случаях заболевания больные могут лечиться амбулаторно при наличии благоприятных бытовых санитарно-гигиенических условий.
По эпидемиологическим показаниям госпитализации подлежат лица из декретированных групп, больные из организованных коллективов, а также пациенты, проживающие в коммунальных квартирах, общежитиях.
Госпитализируются больные, если в семье есть лица, относящиеся к декретированным группам.
В остром периоде болезни больным рекомендуется щадящая диета (стол № 4, при нормализации стула — № 2, в период реконвалесценции — стол № 13).
В легких случаях заболевания достаточно назначения пероральной регидратационной терапии (Глюкосалан, Цитроглюкосалан, Регидрон и др.), количество которых должно в 1,5 раза превышать потери воды с испражнениями.
Показаны ферменты (Панзинорм форте, Фестал, Мезим форте, Креон), энтеросорбенты (Энтеросгель, Энтеродез, Полифепан, Полисорб — в течение 1–3 дней). При легком течении болезни целесообразно использование кишечных антисептиков (Интетрикс по 2 капсулы 3 раза в день, Неоинтестопан после каждого акта дефекации по 2 таблетки — до 14 в сутки, Энтерол по 2 капсулы 2 раза в день) в течение 5–7 дней. Легкие и стертые формы эшерихиозов не требуют назначения этиотропных препаратов.
При лечении больных в условиях стационара показан постельный режим в первые 2–3 дня. Назначается этиотропная терапия. С этой целью при среднетяжелых формах используется один из следующих препаратов: ко-тримоксазол (Бактрим, Бисептол, Септрин) по 2 таблетки 2 раза в день. Из препаратов фторхинолонового ряда назначается ципрофлоксацин — Ципролет — фторхинолон для широкого клинического применения, сочетающий мощное бактерицидное действие, широкий антимикробный спектр и благоприятную фармакокинетику. Механизм действия препарата, связанный с ингибированием ДНК-гиразы и топоизомеразы, обусловливает отсутствие перекрестной резистентности. Максимальные концентрации ципрофлоксацина (Ципролета) в плазме крови достигаются через 60–90 мин. Для препарата характерно быстрое начало действия. Биодоступность препарата более 63–77% и высокий показатель проникновения в ткани, жидкости и клетки обеспечивают его эффективность при назначении в небольших дозировках. Препарат отличается хорошим профилем безопасности и положительной динамикой, проявляющейся в короткие сроки. Также рекомендуются Ципробай, Ципросол по 500 мг 2 раза в сутки перорально, пефлоксацин (Абактал) по 400 мг 2 раза в сутки, офлоксацин (Таривид) по 200 мг 2 раза в сутки, длительность терапии — 5–7 дней.
В тяжелых случаях фторхинолоны применяются вместе с цефалоспоринами II поколения (цефуроксим 750 мг 4 раза в сутки внутривенно или внутримышечно; цефаклор 750 мг 3 раза в сутки внутримышечно; цефтриаксон 1 г 1 раз в сутки внутривенно) и III поколения (цефоперазон 1 г 2 раза в сутки внутривенно или внутримышечно; цефтазидим 2 г 2 раза в сутки внутривенно или внутримышечно).
При дегидратации 2–3-й степени назначают регидратационную терапию внутривенно кристаллоидными растворами (Хлосоль, Ацесоль, Лактосоль, Квартасоль).
Объем регидратационной терапии определяется на основании учета степени обезвоживания и массы тела больного. Лечение проводят в два этапа: ликвидация имеющегося обезвоживания и коррекция продолжающихся потерь жидкости.
Скорость введения полиионных растворов составляет от 60 до 80 мл/мин в зависимости от степени дегидратации. При выраженных симптомах интоксикации используются коллоидные растворы (Гемодез, Реополиглюкин и др.) в объеме 400–800 мл в сутки.
Особое внимание должно быть уделено терапии больных эшерихиозом 0157, так как у них возможно появление тяжелых осложнений.
После приема антибактериальных препаратов при продолжающейся диарее используют эубиотики для коррекции дисбактериозов (Бифиформ, Бифистим, Бифидумбактерин форте, Аципол, Хилак форте, Пробифор и др.) в течение 7–10 дней.
Выписка реконвалесцентов проводится после полного клинического выздоровления при отрицательных результатах бактериологического исследования. Для больных из декретированных групп необходимо наличие двукратного отрицательного бактериологического исследования кала, проведенного через 2 дня после окончания этиотропной терапии.
После выписки из стационара больные находятся на диспансерном наблюдении в кабинете инфекционных заболеваний поликлиник в течение 1 мес. В конце срока наблюдения проводят двукратное бактериологическое исследование кала с интервалом в 2–3 дня (лицам, относящимся к декретированным группам).
Коли-инфекция у взрослых протекает благоприятно, перехода в хронические формы не наблюдается.
Профилактические мероприятия. Основу профилактики эшерихиозов составляют меры по пресечению путей передачи возбудителя. Особенно важно соблюдение санитарно-гигиенических требований на объектах общественного питания, водоснабжения, предупреждение контактно-бытового пути заражения в детских учреждениях, родильных домах, стационарах (использование индивидуальных стерильных пеленок, обработка рук дезинфицирующими растворами после работы с каждым ребенком, дезинфекция посуды, пастеризация, кипячение молока, молочных смесей). Готовые к употреблению и сырые продукты должны разделываться на разных разделочных досках разными ножами. Посуду, в которой транспортируют пищу, необходимо обработать кипятком.
При подозрении на эшерихиоз необходимо обследовать беременных до родов, рожениц, родильниц и новорожденных. Специфической профилактики эшерихиозов нет.
Мероприятия в очаге. Контактировавших с больными в очаге заболевания наблюдают в течение 7 дней. Дети, контактировавшие с больным эшерихиозом по месту жительства, допускаются в детские учреждения после разобщения с больным и трехкратных отрицательных результатов бактериологического исследования кала.
При выявлении больных эшерихиозом в детских учреждениях и родильных домах прекращается прием поступающих детей и рожениц. Персонал, матери, дети, бывшие в контакте с больным, а также дети, выписанные домой незадолго до заболевания, обследуются трехкратно (проводится бактериологическое исследование кала). При выявлении лиц с положительными результатами обследования их изолируют.
Литература
Г. К. Аликеева, кандидат медицинских наук
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
Г. М. Кожевникова, профессор
МГМСУ, Москва
Кишечная палочка в мазке
У некоторых женщин и мужчин определяется кишечная палочка в мазке.
Поговорим о том, насколько опасен этот микроорганизм, и что делать при его обнаружении.
Что такое эшерихия коли?
Эшерихия коли (кишечная палочка) – это бактерия из семейства энтеробактерий.
Она в норме обитает в организме человека, в основном в кишечнике.
Так как выход из него (анальное отверстие) находится совсем рядом с мочеполовыми органами, бактерии могут колонизировать их.
Обычно это не сопровождается симптомами.
Но иногда эшерихия коли способна вызывать воспалительные процессы:
При наличии эшерихий во влагалище или уретре они могут определяться в мазке.
Кишечная палочка в мазке: причины
Причиной обнаружения кишечной палочки в мазке является чрезмерное увеличение количества этого микроорганизма в структурах мочеполовой системы.
В норме их должно быть очень мало.
В малых концентрациях они в мазке не обнаруживаются.
Причины, по которой может определяться кишечная палочка в мазке у женщин:
Причины, по которой может определяться кишечная палочка в мазке у мужчин:
Кишечная палочка в мазке у женщин: симптомы
В большинстве случаев кишечная палочка в мазке симптомы не вызывает.
Она становится случайной находкой при плановом обследовании женщины.
Но при избыточном росте кишечной палочки могут воспаляться органы мочевыделительной или половой системы.
Эта бактерия – самый частый возбудитель цистита у женщин.
В таком случае она определяется в моче и уретре.
Симптомы острого цистита:
Во влагалище кишечная палочка может вызывать вагинит.
Он проявляется такими симптомами:
Может наблюдаться выделение крови из влагалища после полового акта.
Вследствие воспалительного процесса слизистая оболочка разрыхляется и легко травмируется.
Кишечная палочка может стать возбудителем неспецифических воспалительных процессов в малом тазу.
Эти заболевания проявляются:
В самых тяжелых случаях такие патологии сопровождаются гнойным процессом и требуют хирургического лечения.
Кроме того, кишечная палочка – это самый частый возбудитель пиелонефрита.
Пиелонефрит – это воспаление канальцевой системы почки.
Он несет угрозу для жизни женщины и иногда требует хирургического лечения.
Кишечная палочка в мазке у мужчин: симптомы
У мужчин кишечная палочка чаще всего вызывает уретрит.
У мужчин уретра имеют большую длину, чем у женщин.
Поэтому на мочевой пузырь инфекция обычно не распространяется.
Но в редких случаях это возможно.
Симптомы цистита у мужчин такие же, как у женщин.
Кишечная палочка в мазке рассказывает подполковник медицинской службы, врач Ленкин Сергей Геннадьевич
Содержание данной статьи проверено и подтверждено на соответствие медицинским
стандартам врачем дерматовенерологом, урологом, к.м.н.
Ленкиным Сергеем Геннадьевичем
| Наименование | Срок | Цена |
|---|---|---|
| Прием уролога | 900.00 руб. | |
| Посев на флору с определением чувствительности к основному спектру антибиотиков | 7 д. | 940.00 руб. |
Что делать, если нашли кишечную палочку в мазке?
Если обнаружена кишечная палочка в мазке, врач может назначить дополнительные исследования.
Это может быть ПЦР или бак посев мазка на кишечную палочку.
Данные методы диагностики позволяют определить концентрацию возбудителя в клиническом материале.
Если высеялась кишечная палочка в мазке, норма её составляет до 10 4 КОЕ/мл.
В зависимости от клинической ситуации, врач может назначить и другие исследования:
Кишечная палочка в мазке у женщин: лечение
При большой концентрации бактерий в мазке лечить кишечную палочку приходится антибактериальными препаратами.
Они также требуются в случае наличия клинической симптоматики воспалительного процесса, даже если концентрация микроорганизмов в пределах нормы.
Женщинам могут назначаться:
Антибиотики могут назначаться разные.
Препарат врач выбирает на основании антибиотикограммы.
Она составляется в процессе культуральной диагностики инфекции.
После бак посева определяется чувствительность кишечной палочки к разным антибиотикам.
Женщине назначаются препараты, к которым эшерихия наиболее чувствительна.
Обычно это цефалоспорины третьего поколения или защищенные полусинтетические пенициллины.
Могут применяться и фторхинолоны.
Они наиболее предпочтительны при поражении мочевыделительной системы (цистит, пиелонефрит).
Прием таблеток внутрь может дополняться использованием препаратов локального действия.
Им отдают предпочтение при вагините.
Часто воспалительный процесс в половых органах вызывают одновременно несколько возбудителей.
Поэтому весьма популярными лекарствами среди врачей и пациентов остаются свечи или вагинальные таблетки, которые содержат в составе одновременно:
Кроме антибактериальной терапии, лечение кишечной палочки в мазке может включать:
Кишечная палочка в мазке при беременности
Выявление кишечной палочке в мазке при беременности не всегда требует лечения.
Необходимость и целесообразность проведения терапии определяется врачом-гинекологом.
Если риск, который несет в себе кишечная палочка, превышает риск назначения антибиотиков, то лечение проводится.
Оно позволяет предотвратить осложнения (распространение инфекции) и инфицирование плода во время родов.
Выраженный воспалительный процесс непосредственно перед родоразрешением может стать показанием к проведению кесарева сечения.
Если у вас обнаружена кишечная палочка в мазке, обращайтесь в нашу клинику.
Опытный врач проведет расшифровку анализов и назначит лечение.
При выявлении кишечной палочки в мазке обращайтесь к автору этой статьи – венерологу в Москве с 15 летним опытом работы.
Кишечная палочка
Все слышали о таком понятии как микробиота человека (микробиом). Это огромное количество бактерий и других микроорганизмов, постоянно живущие в пищеварительном тракте и играющие важнейшую роль в поддержании жизни и здоровья человека. Количество бактерий в кишечнике близко к общему количеству клеток организма, а вес может достигать 1,5-3 кг!
Помимо поддержания полезной микрофлоры, кишечные палочки E. coli вырабатывают ряд необходимых для человека витаминов: В1, В2, В3, В5, В6, биотин, В9, B12, К, жирные кислоты (уксусную, муравьиную, а ряд штаммов также молочную, янтарную и другие), участвуют в обмене холестерина, билирубина, холина, желчных кислот, оказывают влияние на всасывание железа и кальция.
Существуют разные виды кишечных палочек: полезные выполняют те важные функции, о которых рассказано выше, и есть патогенные штаммы E.coli. Патогенная кишечная палочка вызывает разнообразные болезни под общим название эшерихиозы, или в просторечии эти болезни называют просто «кишечная палочка».
Полезные и патогенные кишечные палочки не отличаются по морфологическим признакам ( по форме, окрасу и т.п.), поэтому при анализе отличить их невозможно.
Вероятно, те палочки, которые живут в кишечнике в симбиозе у человека, не патогенны, т.е. организм к ним приспособлен. Болезнь вызывают попавшие извне E.coli.
Откуда берется патогенная кишечная палочка и какие симптомы она взывает? Как можно заразиться кишечной палочкой?
При потреблении зараженной пищи или заглатывании воды при купании, палочка проникает в организм и начинает активно размножаться в кишечнике, вытесняя полезные микроорганизмы и приводя к болезни.
Разновидности кишечной палочки и симптомы
Патогенные палочки бывают разных видов, и симптомы, ими вызываемые, могут отличаться.
Однако не только эти симптомы кишечной палочки опасны.
Кишечная палочка является самой частой причиной заболеваний мочеполовой сферы у женщин и у мужчин.
У женщин кишечная палочка вызывает циститы, пиелонефриты, и является причиной острого кольпита, вульвовагинита.
Как происходит заражение?
Инфицирование кишечными палочками (а также другими уропатогенными микробами, обитающими в кишечнике) мочеполовых органов, и у мужчин, и особенно у женщин, часто происходит непосредственно из желудочно-кишечного тракта при недостаточном соблюдении гигиены или применении специфических сексуальных практик.
У мужчин кишечные палочки являются причиной:
Именно поэтому задача адекватной терапии кишечной палочки приобретает особую остроту.
Как лечить кишечную палочку?
При более тяжелых состояниях, а также при инфицировании кишечной палочкой мочеполовых путей, назначают антибактериальную терапию. В этих случаях важно выбрать препарат, к которому отмечается наибольшая чувствительность возбудителя.
Макмирор является противомикробным средством, востребованным при заражении E.coli, сальмонеллами, шигеллами, амебами, хеликобактером и многими другими возбудителями.
Поскольку энтерит, вызываемый кишечной палочкой, часто встречается у детей, и он особенно опасен у детей до 1 года и чуть старше, при назначении лечения необходим препарат, который разрешен детям уже с самого раннего возраста. По инструкции, Макмирор может использоваться в лечении детей любого возраста. При этом грудному ребенку выписывать этот препарат обязательно должен врач, определяя нужную дозировку индивидуально. Также Макмирор разрешен к применению у беременных женщин.
Эти свойства препарата Макмирор делают его препаратом выбора в терапии кишечной палочки.
Лечение мочеполовых заболеваний, вызванных кишечной палочкой.
Лечение диареи у детей и диареи путешественников, вызванной кишечной палочкой, помимо антибактериальной терапии, включает:
При инфицировании кишечной палочкой мочевых путей, вместе с препаратом Макмирор, рекомендуется обильное питье для усиления диуреза, применение препаратов для коррекции гормонального статуса и иммунной системы, симптоматическая терапия (НПВС и т.п.).
Вагиниты, вызванные условно-патогенной микрофлорой: рекомендации для практикующих врачей
Сведения об авторе:
Пустотина Ольга Анатольевна, доктор медицинских наук, профессор кафедры акушерства, гинекологии и репродуктивной медицины ФПК МР РУДН Адрес: 117198 Москва, ул. Миклухо-Маклая д. 6, телефон 8 (495) 787-38-27, email: rudn@rudn.ru Pustotina Olga Anatolievna, Doctor of Medicine, Professor of The department of Obstetrics, Gynecology and Reproductive Health, Peoples’ Friendship University of Russia. Address: 117198 Moscow, Mikluho-Maklaya str, 6. Phone 8(495)7873827
Нормальная микрофлора женских половых органов
Таким образом, во влагалище здоровых женщин репродуктивного возраста общая численность бактерий составляет 105-106 КОЕ/мл выделений, 95% которых представлены лактобактериями и только 5% формируется представителями других видов аэробных и анаэробных УПМ.
Вагиниты, вызванные УПМ
Вагиниты бывают воспалительного и невоспалительного характера. Воспалительные вагиниты в зависимости от вида возбудителя разделяют на неспецифические и специфические. К специфическим относятся трихомонадный, хламидийный, гонококковый и грибковый вагинит (вагинальный кандидоз), при обнаружении любых других УПМ вагинит является неспецифическим. Невоспалительный вагинит называется бактериальным вагинозом. Бактериальный ваги- ноз, неспецифический вагинит и вагинальный кандидоз объединяют вагиниты, вызванные УПМ.
Бактериальный вагиноз не относится к инфекциям, передаваемым половым путем (ИППП), но связан с сексуальной активностью женщины и может вызывать симптомы уретрита у мужчин. Происходящие во влагалищном биотопе изменения облегчают восходящее инфицирование ИППП: гонококками, хламидиями, трихо- монадами, ВИЧ-инфекцией и др. Кроме того, накапливаясь в большом количестве, УПМ проникают в полость матки, вызывая хроническую воспалительную реакцию, приводя к бесплодию, невынашиванию беременности и снижению эффективности программ ЭКО [7, 8].
Вагинальный кандидоз-это воспаление слизистой оболочки влагалища, вызванное дрожжевыми грибами рода СапсНс1а, которое встречается у 5-10% женщин репродуктивного периода. Развитие кандидоза в основном расценивают как вторичную эндогенную инфекцию, резервуаром которой является желудочно-кишечный тракт. Основными причинами, способствующими проникновению грибов из аногенитальной области во влагалище и их интенсивному размножению, является прием антибиотиков, глюкокортикоидов, потребление пищи с большим количеством углеводов. Предрасполагающими к заболеванию факторами служат ожирение, сахарный диабет и нарушение правил личной гигиены 11.
Факторы риска вагинитов, вызванных УПМ
Устойчивость экосистемы влагалища определяется факторами эндогенного и экзогенного происхождения. К развитию дисбиотических процессов в вагинальном микроценозе наиболее часто приводят: стресс, лечение антибиотиками, гормональная терапия, эндокринные и аллергические заболевания, снижение иммунной защиты организма, хронические запоры, инфекция мочевых путей. Уменьшение доли лактобацилл и повышение рН в содержимом влагалища происходит при повреждениях эпителиального покрова в результате полового акта, трещин, расчесов, при чрезмерной гигиене наружных половых органов. Нередко женщины при появлении неприятного запаха из половых путей прибегают к спринцеванию. Спринцевание не имеет ни гигиенического, ни профилактического, ни лечебного эффекта, а усугубляет дис- биоз и является фактором риска воспалительных заболеваний органов малого таза. Нарушение экосистемы влагалища может возникать после полового акта вследствие действия спермы с высоким уровнем рН, при частой смене половых партнеров, во время аногенитальных контактов, при использовании некоторых спермицидов. Длительное маточное кровотечение, инородные тела во влагалище (тампоны, пессарии, швы при истмико-цервикальной недостаточности) нередко также сопровождаются патологическими выделениями из половых путей [4, 6, 7, 9].
Клиника и диагностика вагинитов, вызванных УПМ
В основе вагинитов, вызванных УПМ, лежит уменьшение колоний лактобактерий, в результате которого изменяется рН вагинальной среды с кислой на щелочную и создаются условия для разрастания УПМ и их адгезии на освобождающийся эпителий слизистой оболочки влагалища.
Все происходящие изменения вагинального биотопа объединяются диагностическими критериями Амселя: появление специфических белей из половых путей, увеличение рН вагинального отделяемого, «рыбный» запах и наличие «ключевых клеток», представляющих собой эпителиальные клетки, порытые сплошным слоем различных микроорганизмов. По последним данным, даже наличие двух критериев из четырех позволяет установить нарушение вагинального микробиоценоза [5].
Кроме того, возбудители ИППП, такие как хламидии, трихомонады, гонококк и Мусор1а5та депйаПит, также могут колонизировать генитальный тракт, не нарушая нормальный рост лактобактерий и не изменяя рН влагалищного содержимого, в следствие чего до 90% случаев инфицирования ИППП протекают бессимптомно. Поэтому международные и отечественные эксперты 15 рекомендуют дополнительно к микроскопическому исследованию, обладающему низкими диагностическими возможностями в отношении облигатных патогенов, использовать метод полимеразной цепной реакции (ПЦР) для выявления антигенов хламидий, трихо- монад, гонококка и Мусор1а5та депИаИит в отделяемом половых путей.
Таким образом, окончательный диагноз вагинитов, вызванных УПМ, устанавливается при наличии у женщины жалоб на патологические вагинальных выделения и данных микроскопического исследования, и только после исключения ИППП методом ПЦР.
Лечение вагинитов, вызванных УПМ
Первый этап: Противомикробная терапия.
Препаратами выбора для лечения бактериального вагиноза являются производные нитроимидазола и линкозамиды, которые наиболее активно подавляют размножение анаэробной микрофлоры:
Исследования показали, что ни у одной из схем нет преимуществ в эффективности терапии [7], однако при местном использовании значительно реже возникают побочные эффекты [16].
Для лечения неспецифического вагинита рекомендуется использовать клин- дамицин (300 мг 2 р/сут 7 дней, вагинальный крем 2% 5г 7 дней, свечи 100 мг вагинально 3 дня). В сравнении с производными нитроимидазола (метронидазол, тинидазол, орнидазол), он имеет более широкий спектр действия, включающий не только анаэробные, но и аэробные грамположительные и грамотрицательные бактерии [3, 12, 13, 17, 18].
В последние годы опубликованы результаты крупных рандомизированных контролируемых исследований, показавших высокую эффективность лечения нарушений вагинального микробиоценоза еще двумя антибиотиками широкого спектра действия: рифаксимина (250 мг вагинально 5 сут) [19] и нифуратела (250 мг вагинально 10 сут) [20].
Следует отметить, что все выше представленные антибактериальные средства, обладая выраженной подавляющей активностью в отношении УПМ, не влияют на жизнедеятельность полезных молочно-кислых бактерий [15, 19, 20].
Терапия вагинального кандидоза проводится антимикотиками, среди которых препаратами первой линии являются азолы для интравагинального применения (имидазолы):
и азолы для приема внутрь (триазолы):
При остром неосложненном вагинальном кандидозе, вызванном СапсМс1а а1Ысап5, все препараты местного и системного действия одинаково эффективны.
В случаях рецидивирования процесса длительность и количество курсов увеличивается, при этом необходимо идентифицировать вид кандидозной инфекции и исключить возможные факторы риска [10,12-14].
Антисептики:
В настоящее время получено множество доказательств эффективности терапии вагинитов, вызванных УПМ, различными антисептическими средствами, такими как:
Все антисептики обладают широким неспецифическим спектром действия и подавляют рост аэробных и анаэробных микроорганизмов, а также грибов рода СапсМс1а, при этом не влияя на жизнедеятельность колонии лактобактерий [15].
Наибольшая доказательная база (уровень доказательности 1А) продемонстрирована для деквалиния хлорида (флуомизина). В крупномасштабных многоцентровых рандомизированных зарубежных [21 ] и отечественных исследованиях (БИОС-1/М) [18, 22, 24] с участием 321 и 640 пациенток, соответственно, деквалиния хлорид показал сопоставимую эффективность с действием клиндамицина при лечении вагинитов, вызванный УПМ, при значительно лучшей переносимости и меньшей частоте развития кандидоза. Кроме того, вагинальные таблетки деквалиния хлорида обладают хорошей всасываемостью и меньшей текучестью в сравнении с хлоргексидином, поэтому назначаются один раз в сутки, не вызывая аллергических и других побочных эффектов, характерных для повидон-йода, при этом более эффективно уменьшая количество «ключевых клеток» и ПЯЛ в вагинальном мазке [18, 22].
Второй этап: восстановление микробиоценоза
Одной из причин хронизации процесса являются бактериальные пленки, формирующие невосприимчивость микроорганизмов к действию антибактериальных и антисептических средств [23]. В результате уровень излеченности через 3 мес составляет 60-70% и еще ниже через 6 мес [6]. Значительное повышение эффективности терапии вагинитов происходит после проведения второго этапа, направленного на восстановление нормального микробиоценоза [22, 23, 25].
Наилучшие результаты продемонстрировало применение пробиотиков, содержащих живые лактобактерии. Они не только подавляют рост УПМ, ассоциированных с бактериальным вагинозом и неспецифическим вагинитом, за счет образования молочной кислоты, перекиси водорода и бактериоцинов, но и способны разрушать образованные ими биопленки, а также модулируют иммунный ответ и способствуют размножению колоний эндогенных лактобактерий [4, 12, 19, 24, 26, 27].
В качестве дополнительного фактора, улучшающего состояние вагинального микробиоценоза после антимикробной терапии, является применение вагинальных таблеток аскорбиновой кислоты. [28]. В то же время, применение исключительно пробиотиков и/или закисления вагинальной среды без предшествующей антимикробной терапии для лечения вагинитов, вызванных УПМ, недостаточно [7].
Лечение вагинитов, вызванных УПМ, у беременных
Нарушение вагинального микробиоценоза у беременных достоверно сопряжено с повышенным риском преждевременных родов, восходящего инфицирования плода и послеродовых гнойно-септических осложнений [1,8, 29-31 ].
Согласно зарубежным рекомендациям [12, 13] терапия бактериального вагино- за и неспецифического вагинита у беременных женщин не отличается от таковой у небеременных. Препаратом первой линии считается метронидазол для системного и местного применения. При осложненном течении беременности и высоком риске преждевременных родов более эффективным считается назначение клиндамицина, обладающего более широким спектром активности 34. При этом терапию нарушений биоценоза влагалища необходимо проводить с самых ранних сроков беременности [36].
В отечественных рекомендациях [14] антибиотики из группы нитроимидазола и линкозамидов противопоказаны в первом триместре, их применение возможно только местно после 12 нед беременности. Поэтому препаратами выбора для беременных являются вагинальные антисептики широкого спектра действия. Среди антисептических средств только у деквалиния хлорида безопасность применения на любом сроке беременности и в период грудного вскармливания подтверждена в масштабных многоцентровых исследованиях [18, 21, 22, 24]. Беременным с вагинальным кандидозом показано местное применение азолов (клотримазол, миконазол, терканозол и др.) 12. В случаях неэффективности терапии предусмотрено интравагинальное назначение полиенов (натамицин, нистатин) 13. В дальнейшем для профилактики рецидивов вагинальных выделений беременным назначаются пробиотики и средства, подкисляющие вагинальную среду [28, 36].
В заключение хочется отметить, что вагинальный микробиоценоз напрямую связан с состоянием здоровья женщины. Любые нарушения гомеостаза могут сопровождаться патологическими выделениями из половых путей, которые нередко бывают кратковременными, и после нормализации общего состояния самостоятельно проходят. В случаях рецидивирования процесса основной задачей врача является не поиск и идентификация возможных возбудителей, которых при вагинитах, вызванных УПМ, как правило множество, а выяснение причин, приведших к длительному течению заболевания. Для постановки правильного диагноза достаточно простой микроскопии вагинального мазка и метода ПЦР для исключения строгих патогенов. При рецидивирующих патологических вагинальных выделениях необходим также тщательный сбор анамнеза для выявления всех возможных факторов риска, только после устранения которых достигается полноценное восстановление вагинального микробиоценоза.
Список использованной литературы
1. Гуртовой Б.Л., Кулаков В.И., Воропаева С.Д. Применение антибиотиков в акушерстве и гинекологии. – М.: Триада-Х, 2004. – 176с.
2. Sweet RL, Gibbs RS. Infectious diseases of the female genital tract. – 5th ed. Lippincott Williams Wilkins, 2009. 469p.
4. Радзинский В.Е. Бактериальный вагиноз. В кн. Шейка матки, влагалище, вульва. Физиология, патология, кольпоскопия, эстетическая коррекция: руководство для практикующих врачей / Под ред. С.И. Роговской, Е.В. Липовой. – М.: Издат журнала StatusPraesens, 2014. – С.249-280.
5. Mittal V, Jain A, Pradeep Y. Development of modified diagnostic criteria for bacterial vaginosis at peripheral health centres in developing countries/ J Infect Dev Ctries. 2012; 6(5): 373-377.
6. Verstraelen H, Verhelst R. Bacterial vaginosis: an update on diagnosis and treatment/ Expert Rev Anti Infect Ther. 2009;7:1109–1124.
7. Donders GG, Zodzika J, Rezeberga D. Treatment of bacterial vaginosis: what we have and what we miss/ Expert Opin Pharmacother. 2014;15(5): 645-657.
8. Leitich H, Bodner-Adler B, Brunbauer M. et al. Bacterial vaginosis as a risk factor for preterm delivery: a meta-analysis/ Am J Obstet Gynecol. 2003;189: 139–147.
9. Filler SG. Insights from human studies into the host defense against candidiasis/ Cytokine. 2012; 58(1): 129-132.
10. Байрамова Г.Р. Рецидивирующий вульвовагинальный кандидоз: автореф. дис. докт.мед.наук.– М., 2013.
11. Роговская С.И., Липова Е.В., Яковлева А.Б. Вульвовагинальные микозы. В кн. Шейка матки, влагалище, вульва. Физиология, патология, кольпоскопия, эстетическая коррекция: руководство для практикующих врачей / Под ред. С.И. Роговской, Е.В. Липовой. – М.: Изд-во журнала StatusPraesens, 2014. – С.281-308.
12. CDC. Sexually Transmitted Diseases Treatment Guidelines 2010. http://www.cdc.gov/std/treatment/2010/pid.htm
13. Sherrard J, Donders G, White D. European (IUSTI/WHO) Guideline on the management of vaginal discharge in women reproductive age. 2011.
14. Клинические рекомендации РОАГ. Акушерство и гинекология. – 4-е изд./ под ред. В.Н. Серова, Г.Т. Сухих. – М.: ГЭОТАР-Медиа, 2014. – 1024с.
15. Профилактика, диагностика и лечение инфекций, передаваемых половым путем: рук-во для дерматовенерологов, акушеров-гинекологов, урологов и семейных врачей. – М.:Институт здоровья семьи, 2008.
16. Mikamo H, Kawazoe K, Izumi K, et al. Comparative study on vaginal or oral treatment of bacterial vaginosis / Chemotherapy. 1997; 43:60-68.
17. Практическое руководство по антиинфекционной химиотерапии// Под ред. Л.С. Страчунского, Ю.А. Белоусова, С.Н. Козлова. – М., 2007. – 462с.
18. Подзолкова Н.М., Никитина Т.И. Сравнительная оценка различных схем лечения больных с бактериальным вагинозом и неспецифическим вульвовагинитом // Рос вестник акуш гинекол, 2012.- №4. – С.75-81.
19. Donders GG, Guaschino S, Peters K, et al. A multicenter, double-blind, randomized, placebocontroled study of rifaximin for the treatment of bacterial vaginosis/ Int J Gynaecol Obstet. 2013; 120:131-136.
21. Weissenbacher ER, Donders G, Unzeitig V. et al. Fluomizin Study Group. A comparison of dequalinium chloride vaginal tablets (Fluomizin®) and clindamycin vaginal cream in the treatment of bacterial vaginosis: a single-blind, randomized clinical trial of efficacy and safety. Gynecol Obstet Invest.
2012; 73: 8–15.
23. Swidsinski A, Verstraelen H, Loening-Baucke V. et al. Presence of a polymicrobial endometrial biofilm in patients with bacterial vaginosis/ PLoS One. 2013;8:e53997.
25. McMillan A, et al. Disruption of urogenital biofilms by lactobacilli / Colloids Surf B Biointerfase,2011; 86(1): 58-64.
26. Larsson PG, Stray-Pedersen B, Ryttig KR, Larsen S. Human lactobacilli as supplementation of clindamycin to patients with bacterial vaginosis reduce the recurrence rate; a 6-month, double-blind, randomized, placebo-controlled study./ BMC Women Health, 2008;15(8):3.
27. Ya W, Reifer C, Miller L E. Efficacy of vaginal probiotic capsules for recurrent bacterial vaginosis: a double blind, randomized, placebo-controlled study. Am J Obstet Gynecol. 2010; 203:1200–1208.
28. Zodzika J, Rezerberga D, Donders G. et al. Impact of vaginal ascorbic acid on abnormal vaginal microflora / Arch Gynecol Obstet 2013; 288: 1039-1044.
29. Bothuyne-Queste E, et al. Is the bacterial vaginosis risk factor of prematurity? Study of a cohort of 1336 patients in the hospital of Arras/ J Gynecol Obstet Biol Reprod. 2012; 41(3): 262-270.
30. Pustotina OA, Bubnova NI, Yezhova LS. Pathogenesis of hydramnios and oligohydramnios in placental infection and neonatal prognosis /J mat-fetal&neonat med. 2008; 21(1): 267-271.
31. Pustotina OA. Urogenital infection in pregnant women: clinical signs and outcome /J Perinat Med, 2013; 41:135.
32. Simcox R, Sin WT, Seed PT, et al. Prophylactic antibiotics for the prevention of preterm birth in women at rick: a meta-analysis/ Aust N-Z J Obstet Gynaecol. 2007; 47: 368-377.
33. McDonald HM, Brocklehurst P, Gordon A. Antibiotics for treating bacterial vaginosis in pregnancy/Cochr Database Syst Rev. 2007. N1.P.CD000262.
34. Lamont RF, Duncan SLB, Mandal D, et al. Intravaginal clindamycin to reduce preterm birth in women with abnormal genital tract flora/ Obstet Gynecol. 2003;101:516–522.