Чем лечить герпес 6 типа у ребенка 13 лет
Герпес 6 типа у детей

Симптомы герпеса 6 типа у ребенка
Каковы главные симптомы детского герпеса 6 типа?
Надо отметить, что в группе риска находятся, прежде всего, малыши от 4 месяцев. В этом возрасте у активного ребенка может внезапно, казалось бы, беспричинно, подняться температура и держаться до пяти дней. Затем по всему телу малыша появляются обильные высыпания. Эта сыпь, хотя и занимает значительную часть кожных покровов ребенка, обычно не сопровождается зудом и не доставляет особого беспокойства маленькому пациенту. Родителей пугает этот вирус больше, чем ребенка. Диагностировать iii причину высыпаний и лихорадки удается не всегда. Порой, герпетическую инфекцию можно принять за корь, энтеровирусную инфекцию или аллергию. Тем более, что при появлении сыпи ребенок становится вялым, капризным, может потерять аппетит. Можно наблюдать у малыша и увеличение лимфоузлов. Сыпь держится от нескольких часов до нескольких дней. Педиатры всегда рекомендуют при температуре у таких маленьких детей незамедлительно обращаться к специалистам. Кстати, часто герпес может протекать вообще без высыпаний. Точный диагноз можно поставить только после проведения ряда анализов.
Осложнения, которые могут быть связаны с герпесом 6 типа
К сожалению, ВГЧ-6В не всегда ограничивается только лихорадкой и сыпью при первичном инфицировании. Возможны и более серьезные последствия:
Особенности терапии вируса герпеса 6 типа у детей
Как и в случае с ВПГ 1 и ВПГ 2, сегодня не существует препаратов, способных полностью избавить человека от вируса герпеса 6 типа. Как правило, переболев герпесом 6 типа, ребенок приобретает иммунитет, способность подавлять активность вируса. Тем не менее, вирус продолжает существовать в организме человека.
В период болезни врач назначает симптоматическое лечение, которые снижает дискомфорт для ребенка, и облегчает течение болезни.
А вот высыпания на коже малыша можно обрабатывать препаратом ВИФЕРОН Гель. Средство наносится три-пять раз в день. Этот препарат также можно применять в самом раннем возрасте.
Профилактика простудных заболеваний
Несмотря на то, что герпес 6 типа у детей очень заразен и легко передается воздушно-капельным путем, а также через слюну, поцелуи и так далее, ребенка все равно можно попытаться защитить, если не от этой инфекции, то от сочетания герпеса и ОРЗ. Ослабленный вирусом герпеса организм очень чувствителен к другим инфекциям, в том числе респираторным, поэтому терапия таких микст-инфекций может усложниться.
Особенно это касается малышей, которые по тем или иным причинам не получают материнское молоко. Такие дети, как считается, более подвержены вирусным заболеваниям. Перенесение же одновременно герпесвирусной и иной инфекции может быть очень большой нагрузкой для организма ребенка.
Поэтому в возрасте от 4 месяцев до трех лет желательно соблюдать некоторые профилактические меры:
К последнему пункту можно отнести и уж упомянутый ВИФЕРОН Гель. Для профилактики его следует наносить на слизистую внутри носика ребенка, два раза в день.
Врач дерматовенеролог, д.м.н., профессор
iv Никольский М.А., Радыш М.В. Роль вирусов герпеса человека 6 и 7-го типов в возникновении фебрильных судорог у детей // Вопросы диагностики в педиатрии. 2012. Т. 4. № 4. С. 46–48.
Герпес у детей
Простой герпес у детей – болезнь, которая поражает множество тканей и органов ребенка, что сопровождается высыпаниями на коже и слизистых оболочках в виде пузырьков. В большинстве случаев лечение длительное латентное, случаются периодические рецидивы.
Простой герпес у детей, согласно международной классификации, делится на:
Эпидемиология
Инфекции подвержены дети, которые заражаются инфекцией в первые 3 года жизни. Новорожденные не могут заразиться данной болезнью до полугода, т. к. имеют в крови специфические антитела класса lgG. Но бывают очень редкие случаи, когда у матери в крови антитела отсутствуют, а значит – и у ребенка. Тогда при заражении у ребенка возникает генерализированная форма болезни, течение тяжелое. У большинства детей 3-летнего возраста в крови достаточно антител, защищающих организм. Число детей с высоким уровнем антител к ВПГ2 возрастает к 5-7-летнему возрасту.
Инфекцию переносят и распространяют как больные, так и вирусоносители. Пути передачи инфекции: контактный, половой и, предположительно, воздушно-капельный. Заразиться можно, что касается подростков, при поцелуе – через слюну. Также заражение происходит через предметы быта, игрушки и прочие предметы, на которых может оказаться слюна зараженного человека. Ребенок может заразиться в утробе матери или при рождении в родовых путях.
Заболевания встречаются периодически, отдельными случаями по всей стране. Но в зимний период (меньше – в другие сезоны) случаются небольшие эпидемии в детсадах, школах и прочих детских коллективах.
На скорость и масштабы распространения герпеса влияют переохлаждение, плохие санитарно-гигиенические условия, повышенная инсоляция, скученность и др.
Что провоцирует / Причины Герпеса у детей:
Вирус простого герпеса (обозначают аббревиатурой ВПГ) содержит РНК. Диаметр вириона 120-150 нм. Размножение вируса происходит лучше всего в тканях куриного эмбриона. В инфицированных клетках из-за влияния вируса образуются внутриядерные включения и гигантские клетки.
Лучше всего вирус герпеса сохраняется при низкой температуре (- 70 °С). Инактивировать его можно, повышая температуру среды до 50-52 °С на протяжении получаса. Также вирус уничтожается ультрафиолетовыми и рентгеновскими лучами. В высушенном состоянии может сохранять жизнедеятельность около 10 лет.
Вирус простого герпеса делят на ВПГ1 и ВПГ2. Первая группа приводит к поражению кожи лица и слизистой во рту. ВПГ2 поражают гениталии, вызывают менингоэнцефалит. Если ребенок заразился одним типом вируса, может возникнуть также инфекция, вызванная и вторым типом.
Патогенез (что происходит?) во время Герпеса у детей:
Инфекция попадает в организм ребенка через поврежденные слизистые оболочки и травмированную кожу. ВПГ вызывает высыпания в местах поражения. В редких случаях вирус из мест первичной локализации попадает в регионарные лимфатические узлы, еще более редко он проникает в кровоток.
Вирус находится в крови, активируется от «пускового фактора», например, от воздействия ультрафиолетовых лучей, физического напряжения, переохлаждения. Эти факторы стимулируют образование простагландинов и кортикостероидных гормонов, что влияет на высвобождение свободной вирусной ДНК из клеток.
Рецидивы наступают по причине ослабления местного иммунитета или из-за генетически детерминированного дефицита клеточного иммунитета. Если иммунный контроль ослаблен, вирус свободно переходит по клеткам и между ними.
Патоморфология. Патологические изменения зависят от локализации инфекции. Происходит баллотирующая дегенерация эпителия, что проявляется как воспаление в эпидермисе в виде пузырьков. Пузырек лежит на на инфильтрированном и отечном сосочковом слое дермы.
При генерализованных формах заболевания во многих органах и системах организма появляются мелкие очаги коагуляционного некроза. Встречаются изменения в ЦНС. Есть вероятность кровоизлияний в субарахноидальное пространство (полость между паутинной и мягкой мозговыми оболочками).
Обнаруживают картину лептоменингита с и нфильтрацией оболочек и стенок сосудов клеточными лимфогистиоцитарными элементами. Изменения такого же характера могут произойти в легких, печени, костном мозге, селезенке и коре надпочечников.
Симптомы Герпеса у детей:
Клинические проявления
Инкубационный период болезни составляет 6 дней (в среднем), но в разных случаях может длиться 2-14 дней. Локализация патологического процесса позволяет различать такие виды поражений:
В диагнозе обычно указывают, насколько распространены поражения (герпес: локализованный, распространенный или генерализованный простой). Течение заболевания: острое, абортивное, рецидивирующее. Абортивная форма указывает на быстрое, преждевременное прекращение болезненного процесса. Рецидивирующее течение указывает на повторение болезни в виде выздоровления и нового возвращения симптомов. После исчезновения клинических проявлений в крови есть антитела, но вирус присутствует в организме, ничем не проявляясь. В случае появления фактора активизации он проявляется и поражает те же или иные органы человека.
Один из самых распространенных симптомов герпеса у детей – поражение слизистых оболочек. Оно проявляется как острый стоматит или гингивостоматит. Такой симптом может быть у детей любого возраста, но в большинстве случаев – у детей от 2 до 3 лет. Инкубационный период длится от одного дня до восьми. Заболевание имеет острое начало с подъемом температуры до 39—40 °С. Ребенка знобит, он начинает проявлять беспокойство (новорожденные и груднички). Появляется общее недомогание. Малыш отказывается от еды, потому что она вызывает болезненные ощущения во рту. Родители могут отметить активное слюнотечение и характерный запах изо рта. У маленьких детей снижается масса тела, появляются в редких случаях расстройства желудка, возможна дегидратация.
При поражении слизистых оболочек рот внутри отечный и красноватый. Слизистая покрыта высыпаниями размером от 2 до 10 мм, которые выглядят, как пузырьки. Сначала они прозрачные, а затем появляется желтоватое содержимое. Они скоро лопаются, после пузырьков остаются эрозии. Регионарные лимфатические узлы увеличены и болезненны (боль при пальпации). Заболевание продолжается от 1 до 2 недель. На 3-5 сутки температура тела приходит в норму. В некоторых случаях возможны рецидивы болезни.
Пузырьки часто «группируются», такие группы высыпаний окружены зоной гиперемии. Процесс образования и засыхания пузырьков может длиться от 10 до 14 дней. У некоторых заболевших детей пузырьки могут слиться в большую форму-пузырь. После того, как он вскрывается (лопается), на его месте образуется большая эрозия.
ВПГ вызывает локализованные и распространенные поражения кожи. Локализированные характерны тем, что общее состояние заболевшего не ухудшается, температура в норме. Распространенная (диссеминированная) форма отличается острым началом, температура тела достигает 39—40 °С, что порой приводит к ознобу. Общее состояние ребенка ухудшается, появляются головные боли, а также боль в мышцах и суставах. На высоте проявления симптомов случаются рвота (или тошнота), судороги. Под конец первого дня (в редких случаях – на второй или третий день) одновременно на лице, руках и туловище появляются герпетические пузырьки со склонностью к «группировке». Болезнь длится до 14-21 дней. В некоторых случаях – дольше. Эта форма болезни преобладает у младших детей.
Следующая форма герпеса – герпетическая экзема. Возникает у детей, заболевших экземой, нейродермитом и другими дерматозами, при которых имеются эрозивные поражения (через которые инфекция попадает в организм). Болезнь также называется иначе: осповидные высыпания Капоши, вакциниформный пустулез, герпетиформная экзема и т. д.
Инкубационный период при герпетической экземе длится от 3 до 5 суток. Острое начало, иногда непродолжительный продромальный период (до появления «клиники»), температура поднимается до 39—40 °С. Симптомы (такие как беспокойство, вялость, сонливость, состояние прострации) быстро прогрессируют.
Есть вероятность судорог, потеря сознания кратковременная. С первого дня заболевания появляется обильная сыпь, иногда она может проявиться только на 2-3 сутки. Высыпания держатся до 2-3 недель. Случается болезненный регионарный лимфоаденит. Сначала пузырьки прозрачные, затем становятся более мутными и уплотненными. Элементы сыпи на второй день напоминают вакцинальные пустулы. Пузырьки сливаются между собой, лопаются, покрываясь корочкой. В тяжелых случаях сыпь оставляет на коже рубцы. Болезнь может длиться долго, есть вероятность повторных высыпаний на протяжении 2 или 3 недель. На 7-10 день температура тела приходит в норму, общее состояние больного улучшается. После этого начинает очищаться кожа. Если организм ребенка ослаблен, герпетическая экзема имеет тяжелое течение. Патологический процесс затрагивает не только слизистые оболочки и кожу, но и нервную систему, висцеральные органы, глаза, что приводит при несвоевременном лечении и ослабленности организма к летальному исходу.
.Из-за обширности поражения кожных покровов угрозу представляет вторичная бактериальная инфекция.
Поражение глаз (офтальмогерпес) часто развивается из-за заражения вирусом герпеса. Может проявляться как изолированное поражение глаза, но также нередки случаи комбинирования поражения глаза, слизистых оболочек полости рта и кожи. Увеличиваются регионарные лимфатические узлы, развивается фолликулярный, катаральный или везикулезно-язвенный конъюнктивит.
Офтальмогерпес начинается остро, появляется конъюнктивит, язвочки или герметические пузырьки на коже века возле ресниц. Течение поверхностных герпетических кератитов в большинстве случаев доброкачественное. Глубокие дисковидные герпетические кератиты имеют тяжелое течение, что нередко приводит к воспалению переднего отдела сосудистого тракта.
Этоторпидные и часто рецидивирующие процессы. В результате кератоиридоциклита могут случиться помутнение роговицы и «падение» зрения. У младенцев до 6 месяцев может развиться хориоретинит, катаракта и увеит.
Генитальный герпес встречается у детей старшего возраста – подросткового и старше. Передается половым путем. У детей младших возрастных групп сначала проявляется простой герпес, а половые органы поражаются вторично. В таких случаях вирус «подхватывают» через руки, на которых есть инфекция, белье, полотенца. Также возможно, что изначально будут поражены наружные половые органы. Инфицирование происходит контактным путем от родителей с простым герпесом. Заболевание чаще всего вызывает ВПГ 2.
Клинические проявления генитального герпеса различны. Течение в большинстве случаев упорное и рецидивирующее. Генитальный герпес у подростков и детей другого возраста вызывает везикулезные и эрозивно-язвенные высыпания на коже и слизистой оболочке половых органов.
У заболевших женского пола высыпания могут быть локализированы на половых губах (малых и больших), в промежности, реже – на внутренней поверхности бедер. В еще более редких случаях высыпания могут появиться на слизистой оболочке влагалища, клиторе или анусе. У заболевших мужского пола высыпания локализируются на внутреннем листке крайней плоти и коже мошонки. Также возможны случаи появления сыпи на слизистой оболочке уретры, которые переходят в высыпания на мочевом пузыре. Болезнь проявляется лихорадкой, болью, зудом, жжением и пр. на участках, пораженных болезнью. Тяжелее, чем у детей, генитальный герпес протекает у взрослых. После исчезновения симптомов возможно длительное латентное вирусоносительство, что повышает риск заражения окружающих детей и взрослых.
Поражение нервной системы при герпесе. Распространение вируса по кровотоку может привести к инфицированию мозга. Поражение ЦНС может иметь течение, сходное с менингоонцефапитом, энцефалитом, менингитом, менингоэнцефалорадикулита. Самыми распространенными формами герпеса являются энцефалит и менингит, которыми болеют обычно новорожденные и младенцы.
По клиническим проявлениям герпетический энцефалит не отличается от других вирусных энцефалитов. У детей раннего возраста часто возникает первичная генерализованная инфекция, хотя поражение ЦНС возможно одновременно с проявлением высыпаний на губах, глазах и пр. Герпетический энцефалит начинается остро, с очень повышенной температуры. Головная боль сильная, чувствуется озноб, возможны повторяющиеся приступы рвоты. За ребенком нужно наблюдать, тогда можно заметить заторможенность и сонливость, но в некоторых случаях – наоборот – возбужденность. В разгар болезни могут случиться судороги, обмороки, параличи и даже нарушение рефлексов. Течение болезни тяжелое, последствия серьезные. Особо тяжелые случаи кончаются фатальным исходом. В таких случаях вскрытие показывает острый геморрагический некроз в коре головного мозга.
Анализ спинномозговой жидкости показывает лимфоцитарньтй цитоз и повышенный белок.
Висцеральные формы проявляются в виде острого паренхиматозного гепатита, пневмонии, поражения почек и других органов.
Герпетический гепатит распространен в основном среди новорожденных детей, но также встречается и у более старших. Обычно гепатит появляется как следствие генерализации простого герпеса, в результате которого возникает поражение многих органов ребенка. Но возможно также, хоть и редко, изолированное поражение печени больного.
Герпетический гепатит проявляется высокой лихорадкой, выраженными симптомами интоксикации, сонливостью, расстройством дыхания, одышкой, цианозом, увеличением печени, рвотой, увеличением селезенки и т. д. Не исключена и желтуха, как при других формах гепатита.
Герпетическая пневмония и герпетический очаговый нефрит клинически не отличаются от поражений легких и почек другой этиологии. Заболевание имеет течение как у вирусно-бактериальной инфекции. Течение острое или рецидивирующее. В основном – именно рецидивирующее. Болезнь повторяется по причине переохлаждения или перегревания, присоединения/активизации вирусных и бактериальных инфекций. У девочек периодом нового обострения болезни может быть время менструаций. Рецидивы обычно имеют легкое течение.
Осложнения при герпесе возникают в случае присоединения бактериальной инфекции.
Диагностика Герпеса у детей:
Простой герпес определяется врачами по характерным пузырьковым высыпаниям, группирующимся на коже и слизистых оболочках. Лабораторное подтверждение проходит с помощью анализа наличия вируса в пузырьках-высыпаниях, в кожных изъязвлениях, в крови, в спинномозговой жидкости (метод ПЦР). Для диагностики рецидивирующего герпеса определенное значение имеет обнаружение высоких пиров антител IgG или нарастание титра в динамике заболевания.
Прогноз благоприятный при локализированных формах болезни. При генерализированных формах лечение более тяжелое и длительное, не исключены летальные исходы. Особенно тяжелый прогноз при герпетических энцефалитах, менингоэнцефалитах, я также при врожденном герпесе и при заболеваниях новорожденных.
Лечение Герпеса у детей:
Локализированные поражения слизистых и кожи лечат местным способом – мазью ацикловира, 5% линимента циклофероном и другими противовирусными препаратами. Интерферон назначают в форме примочек, мази, полосканий слизистых или ингаляций. Пораженные участки кожи и слизистых оболочек обрабатывают 1—2% спиртовым раствором бриллиантового зеленого, 1—3% спиртовым раствором меч кленового синего. Полость рта обрабатывают 3% раствором перекиси водорода, что дает санирующий эффект при герпетическом стоматите. Чтобы груднички могли питаться без болевых ощущений, применяют обезболивающие средства местно – например, анестезин или лидокаин.
Если температура сильно повышена, больному дают ибупрофен. Тяжелые формы герпеса лечат ацикловиром. Комбинированная терапия предусматривает ацикловир + циклоферон.
При рецидивирующем течении болезни назначают курс виферона, витаминов В, В2, В12, пирогенала. Также назначают экстракт элеутерококка жидкий, настойку женьшеня и др. Также эффективны для лечения специфический противогерпетический иммуноглобулин и противогерпетическая вакцина, особенно в комбинированном применении с циклофероном.
В некоторых случаях назначают индукторы интерферона, например, циклоферон или анаферон детский. Присоединение бактериальной инфекции означает, что к лечению нужно добавить антибактериальную терапию. Противопоказаны для лечения герпеса кортикостероидные гормоны, но их подключают при тяжелых формах герпетического энцефалита и менингоэнцефалита.
При рецидивирующем течении герпеса ацикловир малодейственен, нунжо применять его комплексно, вместе с циклофероном.
Профилактика Герпеса у детей:
Среди профилактических мер выделяют закаливание детей и воспитание навыков гигиены. Инфицированным детям не рекомендованы ультрафиолетовое облучение, физические нагрузки, сильный стресс.
Особенно важно оберегать детей, страдающих экземой и мокнущими формами атонического дерматита. Новорожденные, имевшие контакт с заболевшим герпесом человеком, подлежат изоляции. Если мать заражена герпесом, и высыпания есть у нее на коже и слизистых, при контакте с ребенком она обязана носить хирургическую маску. Пока эрозии после отпадения корочек не заживут, зараженная мать не может прижиматься к коже ребенка и целовать его. Если на груди поражений герпеса нет, кормление разрешено.
Чтобы предупредить внутриутробное заражение малыша, беременных рекомендуется обследовать на ВПГ. Если есть клинические признаки инфицирования, вводят иммуноглобулин (0,2 мл/кг). Если признаки генитального герпеса найдены перед родами, роды должны проходить с помощью кесаревого сечения. Но эта мера не на 100% исключает возможность заражения новорожденного.
Если у матери были признаки герпеса или подозрение на него, новорожденных следует отправить на обследование. При наличии у них вируса герпеса, дети получают лечение ацикловиром. Если же клинических проявлений герпеса у рожденного ребенка нет, за ним ведут наблюдение на протяжении 1-2 месяцев.
Герпес 6-го типа (эпидемиология, диагностика, клиника)
Представлены литературные данные по проблеме изучения герпеса 6-го типа. Приведены история открытия вируса, эпидемиологические данные, особенности структуры вируса. Особое внимание уделено диагностике вируса герпеса 6-го типа, его клиническим формам, особ
Literature review on the issue of 6th type herpes study was presented. History of the virus discovery, epidemiologic data and characteristics of the virus structure were given. The particular attention was paid to the diagnostics of 6th type herpes virus, its clinical forms and characteristic of the immune system reaction.
На сегодняшний день внимание специалистов буквально приковано к герпесвирусным инфекциям, которые являются причиной развития многих соматических и онкологических заболеваний, занимают ведущее место среди причин мертворождаемости, преждевременных родов, младенческой смертности, заболеваемости новорожденных, способствуя ранней инвалидизации детей [1]. Это обстоятельство обусловлено рядом причин: повсеместным распространением герпесвирусов, многообразием вызываемых заболеваний, существованием в организме человека в разных формах (острых, хронических, латентных).
Герпесвирусы (Herpesviridae) — это большое семейство ДНК-содержащих вирусов, вызывающих разнообразные болезни у человека и других млекопитающих. Различают 8 представителей семейства герпесвирусов, поражающих человека. Одним из них является вирус герпеса человека 6-го типа (HHV-6). Согласно международной классификации, HHV-6 — это ДНК-вирус подсемейства Betaherpesvirinae рода Roseolovirus, имеет два серологических подтипа — 6А и 6B [2]. Герпесвирус человека 6-го типа (HHV-6, ВГЧ-6) относительно недавно был внесен в список известных человеческих патогенов и является серьезным претендентом на роль этиологического агента таких заболеваний, как рассеянный склероз, энцефалит, лихорадка у детей с судорожным синдромом, инфекционный мононуклеоз, «внезапная экзантема». Существуют данные о том, что ВГЧ-6 является кофактором СПИДа, некоторых форм карцином шейки матки и назофарингеальных карцином [3].
Изучалась роль ВГЧ-6 в качестве этиологического агента возникновения фебрильных судорог у детей. По данным зарубежных авторов, на долю судорог, обусловленных ВГЧ-6, приходится 20–40% [4, 5]. В исследовании М. А. Никольского и М. В. Радыш изучалась роль ВГЧ-6 и ВГЧ-7 в генезе фебрильных судорог у 29 детей в возрасте от 1 мес до 7 лет, поступивших в стационар с респираторными инфекциями. По результатам исследования в 41% случаев в обследуемой группе фебрильные судороги были сопряжены с ВГЧ-6 [6].
История открытия ВГЧ-6
ВГЧ-6 впервые был обнаружен в 1986 г. у взрослых больных с лимфоретикулярными заболеваниями и зараженных вирусом иммунодефицита человека (ВИЧ) [7]. Через два года K. Yamanishi и соавт. изолировали тот же вирус из крови четырех младенцев с врожденной розеолой [7]. Несмотря на то обстоятельство, что этот «новый» вирус был найден изначально в B-лимфоцитах иммунокомпрометированных взрослых больных, впоследствии выяснилось, что он имеет первоначальное сродство к T-лимфоцитам, и его оригинальное название — человеческий В-лимфотропный вирус (HBLV) — было изменено на ВГЧ-6 [7, 8].
Эпидемиология
Первые клинико-эпидемиологические исследования, проведенные в 1986 г., выявили наличие этой инфекции в зоне отдыха в штате Невада (США). Заболевание выражалось в гриппоподобной симптоматике с повышением температуры, ночным потом, увеличением лимфатических узлов, рядом психологических симптомов (усталость, депрессия). Заболевание получило название «синдром хронической усталости». При этом у 75% больных выявлялись антитела к ВГЧ-6. Год спустя первый больной с клинически сходным заболеванием и антителами к ВГЧ-6 в крови был зарегистрирован в Германии. В дальнейшем эта инфекция была выявлена в Европе (Великобритания, Швеция) и Африке. При этом разные исследователи сообщили о выделении ВГЧ-6 из клеток крови не только от лиц с различными лимфопролиферативными, гематологическими заболеваниями, инфицированных HTLV-1, ВИЧ-1 и ВИЧ-2, больных СПИД, но и от здоровых взрослых. Серологические исследования показали повсеместность случаев ВГЧ-6-инфекции, ее обнаруживали во всех странах, где проводили исследования.
Инфицирование происходит обычно на первом или втором году жизни, и соответственно около 95% взрослых имеют антитела к ВГЧ-6 [8]. В США, Японии установлено, что приобретенная ВГЧ-6-инфекция встречается преимущественно у младенцев 6–18 месяцев жизни. Почти все дети инфицируются в возрасте до трех лет и сохраняют иммунитет на всю жизнь. Наиболее показательным является то, что инфекция ВГЧ-6, приобретенная в детском возрасте, приводит к высокой частоте серопозитивности у взрослых [7, 8]. По данным российских авторов, у 80% здоровых доноров, у 65% ВИЧ-инфицированных и 73% онкологических больных выявляются антитела к ВГЧ-6. При рождении большинство детей серопозитивны за счет материнских антител, титр которых снижается к 5 мес [3]. Однако к концу первого года жизни процент серопозитивных малышей оказывается таким же, как среди старших детей и взрослых. Высокая частота выявления антител и ранний возраст инфицирования указывают на присутствие вируса в ближайшем окружении [2].
Структура вируса
ВГЧ-6 сходен с остальными герпесвирусами, но отличается от них по биологическим, иммунологическим свойствам, спектру чувствительных клеток, антигенной структуре, составу генома, количеству и молекулярной массе структурных вирусных белков. Диаметр вириона равен 160–200 нм, тип симметрии икосаэдрический, содержит 162 капсомера, имеет суперкапсидную липидосодержащую оболочку. Геном представлен двунитчатой ДНК. Рестрикционный анализ ДНК ВГЧ-6 установил вариабельность генома различных изолятов вируса. При сравнении первичной структуры геномов ВГЧ-6 и цитомегаловируса (ЦМВ) было обнаружено их определенное сходство. Степень гомологии между ВГЧ-6 и ЦМВ была большей, чем между ВГЧ-6 и другими герпесвирусами, что свидетельствует о тесной связи геномов этих двух вирусов [9]. Очевидно, именно данной степенью гомологии можно объяснить наибольшую способность к сосуществованию ВГЧ-6 и ЦМВ [9].
Исследования изолятов ВГЧ-6 от людей с различной патологией показали, что они принадлежат двум вариантам: А или В (ВГЧ-6А и ВГЧ-6В). Варианты различаются между собой по клеточному тропизму in vitro, рестрикционному эндонуклеазному профилю, нуклеотидной последовательности, реактивности с моноклональными антителами, сероэпидемиологии и причастности к различным заболеваниям. Инфекция, индуцированная ВГЧ-6А, наблюдается реже, и роль данного варианта вируса в патологии человека недостаточно ясна. Предположительно, штаммы ВГЧ-6А являются нейровирулентными, тогда как ВГЧ-6В является основным этиопатогеном внезапной экзантемы (Exantema subitum), он чаще выделяется у пациентов с лимфопролиферативными и иммуносупрессивными заболеваниями [10].
Репликация in vitro
Выделение ВГЧ-6, определение вирусных белков и ДНК в образцах слюны и мокроты указывают на то, что вирус находится в организме человека в слюнных железах, а эксперименты in vitro показали, что он в латентной фазе сохраняется в моноцитах/макрофагах. В естественных условиях основным путем передачи вируса является воздушно-капельный. Не исключен вертикальный путь заражения: антигены вируса обнаружены в абортивном материале при спонтанных абортах. Не исключается половой путь передачи вируса и перинатальная инфекция. Длительная репродукция при острой инфекции и персистенция ВГЧ-6 в клетках крови внешне здоровых людей, включая доноров, является серьезным фактором риска передачи вируса при переливании крови и ее компонентов, трансплантации органов и тканей [3]. Экспериментальные исследования, проведенные учеными, свидетельствуют о том, что ВГЧ-6 латентно инфицирует моноциты и макрофаги разных тканей, а также стволовые клетки костного мозга, из которых впоследствии происходит его реактивация [7, 8].
Иммунитет
У новорожденных, при наличии материнских антител, может существовать относительная защита против ВГЧ-6. Первичная инфекция отличается виремией, которая стимулирует продукцию нейтрализующих антител, что приводит к прекращению виремии [11, 12]. Специфические антитела IgM появляются в течение первых пяти дней от начала клинических симптомов, в последующие 1–2 месяца IgM снижаются и в дальнейшем не определяются. Специфические IgM могут присутствовать при реактивации инфекции и в небольшом количестве — у здоровых людей. Специфические IgG повышаются в течение второй и третьей недели, при этом возрастает их авидность. IgG к ВГЧ-6 персистируют всю жизнь, но в более низких количествах, чем в раннем детстве. Уровни антител могут колебаться после перенесенной первичной инфекции, возможно, в результате реактивации латентного вируса. Существенное возрастание уровня антител, по данным некоторых ученых, наблюдается в случае заражения другими вирусами с похожими ДНК, например, ВГЧ-7 и ЦМВ [7, 13, 14]. В наблюдениях исследователей указывается, что у детей в течение нескольких лет после первичной инфекции может снова происходить четырехкратное нарастание титра IgG к ВГЧ-6, иногда вследствие острого заражения другим агентом, нельзя исключить и возможной реактивации латентного ВГЧ-6 [7, 8]. Клеточный иммунитет является важным в контроле первичной инфекции ВГЧ-6 и впоследствии в поддержании латентного состояния. Реактивация ВГЧ-6 у иммунологически скомпрометированных больных подтверждает важность клеточного иммунитета. Острая стадия первичной инфекции связана с увеличенной активностью натуральных киллеров, возможно, через интерлейкин ИЛ-15 и индукцию интерферона альфа (ИФН-α). В работе по изучению ВГЧ-6 в условиях in vitro отмечалось снижение репликации вируса под влиянием экзогенного интерферона (ИФН). Выявлено, что ВГЧ-6 индуцирует ИЛ-1β и фактор некроза опухоли альфа (ФНО-α), и это свидетельствует о том, что ВГЧ-6 может модулировать иммунный ответ при первичной инфекции и реактивации посредством стимуляции продукции цитокинов [8].
После первичной инфекции сохраняется персистенция вируса в латентном состоянии или в виде хронической инфекции с продукцией вируса. Компоненты иммунного ответа, важного в контроле хронической инфекции, неизвестны. Реактивация латентного вируса происходит у иммунологически скомпрометированных больных, но может наблюдаться и у иммунокомпетентных людей по неизвестным причинам. ВГЧ-6 ДНК часто обнаруживается после первичной инфекции в моноядерных клетках периферической крови и секретах здоровых людей, но главное местоположение латентной инфекции ВГЧ-6 неизвестно.
Диагностика
Лабораторный диагноз первичной инфекции ВГЧ-6 в настоящий момент устанавливается с помощью современного лабораторного оборудования. Трудна для диагностики персистирующая и латентная формы инфекции. ВГЧ-6 ДНК может обнаруживаться в лимфоцитах периферической крови или в других тканях методом гибридизации (полимеразная цепная реакция, ПЦР). Саузерн-блот-гибридизация менее чувствительна, чем ПЦР. Однако обнаружение ВГЧ-6 ДНК в этих тканях не всегда указывает на первичную инфекцию, наиболее часто это является проявлением персистирующей инфекции, развившейся после первичной инфекции и не сопровождающейся виремией [8, 14]. Обнаружение ВГЧ-6 ДНК в плазме и определение высокого титра вируса — более чувствительный метод для диагностики первичной инфекции (около 90%), однако это может свидетельствовать и о реактивации инфекции. ПЦР с использованием обратной транскриптазы, разработанная недавно, позволяет надежно дифференцировать латентную инфекцию ВГЧ-6 и реактивацию инфекции [7, 8]. Существует целый ряд серологических методов определения ВГЧ-6-инфекции: иммунофлюоресцентный метод, иммуноферментный анализ (ИФА), иммуноблот, иммунопреципитация. Иммуноферментный анализ используется наиболее часто, однако серологический диагноз имеет целый ряд недостатков и редко помогает в диагностике клинической манифестации. Определение титра специфических IgM используют для диагностики острой инфекции или реактивации, но не у всех детей, переносящих первичную инфекцию, отмечается продукция антител IgM, а приблизительно 5% здоровых взрослых имеют антитела IgM к ВГЧ-6 [8]. В связи с тем, что практически у всех взрослых выявляют IgG к ВГЧ-6, обнаружение специфических антител в одном образце незначимо. К тому же повышение их титра не указывает на новую инфекцию или реактивацию. Возможно также выявление перекрестно реагирующих антител к другим ДНК вирусам, особенно ВГЧ-7 [8]. Доступные в настоящий момент серологические тест-системы не позволяют дифференцировать варианты А и B ВГЧ-6. У детей диагноз первичной инфекции ВГЧ-6 требует обнаружения виремии (изоляции ВГЧ-6 в моноядерных клетках периферической крови) и существенного нарастания серологических тестов. ВГЧ-6-виремия наблюдается относительно редко у здоровых детей по сравнению с детьми, переносящими первичную инфекцию. Изоляция ВГЧ-6 требует культивации со стимулированными клетками крови пуповины и последующей идентификации на оборудовании, которое доступно только исследовательским лабораториям [8].
По данным литературы, реинфекция ВГЧ-6 наблюдается у больных с нарушенным иммунным статусом, иммуносупрессией (трансплантация органов, СПИД и др.) [3].
Клиническая симптоматика
Клинически герпес 6-го типа характеризуется полиморфизмом и может проявляться под различными масками. Обусловлено это как формой инфекции, так и штаммовыми различиями вируса [3].
Так, к заболеваниям, ассоциированным с первичной острой ВГЧ-6-инфекцией, относятся: синдром хронической усталости (миалгический энцефаломиелит) — значение ВГЧ-6 в возникновении данного синдрома обсуждается различными авторами, однако доказательства, которые приводятся в подтверждение этой гипотезы, неоднозначны; внезапная экзантема у новорожденных и более старших детей (roseola infantum exanthema subitum); судороги с фебрильной провокацией; инфекционный мононуклеоз у подростков и взрослых, не связанный с Эпштейна–Барр вирусной инфекцией (ВЭБ-инфекцией); гистиоцитарный некротический лимфаденит, некоторые заболевания центральной нервной системы (ЦНС), в частности энцефалит, ассоциированный с ВГЧ-6, и др. [15]. Выделяют также заболевания, ассоциированные с персистентной ВГЧ-6-инфекцией, к которым относятся: лимфопролиферативные (иммунодефицит, лимфаденопатия, поликлональная лимфопролиферация); злокачественные лимфомы (неходжкинская лимфома, периферическая Т-клеточная лейкемия, В-клеточная лимфома, дерматопатическая лимфаденопатия, болезнь Ходжкина, синусоидальная В-клеточная лимфома, плеоморфная Т-клеточная лимфома).
Внезапная экзантема — это самая характерная манифестация первичной инфекции ВГЧ-6, она является, как считают большинство исследователей, главным проявлением первичной ВГЧ-6-инфекции. Типичное течение внезапной экзантемы характеризуется начальными проявлениями в виде высокой лихорадки, интоксикационного синдрома, лимфаденопатии с увеличением шейных и затылочных лимфоузлов, небольшой инъекцией в зеве, иногда энантемой в виде мелкой макулопапулезной сыпи на мягком небе и язычке (пятна Nagayama’s), гиперемией и отечностью конъюнктивы век; барабанные перепонки часто гиперемированы, отчасти из-за лихорадки и легкого катарального отита [15]. Экзантема появляется при снижении температуры. Иногда сыпь наблюдается перед тем, как снижается лихорадка, иногда после того, как в течение дня у ребенка отсутствовала температура. Высыпания розеолезного, макулезного или макулопапулезного характера, розовой окраски, до 2–3 мм в диаметре, они бледнеют при надавливании, редко сливаются, не сопровождаются зудом. Высыпания обычно сразу появляются на туловище с последующим распространением на шею, лицо, верхние и нижние конечности, в некоторых случаях они расположены преимущественно на туловище, шее и лице. Продолжительность высыпаний — от нескольких часов до 1–3 дней, исчезают бесследно, иногда отмечается экзантема в виде эритемы.
По данным литературы, основными причинами поражения ЦНС в 20–27% является цитомегаловирус, в 10–15% — вирус Эпштейна–Барр, в 15–20% — вирус простого герпеса [16–19]. Известно, что герпетические поражения ЦНС протекают особенно тяжело. Болезни, обусловленные вирусом простого герпеса, занимают второе место после гриппа как причина смерти от вирусных инфекций. Анализ данных литературы последних лет, а также данных клинических наблюдений свидетельствует о том, что подавляющая часть спорадических случаев острых вирусных энцефалитов, особенно у детей, имеет герпетическую этиологию [20].
Неврологическими осложнениями ВГЧ-6, кроме фебрильных судорог, являются нейроинфекции (менингит, энцефалит), возможно развитие эпилепсии [6], однако данная тема является до конца не изученной. Причинами фебрильных судорог может быть как прямое повреждающее действие на ЦНС, так и опосредованное за счет активации интерлейкина-8 в ликворе [6]. Вместе с тем в проведенных исследованиях по выявлению ВГЧ-6 в спинномозговой жидкости у детей определение ДНК этих вирусов в ликворе было очень низким, либо количество ВГЧ-6 было крайне малым [6].
Некоторые ученые предполагают ВГЧ-6 как причину развития рассеянного склероза, синдрома полиорганной недостаточности, розового лишая, гепатита, вирусного гемофагоцитоза, идиопатической тромбоцитопенической пурпуры, синдрома чрезмерной чувствительности к лекарственным препаратам, особенно антибактериальным. Однако эти данные спорные и требуют дальнейшего глубокого изучения.
Е. И. Веселова и соавт. (2013) изучали клинические особенности течения острых инфекций у детей раннего возраста (от 1,5 мес жизни до 2 лет 10 мес), ассоциированных с ВГЧ-6 у 102 детей. Был сделан вывод о полиморфизме клинических проявлений. Основными клиническими вариантами течения были ОРВИ с гипертермией, внезапная экзантема, поражение слизистой полости рта, нижних дыхательных путей, ЦНС, кожи [21].
Представляют интерес результаты обследования плодов и новорожденных с экстремально низкой массой тела на вирусы герпеса и краснухи — как причины летальных исходов. В работе исследовались мазки-отпечатки органов 109 погибших плодов и новорожденных с помощью реакции непрямой иммунофлюоресценции (РНИФ) на герпетические вирусы и вирус краснухи. Среди всех исследуемых вирусов немалая роль отводится ВГЧ-6 (41,6%) [22].
Таким образом, инфекция, обусловленная ВГЧ-6, имеет особую актуальность на сегодняшний день. В последние годы были предприняты усилия специалистами различных медицинских профессий, как в нашей стране, так и за рубежом, по изучению строения вируса, методов диагностики инфекции, ее комбинаций с другими герпесвирусами, особенностей клинических форм и вариантов течения. При распространении инфекции ведущая роль принадлежит ближайшему окружению. Выявлено наиболее частое сочетание ВГЧ-6 с ЦМВ. Актуальной является диагностика данной инфекции с преобладанием методик, основанных на выявлении ДНК ВГЧ-6 в плазме и других средах организма. Перспективно разрабатываются и другие методы диагностики (ИФА, энзимные методы и др.). Однако обязательно динамическое обследование, так как однократно взятый анализ оценить бывает трудно.
Инфекция, вызванная ВГЧ-6, рассматривается на сегодняшний день как полиморфная. Прежде были описаны такие клинические ее проявления, как «внезапная экзантема», однако в последние годы выявлены симптомы поражения плода, различные формы поражения ЦНС (менингиты, энцефалиты), длительные субфебрилитеты, респираторные формы. Однако значение ВГЧ-6 в развитии гепатитов, судорожных состояний, эпилепсии и других форм у детей подлежит дальнейшему изучению.
Вопросы терапии ВГЧ-6
Сложность лечения заболеваний, вызванных вирусами герпеса, связана с генотипическими особенностями возбудителя, а также различной чувствительностью к препаратам [23]. В последнее десятилетие исследования по изучению антивирусного действия некоторых препаратов показали, что ВГЧ-6, 7, 8 малочувствительны к аналогам нуклеозидов. С определенным успехом в лечении были использованы ганцикловир и фоскарнет (см. ниже). Однако препаратов, которые были бы достаточно эффективны в лечении инфекции, вызванной ВГЧ-6, 7, 8, пока не найдено [24].
К основным этиотропным лекарственным средствам относят три группы препаратов: ациклические аналоги гуанозина, интерфероны и иммуноглобулины [23]. Ведущее место занимает противовирусная химиотерапия, представленная большой группой ациклических аналогов нуклеозидов. Применение ациклических аналогов гуанозина при герпесвирусных инфекциях соответствует уровню доказательности А. Иммунотерапия герпесвирусных инфекций, которая объединяет препараты интерферонов и иммуноглобулинов, является дополнительной, однако важной составляющей этиотропного лечения (уровень доказательности В) [25].
Противовирусная химиотерапия
Обычно при инфекциях, вызванных альфа-герпесвирусами, более эффективным является ацикловир. По химической структуре ацикловир является ациклическим аналогом дезоксигуанозина, естественного компонента ДНК, где кольцевая структура сахара замещена ациклической боковой цепью. В результате такой модификации вирусная ДНК-полимераза воспринимает молекулу препарата в качестве субстрата для синтеза вирусной ДНК. Для приобретения биологической активности ацикловира необходим этап фосфорилирования, при котором последовательно образуется ацикловир моно-, ди- и трифосфат. В результате ошибки вирусной ДНК-полимеразы ацикловиртрифосфат встраивается в полинуклеотидную цепь герпетической ДНК и прерывает дальнейший синтез молекулы, блокируя тем самым репродукцию вируса [25].
Бесспорными преимуществами ацикловира являются его высокая избирательность и низкая токсичность, а недостатками — неодинаковая эффективность при различных герпетических инфекциях, воздействие только на реплицирующийся вирус и возможность формирования резистентности к препарату. В порядке убывания чувствительности их можно расположить следующим образом: ВГЧ-1, ВГЧ-2, ВГЧ-3 > ВГЧ-4, ВГЧ-5 > ВГЧ-6, ВГЧ-7. Таким образом, ацикловир наиболее эффективен при инфекциях, вызванных вирусами простого герпеса 1-го и 2-го типа, а также вирусом Варицелла–Зостер (ВВЗ), а наименее — при патологии ВГЧ-6- и ВГЧ-7-этиологии. Отличия в чувствительности к ацикловиру обусловлены разным содержанием вирусной тимидинкиназы. У ВГЧ-6 и ВГЧ-7 количество данного фермента наиболее низкое, что обусловливает устойчивость к препарату. Ацикловир имеет ограниченную эффективность при ВЭБ-инфекции и может быть полезен лишь в некоторых случаях инфекционного мононуклеоза, однако неэффективен при инфекциях, вызванных ВГЧ-6, ВГЧ-7 и ВГЧ-8 [25].
Валацикловир представляет собой L-валиновый эфир ацикловира. Препарат обычно хорошо переносится, побочные явления отмечаются редко [24]. К валацикловиру, в отличие от ацикловира, чувствительны все виды герпесвирусов, однако наиболее высокая чувствительность — у представителей альфа-подсемейства. К недостаткам валацикловира относят отсутствие инфузионной формы препарата, что ограничивает его применение при тяжелых острых поражениях.
Фамцикловир по химической природе является диацетатом пенцикловира и относится к группе ациклических аналогов гуанозина. В последнее время появились сообщения об эффективности фамцикловира при ВГЧ-6- и ВГЧ-7-инфекциях. Важно отметить, что фамцикловир в некоторых случаях может быть применен в случае резистентности к ацикловиру [25].
Ганцикловир — синтетический нуклеозидный аналог гуанозина. Механизм действия сходен с таковым у ацикловира, однако не требует активного участия вирусной тимидинкиназы, поэтому препарат применяют преимущественно при тех герпетических инфекциях, при которых недостаточно эффективен ацикловир (ВГЧ-4, ВГЧ-5, ВГЧ-6, ВГЧ-7). Существенным недостатком препарата является его сравнительно высокая токсичность, поэтому ганцикловир следует назначать строго по показаниям — при реактивированных формах указанных инфекций, которые приводят к тяжелым органным поражениям.
Валганцикловир представляет собой L-валиновый эфир ганцикловира. Это пролекарство, которое превращается в ганцикловир после всасывания в кишечнике. Характеризуется более высокой биодоступностью, чем ганцикловир (по крайней мере, в 10 раз выше, чем у этого препарата). Показан только при тяжелых инфекциях, вызванных герпесвирусами, не чувствительными к ацикловиру. К относительным противопоказаниям следует отнести детский возраст до 12 лет, период беременности и грудного вскармливания.
Фоскарнет (фоскарнет натрия) является ингибитором вирусной ДНК-полимеразы и в меньшей степени — РНК-полимеразы. При этом препарат связывается с пирофосфатом и частично ингибирует нуклеозидтрифосфат, что опосредует терапевтический эффект. Эффективен по отношению к ВГЧ-1, ВГЧ-5, ВГЧ-6, ВГЧ-7, однако сравнительно высокая токсичность несколько ограничивает широкое применение этого препарата (считается средством второго ряда).
Новыми и многообещающими противогерпетическими химиопрепаратами являются цидофовир и бривудин. Эти лекарственные средства обладают более высокой эффективностью, чем ацикловир и ганцикловир, однако хуже переносятся, что ограничивает их широкое клиническое применение. Их следует использовать при тяжелых, угрожающих жизни формах герпесвирусных инфекций при условии известной или ожидаемой резистентности к ацикловиру и ганцикловиру.
К недостаткам противовирусной химиотерапии относится воздействие только на реактивированный вирус, невозможность эрадикации инфекции, отсутствие эффекта последействия, ряд побочных эффектов (особенно у ганцикловира и вальганцикловира), развитие резистентности к препарату. Причинами резистентности могут быть частое и нерациональное применение препаратов, наличие иммунодефицита, заражение резистентным штаммом вируса. Учитывая все недостатки, монотерапия ациклическими аналогами гуанозина рекомендована только при легких формах герпесвирусных инфекций [25].
Среди других противовирусных препаратов наибольшую доказательную базу имеет инозин пранобекс, который можно применять per os в дозе 50 мг/кг на протяжении ≥ 21 дня. Было показано, что к инозин пранобексу в рекомендуемой дозе возможно возникновение полной или частичной резистентности со стороны ВГЧ-6 в 30–40% случаев [25]. Однако данный вопрос находится на стадии изучения.
Из других средств с антигерпетическим действием нами было найдено всего лишь одно исследование, которое продемонстрировало, что амантадин (средство против вируса гриппа) эффективен для подавления репродукции ВГЧ-6 при применении в субмаксимальной дозе [26].
Иммунотерапия
Основой современной иммунотерапии герпесвирусных инфекций являются препараты интерферонов и иммуноглобулинов. Назначение такой терапии, исключая отдельные показания, соответствует уровню доказательности В. Иммунотерапия не может полностью заменить противовирусную химиотерапию, однако добавление иммунотерапевтических препаратов позволяет повысить эффективность лечения, сократить курс терапии и предотвратить индукцию резистентности к ациклическим аналогам гуанозина.
В настоящее время только накапливается опыт лечения различных форм ВГЧ-6-инфекций. Мнение экспертов о целесообразности применения тех или иных терапевтических вмешательств, которые не прошли контролируемых исследований, определяется знанием патогенеза болезни и личным опытом терапии. Это уровень доказательности D.
Y. Kawano и соавт. (2000) проводили лечение пациентов с ВГЧ-6-менингоэнцефалитом ганцикловиром, гамма-глобулином и интравентрикулярными инфузиями альфа-интерферона, благодаря чему удалось устранить ДНК вируса из цереброспинальной жидкости [27].
J. A. Cabrera-Gómez, P. López-Saura (1999) настоятельно рекомендуют широкое применение терапии альфа-интерферонами при вирусных нейроинфекциях, в том числе герпесвирусного генеза [28].
При ВГЧ-6-нейроинфекции возможно проведение интратекальной терапии в дозе 0,3 МЕ/сут, используя резервуары Оммайя или Рикхама в случае неэффективности иных доступных методов терапии.
Препараты бета-интерферонов
Препараты бета-интерферонов показаны как средство базисной терапии при рассеянном склерозе с ремиттирующим течением. Лечение эффективно, по крайней мере, у 60% пациентов. Как известно, это аутоиммунное осложнение ассоциировано с инфекциями, вызванными ВЭБ и ВГЧ-6. Противовирусный эффект бета-интерферонов, как минимум, в 10 раз выше, чем у альфа-интерферонов, однако более выраженный иммуносупрессивный эффект ограничивает их широкое применение [26]. В случае нейроинфекций бета-интерфероны могут иметь определенные преимущества, поскольку снижают проницаемость гематоэнцефалического барьера.
На сегодняшний день проведено два рандомизированных контролируемых исследования по изучению эффективности препаратов бета-интерферонов при герпесвирусных нейроинфекциях, которые не продемонстрировали дополнительной пользы от применения этих лекарственных средств [29, 30], однако в одном из исследований [29] показана эффективность бета-интерферонов в подгруппе пациентов с тяжелой формой нейроинфекции (n = 41).
Индукторы интерферонов
Индукторы интерферонов имеют очень ограниченную доказательную базу при герпесвирусных инфекциях, несмотря на широкое применение в клинической практике. В целом индукторы интерферонов не могут позиционироваться как альтернатива препаратам интерферонов, а только как средства второго ряда в случае невозможности прохождения интерферонотерапии [31].
Иммуноглобулинотерапия
В отличие от интерферонов, препараты иммуноглобулинов действуют преимущественно на внеклеточный вирус в виде вирионов. Сегодня пересмотрена роль антител в противовирусном иммунном ответе. Установлено, что клеточные механизмы обеспечивают контроль вируса in situ, а гуморальные предотвращают диссеминацию патогена по биологическим средам. C. Karam и соавт. (2009) описали подострый менингорадикулит, вызванный ВГЧ-6, у 26-летнего пациента и сообщили о полном устранении симптомов при помощи комбинированной терапии валганцикловиром и внутривенно иммуноглобулином [32].
Побочные эффекты при иммуноглобулинотерапии (5%) значительно ниже, чем при применении глюкокортикоидов и нестероидных противовоспалительных препаратов — часто назначаемых в качестве средств патогенетической терапии при герпесвирусных инфекциях. Крайне необходимо развеять миф об опасности терапии препаратами антител [32]. Осложнения наблюдаются крайне редко в виде гриппоподобного синдрома. Устранить их можно путем замедления скорости инфузии препарата. Анафилаксия при правильном применении отмечается крайне редко, казуистически, почти исключительно у пациентов с тотальным дефицитом IgA.
Случаи передачи инфекций через препараты иммуноглобулинов не регистрируются с 1986 г., когда были внедрены новые технологии получения и очистки действующего вещества [24].
Отмечена эффективность тройной терапии (валацикловир + альфа-интерферон + иммуноглобулин) при реактивированной ВГЧ-6-инфекции с различными органными поражениями и герпесвирусной нейроинфекции, осложненной височной медианной эпилепсией [25].
Патогенетическая терапия
Патогенетическую терапию при герпесвирусных инфекциях необходимо проводить по общим правилам, однако следует избегать полипрагмазии и назначения иммуносупрессивных препаратов. Хотя есть много сообщений о реактивации герпесвирусов во время применения глюкокортикоидов, эти препараты в низкой или средней дозе могут быть показаны в некоторых случаях герпесвирусных инфекций, а именно — при лимфопролиферативных синдромах, учитывая способность стероидов вызывать апоптоз лимфоцитов, при нейроинфекциях, учитывая их противоотечное воздействие, а также при диссеминированных инфекциях для купирования синдрома системного воспалительного ответа. Следует учитывать, что ламотриджин (противосудорожный препарат, применяемый в лечении при височной медианной эпилепсии) оказывает противовирусное воздействие по отношению к ВГЧ-6 in vitro [26], поэтому этот антиконвульсант может быть предпочтительнее при ВГЧ-6-нейроинфекции, сопровождающейся судорожным синдромом.
Альтернативная терапия
Акупунктура, фитотерапия, биорезонансная терапия, ультрафиолетовое и лазерное облучение крови на сегодняшний день не имеют надлежащей доказательной базы при герпесвирусных инфекциях, поэтому их применение не может считаться добросовестной клинической практикой.
Литература
* ГБУЗ Морозовская ДГКБ ДЗМ, Москва
** ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Герпесвирусные инфекции у детей: современные возможности терапии
В статье рассматриваются некоторые аспекты этиопатогенеза герпесвирусных заболеваний у детей, современные подходы к лекарственной терапии и профилактике рецидивов.
This article discusses some aspects of the pathogenesis of herpes-associated diseases in children, modern approaches to drug therapy and relapse prevention.
В последние годы среди основных возбудителей вирусных инфекций у детей особое место занимают герпес-вирусы, что связано с их повсеместным распространением, широким разнообразием, полиорганностью поражения, многообразием клинических проявлений, а также высокой частотой хронического течения. Герпес-ассоциированные заболевания входят в число наиболее распространенных и плохо контролируемых инфекций человека. Это связано с тем, что герпес-вирусы могут длительно бессимптомно циркулировать в организме человека с нормальной иммунной системой, а при иммуносупрессии способствовать развитию тяжелых заболеваний, вплоть до угрожающих жизни генерализованных инфекций. Так, по данным Всемирной организации здравоохранения (World Health Organization, WHO), смертность от герпетической инфекции составляет около 16% и находится на втором месте после гепатита среди вирусных заболеваний [1].
Для синтеза вирусных белков и образования оболочки вируса, его капсида и ДНК «дочерних» вирионов необходимы аминокислоты, липопротеиды и нуклеозиды клетки-хозяина. По мере истощения внутриклеточных резервов эти молекулы поступают в инфицированную клетку из межтканевых пространств. В связи с тем, что герпес-вирусы напрямую зависят от интенсивности внутриклеточного обмена организма человека, они колонизируют преимущественно клетки эпителия, слизистых оболочек, крови и лимфоидной ткани, которые обладают наиболее высоким темпом обмена веществ.
Вирионы герпес-вирусов термолабильны — они инактивируются в течение 30 мин при температуре 50–52 °C, в течение 20 ч — при температуре 37,5 °C, но хорошо переносят лиофилизацию. На металлических поверхностях (монеты, дверные ручки, водопроводные краны) герпес-вирусы выживают в течение 2 ч, на пластике и дереве — до 3 ч, на влажных медицинских материалах (вата и марля) — до их высыхания при комнатной температуре (до 6 ч). Уникальность герпес-вирусов заключается в том, что они способны непрерывно или циклично размножаться в инфицированных клетках тропных тканей (персистенция), а также пожизненно сохраняться в морфологически и иммунохимически видоизмененной форме в нервных клетках регионарных нервных ганглиев (латенция) и реактивироваться под влиянием различных экзо- и эндогенных провоцирующих факторов. Однако способность к персистенции и латенции у различных штаммов неодинаковая: наиболее активны в этом отношении вирусы простого герпеса, наименее — вирус Эпштейна–Барр.
По данным многочисленных исследований, к 18 годам более 90% жителей городов инфицируются одним или несколькими штаммами вирусов. Основной путь инфицирования — воздушно-капельный, при прямом контакте или через предметы обихода (общие посуда, полотенца, носовые платки и пр.). Отмечается также оральный, генитальный, трансфузионный, трансплантационный и трансплацентарный пути передачи инфекции. ВПГ 1-го и 2-го типов, цитомегаловирус входят в число возбудителей TORCH-инфекций, способствуют развитию серьезных заболеваний новорожденных и детей младшего возраста. Вирусы простого герпеса, цитомегаловирус, вирус Эпштейна–Барр рассматриваются как индикаторы СПИДа в связи с их частым обнаружением при данном заболевании [3, 4]. С герпес-вирусами связывают развитие синдрома хронической усталости (Chronic fatigue syndrome — CFS) [5].
Клинически герпес-инфекция у детей может протекать в виде ветряной оспы (вирус варицелла зостер), инфекционного мононуклеоза (вирус Эпштейна–Барр), внезапной экзантемы (вирус герпеса человека 6-го и 7-го типов), афтозного стоматита (ВПГ 1-го или 2-го типа), мононуклеозоподобного синдрома (цитомегаловирус). У подростков и взрослых людей часто инфекция протекает бессимптомно, что объясняется как биологическими свойствами штаммов, так и индивидуальными особенностями иммунного ответа. Часто при снижении иммунореактивности организма герпес-вирусы выступают в качестве вирусов-оппортунистов, приводя к более тяжелому течению основного заболевания, развитию осложнений. Велика роль герпесвирусных инфекций, особенно цитомегаловирусной, в формировании младенческой смертности. Наибольшую угрозу для жизни и здоровья детей представляют герпетические нейроинфекции — летальность при них достигает 20%, а инвалидизация — 50%. Тяжело протекают офтальмогерпес (развитие катаракты или глаукомы — до 50%), генитальный герпес, генерализованная форма Эпштейна–Барр-вирусной инфекции (инфекционного мононуклеоза) [1, 6].
Герпесвирусная инфекция относится к трудноконтролируемым заболеваниям. Несмотря на разнообразие лекарственных препаратов, использующихся для лечения данной патологии, средств, обеспечивающих полное излечение, не существует. Это обусловлено генотипическими особенностями возбудителя, формированием резистентности герпес-вирусов и молекулярной мимикрией.
Открытые с помощью методов молекулярной биологии механизмов репликации герпес-вирусов, а также изучение взаимодействия вируса с клеткой позволили создать целый ряд эффективных химиотерапевтических средств, обладающих противогерпетической активностью. Однако, эффективно купируя острые проявления инфекции, они не предотвращают рецидивирования, не всегда снижают частоту рецидивов.
Учитывая, что при герпес-ассоциированных инфекциях, как и при других хронических заболеваниях с длительной персистенцией вируса, развиваются иммунодефицитные состояния, для повышения эффективности лечения в схемы терапии наряду с противовирусными препаратами приходится включать препараты, способствующие коррекции иммунного статуса больного. Все это диктует необходимость правильно подбирать лекарственное средство, его дозу и длительность приема, при необходимости использовать комбинацию различных препаратов, избегая при этом полипрагмазии. Определенную сложность терапии в детском возрасте вызывают возрастные ограничения для ряда лекарственных средств, наличие нежелательных лекарстввенных реакций (НЛР) и противопоказаний.
В настоящее время для лечения герпесвирусных заболеваний и профилактики рецидивов используют следующие группы препаратов (табл.).
При лечении герпес-инфекций следует придерживаться комплексного подхода. Длительность и интенсивность терапии определяются возрастом больного, клинической формой заболевания, тяжестью его течения, а также наличием осложнений и сопутствующей патологии. Лечебно-профилактические мероприятия следует разделять на несколько этапов.
Следует отметить, что сочетанное применение противовирусных препаратов и иммунобиологических средств имеет ряд преимуществ. Во-первых, комплексная терапия обеспечивает синергидный эффект. Во-вторых, позволяет снизить дозу противовирусного химиопрепарата, уменьшая вероятность развития НЛР, сокращая его токсическое воздействие на организм и снижая вероятность возникновения устойчивых штаммов герпес-вирусов. Кроме того, это значительно сокращает продолжительность острого периода болезни и сроки лечения.
Одним из препаратов, показавшим свою эффективность при лечении герпес-ассоциированных заболеваний у детей, является инозин пранобекс. Инозин пранобекс — это синтетическое комплексное производное пурина, обладающее иммуностимулирующей активностью и неспецифическим противовирусным действием. Препарат восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию иммуноглобулина G, интерферонов, интерлейкинов (ИЛ-1 и ИЛ-2), снижает образование провоспалительных цитокинов (ИЛ-4 и ИЛ-10), потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов. Механизм противовирусного действия препарата связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации, усилении подавленного вирусами синтеза мРНК лимфоцитов, что сопровождается угнетением биосинтеза вирусной РНК и трансляции вирусных белков.
Инозин пранобекс малотоксичен, хорошо переносится, в России рекомендован в виде таблеток детям с 3-летнего возраста (масса тела более 15 кг). За рубежом он доступен и в форме сиропа и не имеет возрастных ограничений. Препарат назначается по 50–100 мг/кг/сут внутрь в 3–4 приема в течение всего острого периода болезни (5–10 дней в зависимости от длительности вирусемии и выраженности синдрома интоксикации). В качестве поддерживающей терапии для восстановления иммунологических показателей возможно назначение препарата по иммуномодулирующей схеме (50 мг 2 раза в день в течение 14–28 дней). Доказана высокая эффективность курсовой терапии инозином пранобексом (50 мг/кг массы тела в сутки в 3–4 приема внутрь, три курса лечения по 10 дней с интервалом 10 дней) [7], комбинированной курсовой терапии с использованием инозина пранобекса и рекомбинантного интерферона α-2β (3 курса по 10 дней с интервалом 14 дней) у детей с микст-вирусными инфекциями [8].
Применение инозина пранобекса как препарата с иммунотропным и противовирусным действием на различных этапах лечебно-профилактических мероприятий позволяет избежать полипрагмазии, тем самым снизить медикаментозную нагрузку на организм и уменьшить риск нежелательных эффектов.
Литература
Т. А. Бокова, доктор медицинских наук, профессор
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
Герпесвирусы 6, 7, 8-го типов
За последние 15 лет выделены три новых антропонозных представителя этого семейства — HHV-6, HHV-7, HHV-8, которые характеризуются многообразием клинических проявлений и бессимптомным носительством. HHV-6 Герпесвирус 6-го типа (HHV-6, ВГЧ-6) относительн
За последние 15 лет выделены три новых антропонозных представителя этого семейства — HHV-6, HHV-7, HHV-8, которые характеризуются многообразием клинических проявлений и бессимптомным носительством.
Герпесвирус 6-го типа (HHV-6, ВГЧ-6) относительно недавно внесен в список известных человеческих патогенов и является серьезным претендентом на роль этиологического агента рассеянного склероза и лихорадки новорожденных с судорожным синдромом, инфекционных мононуклеозов негативных по вирусу Эпстайна–Барр (ВЭБ) и цитомегаловирусу (ЦМВ) и ассоциированного с HHV-6 энцефалита. HHV-6 также является кофактором СПИДа, некоторых форм карцином шейки матки и назофарингеальных карцином.
Впервые HHV-6 был выделен в 1986 г. из лимфоцитов периферической крови пациентов с различными лимфопролиферативными заболеваниями, в том числе инфицированных ВИЧ. Новый вирус был назван В-лимфотропным вирусом человека (HBLV — human B-lymphotropic virus). HBLV инфицировал только свежие В-лимфоциты in vitro. Позднее был описан более широкий спектр клеточного тропизма, преимущественно к Т-клеткам, вследствие чего вирус переименовали в HHV-6.
HHV-6 сходен с остальными герпесвирусами, но отличается от них по биологическим, иммунологическим свойствам, спектру чувствительных клеток, антигенной структуре, составу генома, количеству и молекулярной массе структурных вирусных белков. Диаметр вириона — 160–200 нм, тип симметрии икосаэдрический, содержит 162 капсомера, имеет суперкапсидную липидосодержащую оболочку. Геном представлен двунитчатой ДНК. Рестрикционный анализ ДНК HHV-6 установил вариабельность генома различных изолятов вируса. При сравнении первичной структуры геномов HHV-6 и ЦМВ было обнаружено их определенное сходство. Степень гомологии между HHV-6 и ЦМВ была большей, чем между HHV-6 и другими герпесвирусами, что свидетельствует о тесной связи геномов этих двух вирусов.
Исследования изолятов HHV-6 от людей с различной патологией показали, что они принадлежат к двум вариантам: А или В (HHV-6А и HHV-6В). Варианты различаются между собой по клеточному тропизму in vitro, рестрикционному эндонуклеазному профилю, нуклеотидной последовательности, реактивности с моноклональными антителами, сероэпидемиологии и причастности к различным заболеваниям. Инфекция, индуцированная HHV-6А, наблюдается реже, и роль данного варианта вируса в патологии человека недостаточно ясна, а HHV-6В является основным этиопатогеном внезапной экзантемы (Exantema subitum).
Эпидемиология HHV-6-инфекции. Первые клинико-эпидемиологические исследования, проведенные в 1986 г., выявили наличие этой инфекции в зоне отдыха в штате Невада (США). Клинически заболевание выражалось в гриппоподобной симптоматике с повышением температуры, ночным потом, увеличением лимфатических узлов, рядом психологических симптомов (усталость, депрессия). Заболевание получило название «синдром хронической усталости». При этом у 75% больных выявлялись антитела к HHV-6. Год спустя первый больной с клинически сходным заболеванием и антителами к HHV-6 в крови был зарегистрирован в Германии. В дальнейшем эта инфекция была выявлена в Европе (Англия, Швеция) и Африке. При этом разные исследователи сообщили о выделении HHV-6 из клеток крови не только от лиц с различными лимфопролиферативными и гематологическими заболеваниями, инфицированных HTLV-1, ВИЧ-1 и ВИЧ-2 или больных СПИДом, но и от здоровых взрослых.
По данным российских авторов, у 80% здоровых доноров, у 65% ВИЧ-инфицированных и 73% онкологических больных выявляются антитела к HHV-6. При рождении большинство детей серопозитивны за счет материнских антител, титр которых снижается к 5 мес. Однако к одному году процент серопозитивных малышей оказывается таким же, как среди старших детей и взрослых. Высокая частота выявления антител и ранний возраст инфицирования указывают на присутствие вируса в ближайшем окружении. Выделение HHV-6, определение вирусных белков и ДНК в образцах слюны и мокроты указывают на то, что вирус находится в организме человека в слюнных железах, а эксперименты in vitro показали, что он в латентной фазе сохраняется в моноцитах/макрофагах. В естественных условиях основным путем передачи вируса является воздушно-капельный. Нельзя исключить вертикальный путь заражения; антигены вируса присутствовали в абортивном материале в ряде случаев при спонтанных абортах. Также не исключаются половой путь передачи вируса и перинатальная инфекция. Длительная репродукция при острой инфекции и персистенция HHV-6 в клетках крови внешне здоровых людей, включая доноров, является серьезным фактором риска передачи вируса при переливании крови и ее компонентов, трансплантации органов и тканей. Посттрансплантационная серологическая конверсия к HHV-6 отмечается у 43% реципиентов. При этом повышенный титр антител к HHV-6 в крови реципиентов персистировал в течение 2 лет после трансплантации.
Диагностика. Диагностика HHV-6-инфекции основана на сравнительном анализе результатов выделения вируса на чувствительных культурах клеток от больного, обнаружении вирусных белков (при использовании иммунопероксидазного и иммунофлюоресцентного методов, электронной микроскопии) или его генома (при использовании методов гибридизации и полимеразной цепной реакции (ПЦР)) в материалах от больного и выявлении вирусспецифических антител в крови. Вирусспецифические иммуноглобулины класса М (IgM) синтезируются через 2 нед после острой первичной инфекции, достигая титра 1:1280, по данным непрямой иммунофлюоресценции, а класса G (IgG) — на неделю позже и достигают более высокого титра — 1:10240. Поскольку титр IgM быстро снижается и они исчезают через 4–6 нед, острая первичная HHV-6-инфекция диагностируется по наличию IgG (положительным считается титр выше 1:20). Синтез IgM возможен как при первичной, так и при реактивации латентной HHV-6-инфекции. Периодическая реактивация и активная персистентная HHV-6-инфекция у больных с дефектом иммунного ответа, как и при других герпесвирусных инфекциях, приводит к повышению титра вирусспецифических IgG, зачастую без соответствующего повышения титра IgМ.
Первичная HHV-6-инфекция у иммунокомпетентных лиц диагностируется на основании корреляции наличия и нарастания титров вирусспецифических IgG и IgМ с динамикой развития клинических проявлений заболевания. Серологическое исследование должно дополняться выделением вируса и/или обнаружением генома. При иммунных нарушениях и реактивации HHV-6-инфекции число таких геномнесущих клеток возрастает до 50–70, а обнаружение геномнесущих клеток в пределах 200-7500 свидетельствует о патогенетической связи реактивированной HHV-6-инфекции с заболеванием.
Клиника. Спектр заболеваний, связанных с HHV-6, довольно широк. Полиморфизм патологии зависит как от формы инфекции, так и от штаммовых различий вируса.
К заболеваниям, ассоциированным с первичной острой HHV-6-инфекцией, относятся: синдром хронической усталости (миалгический энцефаломиелит); внезапная экзантема у новорожденных и более старших детей (roseola infantum exantema subitum); инфекционный мононуклеоз у подростков и взрослых, не связанный с ВЭБ-инфекцией; гистиоцитарный некротический лимфаденит (KiKuchi’s lymphadenitis).
Заболевания, ассоциированные с персистентной HHV-6-инфекцией, включают: лимфопролиферативные (иммунодефицит, лимфаденопатия, поликлональная лимфопролиферация); злокачественные лимфомы (неходжкинская лимфома, периферическая Т-клеточная лейкемия, В-клеточная лимфома, дерматопатическая лимфаденопатия, болезнь Ходжкина, синусоидальная В-клеточная лимфома, плеоморфная Т-клеточная лимфома).
HHV-6 связывают с различными лимфопролиферативными и иммуносупрессивными заболеваниями, с внезапной экзантемой новорожденных, злокачественными новообразованиями, аутоиммунной патологией, некоторыми заболеваниями ЦНС и др. Реинфекция HHV-6 наблюдается у больных с нарушенным иммунным статусом, иммуносупрессией (трансплантация органов, СПИД и др.).
Доказана этиологическая роль HHV-6 в развитии внезапной экзантемы — широко распространенного заболевания детей в возрасте от 3 мес до 3 лет. В части случаев причиной молниеносной экзантемы является HHV-7. Инкубационный период заболевания — 5–15 дней. Заболевание характеризуется высокой лихорадкой (38,5–40°С) в течение 3–5 дней, в дальнейшем в течение 1–3 дней наблюдаются эритематозная или макулезная кожная сыпь, которая совпадает со снижением температуры. Около половины всех случаев первой в жизни лихорадки новорожденных связаны с первичным инфицированием HHV-6.
С развитием экзантемы связывают преимущественно вариант HHV-6В. В период лихорадки (и даже перед этим) вирус присутствует в CD4+-клетках; в это время выделить вирус из крови больных удается более чем в 90% случаев.
Антитела к HHV-6 отсутствуют в острой фазе болезни и начинают определяться в большинстве случаев на 6–8-й день от начала заболевания. IgM-антитела выделяются на 5-й день лихорадки и обнаруживаются в течение 2–3 нед. IgG-антитела появляются на 7-й день, достигая максимума через 2–3 нед, и персистируют длительное время. Обычно заболевание заканчивается без осложнений, но описаны клинические случаи манифестной инфекции с различными симптомами: лихорадка выше 40°С, воспаление барабанной перепонки, респираторные и гастроинтестинальные симптомы, неврологические осложнения (энцефалиты, менингоэнцефалиты, асептический менингит, судороги с последующей эпилепсией); имеются сообщения о протекании первичной HHV-6-инфекции с гепатоспленомегалией, фатальным фульминантным гепатитом, фатальной диссеминированной инфекцией.
Потенциальная онкогенность HHV-6 и роль в характеризующемся множеством стадий процессе онкогенеза подтверждается следующими фактами. HHV-6 активирует онкопротеины Е6 и Е7 вируса папилломы человека при цервикальной карциноме. ДНК HHV-6 способна индуцировать неопластическую трансформацию клеток NIH3T3 in vitro и на животных моделях.
При анализе образцов слюны от больных назофарингеальной карциномой, методом ПЦР в ряде случаев выявлена ДНК HHV-6. У этих же больных было отмечено достоверное повышение титров антител к HHV-6 класса IgG и, в отличие от здоровой популяции, найдены антитела класса IgA. Таким образом, можно полагать, что наличие антител класса IgA к HHV-6 может служить признаком назофарингеальной карциномы.
Методом ПЦР, гибридизации in situ, ДНК HHV-6 была идентифицирована в тканях и клетках биопсийных образцов ходжкинских, смешанных В- и Т-клеточных неходжкинских лимфом, при ангиоиммунобластоидной лимфаденопатии, африканской лимфоме Беркитта, Т-клеточной острой лимфобластоидной лейкемии, лимфогранулематозе, инфекционном мононуклеозе, не связанном с ВЭБ, и ряде других лимфопролиферативных заболеваний.
Роль HHV-6 в возникновении синдрома хронической усталости обсуждается различными авторами, однако доказательства, которые приводятся в подтверждение этой гипотезы, неоднозначны.
Позднее вирус с аналогичными характеристиками был выделен другими исследователями.
При электронно-микроскопическом исследовании ультратонких срезов клеток, инфицированных HHV-7, выявлены типичные для герпесвируса вирионы диаметром до 170 нм, ДНК 150Кб. Вирионы содержали электронно-плотное цилиндрическое ядро, капсид, тегумент и внешнюю оболочку и имели значительное морфологическое сходство с HHV-6. Гибридизационный анализ показал, что ДНК HHV-7 отличается от ДНК вируса простого герпеса, ВЭБ, опоясывающего лишая и ЦМВ. В то же время ДНК ЦМВ имеет ограниченную перекрестную гибридизацию с ДНК HHV-7 (гомология находится на уровне 36%). Несколько большее сходство выявлено между ДНК HHV и ДНК HHV-7 (по разным данным, гомология находится на уровне 57,5–58,8%). Однако на основании ряда критериев можно сделать вывод, что речь идет о разных вирусах, а не о различных штаммах одного вируса. К настоящему времени HHV-7 классифицируется как член подсемейства β-герпесвирусов.
Распространенность инфекции и пути ее передачи неизвестны. Имеются данные и о выделении HHV-7 из слюны инфицированных, а также персистенции вируса в Т-лимфоцитах, в связи с чем предполагается возможность наличия воздушно-капельного пути передачи инфекции, особенно у детей раннего возраста, и передачи инфекции при переливании крови и ее компонентов. Для выделения и идентификации HHV-7 используют культуру мононуклеаров периферической крови, метод непрямой иммунофлюоресценции, электронной микроскопии, молекулярной гибридизации и сиквенс-анализа ДНК.
Значение HHV-7 в патологии не изучено. HHV-7 ассоциируется с лимфопролиферативными заболеваниями, синдромами хронической усталости и иммунодефицита.
Как самостоятельное заболевание синдром хронической усталости впервые был выделен в 1988 г. Центром по контролю заболеваний (The Centers for Disease Control–CDC, Атланта, США). Поводом для этого послужило внезапное увеличение в штате Невада в 1984 г. числа больных, жалующихся на постоянную усталость, сопровождающуюся рядом соматических и психологических симптомов — при отсутстви видимой причины заболевания. Подобные вспышки заболевания наблюдались и раньше: в Лос-Анжелесе в 1934 г., в Исландии в 1948 г., в Лондоне в 1955 г., во Флориде в 1956 г. Работы по изучению синдрома хронической усталости в США возглавили P. Cheney и D. Peterson. Вскоре в США были открыты специальные клиники для этих больных и создана Национальная ассоциация. Данное заболевание в настоящее время изучается также в Великобритании, Германии, Австралии, Японии и других странах.
В опубликованном CDC в марте 1988 г. в журнале «Annals of Internal Medicine» докладе были сформулированы диагностические критерии (большие и малые) синдрома хронической усталости. Этот диагностический комплекс подвергался пересмотру в 1991, 1992, 1994 гг. К большим (обязательным) диагностическим критериям относят наблюдающиеся в течение не менее 6 мес у ранее здоровых людей постоянную усталость и снижение работоспособности на 50% и более. Вторым обязательным критерием является отсутствие заболеваний или других причин, которые могут вызвать такое состояние.
Малые критерии можно объединить в несколько групп. Первая из них включает симптомы, отражающие наличие хронического инфекционного процесса: субфебрильная температура, хронический фарингит, увеличение лимфатических узлов (шейных, затылочных, подмышечных), мышечные и суставные боли. Вторая группа — психические и психологические проблемы: нарушение сна (гипо- или гиперсомния), снижение памяти, повышенная раздражительность, снижение интеллекта, невозможность концентрации внимания, депрессия и т. д.). Третью группу составили симптомы вегетативно-эндокринной дисфункции: быстрое изменение массы тела, нарушение функции желудочно-кишечного тракта, снижение аппетита, аритмия, дизурия, быстрая физическая утомляемость с последующей продолжительной (более 24 ч) усталостью и др. Четвертая группа объединяет симптомы аллергии и повышенной чувствительности к лекарственным препаратам, инсоляции, алкоголю и некоторым другим факторам.
Согласно диагностическим критериям 1994 г., диагноз синдрома хронической усталости считается достоверным, если у больного выявлены два обязательных критерия и четыре признака из приведенных ниже восьми дополнительных (которые также наблюдаются не менее 6 мес): нарушение памяти или концентрации внимания; фарингит; болезненные шейные лимфатические узлы; мышечные боли; полиартралгии; необычная, новая для больного головная боль; неосвежающий сон; недомогание после физического напряжения.
Распространенность синдрома хронической усталости, по данным большинства исследователей, в разных странах и социально-демографических группах приблизительно одинакова. Заболеванию подвержены люди любого возраста, однако замечено, что женщины в возрасте 25–49 лет болеют чаще, чем мужчины.
Предполагается, что HHV-7 может быть причиной exanthema subitum, но не прямо, а опосредованно, за счет реактивации HHV-6 из латентного состояния. HHV-7 селективно тропен к CD+-Т-клеткам. Показано что вирус инфицирует CD4+ в 42%, а CD8+ в 4% случаев. При взаимодействии HHV-7 и HIV ВИЧ появляется конкурирующий эффект за очередность инфицирования CD+-лимфоцитов.
HHV-8 — это герпесвирус, ассоциированный с саркомой Капоши (KS). Был недавно открыт и идентифицирован молекулярным клонированием с использованием тканей саркомы Капоши. KS — многоочаговая злокачественная опухоль сосудистого происхождения с преимущественным поражением кожных покровов и вовлечением внутренных огранов и лимфатических узлов. Выделяют четыре различные эпидемиологические формы KS: классическая, африканская, ятрогенная и СПИД-ассоциированная KS. HHV-8 подразделяют на три варианта: А, В и С — на основании различий в нуклеотидных последовательностях субсегментов генома.
Вариант А связывают с классической KS и со СПИД-ассоциированными поражениями кожи и внутренних органов, а В и С — с лимфопролиферативными заболеваниями (лимфомами, генерализованными лимфаденопатиями, болезнью Кастлемана).
Вирусная теория развития KS первые была выдвинута в 1967 г. B. MacKinney, изучавшим ее эпидемиологию у жителей Африки. В дальнейшем эту концепцию поддержали многие другие ученые, предполагавшие причастность к этому заболеванию вирусов группы Herpes: ВЭБ, ЦМВ в ассоциации с вирусом простого герпеса 1-го и 2-го иммунотипа, также вируса Т-клеточной лимфомы человека (HTLV).
Новый этап в понимании роли вирусов в развитии KS наступил в 1994 г., когда Y. Chang и соавторы обнаружили в ПЦР с использованием синтезированного ими праймера KS 330233 присутствие уникальной ДНК-последовательности в геноме опухолевых клеток, выделенных из биоптата очагов поражений кожи больного со СПИД-ассоциированным типом KS.
С учетом высокой частоты обнаружения HHV-8 в клетках очагов поражений KS, данных эпидемиологических исследований (обнаружение HHV-8 в очагах поражений больных различными типами KS как из эндемичных, так и неэндемичных регионов), а также подтверждения трансформирующего потенциала некоторых его генов, этот вирус в настоящее время рассматривается как наиболее вероятный кандидат на роль этиологического фактора данного заболевания. Это подтверждается и биологическими свойствами HHV-8: было установлено, что он кодирует белки, контролирующие рост и пролиферацию клеток, и обладает генетическим сродством по отношению к представителям подсемейства радиновирусов, обладающих трансформирующими свойствами. Этиологическая роль HHV-8 в развитии KS также была подтверждена в России. Причем сывороточные антитела к этому вирусу у здоровых доноров из России обнаруживались в 9,6% случаев.
Данные подтверждают возможность персистенции вируса в группах здоровых лиц и его активации в условиях иммуносупресии.
Высокая частота выявления HHV-8 в эякуляте здоровых доноров жителей Италии, которая также является эндемичным по KS регионом, не исключает возможности полового пути передачи данной инфекции. В связи с этим представляют интерес данные S. Lin и соавторов (1995), показавших, что у 13 из 30 ВИЧ-позитивных пациентов с наличием в эякуляте HHV-8 в течение 5 лет развилась KS, тогда как в эякуляте 30 ВИЧ-негативных пациентов без HHV-8 в те же сроки наблюдения KS не развилась ни в одном случае. Проведенные исследования отечественных авторов и полученные ими данные свидетельствуют о том, что ткани урогенитального тракта в некоторых случаях могут быть местом латенции HHV-8. При этом высокая частота хронических воспалительных поражений мочеполовых органов в группе больных c KS должна рассматриваться в качестве фактора, нарушающего гематотестикулярный барьер и тем самым способствующего проникновению в эякулят клеток воспаления, включая инфицированные HHV-8 В-лимфоциты. Необходимо учитывать роль хронического воспаления в снижении общего иммунитета и местного иммунного контроля в тканях репродуктивной системы.Такое воспаление может приводить к активации персистирующего там HHV-8. Установлено, что до 10% вирусов HHV-8, выявляемых в очагах поражения KS, находятся в литической фазе, в связи с чем этот вирус должен с высокой частотой обнаруживаться в лимфоцитах периферической крови. Однако HHV-8 в лимфоцитах периферической крови выявляется, как правило, только у больных с выраженной иммуносупрессией (СПИД-ассоциированным и иммуносупрессивным типом заболевания), тогда как у пациентов с другими типами KS инфицированные клетки содержатся в очагах поражения в эякуляте, а из крови, по-видимому, достаточно эффективно элиминируются. HHV-8 обнаруживали в эякуляте только при наличии у больных с KS хронического воспалительного процесса мочеполовых органов (хронический уретропростатит). Таким образом, эякулят у больных с KS является естественным резервуаром инфекции HHV-8. Инфицированные вирусом HHV-8 лимфоциты проникают в эякулят и сохраняются в нем в условиях аккумуляции CD8+ Т-лимфоцитов, ингибирующих иммунный ответ не только на сперматозоиды, но и на эти инфицированные клетки.
Вирус широко распространен в популяции: более 25% взрослого населения и 90% ВИЧ-инфицированных имеют антитела к литическим белкам HHV-8. HHV-8, как и ВЭБ или HVS, инфицирует в первую очередь лимфоциты и ассоциирован с клеточной трансформацией и иммортализацией. HHV-8 является возможным этиологическим агентом всех форм KS, связан с развитием некоторых В-клеточных лимфом, ангиоиммунобластоидной лимфаденопатии, болезни Кастлемана и ряда других лимфопролиферативных заболеваний.
Несмотря на большой арсенал антигерпетических препаратов терапия заболеваний, вызванных данными вирусами, представляет значительные трудности. Это обусловлено генотипическими особенностями возбудителя, длительной персистенцией вируса в организме, различной чувствительностью к препаратам. Исследования антивирусного действия некоторых препаратов показали, что HHV-6, 7, 8 малочувствительны к аналогам нуклеозидов. С определенным успехом в лечении были использованы ганцикловир и фоскарнет. Однако препаратов, которые были бы достаточно эффективны в лечении инфекции, вызванной HHV-6, 7, 8, пока не найдено.
Литература
Е. Г. Белова, кандидат медицинских наук, доцент
Т. К. Кускова, кандидат медицинских наук
МГМСУ, Москва
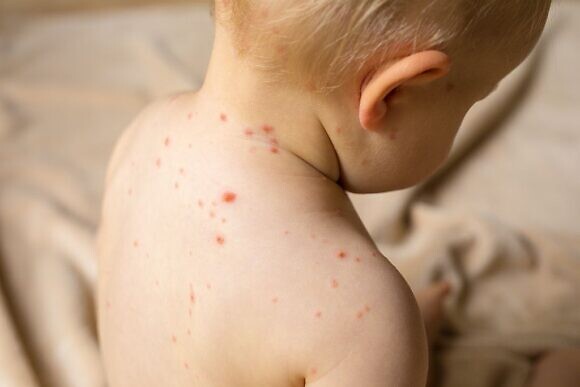

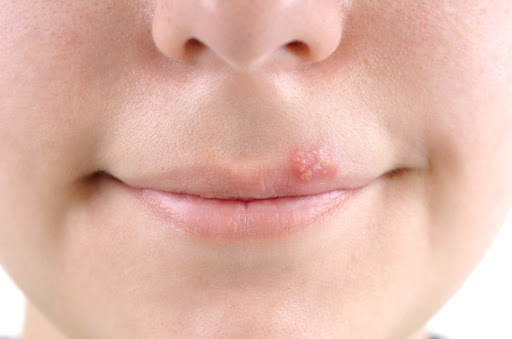
.jpg)
_575.gif)