Чем лечить гипоксию головного мозга у ребенка до года
Гипоксия в родах. Помощь остеопата
Гипоксически-ишемическое поражение центральной нервной системы перинатального генеза – это очень частый диагноз, с которым обращаются родители со своими детьми. 75-85% заболеваний нервной системы у детей своими истоками уходят в ранние сроки внутриутробного развития или проблемы в родах. Внутриматочная гипоксия и гипоксия в родах обуславливают нарушения маточно-плацентарного кровообращения, что может сопровождаться недостатком кислорода у плода. Гипоксические нарушения у детей часто связаны с функциональным дисбалансом, ограничением кровотока и движения ликвора. Остеопатия нормализует движения в теле и способствует питанию мозга, исправлению негативных послествий перенесенной гипоксии.
Гипоксия и асфиксия, происходящие в родах и в период новорожденности, не проходят бесследно и могут оказать негативное воздействие на развивающийся мозг. Исходом может стать значительная потеря нейронов, дистрофические изменения нервных клеток в коре головного мозга и в подкорковых структурах и желудочках головного мозга.
В клинической картине могут быть такие симптомы:
Диагностика гипоксии
Дети с диагнозом перинатальное постгипоксическое поражение ЦНС наблюдаются неврологом в течение 2 лет. По истечении этого срока диагноз снимается, либо меняется на более сложный (ДЦП, гидроцефалия и тд).
Методы диагностики постгипоксического состояния:
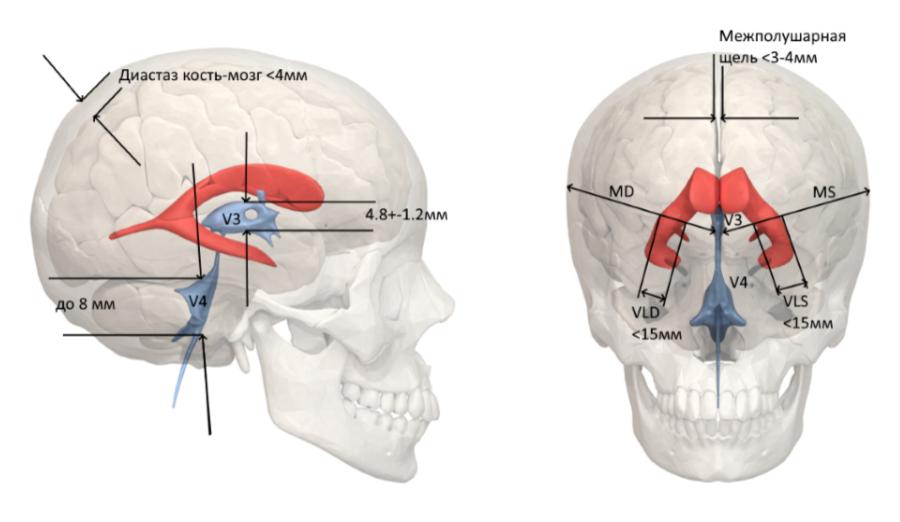
На УЗИ головного мозга определяются следующие постгипоксические изменения:
Периодичность проведения исследований у детей, перенесших гипоксию, 1 раз в 3 месяца до года и 1 раз в 6 мес. на втором году жизни.
Оценка по шкале Апгар не единственный критерий перенесенной гипоксии. Например, у плода, в ответ на недостаток кислорода, открывается сфинктер прямой кишки и меконий выходит в околоплодные воды, из-за чего они становятся зелеными. О кислородном голодании может свидетельствовать также состояние плаценты (преждевременное старение, аномалия развития сосудов, и т.д.). Иногда такие дети рождаются с высокой оценкой по шкале Апгар, но гипоксия все-таки имела место.
Мозг детей в первые 2 года жизни очень пластичный и с удовольствием принимает все методы лечения, быстро откликается и выдаёт прекрасные результаты. В последнее время остеопатическое лечение занимает заслуженное место в программе лечения детей, перенесших гипоксию.
Последствия гипоксии
Ранее мы рассматривали причины и диагностику постгипоксических состояний и договорились о том, что дети, родившиеся с оценкой 7 баллов по Апгар и ниже, рассматриваются как перенесшие гипоксию. К этой группе также относятся дети, имевшие обвитие пуповиной, недоношенные дети и т.д.
Крайне важно регулярно проводить осмотры таких детей в динамике в определенные возрастные периоды: 1 мес., 3 мес., 6 мес., 9 мес., 1 год. Целью осмотра и наблюдения является профилактика и уменьшение хронических заболеваний и снижение степени отдаленных последствий. Около 83% детей, перенесших гипоксию, имеют поражения ЦНС в различных проявлениях и сочетаниях.
В течении заболевания выделяют 3 периода:
Самые частые симптомы поражения ЦНС в остром и восстановительном периоде. Иногда эти симптомы проявляются в сочетании друг с другом:
Выражается гипертнусом икроножных мышц, тугоподвижностью в голеностопных суставах, хождением на цыпочках, задержкой темпов речевого развития, а также двигательного.
При наличии данных симптомов не стоит дожидаться планового осмотра, лучше сразу обратиться к неврологу и остеопату для ранней диагностики и лечения.
Лечение гипоксии
Постгипоксическое поражение ЦНС требует этапного лечения после проведения реанимационных мероприятий (если они были необходимы) начинается восстановительный период, применяется:
Остеопатическое лечение гипоксии в родах
Остеопатическое лечение по праву занимает одно из ведущих мест в реабилитации детей, перенесших гипоксию. Балансировка костей черепа позволяет снять напряжение с твердой мозговой оболочки и с полушарий головного мозга, тем самым обеспечивая максимально полноценное функционирование ЦНС.
Остеопатические методики позволяют осуществить дренаж венозных синусов, в результате чего налаживается резорбция ликвора и нормализуется внутричерепное давление. Освобождение шейного отдела позвоночника, устранение кривошеи способствует адекватному кровоснабжению головного мозга.
Раннее проведение остеопатического лечения на первом году жизни позволяет детям не только не отставать в развитии от своих сверстников, но иногда даже развиваться с опережением. Очень важно проводить это лечение с первых месяцев жизни, так как это поможет избавиться от отдаленных клинических патологических симптомов. Сеансы остеопатии детям проводятся начиная с первого месяца жизни. Остеопатическое лечение, создавая оптимальное функционирование ЦНС останавливает процесс постгипоксических изменений в нейронах, тем самым как-бы перепрограммирует мозг на полноценное развитие.
Не нужно бояться гипоксии, нужно предпринять весь комплекс мер для реабилитации после неё. Тем более, что современная медицина даёт нам множество инструментов для этого.
Преимущества лечения последствий гипоксии родов в нашем медицинском центре Неонатус Санус
Мы умеем и любим работать с маленькими детьми!
В нашей клинике работают опытные врачи-остеопаты, неврологи. Каждому малышу уделяется много внимания, чтобы понять ребенка, точно оценить его состояние, дать рекомендации родителям и при необходимости провести эффективное остеопатическое лечение.
В нашем центре вы можете получить лучшее обследование, лечение и рекомендации от ведущих специалистов Санкт-Петербурга.
Клинический пример лечения последствий гипоксии в нашем остеопатическом центре
Отзыв наших пациентов о лечении гипоксии
Катюша родилась от первой беременности на сроке 40 недель. Состояние после рождения было тяжелым за счёт асфиксии. Оценка по шкале Апгар 1/4 балла. Через 3 часа в связи с дыхательной недостаточностью и судорогами была переведена на реанимационное отделение. Проводилась искусственная вентиляция легких, гипотермия мозга.
Результатом тяжелой гипоксии мозга явился диагноз: Детский Церебральный Паралич, правосторонний спастический гемипарез. В возрасте 1 года 6 месяцев она впервые появилась в нашем центре. Основной жалобой была задержка двигательного развития, ходьба самостоятельная появилась только в 1год и 4 месяца. При ходьбе испытывала большие проблемы в связи с высоким гипертонусом мышц по всей правой стороне, отмечалось косоглазие и беспокойное поведение.
После проведённого лечения у девочки практически нормализовался мышечный тонус, походка максимально приблизилась к физиологической, у девочки прекрасное речевое развитие, она с удовольствием ходит в детский сад и общается со сверстниками.
Благодарим родителей за предоставленный видеоматериал.
Чем лечить гипоксию головного мозга у ребенка до года
Иркутская государственная медицинская академия последипломного образования — филиал ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Иркутск, Россия
Иркутская государственная медицинская академия последипломного образования — филиал ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Иркутск, Россия
Гипоксически-ишемические поражения головного мозга у недоношенных новорожденных
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2019;119(8-2): 63-69
Анурьев А. М., Горбачев В. И. Гипоксически-ишемические поражения головного мозга у недоношенных новорожденных. Журнал неврологии и психиатрии им. С.С. Корсакова. Спецвыпуски. 2019;119(8-2):63-69.
Anuriev A M, Gorbachev V I. Hypoxic-ischemic brain damage in premature newborns. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2019;119(8-2):63-69.
https://doi.org/10.17116/jnevro201911908263
Иркутская государственная медицинская академия последипломного образования — филиал ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Иркутск, Россия
Одной из главных причин церебральной дисфункции у недоношенных новорожденных является гипоксия. Высокая смертность и пожизненная инвалидизация у этих детей — частый результат неонатального гипоксического повреждения головного мозга. В статье представлены данные по распространенности неврологических заболеваний, возникших в перинатальном периоде, отмечены ключевые этиологические факторы, приводящие к гипоксии как в интранатальном, так и в раннем постнатальном периоде. Подробно описан патогенез гипоксически-ишемических поражений головного мозга у недоношенных новорожденных. Рассмотрены система глутатиона, защищающая от процессов перекисного окисления липидов, глутамат-кальциевый каскад и опосредованная им эксайтотоксичность, а также процессы некроза и апоптоза нервных клеток. Отмечены преимущества и недостатки современных методов диагностики церебральных повреждений, а также проанализированы принципы терапии данных нарушений.
Иркутская государственная медицинская академия последипломного образования — филиал ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Иркутск, Россия
Иркутская государственная медицинская академия последипломного образования — филиал ФГБОУ ДПО «Российская медицинская академия непрерывного профессионального образования» Минздрава России, Иркутск, Россия
Преждевременные роды являются главной причиной младенческой смертности и серьезным фактором утраты человеческого потенциала выживших детей в течение последующей жизни. По данным зарубежных авторов, во всем мире ежегодно рождаются несколько миллионов детей с очень низкой массой тела (ОНМТ) [1]. В США 90% из 65 000 новорожденных младенцев с ОНМТ переживают неонатальный период из-за больших успехов в интенсивной терапии, однако у 5—10% этих детей позже обнаруживают детский церебральный паралич [2].
Внедрение современных медицинских технологий в последнее десятилетие отмечено снижением перинатальной и младенческой смертности. Вместе с тем повышение коэффициента выживаемости детей с ОНМТ и экстремально низкой массой тела (ЭНМТ) при рождении влечет за собой повышение заболеваемости и формирование ранней инвалидности [3]. Среди причин детской инвалидности патология нервной системы занимает первое место, а вклад перинатальных поражений достигает 60—80% всех неврологических заболеваний [4]. В России ежегодно из числа освидетельствованных инвалидов с детства признаются трудоспособными не более 2,5—5% по сравнению с 50% за рубежом [5].
Среди факторов, неблагоприятно влияющих на антенатальный период, большое значение имеет нарушение маточно-плацентарного кровообращения, причиной которого могут быть как экстрагенитальная, так и соматическая патология матери [6]. Нарушения маточно-плацентарного кровотока в свою очередь приводят к развитию гипоксии, являющейся центральным звеном патогенеза антенатального повреждения плода, и в первую очередь центральной нервной системы (ЦНС). В работах многих авторов установлен целый комплекс физиологических приспособительных реакций плода к неблагоприятным условиям развития, в частности к гипоксии [7—10]. Однако информации о биохимическом статусе нервной ткани плода и новорожденного при данной патологии недостаточно. Большой интерес в этом плане представляет изучение метаболизма глюкозы, особенностей свободнорадикального окисления и обмена глутамата, процессов некроза и апоптоза.
Внутриутробно плод находится в состоянии гипоксии, однако эта среда для него является физиологической, более того, на ранних этапах эмбрионального периода она необходима для нормальной дифференцировки клеток. Оксигенация плода зависит от градиентов парциального давления кислорода между материнской и плацентарной кровью, плодной кровью и плодной тканью. Известно, что в первые недели после зачатия в эмбриональном периоде уровень парциального давления кислорода (рО2) чрезвычайно низок и составляет около 18—20 мм рт.ст. Предположительно, это необходимо для защиты эмбриона, который очень чувствителен к повреждающему действию реактивных форм кислорода [11]. Гипоксия в эмбриональном периоде вызывает ангиогенез и является предпосылкой для поддержания плюрипотентности стволовых клеток [12]. Примечательно, что в I триместре беременности эмбриональные стволовые клетки развиваются при уровне рО2 около 10—15 мм рт.ст., тогда как в эндометрии рО2 составляет около 25 мм рт.ст. Стволовые клетки демонстрируют более эффективный рост и дифференцировку при низких давлениях кислорода — 10—15 мм рт.ст. [13]. Длительная гипоксия будет стимулировать ангиогенез посредством транскрипционной и посттранскрипционной регуляции факторов роста: фактор роста эндотелия сосудов, эритропоэтин, фактор роста плаценты и ангиопоэтин1 [14].
Основным регулятором адаптивных ответов клетки на гипоксию является индуцированный гипоксией фактор1 (ИГФ-1), гетеродимерный транскрипционный фактор, включающий субъединицы (ИГФ-1α и ИГФ-1β). ИГФ-1α стабилизируется, когда концентрация кислорода ниже определенного критического порога, таким образом, накапливаясь в гипоксической среде. ИГФ-1β присутствует в ядре клетки, и в условиях гипоксии он димеризуется с ИГФ-1α, улучшая доставку кислорода в ткань [15, 16]. На 14—16-й неделе беременности рО2 поднимается до стабильных значений 45—50 мм рт.ст. и сохраняется таковым до конца беременности. На поздних сроках беременности скорость пролиферации и дифференцировки клеток снижается [17, 18]. Процессы перекисного окисления липидов присутствуют с самого начала беременности, что способствует нормальному развитию плода. В конце I триместра физиологический окислительный стресс вызывает регрессию ворсинок, которые были сформированы на всей поверхности хорионического мешка, чтобы сформировать окончательную дискоидную плаценту [19]. Постнатальное увеличение концентрации кислорода вызывает всплеск образования его активных форм, при этом экспрессия антиоксидантных ферментов, таких как супероксиддисмутаза, каталаза и глутатионпероксидаза, динамически увеличиваются в течение последних недель беременности. Аналогичным образом повышается доступность наиболее важных неферментативных антиоксидантов: глутатиона, гемоксигеназы, витаминов С и Е, β-каротинов и т. д. [20]. Недоношенный ребенок более подвержен риску свободнорадикального повреждения [21]. Считается, что использование высоких концентраций кислорода во время реанимации новорожденных вызывает гипероксемию. При этом была обнаружена значительная корреляция между окисленным глутатионом (GSSG), рО2 и активностью ферментов окислительно-восстановительного цикла глутатиона [22, 23]. Многие заболевания, связанные с недоношенностью, такие как ретинопатия, бронхолегочная дисплазия, внутрижелудочковые кровоизлияния, связаны со свободнорадикальным повреждением в результате незрелости антиоксидантной системы недоношенных детей [24].
— Недостаток кислорода. Дефицит кислорода как акцептора электронов в тканях приводит к нарушению транспорта электронов в цикле Кребса и дыхательной цепи, восполнению энергии путем увеличения мозгового кровотока и анаэробного метаболизма [28].
— Роль свободных радикалов. Гипоксия-ишемия вызывает неадекватное насыщение митохондриальной цитохромоксидазы, нарушение транспорта электронов в митохондриях, что приводит к повышению концентрации супероксид-аниона и поступлению свободных радикалов из митохондрий в цитоплазму [31]. Повышение концентрации внутриклеточного Са 2+ активирует NO-синтетазу, циклооксигеназу и липооксигеназу, что способствует образованию свободных радикалов. Их избыток приводит к дополнительному высвобождению возбуждающих аминокислот и активации NMDA-рецепторов [32].
— Факторы воспаления. Действие гипоксии — ишемии на микроглию способствует синтезу цитокинов, интерлейкина-1β (ИЛ-1β), фактора некроза опухоли α (TNFα) [33]. Активность ИЛ-1β сопровождается продукцией специфических протеаз и развитием апоптоза. Избыточное образование TNFα обладает прямым токсическим эффектом и вызывает сосудистую инфильтрацию с высвобождением цитотоксических факторов, активных форм кислорода и цитокинов [34].
— Роль оксида азота (NO). NO-синтетаза содержится в эндотелиальных клетках, астроцитах, нейронах. Существует 3 изоформы NO-синтетазы: нейронная (регулирует синаптогенез и ремоделирование и зависит от Са 2+ ); эндотелиальная (регулирует сосудистый тонус, особенно вазодилатацию, и зависит от Са 2+ ); индуцируемая (присутствует в макрофагах и астроцитах, индуцируется цитокинами, независима от Са 2+ ) [35]. Активация NMDA-рецепторов вызывает продукцию нейронной NO-синтетазы, которая способствует образованию радикала оксида азота (NO.) и повреждению нейрональной ДНК [36].
Наиболее значительные потери клеток нервной ткани развиваются спустя 2—6—48 ч после рождения, вследствие патологического окислительного стресса. В таких условиях в первые часы и сутки жизни после рождения у новорожденных, перенесших гипоксию, развивается выраженный дисбаланс в системе регуляции церебрального кровообращения, который обостряет течение ишемического процесса [39].
Особенностью недоношенных детей является незрелость антиоксидантной системы, поскольку физиологическое увеличение антиоксидантной способности происходит в конце беременности, именно поэтому они более подвержены воздействию окислительного стресса, особенно когда их состояние требует проведения респираторной терапии [40]. В связи с этим возникает необходимость изучения окислительного стресса у этих детей, в частности путем измерения продуктов перекисного окисления липидов и компонентов антиоксидантной системы.
Известно, что антиоксиданты обладают противовоспалительной активностью, а систему глутатиона рассматривают как критический фактор развития воспаления и иммунных ответов [41, 42]. Это подтверждается изменением уровня цитокинов, острофазных белков и глутатиона во время воспаления [43, 44]. Система глутатиона включает его формы, ряд ферментов его синтеза и катаболизма, и механизмы транспорта. Все эти компоненты вносят важный вклад в изменение глутатионового статуса [45].
Изучая классификацию церебральных поражений у новорожденных, необходимо отметить, что наиболее популярной у неонатологов является классификация гипоксической энцефалопатии по H. Sarnat и M. Sarnat [46]. Она объединяет клинические признаки церебральной ишемии и результаты электроэнцефалографии (ЭЭГ). В данной классификации оцениваются основные показатели новорожденного: уровень сознания, нерво-мышечный статус, рефлексы, вегетативная функция, наличие судорог, ЭЭГ. В зависимости от выраженности церебральной дисфункции устанавливают I, II или III стадию энцефалопатии. Канадские неонатологи модифицировали классификацию Sarnat, дополнив ее расстройствами терморегуляции и исключив ЭЭГ и некоторые другие показатели [47]. Неонатологи Великобритании используют классификацию гипоксических церебральных нарушений L. Dubowitz и соавт.[48]. В международной классификации болезней 11-го пересмотра (МКБ-11) гипоксически-ишемические поражения головного мозга у новорожденных относятся к группе «неврологических расстройств, характерных для перинатального и неонатального периодов» [49]. Основным отличием от классификации 10-го пересмотра является то, что в МКБ-11 данная группа дополнена заболеваниями, которые ранее не выделяли отдельно. Например, перинатальный артериальный инсульт и неонатальный церебральный синовенозный тромбоз. В то же время из предложенной классификации была исключена врожденная гидроцефалия. Диагноз асфиксии новорожденного поместили в «группу других нарушений, возникающих в перинатальном периоде». При этом отдельно выделили асфиксию новорожденного с оценкой по шкале Апгар 0—3 балла и асфиксию новорожденного с оценкой по шкале Апгар 4—6 баллов. Что касается церебральных повреждений гипоксически-геморрагического характера, то их отнесли к группе «геморрагических и гематологических нарушений у плода и новорожденного». При этом несколько изменилась классификация внутрижелудочковых кровоизлияний. В МКБ-11 принято выделять 4 степени внутрижелудочковых кровоизлияний, в то время как в МКБ-10 3-я и 4-я степени были объединены.
Симптомы тяжелого повреждения ЦНС могут проявляться не сразу после рождения, а спустя несколько часов. При этом клиническая симптоматика не всегда отражает истинную степень тяжести заболевания. В связи с этим особую актуальность приобретает прижизненная оценка изменений, возникающих в клетках нервной ткани в раннем неонатальном периоде. Ультразвуковое исследование (УЗИ) позволяет выявить структурные изменения головного мозга новорожденных при перинатальном гипоксическом поражении ЦНС. Анализ ультразвуковых и патоморфологических данных свидетельствует о том, что характер ишемического поражения головного мозга зависит не только от тяжести перинатальной гипоксии, но и от зрелости ребенка [50]. У доношенных новорожденных ишемия мозга сопровождается возникновением избирательного нейронального некроза, субкортикальной и мультикистозной энцефаломаляциями, инфарктами мозга [51]. Тяжелая перинатальная гипоксия у недоношенных 34—37-й недель гестации, как правило, приводит к развитию перивентрикулярной лейкомаляции. В связи с выхаживанием глубоко недоношенных детей с ЭНМТ при УЗИ стали чаще выявлять такие формы ишемического повреждения, как диффузная лейкомаляция и перивентрикулярный геморрагический инфаркт. Следует отметить, что в первые 24—48 ч дебюта неонатального артериального ишемического инсульта данный метод не обладает достаточной чувствительностью и специфичностью, так как очаг ишемического поражения начинает появляться только на 2—3-и сутки от начала ишемии, что связано с ходом патогистологических процессов. Выраженность воспалительной реакции, интенсивность некроза и апоптоза достигают своего пика через 48—72 ч после нарушения кровообращения [52]. Это приводит к изменению эхогенности поврежденной мозговой паренхимы. Дальнейшая оценка эволюции ишемического очага не уступает по информативности магнитно-резонансной томографии (МРТ) [53, 54]. Повысить чувствительность УЗИ на ранних сроках церебрального повреждения помогает применение ультразвуковой допплерографии. Дуплексное сканирование позволяет объективно оценить гемодинамические характеристики церебральных сосудов. Ценность ультразвуковой допплерографической методики в остром периоде заболевания — выявление фазы вазодилатации, наиболее раннего признака ишемического повреждения, возникающего уже через 30 мин после развития сосудистой катастрофы и сохраняющегося в течение первых 5—6 сут [55]. Вазодилатация развивается в ответ на действие различных метаболитов и способствует увеличению поступления в ишемизированную ткань глюкозы и кислорода. Ее характерными признаками являются повышение скорости кровотока и снижение индексов периферического сопротивления в поврежденном сосудистом бассейне [56, 57]. МРТ стала наиболее информативным методом диагностики перинатальных повреждении головного мозга. Наличие различных импульсных последовательностей обеспечивает высокую чувствительность и специфичность, даже на ранних сроках развития сосудистой катастрофы [58, 59]. МРТ с получением диффузионно-взвешенных изображений и построением карт измеряемого коэффициента диффузии (ИКД) позволяет выявить ишемический очаг уже через 30 мин от момента его возникновения. ИКД служит количественной характеристикой диффузии в ткани и отражает наличие внутриклеточного отека [60]. Представленные диагностические методы необходимы для выявления, определения локализации, степени тяжести повреждения мозга и прогноза. Недостатками их являются короткий временной диагностический интервал и ограниченная возможность повторного исследования [61]. В течение последних 20 лет для прогнозирования исходов церебрального повреждения у новорожденных изучается диагностическая ценность биомаркеров [62, 63]. Учитывая патофизиологические изменения, происходящие в результате повреждения ткани головного мозга, были подробно изучены нейропротеины, кальций-связывающий белок, вазоактивные вещества, маркеры окислительного стресса, медиаторы воспаления и т. д. [64—67]. Однако, несмотря на перспективность изучения биомаркеров, отсутствуют данные о практическом их применении в медицине.
Лечение гипоксических поражений головного мозга является предметом жарких дискуссий и крайних мнений — от полного отказа в необходимости лечения нейротропными препаратами до агрессивной полипрагмазии [26]. Согласно современным воззрениям гипоксически-ишемическая энцефалопатия возникает при асфиксии, как правило, в структуре полиорганных расстройств, поэтому основной принцип терапии заключается в выведении ребенка из асфиксии и поддержании витальных функций [68]. Специфическое лечение гипоксически-ишемической энцефалопатии — терапия отека головного мозга и нейропротекция, которая подразумевает в первую очередь контроль объема цереброспинальной жидкости (ЦСЖ), церебральной перфузии и объема вещества мозга. Церебральная перфузия зависит от артериального притока, венозного оттока и интенсивности метаболизма нервной ткани. На этом этапе большое значение имеет адекватность проводимой искусственной вентиляции легких и эффективность гипотермии. Необходимо отметить, что гипотермия проводится у новорожденных с гестационным возрастом не менее 36 нед при наличии по крайней мере одного из признаков, изложенных в специальных критериях [69]. Контроль объема жидкости в ЦСЖ-путях осуществляется за счет торможения выработки ЦСЖ и улучшения ее оттока. Контроль объема мозга подразумевает усиление активного транспорта и стабилизацию мембран нейронов. Следует отметить, что на данный момент применение лекарственных препаратов в неонатологии ограничено из-за высокого риска развития побочных эффектов и отсутствия доказательной базы. Однако поиск таких препаратов продолжается по настоящее время. В частности, за последние два десятилетия произошли значительные изменения в понимании роли эритропоэтина в качестве нейропротектора. Доказано, что эритропоэтин участвует в нейрогенезе и ангиогенезе во время эмбрионального развития и активируется после травмы головного мозга [70], а также оказывает цитопротективное действие на эндотелиальные, глиальные клетки и нейроны [71]. Впервые нейропротективная роль эритропоэтина была выявлена в нескольких исследованиях in vitro и in vivo [72]. При этом удалось выяснить, что эритропоэтин обладает антиапоптотическим [73], антиоксидантным [74] и противовоспалительным эффектами [75]. Кроме того, он ослабляет эффекты воспаления, снижая реактивный астроцитоз и подавляя активацию микроглии, и уменьшает количество иммунных клеток в месте воспаления [76]. Известно, что отсутствие эндогенного эритропоэтина увеличивало ишемическое повреждение головного мозга и ухудшало выживаемость нейронов [77]. Установленные защитные эффекты эритропоэтина во время ишемии и реперфузии побудили использовать рекомбинантный эритропоэтин у недоношенных детей с церебральной ишемией, внутрижелудочковыми кровоизлияниями и перивентрикулярной лейкомаляцией [78]. Так, в одном из исследований оценивали эффективность и безопасность применения эритропоэтина при неонатальной гипоксически-ишемической энцефалопатии. В данное исследование были включены 167 новорожденных с умеренным и тяжелым церебральным поражением. Всех детей разделили на две группы. Дети первой группы получали стандартную терапию гипоксически-ишемической энцефалопатии, а детям второй группы к стандартной терапии был добавлен эритропоэтин в дозировке 300 и 500 ЕД/кг. Препарат вводили в первые 48 ч через день в течение 2 нед. Оказалось, что летальность и инвалидность на 19,2% чаще встречалась в группе детей, не получавших эритропоэтин [79].
Таким образом, проблема церебрального повреждения ишемического типа у недоношенных новорожденных является весьма актуальной. Прежде всего это подтверждается высокой частотой встречаемости данной патологии и большим риском летального исхода и инвалидизации детей. Остается открытым вопрос комплексной диагностики церебральных нарушений у недоношенных детей, потому как не существует единого алгоритма, объединяющего данные клинической картины, инструментальных и лабораторных методов исследования. Большой интерес представляет поиск предикторов неблагоприятного исхода с целью оптимизации лечебных подходов.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Чем лечить гипоксию головного мозга у ребенка до года
Гипоксия у новорожденных и детей старшего возраста
Гипоксия (или кислородное голодание) — довольно частая патология, которая встречается у детей всех возрастов и особенно у новорожденных.
У новорожденных, гипоксия зачастую спровоцирована заболеваниями матери, которые влияют на внутриутробное развитие ребенка и затрудняющих процесс родов. В их число входят проблемы с кровеносной системой, сердечная недостаточность, неправильный образ жизни – курение, алкоголь, прием запрещенных при беременности препаратов, – и многое другое. Если к гипоксии ребенка, возникшей от заболеваний матери, присоединяется еще и патологические роды, то степень гипоксии может увеличиваться во много раз.
В данной статье мы будем рассматривать начальные проявления недостаточности кровоснабжения мозга.
Повреждение шейного отдела позвоночника, перинатальная энцефалопатия, асфиксия и другие диагнозы могут быть выставлены ребенку сразу после родов, которые и будут являться распространенными причинами развития гипоксии головного мозга. Родители чаще всего приходят к детскому неврологу или другому узкому специалисту, когда нервная система ребенка получает повышенную нагрузку – диагноз ставится непосредственно перед школой или в первом классе. Причем, по оценке специалистов, число таких детей сегодня составляет 70-80%. Самыми частыми жалобами родителей является:
Несмотря на то, что очень часто гипоксию головного мозга в результате сосудистых нарушений диагностируется очень часто у школьников, ее первые симптомы можно заметить на первом году жизни ребенка. Такие дети буквально с первых дней отличаются повышенной возбудимостью, у них присутствуют нарушения сна и аппетита, повышенный тонус мышц, угнетение безусловных рефлексов.
Основной и самой частой причиной появления гипоксии у детей является родовая травма. Стремительные роды, стимуляция родовой деятельности, кесарево сечение являются пусковым механизмом для ослабления той или иной функции детского организма, в результате чего появляются симптомы характерные для сосудистых нарушений. Во время движения по родовым путям шейный отдел ребенка испытывает огромные нагрузки, что может вызвать смещение шейных позвонков и привести к нарушению кровоснабжения головного мозга.
Не менее распространено и опасно сдавливание, деформация и повреждение костей черепа. Все это напрямую отражается на оболочках головного мозга и на кровообращении и снабжении его кислородом.
Нервная система вместе с мышечной, костной, системой кровообращения и другими системами является частью единого целого организма и нарушения или изменения функции и структуры в одной из них всегда вызывает сбой в других. Поэтому сосудистые нарушения головного мзга – это всегда комплекс нарушений и симптомов, характеризующийся индивидуальностью для каждого ребенка. И если некоторые из этих проявлений есть у вашего ребенка, желательно не откладывать визит к специалистам.
Лечение ребенка с гипоксией всегда должно быть комплексным: главное в процессе лечения сосудистых нарушений – благоприятная атмосфера в семье, режим и коррекционные мероприятия, способствующие выздоровлению малыша, наблюдение у невропатолога, логопеда, ортопеда и других специалистов. В лечении гипоксии хорошо зарекомендовала себя остеопатия, так как остеопат в ходе коррекции рассматривает организм ребенка в качестве целостной системы.
Ошибочно считать, что остеопат вылечит от всех болезней и навсегда избавит вашего ребенка от всех адаптационных симптомов сосудистых нарушений головного мозга, сделает его хорошим учеником и успешным человеком в жизни. Остеопатия лишь вносит некоторые изменения, воздействуя на сосудистую и нервную систему, систему кровообращения ребенка и другие системы. Так как самая частая причина гипоксии – травматическое повреждение, спровоцировавшее нарушение кровообращение головного мозга, остеопат должен найти основной источник проблемы и восстановить эти процессы при помощи мягких техник. Остеопатическая коррекция оказывается особенно эффективной в тех случаях, когда причина нарушения кроется в смещении позвонков, блоке швов свода и основания черепной коробки или травмах шейного отдела позвоночного столба. Ведь именно от правильного расположения мозговых оболочек, костей черепа и позвонков и возможности свободных микродвижений, зависит кровоснабжение головного мозга.
Во время лечения положительная динамика наблюдается не сразу. Остеопат может работать как с крупными органами, костями и мышцами, так и с очень тонкими материями и не столько излечивает их, сколько направляет организм ребенка к самостоятельной адаптации и исправлению врожденных и приобретенных нарушений.
Желательно, чтобы остеопатическое лечение сочеталось с комплексом других лечебных и профилактических мероприятий, включающих лечебную физкультуру, постоянные занятия и упражнения с ребенком, работой по его воспитанию и т.д. Например, при нарушении кровообращения речевых участков головного мозга, ребенок может неправильно произносить слова или буквы. При остеопатическом лечении, восстановление кровоснабжения данных участков, улучшит состояние поврежденных нейронных связей, а речевой аппарат ребенка будет иметь больше возможностей приспособиться к новым условиям организма. Этот момент будет самым плодотворным, если с ребенком заниматься, прививая ему правильное произношение. В результате регулярных занятий он научится грамотно говорить и мыслить уже без посторонней помощи. Те же самые процессы мы можем наблюдать и при нарушениях в физическом развитии, психологическом состоянии и т.д.
Очевидно, что никакими лекарственными средствами механические последствия травмы устранить невозможно. В арсенале остеопата большое множество мягких мануальных техник, с помощью которых можно устранить первопричину и тем самым убрать препятствия для хорошего кровообращения и тока ликвора. А организм дальше начнёт работать сам, т.к. запустится процесс самовосстановления.
Остеопатические сеансы для детей с сосудистыми нарушениями головного мозга назначаются обычно раз в неделю и длятся не более 30-60 мин. Длительность терапевтического курса подбирается в каждом случае индивидуально. Как правило, уже после четырех-пяти сеансов удается нормализовать состояние пациента и создать условия, необходимые для правильного развития его организма. Поэтому, если для родителей важно не упустить чтобы легкая гипоксия головного мозга их ребенка перешли в более тяжелые формы, желательно при наличии любых отклонениях, показаться специалисту.
ПОЛУЧИТЕ БЕСПЛАТНУЮ КОНСУЛЬТАЦИЮ ПО ТЕЛЕФОНУ
Задержка развития у ребенка до 3 лет
Кто в группе риска?
Если ребенок вынашивался или рождался с какими-либо проблемами, даже на первый взгляд незначительными, он оказывается в группе риска по формированию неврологической патологии.
Патология нервной системы может проявиться как минимальными и быстро компенсированными симптомами, так и стать причиной для значимых нарушений здоровья ребенка, вплоть до инвалидизации. Дети, рожденные недоношенными, пережившие гипоксию во время беременности, асфиксию в родах или внутриутробную инфекцию, на первом году жизни должны посещать кабинет невролога один раз в 3 месяца. Как правило, такие дети проходят ряд обследований: начиная с нейросонографии, ЭЭГ, ЭНМГ и заканчивая МРТ головного мозга, которое проводится строго по показаниям.
Причины задержки развития очень неоднородны. В зависимости от того, какая патология привела к нарушению в развитии малыша, он наблюдается либо только у невролога, либо у невролога и эндокринолога, или невролога и нейрохирурга, реже – у психиатра. В любом случае, «первым звеном» в определении факта наличия задержки развития является районный невролог, который регулярно осматривает ребенка.
Каждый пациент с задержкой развития уникален, каждый случай заслуживает внимания и особого подхода, который обеспечивает маленьким пациентам научно-практический центр детской психоневрологии.
Задержки моторного развития
ЗМР – это особенность развития, при которой малыш не осваивает двигательные навыки или приобретает их с заметным отставанием от нормы. При темповой задержке происходит отставание ребенка в развитии на один декретированный срок, то есть, малыш получает навыки последовательно, но медленно. Это повод наблюдаться у невролога, но, как правило, ситуация не предвещает существенных проблем со здоровьем. Если следовать указаниям врача, то в дальнейшем ребенок с таким типом задержки ничем не будет отличаться от сверстников.
Ситуация более серьезная и требует постоянного контроля, если:
А) Отставание в развитии более серьезное: например, ребенок к 1 году не сидит, или в 7-8 месяцев не переворачивается;
Б) Развитие происходит неравномерно или наблюдаются «откаты» в развитии: это когда ребенок, научившийся уверенно сидеть или ходить, вдруг начинает делать это неуверенно или перестаёт делать вовсе.
В этих случаях врач-невролог может поставить ребенку один из следующих диагнозов
Выраженная задержка моторного развития. Это не обязательно ДЦП, есть масса других патологий, которые имеют схожую клиническую картину – например, пороки развития головного мозга, заболевания, связанные с нарушением обмена веществ, синдромальные формы задержки развития, которые могут быть обусловлены рядом нарушений на хромосомном уровне, и многое другое).
Избирательное нарушение двигательной функции. Это асимметричная слабость мышц, наблюдается только с одной стороны тела: ребенок переворачивается только на одну сторону, ходит прихрамывая, тянется к игрушкам только одной рукой, неровно держит голову (гемипарез). Еще один симптом – появление «лишних» движений, гиперкинезов.
Нарушение осанки, снижение мышечного тонуса. Если осевая мускулатура ребенка не имеет достаточной поддержки, у малыша нарушается осанка и походка, и это тоже неврологическая проблема. Такие дети часто страдают от дисплазии соединительной ткани и поэтому склонны к травмированию суставов.
ДЦП (детский церебральный паралич). Собирательный термин для определения персистирующих двигательных нарушений, в основе которых лежит непрогрессирующее поражение мозга, обусловленное воздействием ряда неблагоприятных факторов в пренатальном, перинатальном и раннем постнатальном периодах. Много лет назад этот диагноз звучал как приговор, но сейчас специалисты-неврологи располагают большим арсеналом современных и высокоэффективных методик. При раннем обращении к врачу и грамотном подборе лечения можно добиться прекрасных результатов и жить полноценной жизнью.
Задержки психоречевого развития
Связаны с отставанием в психическом развитии ребенка, формировании основных психических функций мозга. Чаще диагностируется у детей старше 3 лет, однако некоторые первые симптомы заметны уже в самом раннем возрасте:
Отсутствие улыбки, выражения эмоций, контакта глазами с матерью, безучастность к внешнему миру;
Отсутствие разделения взрослых на своих и чужих, отсутствие страха перед незнакомцами или, наоборот, ребенок каждого взрослого, кроме мамы, встречает как чужого;
Немотивированная агрессия и аутоагрессия (бьет, щиплет себя, вырывает у себя волосы);
Нарушение пищевого поведения: ребенок плохо жует, крайне избирателен в еде или не может насытится и т.д.;
Нарушение формирования собственной (экспрессивной) речи и понимания обращенной речи.
Задержка психоречевого развития может быть просто особенностью на пути формирования ребенка как социальной единицы, но в отдельных случаях это первый симптом расстройства аутистического спектра (РАС). Причины РАС до сих пор доподлинно не установлены; над решением вопросов этиологии РАС бьются специалисты из многих медицинских и немедицинских специальностей (генетики, биологи, неврологи, психиатры, педиатры, иммунологи и многие другие)
Самое главное о задержках развития у детей:
Многие патологические состояния, выявленные в раннем детстве, удается компенсировать, и в большинстве своем успешно лечить. Но даже очень внимательные родители могут не видеть полной картины симптомов, поэтому крайне важно приходить на прием к врачу подготовленными. Ведь на приеме, в суете осмотра, раздевания и одевания ребенка, как правило, родители забывают часть симптомов, о которых они хотели сообщить специалисту, и решение проблемы, постановка диагноза, а соответственно и начало лечения затягивается на неопределенный срок.
Чтобы подготовиться к приему у детского невролога, следуйте несложным правилам:
Заранее составьте перечень всех волнующих вас вопросов;
Наблюдайте за малышом и фиксируйте (записывайте, запоминайте, снимайте на видео) все, что кажется вам странным, необычным, непривычным и т.д.;
Если состояние ребенка изменилось, запомните и отметьте тот момент, когда вы обнаружили эти изменения;
Не откладывайте посещение врача. То, что на бытовом уровне кажется незначительным и не требующим срочного лечения, может быть важным и серьезным симптомом.
Возможности применения нейропротективных препаратов в реабилитации детей первого года жизни с перинатальными гипоксическими поражениями центральной нервной системы
Опубликовано в журнале:
Журнал неврологии и психиатрии №5, 2013; Вып. 2
Г.С. Голосная
Кафедра неврологии, нейрохирургии и медицинской генетики педиатрического факультета Российского национального исследовательского медицинского университета им. Н.И. Пирогова
Ключевые слова: дети первого года жизни, гипоксия ЦНС, перинатальная патология, лечение.
The possibility of the use of neuroprotective drags in rehabilitation treatment of infants with perinatal hypoxic damage of central nervous system
G.S. Golosnaya
Pirogov Russian National Medical Research University, Moscow
Key words: infants, hypoxy of CNS, perinatal pathology, treatment.
Гипоксические повреждения головного мозга занимают одно из первых мест среди перинатальных повреждений нервной системы и являются основными причинами перинатальной смертности, составляя от 20 до 50% в ее структуре [1—3]. Это связано с тем, что развивающийся мозг новорожденного чрезвычайно чувствителен к воздействию гипоксии, которая не только нарушает клеточную дифференциацию и вызывает очаговые повреждения мозговой ткани, но и задержку развития сосудистой системы. Толерантность к воздействию повреждающих факторов у каждого ребенка различна. Поэтому при сравнительно равных условиях у детей могут развиваться различные по степени выраженности клинические проявления.
В настоящее время получено достаточно большое количество новой информации о патогенезе, молекулярных и биологических основах гипоксического перинатального поражения ЦНС. Доказано, что формирование грубых структурных изменений ткани мозга под влиянием гипоксии обусловлено в том числе и неспособностью нейрональных структур синтезировать факторы защиты. В свою очередь антигены, влияющие на деструктивные процессы, обнаруживаются в сыворотке крови новорожденных в значительно превышающих нормативные значения концентрациях уже в первые сутки жизни [3].
В соответствии с современными представлениями о механизмах нейронального повреждения при гипоксии и ишемии большое практическое значение приобретает изучение возможности применения в комплексной терапии реабилитационных программ у детей первого года жизни нейропротективных препаратов [4—8]. В связи с этим привлекают к себе внимание препараты, воздействующие на обмен центральных медиаторов, особенно лекарственные средства, влияющие на метаболизм тормозного медиатора — гамма-аминомасляной кислоты (ГАМК).
Одним из таких препаратов ГАМК является пантогам. С 1995 г. он выпускается российской компанией «ПИК-Фарма». Пантогам по химической структуре представляет собой кальциевую соль D(+)-пантоил-гамма-аминомасляной кислоты и относится к ноотропным препаратам смешанного типа с широким спектром активности, что определяет его особое место среди лекарственных средств.
От других ГАМК-производных препаратов пантогам отличается сбалансированным влиянием на центральную нервную систему. Благодаря присутствию в молекуле пантогама пантоильного радикала, препарат проникает через гематоэнцефалический барьер и оказывает выраженное воздействие на функциональную активность ЦНС.
Фармакологические эффекты пантогама обусловлены его прямым влиянием на ГАМК-рецепторно-канальный комплекс. Препарат оказывает также активирующее влияние на образование ацетилхолина, улучшает утилизацию глюкозы и кровоснабжение мозга, повышает устойчивость мозга к гипоксии, воздействию токсических веществ, стимулирует анаболические процессы в нейронах. В организме пантогам практически не метаболизируется и в течение 48 ч почти полностью выводится.
Пантогам применяется при лечении неврологических и психических заболеваний у детей разного возраста в режиме как монотерапии, так и в комбинации с другими лекарственными средствами. Сочетание мягкого психостимулирующего и умеренно седативного эффектов пантогама позволяет активировать когнитивные функции у детей, снижает тревожность, нормализует сон ребенка. Препарат хорошо переносится детьми.
В раннем возрасте применение пантогама в комплексной терапии оптимально при самых первых признаках задержки психомоторного развития (ПМР), в том числе при нарушениях темпа предречевого и речевого развития с одного года до трех лет. Обладая нейрометаболическим, нейропротекторным и нейротрофическим действием, пантогам улучшает когнитивные функции, повышает психическую активность и объем познавательной деятельности.
В настоящее время существует две лекарственные формы пантогама — таблетки и 10% сироп (не содержащий сахар). Последняя форма может применяться у детей с первых месяцев жизни.
Цель настоящей работы — изучение эффективности и переносимости препарата пантогам в форме 10% сиропа для коррекции нарушений ПМР у детей первого года жизни, перенесших гипоксическое поражение ЦНС.
Следует отметить, что выбранная нами группа пациентов состояла из перенесших гипоксию доношенных детей с задержкой ПМР легкой и средней степени. Не всегда указанные степени задержки ПМР приводят к более тяжелым расстройствам. Более того, несмотря на достаточную тяжесть состояния детей при рождении, в дальнейшем в этих случаях выявляется способность к компенсации нарушений в течение 3—4 мес жизни. Поэтому именно у таких детей показано применение ноотропных препаратов, которые могут способствовать прогрессу психофизиологического развития.
Говоря о препарате, важно отметить, что он давно и успешно используется в детской неврологической практике. Но хотелось выделить именно эффективность применения его в терапии нарушений психомоторного развития в группе доношенных детей, перенесших гипоксию. Во-первых, эти пациенты не всегда рассматриваются как угрожаемые по формированию двигательных нарушений. Это часто обусловлено тем, что, несмотря на тяжесть состояния, перенесенного при рождении, дети способны хорошо компенсировать нарушения в период до 3—4 мес жизни. Второй момент, который в определенной степени является спорным, — отсутствие четких морфологических маркеров повреждения мозга при проведении нейросонографии. В третьих, выбранная группа доношенных детей позволяет сравнить развитие с нормативным.
Несомненно, что практикующие неврологи учитывают в реабилитационных программах у детей первого года жизни все симптомы, отрицательно влияющие на развитие (внутричерепная гипертензия, судорожные состояния и т.д.), поэтому мы включили в исследование только доношенных детей с определенными нарушениями, ведущим из которых явилась задержка психомоторного развития легкой и средней степени.
Материал и методы
Под нашим наблюдением находились 60 доношенных детей в возрасте 5—12 мес. Все дети родились от женщин с отягощенным акушерско-гинекологическим и соматическим анамнезом. По данным амбулаторных карт, во всех случаях отмечалась хроническая внутриутробная гипоксия.
Критерии включения: согласие родителей, возраст детей 5—12 мес, наличие нарушений ПМР легкой и средней степени, без признаков органических поражений ЦНС.
Критерии исключения: непереносимость препарата или его компонентов, тяжелая задержка развития, наличие органических поражений ЦНС, прогрессирующая внутричерепная гипертензия, генетические заболевания, судорожные состояния в анамнезе, дети с гестационным возрастом при рождении менее 37 нед, участие в каких-либо исследованиях за 4 нед до включения в настоящее исследование, несоблюдение родителями условий исследования: непосещение врача в соответствии с установленным расписанием в течение времени наблюдения, прием препарата не по схеме.
Дети были разделены на две группы — основную и контрольную. В основную группу вошли 30 детей, лечившихся пантогамом в виде сиропа. В контрольной группе было также 30 детей, лечившихся другими ноотропными препаратами. В зависимости от использовавшегося препарата они были разделены на 2 подгруппы по 15 человек, лечившихся энцефаболом и кортексином.
Пантогам в виде сиропа назначался по 0,5 г 2 раза в день, утром и днем за 15—20 мин до еды в течение 56 дней. Энцефабол — по 50 мг 1 раз в день утром в течение 56 дней. Кортексин — по 0,5мг/кг 1 раз в сутки, внутримышечно в течение 10 дней.
Необходимо отметить, что все дети в рамках комплексной реабилитационной программы обязательно получали массаж, гимнастику, сеансы плавания, при необходимости — курсы физиотерапии.
Обследование больных начиналось только после получения информированного согласия от родителей. Все дети постоянно находились под наблюдением педиатра, невролога, офтальмолога. Всем наблюдаемым детям была проведена электроэнцефалография и повторно (в среднем 2 раза) — ультразвуковое исследование головного мозга — нейросонография, спектральная допплерография сосудов. Исследования проводили по общепринятой методике.
При оценке степени ПМР применялись шкалы О.В. Баженовой и Журбы—Мастюковой.
До начала обследования все дети находились под тщательным наблюдением невролога, который осматривал их не реже 1 раза каждые 3—4 нед.
В процессе выполнения исследования дети обследовались до начала терапии, на 28-й и 56-й дни.
Результаты и обсуждение
Основные клинические нарушения, отмечавшиеся в неврологическом статусе детей в раннем неонатальном периоде, свидетельствовали о том, что они перенесли длительную хроническую внутриутробную гипоксию.
Во всех группах детей преимущественными сроками формирования нарушения ПМР были периоды с 3-го по 5-й месяц жизни, и к периоду начала исследования задержка ПМР оценивалась как легкая и средней степени. Тяжелой степени задержки в изученных случаях не было.
В основной группе задержка легкой степени была выявлена у 19 детей, средней степени — у 11. Расширение боковых желудочков и наружных ликворных пространств обнаружено у 14 детей. Изменения на глазном дне сосудистого рисунка (венозное полнокровие, вазоспазм) отмечалось у 22 детей. У детей основной группы были отмечены также сопутствующие соматические заболевания: рахит у 27 детей, атопический дерматит — у 3, железодефицитная анемия легкой степени — у 1 ребенка.
В 1-й подгруппе контрольной группы (лечившихся энцефаболом) задержка моторного развития легкой степени была отмечена у 7 детей, средней — у 8. Расширение боковых желудочков и наружных ликворных пространств было у 8 детей. Изменения на глазном дне (венозное полнокровие, вазоспазм) выявлены у 13 детей. В 1-й подгруппе были отмечены также сопутствующие соматические заболевания: рахит — у 12 детей, атопический дерматит — у 2, железодефицитная анемия легкой степени — у 2.
Во 2-й подгруппе контрольной группы (лечившихся кортексином) встречались аналогичные изменения: задержка моторного развития легкой степени отмечена у 9 детей, средней — у 6. Расширение боковых желудочков и наружных ликворных пространств у 9 детей. Изменения на глазном дне сосудистого рисунка (венозное полнокровие, вазоспазм) — у 12 детей. В этой подгруппе были также отмечены сопутствующие соматические заболевания: рахит — у 10 детей, атопический дерматит — у 4, железодефицитная анемия легкой степени — у 4.
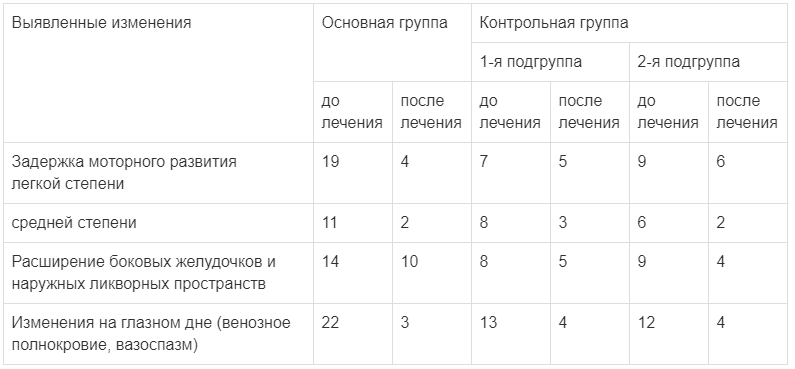
Изменения, выявленные до и после начала терапии, представлены в табл. 1.
Таблица 1.
Число больных с различными признаками задержки ПМР
Патологических изменений на ЭЭГ не было выявлено ни у одного из обследованных детей.
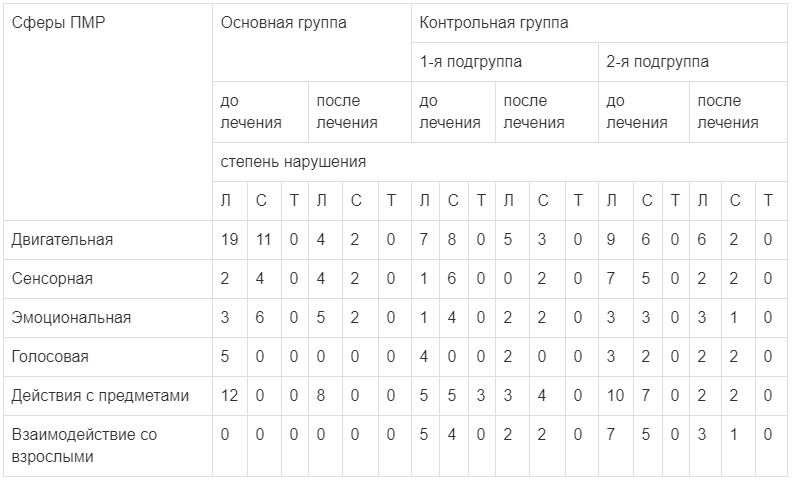
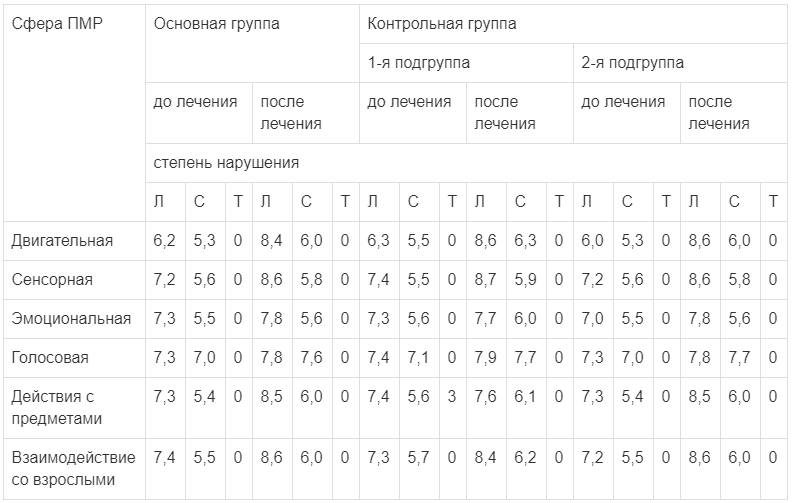
Изучение структуры ПМР показало различия в исходном состоянии отдельных сфер психофизиологической активности — двигательной, сенсорной, эмоциональной, голосовой, способности к манипулированию с предметами и взаимодействию со взрослыми. В дальнейшем под влиянием использовавшихся для лечения препаратов происходило их изменение, чаще в сторону уменьшения выраженности нарушений. Эти данные представлены в табл. 2.
Таблица 2.
Распределение детей разных групп с легкой и средней степенью задержки ПМР в разных сферах до и после лечения
Примечание. Здесь и в табл. 3: Л — легкая степень, С — средняя, Т — тяжелая степень задержки, которая выявлена не была.
Данные, приведенные в табл. 1 и 2, показывают, что при использовании пантогама положительные сдвиги в степени выраженности патологии отмечались во всех случаях, хотя и были разной степени выраженности по отдельным сферам ПМР. Тенденция к таким изменениям имела место и при использовании энцефабола и кортексина (в подгруппах контрольной группы), но изменения были меньше выражены, чем в основной группе. Этот вывод, естественно, нуждается в подтверждении с расширением числа наблюдений, использованием методов доказательной медицины и необходимых статистических показателей.
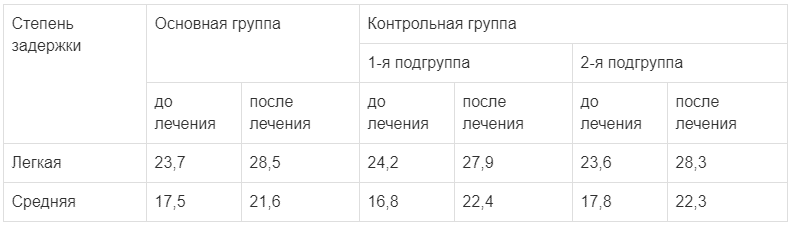
Дополнительно к представленным данным приводим изменения степени задержки ПМР в баллах по шкалам О.В. Баженовой (табл. 3) и Журбы—Мастюковой (табл. 4).
Таблица 3.
Характеристика ПМР и степень задержки различных сфер наблюдаемых у детей при оценке по шкале О.В. Баженовой, баллы
Таблица 4.
Результаты оценки по шкале Журбы—Мастюковой, баллы
Примечание. Норма — 30 баллов, задержка ПМР средней степени — 13—22 балла, риск развития нарушения ПМР — 23—26 баллов.
Оценка развития по шкале Журбы—Мастюковой от оценки по О.В. Баженовой принципиально не отличалась в начале и конце применения препаратов (см. табл. 4).
Что касается нежелательных явлений, то они развились только в 1 случае — высыпание на коже аллергического характера, которое исчезло в течение 3 дней.
Таким образом, в настоящем исследовании была выявлена достаточно высокая эффективность пантогама в виде 10% сиропа в лечении нарушений психомоторного развития вследствие гипоксического поражения ЦНС у детей первого года жизни. Показана его хорошая переносимость и безопасность. Установлено, что пантогам обладает более высокой эффективностью в сравнении с кортексином и энцефаболом.
Необходимо отметить, что назначение препарата пантогама в виде 10% сиропа имеет ряд преимуществ в связи с более удобной формой применения у детей первого года жизни и меньшей ценой.
ЛИТЕРАТУРА
1. Барашнев Ю.И., Розанов А.В., Панов В.О., Волобуев А.И. Роль гипоксически-травматических повреждений головного мозга в формировании инвалидности с детства. М: Рос вестн перинат и педиат 2006; 4: 41-46.
2. Белоусова Т.В. Комплексная терапия критических состояний у новорожденных с перинатальными повреждениями ЦНС. Перинатология и педиатрия 2007; 2: 30: 41-43.
3. Голосная Г.С. Нейрохимические аспекты патогенеза гипоксических поражений мозга у новорожденных. М: ИД «Медпрактика-М» 2009; 128.
4. Голосная Г.С. Применение кортексина в реабилитации детей первого года жизни с перинатальными гипоксическими поражениями ЦНС. Эффективная фармакотерапия. Педиатрия 2010; 4: 42-46.
5. Голосная Г.С. Проблемы лечения заболеваний нервной системы у детей раннего возраста. Практика педиатра 2011; 2: 33-36.
6. Петрухин А.С. Неврология детского возраста. М 2004.
7. Шабалов Н.П., Платонова Т.Н., Скоромец А.П. Кортексин в нейропедиатрии. Метод. рекомендации. СПб 2006; 63.