Чем лечить стеноз печени
Стеатоз печени – широко распространенное и трудно излечимое заболевание
Нужно ли лечить стеатоз печени?
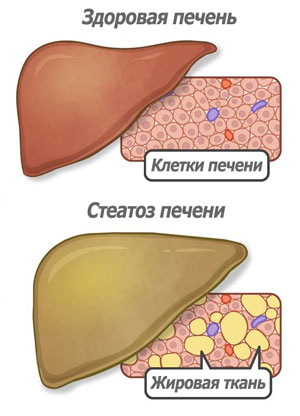
Безусловно, стеатоз это болезнь, которая выражается в том, что внутри печени формируется жировая ткань вместо тканей печени, не выполняющаяя функцию печени и отличается от ткани печени по своей структуре высокой плотностью. При стеатозе постепенно количество здоровой печени уменьшается и со временем оставшаяся здоровая часть не сможет обеспечить жизнедеятельность организма. Эта стадия заболевания называется цирроз печени и трудно поддается лечению.
Проблема осложняется тем, что печень не болит, и даже при серьезном ее поражении у пациента не возникает никаких жалоб, за исключением возможного чувства тяжести в правом подреберье. Чаще всего, тяжесть и дискомфорт в правом подреберье при стеатозе, как и при и других патологиях печени, обусловлены увеличением её размеров.
Причины стеатоза печени
Что является причиной стеатоза печени, почему по статистике Европейской ассоциации гепатологов эта болезнь распространена как эпидемия? Самое распространенное мнение – это неправильное питание и малоподвижный образ жизни. И это большая ошибка. Причина стеатоза – не в неправильном образе жизни, а в гормональных и метаболических изменениях, это болезнь, которая, помимо коррекции образа жизни, питания и физических нагрузок, также требует наблюдения у гепатолога и эндокринолога!
Лечение стеатоза печени
Как и любое заболевание печени, при котором идет ее разрушение с возможным исходом в цирроз, лечение стеатоза возможно только медикаментозное, действующее на причину болезни. В случае стеатоза причиной заболевания являются обменные и гормональные нарушения, которые и вызывают изменение структуры печеночной ткани. Внутреннее ожирение печени сопровождается всегда патологическим поступлением жира также в поджелудочную железу, сердце и сосуды, почки. Это системное заболевание, угрожающее жизни, называется метаболический синдром.
Метаболический синдром лечит врач гепатолог совместно с эндокринологом, воздействуя как на причины заболевания, так и на следствие – стеатоз. Результатом лечения всегда является выздоровление, если лечение назначено вовремя. Кроме медикаментозной коррекции обменных нарушений, в комплекс лечения входят рекомендации по правильному питанию и физическим нагрузкам, которые сами по себе, без лечения, не дают результатов. Трудность лечения обусловлена тем, что доля успеха в лечении зависит от поведения пациентов, поэтому так важна серьезная информированность пациента и его желание получить результат.
Необходимые обследования для назначения и контроля лечения стеатоза печени
Для назначения лечения стеатоза ппнчени необходимо пройти обследование, выявляющее степень поражения печени и выраженность показателей метаболического синдрома. Современное оборудование нашего центра позволяет не только обнаружить жировую ткань в печени, но и посчитать сколько в процентном отношении в печени нормальной здоровой ткани и сколько неработающей жировой! Это важно для тактики лечения и прогнозов на выздоровление.
Аппарат Фиброскан с дополнительным датчиком оценки стеатоза позволяет не только оценить количественно жировую ткань в печени по степени стеатоза от 0 до 3, но и позволяет измерить результат лечения, который в большинстве случаев приводит к полной нормализации структуры печени (стеатоз 0). Лечение назначается индивидуально в зависимости от результатов обследования. Общей для всех схемы лечения нет, так как обменные и гормональные нарушения могут быть по-разному выражены.
Опыт лечения стеатоза печени
За более чем десять лет успешного лечения метаболического синдрома и стеатоза мы вылечили несколько тысяч пациентом, которые не только получили в результате лечения здоровую печень без стеатоза, но и расстались с лишним весом, иногда доходящим до 140 кг!
Результаты лечения стеатоза печени
Отзыв пациента:
В преддверии Нового 2019 года хочу пожелать и вам тоже здоровья, семейных радостей и любви! с наилучшими пожеланиями, ваш пациент из Казани» >>>
Результат:
Неалкогольный стеатоз печени, диагностика, лечебные подходы
Рассмотрены факторы риска развития неалкогольной жировой болезни печени, первичная и фторичная формы заболевания, подходы к диагностике стеатоза и фиброза печени, общие принципы лечения пациентов, включая диетотерапию, воздействие на метаболический сндром
Factors of non-alcoholis fatty disease of liver development risk have been analyzed, as well as primary and secondary forms of disease, approaches to diagnostic of steatosis hepatis and fibrosis, general principles of treatment including diet therapy, metabolic syndrome effect, gastroprotectors application.
Неалкогольный стеатоз печени (неалкогольная жировая болезнь печени (НАЖБП), жировая дистрофия печени, жировая печень, жировая инфильтрация) — первичное заболевание печени или синдром, формируемый избыточным накоплением жиров (преимущественно триглицеридов) в печени. Если рассматривать эту нозологию с количественной точки зрения, то «жир» должен составлять не менее 5–10% веса печени, или более 5% гепатоцитов должны содержать липиды (гистологически) [1].
Если не вмешиваться в течение болезни, то в 12–14% НАЖБП трансформируется в стеатогепатит, в 5–10% случаев — в фиброз, в 0–5% фиброз переходит в цирроз печени; в 13% случаев стеатогепатит сразу трансформируется в цирроз печени [2].
Эти данные позволяют понять, почему эта проблема на сегодняшний день вызывает всеобщий интерес, если при этом будут ясны этиология и патогенез, то будет понятно, как наиболее эффективно лечить эту часто встречаемую патологию. Уже сейчас понятно, что у части больных это может оказаться болезнью, а у части — симптомом или синдромом.
Признанными факторами риска развития НАЖБП являются:
Перечисленные факторы риска НАЖБП показывают, что значительная часть их является компонентами метаболического синдрома (МС), который представляет собой комплекс взаимосвязанных факторов (гиперинсулинемия с инсулинорезистентностью — сахарный диабет 2-го типа (СД 2-го типа), висцеральное ожирение, атерогенная дислипидемия, артериальная гипертензия, микроальбуминурия, гиперкоагуляция, гиперурикемия, подагра, НАЖБП). МС составляет основу патогенеза многих сердечно-сосудистых заболеваний и указывает на тесную связь их с НАЖБП. Таким образом, круг заболеваний, который формирует НАЖБП, заметно расширяется и включает не только стеатогепатит, фиброз, цирроз печени, но и артериальную гипертонию, ишемическую болезнь сердца, инфаркт миокарда и сердечную недостаточность. По крайней мере, если прямые связи этих состояний требуют дальнейшего изучения доказательной базы, их взаимное влияние несомненно [6].
Эпидемиологически различают: первичную (метаболическую) и вторичную НАЖБП. К первичной форме относят большинство состояний, развивающихся при различных метаболических расстройствах (они перечислены выше). К вторичной форме НАЖБП относят состояния, которые формируются: алиментарными нарушениями (переедание, голодание, парентеральное питание, трофологическая недостаточность — квашиоркор); лекарственными воздействиями и взаимоотношениями, которые реализуются на уровне печеночного метаболизма; гепатотропными ядами; синдромом избыточного бактериального роста кишечника; заболеваниями тонкой кишки, сопровождаемыми синдромом нарушенного пищеварения; резекцией тонкой кишки, тонкотолстокишечным свищом, функциональной недостаточностью поджелудочной железы; болезнями печени, в т. ч. и генетически детерминированными, острой жировой болезнью беременных и др. [7–9].
Если врач (исследователь) располагает морфологическим материалом (биопсия печени), то морфологически различают три степени стеатоза:
Приведя морфологическую классификацию, мы должны констатировать, что эти данные носят условный характер, так как процесс никогда не носит равномерно-диффузного характера, и в каждый конкретный момент мы рассматриваем ограниченный фрагмент ткани, и уверенности в том, что в другом биоптате мы получим то же самое, нет, и, наконец, 3-я степень жировой инфильтрации печени должна была бы сопровождаться функциональной печеночной недостаточностью (хотя бы по каким-либо компонентам: синтетическая функция, дезинтоксикационная функция, билиарная состоятельность и др.), что практически не свойственно НАЖБП.
В вышеизложенном материале показаны факторы и состояния метаболизма, которые могут участвовать в развитии НАЖБП, а в качестве современной модели патогенеза предложена теория «двух ударов»:
первый — развитие жировой дистрофии;
второй — стеатогепатит.
При ожирении, особенно висцеральном, увеличивается поступление в печень свободных жирных кислот (СЖК), при этом развивается стеатоз печени (первый удар). В условиях инсулинорезистентности увеличивается липолиз в жировой ткани, а избыток СЖК поступает в печень. В итоге количество жирных кислот в гепатоците резко возрастает, формируется жировая дистрофия гепатоцитов. Одновременно или последовательно развивается окислительный стресс — «второй удар» с формированием воспалительной реакции и развитием стеатогепатита. Это связано в значительной степени с тем, что функциональная способность митохондрий истощается, включается микросомальное окисление липидов в системе цитохрома, что приводит к образованию активных форм кислорода и повышению продукции провоспалительных цитокининов с формированием воспаления в печени, гибели гепатоцитов, обусловленной цитотоксическими эффектами TNF-альфа1 — одного из основных индукторов апоптоза [10, 11]. Последующие этапы развития патологии печени и их интенсивность (фиброз, цирроз) зависят от сохраняющихся факторов формирования стеатоза и отсутствия эффективной фармакотерапии.
Диагностика НАЖБП и состояний ее прогрессирования (стеатоз печени, стеатогепатит, фиброз, цирроз)
Жировая дистрофия печени — формально морфологическое понятие, и, казалось бы, диагностика должна была бы сводиться к биопсии печени. Однако такого решения международными гастроэнтерологическими ассоциациями не принято и вопрос обсуждается. Это связано с тем, что жировая дистрофия — понятие динамическое (она может активизироваться или подвергаться обратному развитию, может носить как относительно диффузный, так и очаговый характер). Биоптат всегда представлен ограниченным участком, и трактовка данных всегда достаточно условна. Если признать биопсию как обязательный диагностический критерий, то ее нужно проводить достаточно часто; сама биопсия чревата осложнениями, а метод исследования не должен быть опаснее самой болезни. Отсутствие решения о биопсии не является отрицательным фактором, тем более что на сегодняшний день стеатоз печени это понятие клинико-морфологическое с наличием многих факторов, участвующих в патогенезе.
Из представленных выше данных видно, что диагностика может начаться на разных стадиях болезни: стеатоз → стеатогепатит → фиброз → цирроз, и в диагностический алгоритм должны входить методы, определяющие не только жировую дистрофию, но и стадию ее.
Так, на стадии стеатоза печени основным симптомом является гепатомегалия (обнаруженная случайно или при диспансерном обследовании). Биохимический профиль (аспартатаминотрансфераза (АСТ), аланинаминотрансфераза (АЛТ), щелочная фосфотаза (ЩФ), гаммаглутамилтранспептидаза (ГГТ), холестерин, билирубин) устанавливает при этом наличие или отсутствие стеатогепатита. При повышении уровня трансаминаз необходимо проведение вирусологических исследований (которые либо подтвердят, либо отвергнут вирусные формы гепатита), а также диагностика других форм гепатита: аутоиммунного, билиарного, первичного склерозирующего холангита. Ультрозвуковое исследование не только устанавливает увеличение размеров печени и селезенки, но и признаки портальной гипертензии (по диаметру селезеночной вены и размерам селезенки). Менее употребляемым (а может быть, и известным) является оценка жировой инфильтрации печени, состоящая в измерении «столба затухания», по динамике которого в разные промежутки времени можно судить о степени жировой дистрофии (рис.) (методика УЗИ описана) [12].
Более ранние модели ультразвуковых аппаратов оценивали денситометрические показатели (по динамике которых можно было судить о динамике и степени стеатоза). В настоящее время денситометрические показатели получают с помощью компьютерной томографии печени. Рассматривая патогенез НАЖБП, оценивают общий осмотр, антропометрические показатели (определение массы тела и окружности талии — ОТ). Так как МС занимает значительное место в формировании стеатоза, то в диагностике необходимо оценивать: абдоминальное ожирение — ОТ > 102 см у мужчин, > 88 см у женщин; триглицериды > 150 мг/дл; липопротеины высокой плотности (ЛПВП): 130/85 мм рт. ст; индекс массы тела (ИМТ) > 25 кг/м 2 ; гликемия натощак > 110 мг/дл; гликемия через 2 часа после нагрузки глюкозой 110–126 мг/дл; СД 2-го типа, инсулинорезистентность.
Представленные выше данные рекомендуются ВОЗ и Американской ассоциацией клинических эндокринологов. Важным диагностическим аспектом является также установление фиброза и его степени. Несмотря на то, что фиброз также понятие морфологическое, его определяют по различным расчетным показателям. С нашей точки зрения дискриминантная счетная шкала Bonacini, определяющая индекс фиброза (ИФ), является удобным методом, соответствующим стадиям фиброза. Мы провели сравнительное изучение расчетного показателя ИФ с результатами биопсий. Эти показатели представлены в табл. 1 и 2.
Практическое значение ИФ:
1) ИФ, оцененный по дискриминантной счетной шкале, достоверно коррелируется со стадией фиброза печени по данным пункционной биопсии;
2) изучение ИФ позволяет с высокой степенью вероятности оценить стадию фиброза и использовать его для динамического наблюдения за интенсивностью фиброзообразования у больных с хроническим гепатитом, НАЖБП и другими печеночными диффузными заболеваниями, в том числе и для оценки эффективности проводимой терапии [13].
И наконец, если проводится пункционная биопсия печени, то она назначается, как правило, в случае дифференциальной диагностики опухолевых образований, в т. ч. и очаговой формы стеатоза. При этом в ткани печени этих больных выявляются:
Диагноз НАЖБП (стеатоз печени) формулируется на основании совокупности следующих симптомов и положений:
Диагностика также предполагает исключение основных печеночных нозологических форм:
Таким образом, диагноз формируется с определения гепатомегалии, определения патогенетических факторов, способствующих стеатозу, и исключения других диффузных форм поражения печени.
Лечебные принципы
Так как основным фактором развития неалкогольного стеатоза печени является избыточная масса тела (МТ), то снижение МТ является основополагающим условием лечения больных НАЖБП, что достигается изменением образа жизни, включающем диетические мероприятия и физическую активность, в т. ч. и в случаях, когда необходимость в снижении МТ отсутствует [14]. Диета должна быть гипокалорийной — 25 мг/кг в сутки с ограничением жиров животного происхождения (30–90 г/день) и уменьшением углеводов (особенно быстро усваиваемых) — 150 мг/сутки. Жиры должны быть преимущественно полиненасыщенными, которые содержатся в рыбе, орехах; важно употреблять не менее 15 г клетчатки за счет фруктов и овощей, а также продукты, богатые витамином А.
Помимо диеты необходимо как минимум 30 минут ежедневных аэробных физических нагрузок (плавание, ходьба, гимнастический зал). Физическая активность сама по себе снижает инсулинорезистентность и улучшает качество жизни [15].
Вторым важным компонентом терапии является воздействие на метаболический синдром и инсулинорезистентность в частности. Из препаратов, ориентированных на ее коррекцию, наиболее изучен метформин [16, 17]. При этом показано, что лечение метформином приводит к улучшению лабораторных и морфологических показателей воспалительной активности в печении. При СД 2-го типа используются инсулиновые сенситайзеры, при этом метаанализ не показал преимуществ их влияния на инсулинорезистентность [18].
Третьим компонентом терапии является исключение использования гепатотоксических лекарственных средств и препаратов, вызывающих повреждение печени (основным морфологическим субстратом этого повреждения является стеатоз печени и стеатогепатит). В этом отношении важным является сбор лекарственного анамнеза и отказ от препарата (препаратов), повреждающих печень.
Так как синдром избыточного бактериального роста (СИБР) играет важную роль в формировании стеатоза печени, то его необходимо диагностировать и проводить коррекцию (препараты с антибактериальным действием — желательно не всасывающиеся; пробиотики; регуляторы моторики, печеночные протекторы), причем выбор терапии зависит от исходной патологии, формирующей СИБР.
Не совсем корректно на сегодняшний день решается вопрос об использовании печеночных протекторов. Есть работы, показывающие их малую эффективность, есть работы, которые показывают их высокую эффективность. Создается впечатление, что их использование не учитывает стадию НАЖБП. Если есть признаки стеатогепатита, фиброза, цирроза печени, то их использование представляется обоснованным. Хотелось бы представить аналитические данные, на основании которых и в зависимости от количества факторов, участвующих в патогенезе НАЖБП, можно выбрать гепатопротектор (табл. 3).
Из представленной таблицы видно (введены наиболее употребляемые протекторы, при желании ее можно расширить, введя другие протекторы), что препараты урсодезоксихолевой кислоты (Урсосан) действуют на максимальное количество патогенетических звеньев поражения печени.
Мы хотим представить результаты лечения Урсосаном больных НАЖБП. Изучено 30 больных (у 15 из них в основе лежало ожирение, у 15 — МС; женщин было 20, мужчин — 10; возраст от 30 до 65 лет (средний возраст 45 ± 6,0 лет).
Критериями отбора служили: повышение уровня АСТ — в 2–4 раза; АЛТ — в 2–3 раза; ИМТ > 31,1 кг/м 2 у мужчин и ИМТ > 32,3 кг/м 2 у женщин. Больные получали Урсосан в дозе 13–15 мг/кг веса в сутки; 15 больных в течение 2 месяцев, 15 больных продолжали прием препарата до 6 месяцев. Результаты лечения представлены в табл. 4–6.
Критерием исключения служили: вирусная природа болезни; сопутствующая патология в стадии декомпенсации; прием препаратов, потенциально способных формировать (поддерживать) жировую дистрофию печени.
2-я группа продолжала получать Урсосан в той же дозе 6 месяцев (при нормальных биохимических показателях). При этом стабилизировался аппетит, постепенно (1 кг/месяц) уменьшалась масса тела. По данным УЗИ — структура и размер печени существенно не изменились, продолжалась динамика по «столбу затухания» (табл. 6).
Таким образом, по нашим данным использование печеночных протекторов у больных НАЖБП в стадии стеатогепатита эффективно, что выражается в нормализации биохимических показателей и уменьшении жировой инфильтрации печени (по данным УЗИ — уменьшение «столба затухания» сигнала), что в целом является важным обоснованием их использования.
Литература
О. Н. Минушкин, доктор медицинских наук, профессор
ФГБУ УНМЦ Управления делами Президента РФ, Москва
Что такое стеатоз печени
и как с ним бороться
Виды стеатоза
Развитие стеатоза
Основной фактор риска развития алкогольной болезни печени — хроническое злоупотребление алкоголем.
В случае НАЖБП выделяют намного больше факторов риска 2 :
Избыточная масса тела.
Нарушение обмена липидов, которое вызывает перекисное окисление липидов и впоследствии развитие оксидативного стресса.
Нечувствительность к инсулину (инсулинорезистентность) и сахарный диабет 2 типа; нарушения всасывания (мальабсорбция); заболевания желудочно-кишечного тракта.
Слишком быстрое снижение веса и голодание.
Прием некоторых лекарств, которые могут оказывать токсическое действие на печень: глюкокортикостероиды, нестероидные противовоспалительные средства, эстрогены, антибиотики и др.
Накопление в печени меди, железа вследствие различных заболеваний обмена веществ.
Диагностика
НАЖБП обычно сопровождается:
Лечение НАЖБП
Лекарства могут помочь при заболевании печени, но также очень важно соблюдать рекомендации врача по изменению образа жизни.
И снижение веса, и правильное питание, и лекарства могут помочь при стеатозе. Но помните, что самое важное при заболевании — его своевременное выявление. Внимательно следите за своим здоровьем и не забывайте регулярно обследоваться.
Чем лечить стеноз печени
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Последствия злоупотребления алкоголем представляют собой общемировую проблему, включающую не только органную патологию, но также несчастные случаи и преступления, связанные с состоянием опьянения. Так, в Европе 11% летальных исходов у мужчин и 1,8% у женщин рассматриваются в ассоциации с алкоголизмом [1]. Если анализировать структуру поражений внутренних органов, то доминирующую позицию среди них занимает именно алкогольная болезнь печени (АБП), ведущая к развитию цирроза печени и гепатоцеллюлярной карциномы [2]. Несмотря на то, что в последние годы на пути изучения патогенеза поражения печени достигнуты серьезные успехи, лечение тяжелых форм АБП в определенной мере «законсервировалось», не давая основания говорить о революционном прорыве в ближайшем будущем. Тем не менее, определенные направления в терапии АБП можно расценивать как перспективные, причем это относится не только к методам, которые не вышли пока за рамки экспериментальных, но и к давно известным средствам, открывающим новые грани в процессе углубленного изучения.
Естественное течение АБП: от стеатоза к циррозу
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20% [3, 4]. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение АБП определяется в первую очередь паттерном употребления спиртных напитков: постоянным или перемежающимся типом пьянства; периодами запоев, сменяющихся абстиненцией; нарастанием или сокращением суточной дозы алкоголя Учитывая обстоятельство, что большинство пациентов обращаются за медицинской помощью на поздних стадиях, оптимальной моделью наблюдения служат больные после трансплантации печени [5].
Генетическая предрасположенность к АБП также служит предметом активного изучения. Недавние исследования выявили значимую корреляцию определенных аллельных вариантов адипонутрина (PNPLA3) и прогрессированием фиброгенеза [6, 7]. Более того, генетический полиморфизм адипонутрина ассоциирован и с развитием ГЦК [8]. В то же время попытки идентифицировать генетические маркеры предрасположенности к АБП, в том числе полиморфизм генов, участвующих в метаболизме этанола, пока не увенчались успехом [9].
В ретроспективном исследовании S. Naveau, включавшем более 2000 злоупотребляющих алкоголем пациентов, по данным биопсии печени у 34% выявлен цирроз, у 9% — активный гепатит, у 46% — стеатоз печени с наличием или отсутствием фиброза, а у 11% патологические изменения печени отсутствовали [10]. По данным T. Poynard, вероятность развития цирроза нарастает с возрастом, достигая при регулярном употреблении высоких доз алкоголя 50% к 61 году, причем у женщин сроки формирования цирроза короче [11]. Суммируя опубликованные результаты ретроспективных исследований, можно констатировать, что среди госпитализированных алкоголиков частота обнаружения цирроза составляет около 20% [2].
Стеатоз обычно предшествует образованию соединительной ткани, но влияние аккумуляции жира в печени на фиброгенез изучено недостаточно [2, 13, 14]. Долгосрочная выживаемость пациентов с алкогольным стеатозом в отсутствии воспаления и фиброза сопоставима с таковой у трезвенников. Если сравнивать течение неалкогольной жировой болезни печени (НАЖБП) и АБП, можно констатировать более высокие темпы прогрессирования последней. В течение 10 лет у больных алкогольным стеатозом значительно чаще развивается цирроз (21% vs. 1%) и наблюдаются летальные исходы (74% vs. 25%) [15]. Интересно, что у больных алкогольным циррозом повышен риск аутоиммунных заболеваний [16]. Можно предположить, что ацетальдегид, образующийся в разных тканях под действием алкогольдегидрогеназы, образует прочные комплексы с белками, выступающие в роли неоантигенов.
Цирроз печени рассматривается в качестве причины смерти 25% алкоголиков, занимая первое место среди летальных исходов [1, 2, 15]. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Это состояние проявляется желтухой, в тяжелых случаях энцефалопатией и гипокоагуляцией, и требует обязательного отражения в диагнозе, так как принципиально меняет прогноз и подходы к лечению.
Недавно завершенные исследования, основанные на биопсийном материале, убедительно продемонстрировали, что у подавляющего большинства пациентов с тяжелым алкогольным гепатитом имеется исходный цирроз или септальный фиброз печени [9, 18]. Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет [2].
В то время как ожирение является общепризнанным коморбидным фактором стеатоза, имеются также сведения о его влиянии на развитие алкогольного гепатита и фиброза печени. В качестве ключевых патогенетических факторов называются инсулинорезистентность и гипергликемия [19]. С другой стороны, небольшие дозы этанола способствуют замедлению прогрессирования неалкогольной жировой болезни печени [20].
Лечение АБП: акцент на абстиненцию
К вопросу о безопасной дозе алкоголя
Необходимость обсуждения лимита употребляемого алкоголя, превышение которого ведет к повреждению печени, в аспекте лечения АБП определяется тем, что соблюдение пациентом полной абстиненции является важной, но зачастую недостижимой целью. Так, в США 67–81% больных возобновляют прием алкоголя в течение одного года [21]. В последние годы дозу этанола часто измеряют в «дозах» (drinks), равных 10–14 г чистого этанола. «Доза» примерно соответствует бокалу пива, фужеру сухого вина или рюмке крепкого напитка. Показано, что прием ≤ 2 «доз» в день для мужчин и ≤ 1 «дозы» в день для женщин не ассоциировано с повышенной вероятностью развития органной патологии по сравнению с трезвенниками [2]. Другие исследования демонстрируют сходные результаты. Согласно метаанализу G. Corrao, употребление > 25 г этанола в день увеличивает относительный риск цирроза печени [22]. В итальянском исследовании Dionysos у лиц, ежедневно принимающих ≥ 30 г этанола, цирроз наблюдался в 2,2% случаев, тогда как у непьющих — в 0,08%. Риск цирроза экспоненциально возрастал по мере увеличения доз алкоголя, достигая 13,5% у употребляющих > 120 г в день [23].
Средства для лечения алкогольной зависимости
Ввиду того, что большинство пациентов нарушают предписанный режим абстиненции, в последние годы активно изучаются препараты, снижающие потребность в алкоголе: налтрексон, акампрозат, топирамат, баклофен и др. Наибольшее число исследований на сегодняшний день выполнено с агонистом баклофеном, продемонстрировавшим эффективность и безопасность при тяжелых формах АБП [24].
Метадоксин, зарегистрированный в ряде европейских стран для лечения алкогольной интоксикации, в нескольких небольших исследованиях значимое снижение употребления алкоголя, что сопровождалось редукцией биомаркеров АБП (трансаминазы, γ-глутамилтранспептидаза, средний объем эритроцитов) [25]. Сходные результаты получены в исследовании внутривенной формы глицирризиновой кислоты. Интересно, что соблюдение предписанного режима абстиненции коррелировало со снижением сывороточного уровня фактора некроза опухоли-α [26].
Коррекция трофологического статуса
Нутритивная поддержка наиболее важна для больных тяжелым алкогольным гепатитом, хотя и при других формах АБП у большинства пациентов наблюдаются те или иные формы нарушения трофологического статуса [2]. В исследовании С. Mendenhall et al. показано, что у пациентов, самостоятельно принимающих пищу с энергетической ценностью более 3000 ккал в сутки, отмечалась нулевая летальность, в то время как из потреблявших менее 1000 ккал в сутки умерло более 80% [27]. Несмотря на безусловную ценность этих данных, нельзя игнорировать высокую вероятность более тяжелого течения гепатита у больных второй группы, к типичным проявлениям которого относится анорексия [28].
Общие рекомендации по коррекции трофологического статуса у больных тяжелым алкогольным гепатитом предусматривают суточное потребление 1500–2500 ккал. Диета должна быть сбалансирована по содержанию основных нутриентов и витаминов, ограничение белка показано лишь в случаях его индивидуальной непереносимости. Следует помнить о преимуществе перорального приема пищи над зондовым и парентеральным; последнее назначается только при невозможности физиологического питания (повторная рвота, нарушения сознания).
Как отмечалось выше, избыточная масса тела и ожирение тоже способствуют прогрессированию повреждения печени ввиду общности ряда патогенетических звеньев алкогольного и неалкогольного стеатогепатита [10, 29], что необходимо учитывать при разработке программы лечения.
Кортикостероиды применяются для лечения тяжелого алкогольного гепатита на протяжении более 40 лет. Наиболее хорошо изучена схема с пероральным преднизолоном 40 мг в сутки в течение одного месяца, с одномоментной отменой или постепенным снижением дозы. Хотя многочисленные исследования весьма разнородны по дизайну и отбору пациентов, метаанализ показал достоверное повышение краткосрочной выживаемости по сравнению с больными, не получавшими преднизолон [14]. Оценка эффективности терапии обычно осуществляется с помощью индекса Лилле (Lille), который рассчитывается через семь дней лечения по формуле:
R = 3,19 — 0,101 (возраст в годах) + 0,147 (альбумин в день поступления, ) + 0,0165 (сывороточный билирубин, мкмоль) + 0,206 (наличие почечной недостаточности — 0 или 1) + 0,0065 (сывороточный билирубин в день поступления, мкмоль) + 0,0096 (протромбиновое время, с)
Индекс Лилле = Exp ® /[1 +Exp ® ]
Значение индекса Лилле > 0,45 указывает на неэффективность преднизолона и 75%-ю вероятность летального исхода в течение шести месяцев. С почти пятикратным ростом летальности сопряжено также отсутствие снижения уровня сывороточного билирубина, по меньшей мере, на 25% за аналогичный срок стероидной терапии [30]. У этой когорты больных дальнейшее применение преднизолона нецелесообразно, с учетом повышения риска инфекционных осложнений, особенно легочного аспергиллеза [31]. В упомянутом метаанализе выделены три группы пациентов в зависимости от реакции на преднизолон: с полным, частичным и нулевым ответом. Краткосрочная выживаемость в этих группах составила 91%, 79% и 53%, соответственно [14].
В первом сообщении о применении пентоксифиллина при тяжелом алкогольном гепатите были представлены обнадеживающие результаты, свидетельствующие о существенном снижении риска гепаторенального синдрома (ГРС) [32]. Большое рандомизированное контролированное исследование STOPAH, включавшее более 1000 пациентов, не продемонстрировало преимущество пентоксифиллина перед плацебо в отношении краткосрочной выживаемости [33]. Хотя необходимо принимать во внимание, что из исследования были исключены наиболее тяжелые больные — с ГРС, сепсисом и манифестной энцефалопатией — целесообразность применения пентоксифиллина представляется сомнительной.
Комбинация преднизолона и пентоксифиллина не выявила преимуществ по сравнению с монотерапией преднизолоном [13]. Таким образом, на сегодняшний день улучшение прогноза больных тяжелым алкогольным гепатитом, резистентных к кортикостероидам, возможно только путем выполнения срочной трансплантации печени [14].
Метаболические препараты («гепатопротекторы»)
Международные гепатологические ассоциации не рекомендуют применение лекарственных средств данной группы при АБП, что обусловлено слабой доказательной базой.
В исследовании J. Mato пероральное применение в дозе 1200 мг в сутки на протяжении двух лет сопровождалось более низкой летальностью или потребностью в трансплантации печени по сравнению с группой плацебо у больных компенсированным и субкомпенсированным алкогольным циррозом (класс, А и В по ) — 12% и 29% (p = 0.04), соответственно. Количество пациентов, прекративших и продолживших употребление алкоголя, было сопоставимо в обеих группах [35].
Результаты недавно опубликованного исследования и соавторов указывают на более низкую частоту ГРС у больных, получавших комбинацию преднизолон + по сравнению с монотерапией преднизолоном (p = 0.035). Показатели летальности в группах при этом статистически значимо не различались [28].
и соавторы представили результаты парентерального применения глицирризиновой кислоты у пациентов с алкогольным стеатогепатитом. Помимо отмеченного выше позитивного влияния на алкогольную зависимость, констатировано значимое снижение активности трансаминаз и уровня сывороточного билирубина [26].
L- ускоряет метаболизм аммиака, уменьшая проявления печеночной энцефалопатии. Показано, что препарат обладает способностью улучшать биохимические параметры у пациентов с хронической патологией печени, в том числе АБП [36]. Не исключено, что этот эффект обусловлен дезинтоксикацией обладающего универсальным цитотоксическим действием аммиака.
Неудовлетворительные результаты лечения тяжелых форм АБП служат основанием для разработки новых подходов, базирующихся на ключевых патогенетических механизмах. К находящимся на разных стадиях изучения, относятся модулирование иннатного иммунного ответа, подавление кишечной бактериальной и эндотоксиновой транслокации, блокирование апоптоза и активация фарнезоидного Х рецептора. В качестве многообещающего направления рассматривается технология индукции плюрипотентных стволовых клеток [37].
История медицины свидетельствует о том, что именно элиминация этиологического фактора определяет успех лечения большинства болезней, в том числе в эпидемиологическом ракурсе. Так, широкое внедрение в клиническую практику антигеликобактерной терапии позволило значимо снизить распространенность язвенной болезни желудка и двенадцатиперстной кишки, а противовирусных препаратов — эффективно контролировать заболеваемость гепатитом С. Казалось бы, в отношении АБП и других заболеваний решение проблемы лежит на поверхности: абстиненция ведет к выздоровлению или, по крайней мере, резкому снижению риска фатальных последствий. Однако этот постулат вызывает, по крайней мере, два вопроса: 1) что делать с больными, которые хотят, но не могут отказаться от алкоголя вследствие зависимости; 2) какой тактики ведения следует придерживаться в случае прогрессирования патологических изменений, несмотря на абстиненцию. Следовательно, весьма актуальным остается вопрос о медикаментозном лечении АБП, особенно тяжелых ее форм — гепатита и цирроза. Достижения в этой области не столь грандиозны, как в других разделах гепатологии. Многие лекарственные средства, на которые ранее возлагались надежды, основанные на результатах экспериментальных и пилотных данных, не оправдали их в рандомизированных контролированных исследованиях; показательным примером могут служить эссенциальные фосфолипиды. Тем важнее выбрать из относительно небольшого терапевтического арсенала препараты, проверенные временем и зарекомендовавшие себя с позиций доказательной медицины.
European Association for the Study of Liver. EASL clinical practical guidelines: management of alcoholic liver disease. J. Hepatol. 2012; 57: 399–420.
Mathurin P., Bataller R. Trends in the management and burden of alcoholic liver disease. J. Hepatol. 2015; 62(1S): S..
Lefkowitch of alcoholic liver disease. Clin. Liver Dis. 2005; 9: 37–53.
Lucey M., Mathurin P., Morgan hepatitis. N. Engl. J. Med. 2009; 360: 2758–2769.
DiMartini A., Dew M.A., Day N. et al. Trajectories of alcohol consumption following liver transplantation. Am. J. Transplant. 2010; 10: 2305–2312.
Stickel F., Buch S., Lau K. et al. Genetic variation in the PNPLA3 gene is associated with alcoholic liver injury in Caucasians. Hepatology. 2010; 53: 86–95.
Trépo E., Gustot T., Degré D. et al. Common polymorphism in the PNPLA3/adiponutrin gene confers higher risk of cirrhosis and liver damage in alcoholic liver disease. J. Hepatol. 2011; 55: 906–912.
Liu Y.L., Patman G.L., Leathart J.B. et al. Carriage of the PNPLA3 rs738409 C >G polymorphism confers an increased risk of fatty liver disease associated hepatocellular carcinoma. J. Hepatol. 2014; 61: 75–81.
Bataller R., North K. Brenner polymorphisms and the progression of liver fibrosis: a critical appraisal. Hepatology. 2003; 37: 493–503.
Naveau S., Giraud Borotto E. et al. Excess weight risk factor for alcoholic liver disease // Hepatology. 1997; 25: 108–111.
Poynard T., Mathurin P., Lai C.L. et al. A comparison of fibrosis progression in chronic liver diseases. J. Hepatol. 2003; 38: 257–265.
Song M., Chen T., Prough alcohol consumption causes liver injury in male mice through enhanced hepatic inflammatory response. Alcohol. Clin. Exp. Res. 2016; 40(3): 518–528.
Mathurin P., Louvet A., Duhamel A. et al. Prednisolone with vs. without pentoxifylline and survival of patients with severe alcoholic hepatitis: a randomized clinical trial. JAMA. 2013; 310: 1033–1041.
Mathurin P., Moreno C., Samuel D. et al. Early liver transplantation for severe alcoholic hepatitis // N. Engl. J. Med. 2011; 365: 1790–1800.
S., Franzmann M., Andersen I.B. et al. Longterm prognosis of fatty liver: risk of chronic liver disease and death. Gut. 2004; 53: 750–755.
Raynard B., Balian A., Fallik D. et al. Risk factors of fibrosis in liver disease. Hepatology. 2002; 35: 635–638.
Dunn W., Sanyal A.J., Brunt E.M. et al. Modest alcohol consumption is associated with decreased prevalence of steatohepatitis in patients with fatty liver disease (NAFLD) J. Hepatol. 2012; 57: 384–391.
Miller W.R, Walters S.T., Bennett effective is alcoholism treatment in the United States? J. Stud. Alcohol. 2001; 62: 211–220.
Corrao G., Bagnardi Zambon A., Torchio P. of alcohol intake in relation to risk of liver cirrhosis. Alcohol Alcohol. 1998; 33: 381–392.
Bellentani S., Saccoccio G., Costa G. et al. Drinking habits as cofactors of risk for alcohol induced liver damage. The Dionysos Study Group. Gut. 1997; 41: 845–850.
Vuittonet C.L., Halse M., Leggio L et al. Pharmacotherapy for alcoholic patients with alcoholic liver disease. Am. J. Health Syst. Pharm. 2014; 71(15): 1265–1276.
Leggio L., Kenna G.A., Ferrulli A. et al. Preliminary findings on the use of metadoxine for the treatment of alcohol dependence and alcoholic liver disease. Hum. Psychopharmacol. 2011; 26: 554–559.
Никитин И.Г, Байкова И.Е., Волынкина В.М. и др. Опыт использования глицирризиновой кислоты в лечении пациентов с алкогольной болезнью печени. Росс. журн. гастроэнтерол. гепатол. колопроктол. 2009; 19(1): 53–58.
Mendenhall C., Roselle G.A., Gartside P., Moritz T. Relationship of protein calorie malnutrition to alcoholic liver disease: A reexamination of data from two Veterans Administration Cooperative Studies. Alcoholism: Clinical and Experimental Research. 1995; 19(3): 635–641.
Tkachenko P, Maevskaya M, Pavlov A et al. Prednisolone plus S- in severe alcoholic hepatitis. Hepatol Int. 2016 Jun 23.
Diehl and alcoholic liver disease. Alcohol. 2004; 34: 81–87.
Louvet A., Naveau S., Abdelnour M. et al. The Lille model: a new tool for therapeutic strategy in patients with severe alcoholic hepatitis treated with steroids. Hepatology. 2007; 45: 1348–1354.
Gustot T., Maillart E., Bocci M. et al. Invasive aspergillosis in patients with severe alcoholic hepatitis. J. Hepatol. 2014; 60: 267–274.
Thursz M., Richardson P., Allison M.E. et al. Steroids or pentoxifylline for alcoholic hepatitis: results of the STOPAH trial. Hepatology. 2014; 60: LB1.
E., Thevenot T., Piquet M.A. al. Glucocorticoids plus in severe alcoholic hepatitis. N. Engl. J. Med. 2011; 365: 1781–1789.
Грюнграйф К., Й. Эффективность гранул L- при лечении хронических заболеваний печени. Сучасна гастроентерология. 2008; 2: 59–66.
Saberi B, Dadabhai AS, Jang YY Current Management of Alcoholic Hepatitis and Future Therapies. J Clin Transl Hepatol. 2016; 4(2): 113–122.
Рисунок. Схема стадийного течения алкогольной болезни печени (по P. Mathurin, R. Bataller, 2015, с изменениями).

.jpg)
_550.gif)
_550.gif)
.gif)



