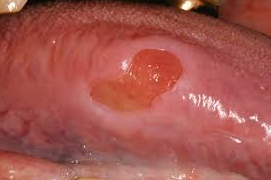
Чем лечить стоматит у взрослых после химиотерапии лечение
Алиментарные мукозиты онкологических больных: новые пути нутритивной поддержки
Мукозит — объединяющий термин для воспалительных (эритематозных и эрозивно-язвенных) поражений слизистой рта, глотки, пищевода и в целом желудочно-кишечного тракта (ЖКТ) в результате противоопухолевого лечения [1]. Мукозит существенно повышает расходы на лечение, так как увеличивает продолжительность госпитализации, потребность в нутритивной поддержке и медикаментах [2]. Он может привести к летальному исходу: косвенно — в результате тяжелой нутритивной недостаточности и ее осложнений, либо непосредственно — вследствие сепсиса.
Тяжелый мукозит, особенно при поздно начатом лечении, приводит к вторичному инфицированию, болевому синдрому, психоэмоциональным проблемам, анорексии, невозможности энтерального питания. Разрушение естественного слизистого барьера создает повышенный риск инфекции, как локальной, так и системной [3].
Мукозит чаще всего развивается на 7–10 день от начала химиотерапии, продолжаясь на фоне нейтропении до 2–3 недель. Инфекции, связанные с мукозитом, часто обусловлены бактериальной флорой ротовой полости (грамположительной) и кишечника (грамотрицательной и анаэробной), грибами рода Candida и герпес-вирусами [4].
Мукозит: определение, частота и последствия
Оральный мукозит — часто регистрируемое и потенциально опасное осложнение противоопухолевой терапии. Воспаление и изъязвление слизистой оболочки ротовой полости снижают способность к глотанию, приему пищи и питью, что приводит к анорексии и потере веса. Гастроинтестинальный мукозит может развиваться в ответ на системную химиотерапию или лучевую терапию и сопровождается такими симптомами, как понос, вздутие живота, недержание кала и боли в животе.
Данное терминологическое разделение мукозита на оральный или гастроинтестинальный в зависимости от его локализации длительно сохранялось в англоязычной литературе. Однако, по мере развития клинических рекомендаций по лечению мукозита, стало преобладать мнение об искусственности этого деления, так как ЖКТ — единая структура в эмбриологическом и функциональном отношении. Мукозит может встречаться на любом уровне ЖКТ, но с различными клиническими проявлениями, что обусловлено специфической структурой и функцией слизистой различных его отделов [5]. Впоследствии появилась новая терминология. «Алиментарный мукозит» стал предпочтительным термином, описывающим воспаление слизистой вследствие противоопухолевой терапии, в любой точке ЖКТ, от ротовой полости до ануса.
Получение корректных и сопоставимых данных об истинной частоте и распространенности мукозита является непростой исследовательской задачей. Это обусловлено существующим разнообразием групп пациентов (вид опухоли, ее локализация, стадия) и методов лечения (трансплантация, химиотерапия, лучевая терапия, комбинированные режимы). Только недавно мукозит стал самостоятельным объектом клинических исследований. Кроме того, методика оценки тяжести мукозита редко является стандартизованной, что мешает судить о качестве полученных данных [2, 6].
Частота выявления мукозита у пациентов с опухолями головы и шеи, получающих лучевую терапию, и у больных после трансплантации гемопоэтических стволовых клеток (ТГСК) варьирует от 85% до 100% и от 75% до 100% соответственно [3, 7]. Таким образом, хотя только 4% всех описанных мукозитов наблюдались у пациентов, перенесших трансплантацию [8], частота мукозита в данной группе больных может достигать 100%.
Вследствие существенных клинических последствий орального мукозита, его экономическое бремя также является значительным. Данные из США свидетельствуют об удвоении затрат на пациентов, перенесших противоопухолевую терапию, у которых развился мукозит, по сравнению с теми пациентами, у которых данное воспаление отсутствовало [9]. Специфические затраты при мукозите включают в себя: 1) отсроченное или прерванное лечение (в 35% химиотерапия у пациентов отсрочена и прекращена у 30%); 2) энтеральное питание (87% пациентов, получивших ТГСК, нуждаются в зондовом питании); 3) назначение медикаментов, включая антибиотикотерапию и опиоидные аналгетики (в последних нуждаются до 80% пациентов ТГСК); и, наконец, 4) удлинение сроков госпитализации (у больных с солидными опухолями, получающими миелосупрессивную терапию, возникновение мукозита удвоило количество дней госпитализации за один цикл) [2, 9].
Клиническая оценка мукозита
Как в научных исследованиях, так и в терапевтической практике оценочные шкалы мукозита должны быть объективными, комплексными, воспроизводимыми и стандартными. К сожалению, ни одна шкала не отвечает всем названным критериям и не принята единодушно всеми профессиональными сообществами онкологов. Тем не менее, их широкое использование в онкологии позволяет провести ретроспективное сравнение токсичности между различными исследованиями.
Клинические рекомендации по профилактике и лечению мукозита
Первые клинические рекомендации [6] по ведению алиментарного мукозита были изданы в 2004 году и основывались на обзоре результатов исследований 14 рабочих групп. В данных рекомендациях подчеркивалась нехватка качественных научных публикаций по проблеме мукозита, соответствующих требованиям доказательной медицины. В целом эти рекомендации более фокусировались на рутинном уходе за больными, чем на препаратах с доказанной эффективностью. Тем не менее, среди них был рекомендован цитопротектор амифостин (Этиол) для профилактики эзофагита у пациентов, получающих лучевую терапию при немелкоклеточном раке легкого. Никакие специальные виды нутритивной поддержки не были включены в указанный документ. Однако из 205 источников, использованных при его составлении, четыре публикации касались супплементации глютамином [10–13].
Обновленные клинические рекомендации были изданы в 2007 году [14]. Основные изменения касались: рекомендаций к применению фактора роста кератиноцитов-1 (KGF-1), Kepivance для профилактики орального мукозита у пациентов ТГСК и рекомендаций против системного (парентерального) использования глютамина [15].
Эти клинические рекомендации представляют собой большой шаг вперед в разработке проблемы мукозита. Однако только очень небольшое количество практикующих врачей слышали об этих клинических рекомендациях и лишь неутешительно низкий процент врачей стал их использовать в своей практике. Таким образом, на первый план в будущем выдвигаются обучающие программы для профессионалов по ведению алиментарного мукозита [8, 16].
Общепризнанными принципами профилактики мукозита являются: соблюдение оральной гигиены, санация кариозных зубов и проявлений периодонтита перед началом химиотерапии. Стандартные профилактические правила ухода за полостью рта включают чистку зубов специальной мягкой щеткой или даже тампоном (при агранулоцитозе), частые полоскания раствором пищевой соды, антисептиками и противомикробными препаратами. Важно не использовать в питании раздражающие продукты (кислые, горькие, соленые) и пищу, агрессивную термически и механически (леденцы, семечки, сухарики, мелкие косточки). Лечение мукозита также включает регулярное полоскание полости рта для удаления зубного налета и поддержания влажности слизистой. Для снятия боли могут использоваться анальгезирующие препараты (лидокаин и др.), при выраженной боли необходимы системные аналгетики, включая опиоиды. Лечение вторичных инфекций (бактериальных, грибковых, вирусных), осложняющих мукозит, проводится по общим принципам лечения инфекций у иммунокомпрометированных больных [4]. В отличие от вышеперечисленных терапевтических положений, клиническое питание и нутритивная поддержка больных, страдающих мукозитом, разработаны в гораздо меньшей степени.
Мукозит: роль нутритивной поддержки
Нутритивная поддержка пациентов со злокачественными опухолями тазовой области, получавших лучевую терапию. У пациентов со злокачественными опухолями области таза, получающих лучевую терапию и химиотерапию, тяжелая нутритивная недостаточность встречается нечасто, однако острый гастроинтестинальный мукозит является типичной проблемой. В недавнем обзоре результатов нутритивной поддержки пациентов, получавших лучевую терапию на область таза (n = 2?646), делается заключение о том, что диеты с низким содержанием жира, среднецепочечные триглицериды (Medium Chain Triglycerides, MCTs), пробиотики и элементные диеты заслуживают дальнейшего изучения [17]. Основной причиной ограничения блюд обычного рациона и даже полимерных питательных смесей для клинического питания больных с гастроинтестинальным мукозитом является недостаточность ферментативного гидролиза в тонкой кишке. Так называемые элементные диеты, содержащие основные питательные вещества в виде гидролизатов и мономерных продуктов, традиционно используемые при мальабсорбции самого различного генеза, все шире применяются при гастроинтестинальных мукозитах у онкологических больных. Результаты первоначальных исследований вкусовой привлекательности и переносимости данных продуктов [18, 19] были впечатляющими [19], хотя число пациентов, употреблявших элементную диету на фоне лечения, снизилось с 92% в первую неделю до 46% в пятую неделю [19].
Новые компоненты питания при лучевой и химиотерапии:глютамин и TGF-бета
Оба названных компонента направлены на снижение активности воспалительного процесса, составляющего патогенетическую сущность алиментарного мукозита. Роль глютамина в профилактике токсичности, вызванной химиолучевой терапией, продолжает изучаться [20]. Глютамин — условно незаменимая аминокислота со многими биологическими функциями. Помимо его роли в регуляции внутриклеточного редокс-потенциала (предшественник глютатиона), глютамин способен сократить выработку провоспалительных цитокинов и снизить интенсивность связанного с ними апоптоза. Цитотоксическая химиотерапия увеличивает потребность клеток в глютамине. В таблице суммируются недавние исследования перорального приема глютамина для профилактики мукозита при лечении различных онкологических заболеваний [10, 11, 21–29].
Более новый компонент клинического питания при мукозите — трансформирующий фактор роста бета-2 (Transforming Growth Factor beta-2, TGF-beta-2). Его натуральным источником является молочный белок казеин. TGF-бета (существующий в трех изоформах) может быть классифицирован и как цитокин, и как фактор роста. Он вовлечен в регуляцию множества процессов, включая контроль клеточного цикла и процесс репарации [30]. Питательные смеси, содержащие казеин и богатые TGF-бета, показали свою эффективность в индукции ремиссии при болезни Крона [31], возможно, за счет прямого противовоспалительного эффекта в отношении слизистой кишечника [32]. В исследованиях на животных рацион, обогащенный TGF-бета, был продемонстрирован как протективный в отношении воспаления тонкого кишечника [33, 34]. Уникальной питательной смесью для клинического питания больных с алиментарным мукозитом является сухая полимерная безглютеновая и безлактозная смесь Модулен IBD, cодержащая терапевтические концентрации TGF-бета. Технология изготовления смеси для энтерального клинического питания Модулен IBD позволила сохранить в ее составе этот естественный противовоспалительный фактор роста, содержащийся в непастеризованном женском и коровьем молоке. Терапевтическая эффективность TGF-бета в профилактике и лечении мукозита еще не полностью оценена в клинической практике. Научный поиск в этой области начат относительно недавно, однако в число стандартных показаний к применению питательной смеси с противовоспалительным эффектом Модулен IBD уже включена профилактика и/или оказание дополнительного лечебного эффекта при поражениях слизистых, вызванных противоопухолевой терапией (мукозитах).
Нутритивная поддержка при ТГСК у пациентов с высоким риском мукозита
Традиционно парентеральное питание было основным предметом исследований в этой области. Однако в последние годы интерес к данному виду нутритивной поддержки снизился из-за его значительных недостатков, включая риск инфекций, связанных с центральным венозным катетером, увеличением длительности госпитализации, а также финансовых затрат. Однако, несмотря на это, при мукозите IV степени по шкале ВОЗ парентеральное питание остается единственным средством нутритивной поддержки пациента и, таким образом, продолжает играть важную роль для предотвращения нутритивной недостаточности [35].
Наряду с этим, имеются исследования, доказывающие, что энтеральное питание является безопасным и эффективным методом питания после аллогенной трансплантации [36], хотя необходимы дальнейшие рандомизированные исследования в этой области. Возможно, ключевым моментом в использовании энтерального питания является выбор времени введения пищевого зонда и начала питания [37], так как после развития алиментарного мукозита установка пищевого зонда трудно переносима и неоправданно травматична. Другой возможный подход к расширению объема энтерального питания — это использование назоеюнального зонда с целью прекращения рвоты, вызванной питанием элементными смесями [38]. ЃЎ
По вопросам литературы обращайтесь в редакцию.
Е. В. Полевиченко, доктор медицинских наук, профессор
ГОУ ВПО «Ростовский государственный медицинский университет», Ростов-на-Дону
Осложнения после химиотерапии
На протяжении последних десятилетий химиотерапия является одним из эффективных методов лечения опухолей. Основной механизм действия химиопрепаратов – воздействие на клетки опухоли таким образом, что происходит замедление или прекращение их размножения.
К сожалению химиотерапия не обладает специфичностью: помимо клеток опухоли, повреждаются и клетки здоровых тканей и органов. В первую очередь это касается тех органов, ткани которых могут быстро расти, размножаться – волосяные фолликулы, клетки слизистой оболочки кишечника и ротовой полости, костный мозг. Наиболее часто, 80-90% осложнений после химиотерапии при раке наблюдается со стороны системы крови и пищеварительного тракта.
Осложнения делятся по степени выраженности. Всемирная организация здравоохранения выделяет 3 степени тяжести осложнений:
Осложнения со стороны пищеварительной системы
К наиболее частым осложнениям со стороны пищеварительной системы при проведении лекарственной терапии относятся:
Тошнота и рвота занимают лидирующие позиции среди жалоб пациентов. Причина возникновения тошноты и рвоты до сих пор до конца не ясна. Известно, что химиотерапия вызывает тошноту и рвоту посредством высвобождения эметогенных соединений, таких как допамин, серотонин и субстанция Р, воздействующих на рецепторы пищеварительной системы и центральной нервной системы, запуская рвотный рефлекс. Другими словами, развитие тошноты и рвоты связано с раздражением рецепторов в желудке и головном мозге.
Виды тошноты и рвоты
Вид тошноты и рвоты определяется временем его возникновения на протяжении цикла химиотерапии:
острая — в первые сутки после введения цитостатиков
отсроченная — в течение 2-5 суток после введения цитостатиков.
При последующих введениях препарата возможно появление «преждевременной рвоты» (тошнота и рвота «ожидания») — в течение нескольких часов до введения цитостатиков. Она, как правило, развивается у больных, получавших ранее высокоэметогенные режимы ПХТ и страдавших от ее осложнений. Ее могут провоцировать запахи, вкусовые ощущения, вид предметов и обстановки, напоминающих о лечении. Для профилактики такой тошноты и рвоты используются транквилизаторы, психотренинг, гипноз.
К сожалению, часто пациенты могут не сообщать о развитии у них осложнений. Данное поведение обусловлено широким распространением заблуждений относительно процесса химиотерапии, таких как:
Некоторые пациенты преуменьшают силу и значение развивающихся осложнений и не хотят лишний раз беспокоить медицинский персонал. Такое поведение сильно затрудняет конструктивное взаимодействие между пациентом и доктором и создает дополнительные риски для здоровья.
Факторы риска развития тошноты и рвоты
Существуют различные причины, предрасполагающие к появлению тошноты и рвоты. В первую очередь, это особенности используемого препарата или их комбинации.
Большое значение имеют индивидуальные особенности пациента:
Наиболее тяжело химиотерапию переносят женщины и больные моложе 30 лет.
Эффективность противорвотной терапии
Лечение таких осложнений после химиотерапии, как тошнота и рвота, может дать хороший эффект. Арсенал препаратов, которые обеспечивают профилактику и лечение тошноты и рвоты, очень большой. Комплексное их использование способно предотвратить появление этих симптомов в 90% случаев.
Полный контроль: отсутствие рвоты после введения противорвотных препаратов,
Частичный контроль: один эпизод рвоты или умеренная тошнота
Образ жизни и питание при проведении химиотерапии
Большое значение имеет образ жизни и питание при проведении химиотерапии. Рекомендуется двигательная активность, свежий воздух, дыхательная гимнастика. Двигательная активность помогает избежать осложнений.
Необходимо правильно питаться – голод усиливает тошноту. Прием пищи нужно начинать до появления голода, а есть необходимо медленно и небольшими порциями.
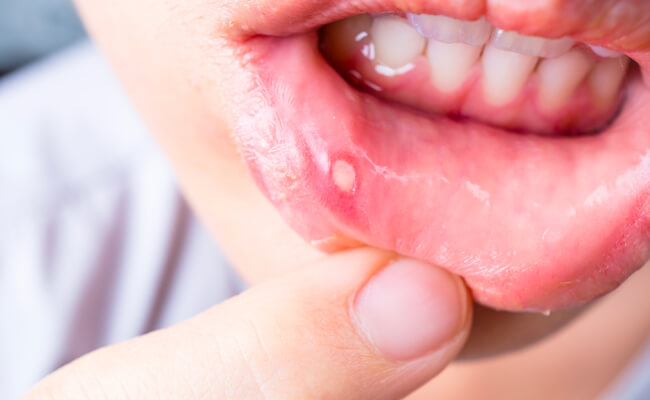
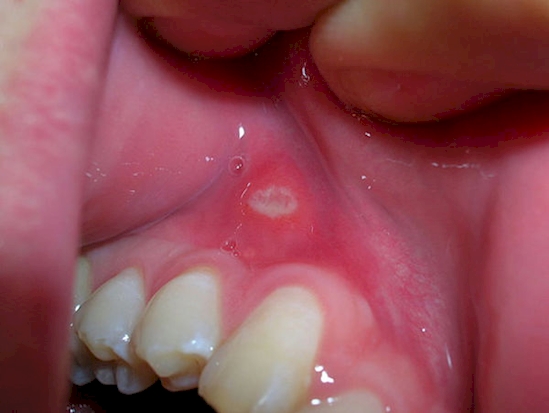
Стоматит
Стоматит — это воспаление ротовой полости, которое наблюдается примерно у трети пациентов. Воспаление чаще всего вызвано активацией бактериальной и грибковой инфекции на поврежденных цитостатиками участках слизистой оболочки. Стоматит является проявлением скрытых осложнений.
При отсутствии своевременного лечения, может развиться выраженное воспаление, обезвоживание, прием пищи станет затруднен.
Предрасполагающие факторы развития стоматита
Профилактика стоматита включает в себя максимальное санирование полости рта до начала химиотерапии. Очень часто мы до начала лечения отправляем пациентов к стоматологу чтобы избежать последующих осложнений.
Гигиенические мероприятия включают чистку зубов мягкой зубной щеткой, полоскание слабым раствором перекиси водорода, фурацилина, хлоргексидина.
Если стоматит все же развился, необходимо максимально щадить ротовую полость при питании – исключить те продукты, которые могут вызвать раздражение.
Питание при стоматите:
Сама по себе химиотерапия не накладывает ограничений на питание, но для ускорения восстановления поврежденных клеток, мы рекомендуем употреблять больше белка и вообще здоровую полноценную разнообразную пищу.
Местное лечение направлено на удаление из ротовой полости зубного налета и поддержание влажности слизистых оболочек. Обезболивание местными анестетиками (прокаин, лидокаин). При развитии эзофагита применяют антацидные препараты, обволакивающие средства, спазмолитики.
Диарея
Третья группа осложнений — диарея или жидкий стул. Также встречается довольно часто (25-30% пациентов).
Диета при диарее должна быть максимально щадящей для кишечника. В первые дни можно применить водную диету чтобы кишечник максимально успокоился. Продукты, которые максимально легко усваиваются.
Авторская публикация:
СЕМЕНОВА АННА ИГОРЕВНА
химиотерапевт, онколог, кандидат медицинских наук
Стоматит после химиотерапии — лечение и профилактика
Содержание:
При лечении рака воспалительные процессы слизистой оболочки ротовой полости отнюдь не редкость, а скорее даже закономерность, ведь усиленное химическое воздействие на организм снижает его сопротивляемость инфекциям, большинство из которых попадают через рот.
Кроме того, химиотерапевтическое лечение воздействует на механизм деления клеток организма. За счет этого поврежденных опухолевых клеток со временем становится все меньше и меньше, но и здоровые клетки повреждаются и на какое-то время теряют природную способность к самовосстановлению. Это приводит к повреждению эпителиальных клеток, из которых состоит слизистая ротовой полости, что, в свою очередь, ведет к стоматиту. Из-за пересыхания слизистой оболочки возникают небольшие язвочки и трещины, не редко начинают кровоточить десны.
Как снизить риск возникновения стоматита
Стоматит после химиотерапии — явление хоть и крайне болезненное, но временное. Такие осложнения проходят после завершения химиотерапевтического лечения и восстановления уровня лейкоцитов в крови. Более того, существует масса способов снизить риск появления стоматита при онкологии. Для этого вам следует соблюдать ряд простых правил:
Лечение при химиотерапии
Что же делать, если вы уже столкнулись со стоматитом, сопутствующим химиотерапии? В первую очередь не поддавайтесь панике. К сожалению, стоматит часто сопровождает рак и не все знают, как его предотвратить, а врачам зачастую некогда объяснять каждому пациенту способы профилактики.
Самым первым советом будет обращение к специалисту. Он не только пропишет вам препараты, совместимые с химическим лечением, но и посоветует, как снять болевые ощущения.
Когда язвочками поражена вся полость рта и десны, человеку становится больно даже пережевывать пищу, вот почему неотъемлемой частью лечения стоматита после химиотерапии является правильное питание:
Даже если у вас последняя стадия стоматита, не отказывайте себе в приеме пищи из-за болезненных ощущений. Ведь нарушение питания и поступления полезных веществ в организм могут его ослабить куда больше, чем медицинское лечение. Лучше употреблять пюреобразные и кашеобразные продукты, не требующие пережевывания, чем не употреблять их вовсе.
Группа риска
Спрогнозировать появление стоматита при лечении онкологических заболеваний можно у некоторых людей, которые в наибольшей степени подвержены возникновению язв и повреждений ротовой полости. Зачастую это помогает предупредить и предотвратить это неприятное заболевание.
Так, к примеру, наибольшему риску подвержены люди, не соблюдающие гигиену полости рта и не посещающие стоматологию для прохождения профилактических осмотров. Хронические заболеваний зубов и горла (гингивиты, пародонтиты, фарингиты, ларингиты, тонзиллиты) также способствуют возникновению стоматита из-за постоянного присутствия в горле болезнетворных инфекций (стрептококков, стафилококков и других).
Заболевания нервной системы, подверженность стрессам, авитаминозы, нарушение обмена веществ и заболевания внутренних органов, равно как и курение, сильно повышают риск возникновения воспалений. А наличие в анамнезе ранее полученной лучевой терапии увеличивает «шансы» на образование стоматита в разы. Кроме того, у некоторых пациентов имеется склонность к воспалительным процессам в ротовой полости из-за употребления горячей или холодной пищи и определенных групп продуктов.
Вот почему при появлении первых признаков стоматита следует немедленно обратиться к врачу. Диагностировать их вы можете следующим образом:
Если не остановить стоматит на ранней стадии и не начать лечение, вскоре состояние усугубится, и небольшое воспаление может перерасти в язвенно-некротическое, глубокое поражение мягких тканей, с трудом поддающееся лечению.
Стоматит (мукозит полости рта) на фоне комбинированного лечения
Это поражение слизистой оболочки полости рта, приводящее к воспалению, а при тяжелых формах к болезненным язвам и инфекции. Риск стоматита напрямую связан с типом противоопухолевого лечения, интенсивностью и режимом назначения.
Стоматит может развиваться уже после первого введения химиотерапии, а может и к концу курса, что зависит от агрессивности препаратов и сопротивляемости организма. Комбинированная терапия (например, лучевая терапия по поводу рака головы и шеи в сочетании с одновременной химиотерапией) может увеличить выраженность стоматита.
Сложнее всего стоматит протекает у детей и людей преклонного возраста.
Какие препараты чаще всего вызывают развитие стоматита?
Предрасполагающие факторы развития мукозита полости рта
Как стоматит классифицируется?
Шкала пероральной токсичности по ВОЗ
| СТЕПЕНЬ ТЯЖЕСТИ | КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ | ВОЗМОЖНОСТЬ ПИТАТЬСЯ |
| I | эритема и зуд, нет язв. повреждение слизистой оболочки ротовой полости (атрофия) с/без эритемы | Пациент в состоянии есть твердую пищу. |
| II | Имеются язвы с/без эритемы | Пациент в состоянии есть твердую пищу. |
| III | Имеются язвы с/без эритемы | Требуется жидкая диета, пациент не в состоянии есть твердую пищу. |
| IV | Имеются многочисленные язвы | Пациент не в состоянии употреблять пищу (твердую, жидкую). Необходимость парентерального питания или трубки для кормления. Обычное питание при такой стадии мукозита невозможно. |
Общие критерии токсичности национального института рака (США) (NCI, 2010)
| СТАДИЯ | КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ | ВЫРАЖЕННОСТЬ СИМПТОМОВ |
| I | Покраснение слизистой | Симптомы не выраженные или слабо выраженные; вмешательство не требуется. |
| II | Имеются бляшки или псевдомембранные поражения кожи | Умеренная боль; нет помех при оральном приеме пищи и жидкости; требуется изменение диеты. |
| III | Имеются сливающиеся изъязвления или псевдомембранные поражения кожи; могут быть кровотечения при незначительных повреждениях | Сильная боль; затруднения при глотании. |
| IV | Некроз тканей | Значительные спонтанные кровотечения, угрожающие жизни последствия. Требуется экстренное вмешательство. |
| V | Летальный исход |
Cимптомы мукозита
Ранки, язвочки, покраснения на слизистой и покрытие ее белым налетом. Клиническая картина зависит от формы заболевания:
Как проводить профилактику стоматита/мукозита?
Возможные варианты полосканий:
Лечение стоматита/мукозита полости рта
Хлоргексидин не рекомендуется для лечения выявленного стоматита.
Сукралфат не рекомендован для лечения стоматита, вызванного лучевой терапией.
Ацикловир и его аналоги не рекомендуются для предотвращения стоматитов на фоне стандартной химиотерапии.
Реабилитация при стоматите/мукозите полости рта
Низкоинтенсивная лазеротерапия (НИЛИ): В 2011 году на заседании Американской Ассоциации Онкологов (ASCO) НИЛИ была отмечена, как эффективная методика, достоверно уменьшающая тяжесть течения и частоту развития стоматита.
Международная Ассоциация Поддерживающей Терапии в Онкологии (MASCC) и Международное Общество по лечению опухолей полости рта (International Society for Oral Oncology (ISOO)) в 2013 году утвердила НИЛИ, как эффективное и безопасное лечение стоматита у онкологических больных.