Чем лечить жировой алкогольный гепатоз
Жировой гепатоз печени — симптомы, лечение у женщин, мужчин, диета
Жировой гепатоз — это заболевание, характеризующееся постепенным накоплением капель жира в межклеточном пространстве и клетках печени. Распространенность данной патологии среди взрослого населения развитых стран достигает 25%. В группе риска находятся женщины, достигшие возраста 40 лет и имеющие избыточную массу тела.
Этиологические факторы жирового гепатоза могут быть связаны с различными факторами. Но ранняя диагностика затрудняется отсутствием явных клинических проявлений. Многие люди не догадываются о прогрессировании болезни до появления выраженных симптомов, когда появляется болевой синдром и больной замечает увеличение печени в размерах.
Причинами жировой инфильтрации печени являются:
В отдельных случаях причиной жирового гепатоза становится наследственная недостаточность ферментов, принимающих участие в обмене липидов. Патологический процесс может быть первичным, когда заболевание развивается без сопутствующих патологий, а также вторичным — на фоне имеющихся нарушений.
Диагностика и клинические проявления
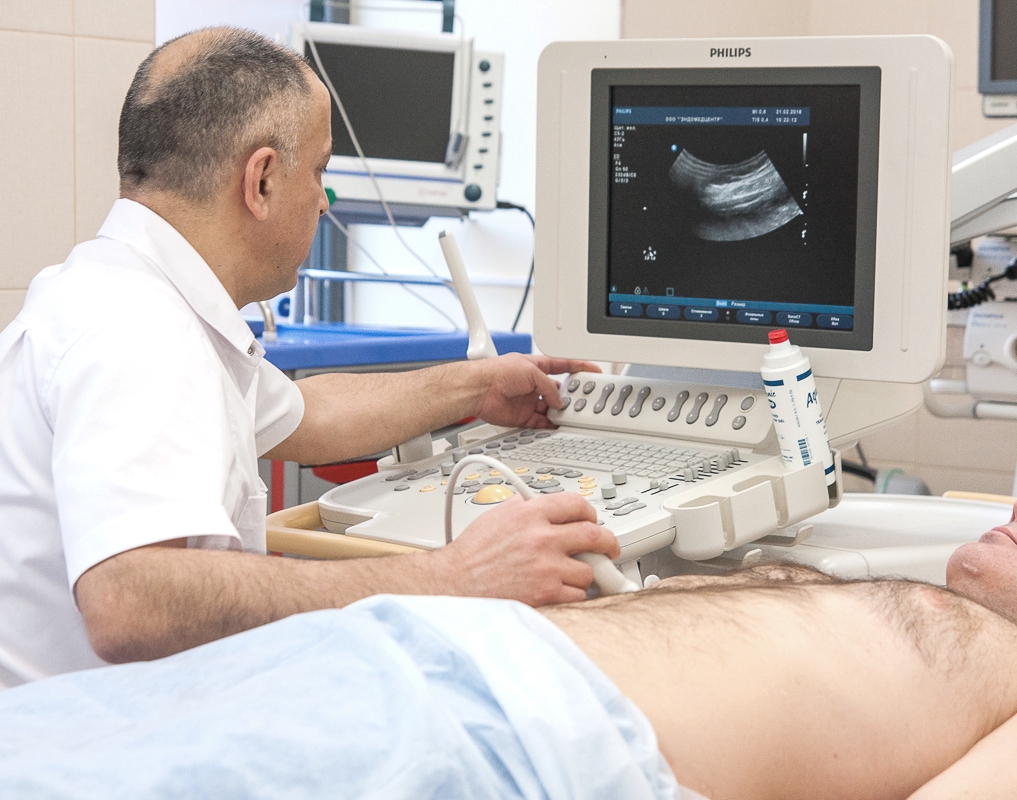
Диагностика жирового гепатоза затрудняется тем, что у заболевания отсутствуют специфические симптомы. Рекомендуется проводить скрининговые исследования при наличии лишнего веса, сахарного диабета, инсулиновой резистентности.
Основные методы диагностики:
Важно выявить все имеющиеся нарушения в рамках комплексной диагностики органов ЖКТ, эндокринных желез. Это необходимо для выбора наиболее эффективной лечебной схемы и профилактики опасных для жизни осложнений.
На развитие патологии могут указывать следующие признаки:
Диффузное поражение тканей печени может сопровождаться кровоизлияниями, снижением артериального давления и обморочными состояниями. До 70% больных — это женщины с лишней массой тела.
Лечение подбирает врач на основании результатов диагностики. При необходимости назначаются консультации эндокринолога.
Лечение жирового гепатоза проводят в амбулаторных условиях. Программа терапии включает:
Заболевание имеет благоприятный прогноз. Своевременное обращение к врачу и устранение факторов, провоцирующих развитие жирового гепатоза, позволяет полностью восстановить структуру и функциональность пораженной печени, значительно повысить качество жизни пациента.
Чем лечить жировой алкогольный гепатоз
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20%. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение алкогольной болезни печени (АБП) определяется в первую очередь паттерном употребления спиртных напитков. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет. Возможности терапии АБП ограничены. При гепатите тяжелого течения, наряду с коррекцией трофологического статуса, назначаются преднизолон и пентоксифиллин. Для лечения хронических форм АБП в настоящее время применяются средства для лечения алкогольной зависимости. Эффективность препаратов метаболического (гепатопротективного) действия ставится под сомнение, хотя в отдельных исследованиях получены обнадеживающие результаты.
Последствия злоупотребления алкоголем представляют собой общемировую проблему, включающую не только органную патологию, но также несчастные случаи и преступления, связанные с состоянием опьянения. Так, в Европе 11% летальных исходов у мужчин и 1,8% у женщин рассматриваются в ассоциации с алкоголизмом [1]. Если анализировать структуру поражений внутренних органов, то доминирующую позицию среди них занимает именно алкогольная болезнь печени (АБП), ведущая к развитию цирроза печени и гепатоцеллюлярной карциномы [2]. Несмотря на то, что в последние годы на пути изучения патогенеза поражения печени достигнуты серьезные успехи, лечение тяжелых форм АБП в определенной мере «законсервировалось», не давая основания говорить о революционном прорыве в ближайшем будущем. Тем не менее, определенные направления в терапии АБП можно расценивать как перспективные, причем это относится не только к методам, которые не вышли пока за рамки экспериментальных, но и к давно известным средствам, открывающим новые грани в процессе углубленного изучения.
Естественное течение АБП: от стеатоза к циррозу
Хотя стеатоз печени обнаруживается у 90% злоупотребляющих лиц, стеатогепатит развивается у относительно небольшой их части, а цирроз формируется лишь у 10–20% [3, 4]. Стеатоз протекает, как правило, бессимптомно и полностью регрессирует в условиях абстиненции. Естественное течение АБП определяется в первую очередь паттерном употребления спиртных напитков: постоянным или перемежающимся типом пьянства; периодами запоев, сменяющихся абстиненцией; нарастанием или сокращением суточной дозы алкоголя Учитывая обстоятельство, что большинство пациентов обращаются за медицинской помощью на поздних стадиях, оптимальной моделью наблюдения служат больные после трансплантации печени [5].
Генетическая предрасположенность к АБП также служит предметом активного изучения. Недавние исследования выявили значимую корреляцию определенных аллельных вариантов адипонутрина (PNPLA3) и прогрессированием фиброгенеза [6, 7]. Более того, генетический полиморфизм адипонутрина ассоциирован и с развитием ГЦК [8]. В то же время попытки идентифицировать генетические маркеры предрасположенности к АБП, в том числе полиморфизм генов, участвующих в метаболизме этанола, пока не увенчались успехом [9].
В ретроспективном исследовании S. Naveau, включавшем более 2000 злоупотребляющих алкоголем пациентов, по данным биопсии печени у 34% выявлен цирроз, у 9% — активный гепатит, у 46% — стеатоз печени с наличием или отсутствием фиброза, а у 11% патологические изменения печени отсутствовали [10]. По данным T. Poynard, вероятность развития цирроза нарастает с возрастом, достигая при регулярном употреблении высоких доз алкоголя 50% к 61 году, причем у женщин сроки формирования цирроза короче [11]. Суммируя опубликованные результаты ретроспективных исследований, можно констатировать, что среди госпитализированных алкоголиков частота обнаружения цирроза составляет около 20% [2].
Стеатоз обычно предшествует образованию соединительной ткани, но влияние аккумуляции жира в печени на фиброгенез изучено недостаточно [2, 13, 14]. Долгосрочная выживаемость пациентов с алкогольным стеатозом в отсутствии воспаления и фиброза сопоставима с таковой у трезвенников. Если сравнивать течение неалкогольной жировой болезни печени (НАЖБП) и АБП, можно констатировать более высокие темпы прогрессирования последней. В течение 10 лет у больных алкогольным стеатозом значительно чаще развивается цирроз (21% vs. 1%) и наблюдаются летальные исходы (74% vs. 25%) [15]. Интересно, что у больных алкогольным циррозом повышен риск аутоиммунных заболеваний [16]. Можно предположить, что ацетальдегид, образующийся в разных тканях под действием алкогольдегидрогеназы, образует прочные комплексы с белками, выступающие в роли неоантигенов.
Цирроз печени рассматривается в качестве причины смерти 25% алкоголиков, занимая первое место среди летальных исходов [1, 2, 15]. Нередко в качестве непосредственной причины смерти выступает не декомпенсация цирроза и не гепатоцеллюлярная карцинома, а алкогольный гепатит, «наслоившийся» на хроническую патологию печени и ведущий к острой печеночной недостаточности на фоне хронической ( liver failure). Это состояние проявляется желтухой, в тяжелых случаях энцефалопатией и гипокоагуляцией, и требует обязательного отражения в диагнозе, так как принципиально меняет прогноз и подходы к лечению.
Недавно завершенные исследования, основанные на биопсийном материале, убедительно продемонстрировали, что у подавляющего большинства пациентов с тяжелым алкогольным гепатитом имеется исходный цирроз или септальный фиброз печени [9, 18]. Тяжелый алкогольный гепатит характеризуется высокой летальностью, достигающей 30–50% в течение трех месяцев. У выживших больных наблюдается ускоренное формирование фиброза с нередким формированием цирроза в течение 1–2 лет [2].
В то время как ожирение является общепризнанным коморбидным фактором стеатоза, имеются также сведения о его влиянии на развитие алкогольного гепатита и фиброза печени. В качестве ключевых патогенетических факторов называются инсулинорезистентность и гипергликемия [19]. С другой стороны, небольшие дозы этанола способствуют замедлению прогрессирования неалкогольной жировой болезни печени [20].
Лечение АБП: акцент на абстиненцию
К вопросу о безопасной дозе алкоголя
Необходимость обсуждения лимита употребляемого алкоголя, превышение которого ведет к повреждению печени, в аспекте лечения АБП определяется тем, что соблюдение пациентом полной абстиненции является важной, но зачастую недостижимой целью. Так, в США 67–81% больных возобновляют прием алкоголя в течение одного года [21]. В последние годы дозу этанола часто измеряют в «дозах» (drinks), равных 10–14 г чистого этанола. «Доза» примерно соответствует бокалу пива, фужеру сухого вина или рюмке крепкого напитка. Показано, что прием ≤ 2 «доз» в день для мужчин и ≤ 1 «дозы» в день для женщин не ассоциировано с повышенной вероятностью развития органной патологии по сравнению с трезвенниками [2]. Другие исследования демонстрируют сходные результаты. Согласно метаанализу G. Corrao, употребление > 25 г этанола в день увеличивает относительный риск цирроза печени [22]. В итальянском исследовании Dionysos у лиц, ежедневно принимающих ≥ 30 г этанола, цирроз наблюдался в 2,2% случаев, тогда как у непьющих — в 0,08%. Риск цирроза экспоненциально возрастал по мере увеличения доз алкоголя, достигая 13,5% у употребляющих > 120 г в день [23].
Средства для лечения алкогольной зависимости
Ввиду того, что большинство пациентов нарушают предписанный режим абстиненции, в последние годы активно изучаются препараты, снижающие потребность в алкоголе: налтрексон, акампрозат, топирамат, баклофен и др. Наибольшее число исследований на сегодняшний день выполнено с агонистом баклофеном, продемонстрировавшим эффективность и безопасность при тяжелых формах АБП [24].
Метадоксин, зарегистрированный в ряде европейских стран для лечения алкогольной интоксикации, в нескольких небольших исследованиях значимое снижение употребления алкоголя, что сопровождалось редукцией биомаркеров АБП (трансаминазы, γ-глутамилтранспептидаза, средний объем эритроцитов) [25]. Сходные результаты получены в исследовании внутривенной формы глицирризиновой кислоты. Интересно, что соблюдение предписанного режима абстиненции коррелировало со снижением сывороточного уровня фактора некроза опухоли-α [26].
Коррекция трофологического статуса
Нутритивная поддержка наиболее важна для больных тяжелым алкогольным гепатитом, хотя и при других формах АБП у большинства пациентов наблюдаются те или иные формы нарушения трофологического статуса [2]. В исследовании С. Mendenhall et al. показано, что у пациентов, самостоятельно принимающих пищу с энергетической ценностью более 3000 ккал в сутки, отмечалась нулевая летальность, в то время как из потреблявших менее 1000 ккал в сутки умерло более 80% [27]. Несмотря на безусловную ценность этих данных, нельзя игнорировать высокую вероятность более тяжелого течения гепатита у больных второй группы, к типичным проявлениям которого относится анорексия [28].
Общие рекомендации по коррекции трофологического статуса у больных тяжелым алкогольным гепатитом предусматривают суточное потребление 1500–2500 ккал. Диета должна быть сбалансирована по содержанию основных нутриентов и витаминов, ограничение белка показано лишь в случаях его индивидуальной непереносимости. Следует помнить о преимуществе перорального приема пищи над зондовым и парентеральным; последнее назначается только при невозможности физиологического питания (повторная рвота, нарушения сознания).
Как отмечалось выше, избыточная масса тела и ожирение тоже способствуют прогрессированию повреждения печени ввиду общности ряда патогенетических звеньев алкогольного и неалкогольного стеатогепатита [10, 29], что необходимо учитывать при разработке программы лечения.
Кортикостероиды применяются для лечения тяжелого алкогольного гепатита на протяжении более 40 лет. Наиболее хорошо изучена схема с пероральным преднизолоном 40 мг в сутки в течение одного месяца, с одномоментной отменой или постепенным снижением дозы. Хотя многочисленные исследования весьма разнородны по дизайну и отбору пациентов, метаанализ показал достоверное повышение краткосрочной выживаемости по сравнению с больными, не получавшими преднизолон [14]. Оценка эффективности терапии обычно осуществляется с помощью индекса Лилле (Lille), который рассчитывается через семь дней лечения по формуле:
R = 3,19 — 0,101 (возраст в годах) + 0,147 (альбумин в день поступления, ) + 0,0165 (сывороточный билирубин, мкмоль) + 0,206 (наличие почечной недостаточности — 0 или 1) + 0,0065 (сывороточный билирубин в день поступления, мкмоль) + 0,0096 (протромбиновое время, с)
Индекс Лилле = Exp ® /[1 +Exp ® ]
Значение индекса Лилле > 0,45 указывает на неэффективность преднизолона и 75%-ю вероятность летального исхода в течение шести месяцев. С почти пятикратным ростом летальности сопряжено также отсутствие снижения уровня сывороточного билирубина, по меньшей мере, на 25% за аналогичный срок стероидной терапии [30]. У этой когорты больных дальнейшее применение преднизолона нецелесообразно, с учетом повышения риска инфекционных осложнений, особенно легочного аспергиллеза [31]. В упомянутом метаанализе выделены три группы пациентов в зависимости от реакции на преднизолон: с полным, частичным и нулевым ответом. Краткосрочная выживаемость в этих группах составила 91%, 79% и 53%, соответственно [14].
В первом сообщении о применении пентоксифиллина при тяжелом алкогольном гепатите были представлены обнадеживающие результаты, свидетельствующие о существенном снижении риска гепаторенального синдрома (ГРС) [32]. Большое рандомизированное контролированное исследование STOPAH, включавшее более 1000 пациентов, не продемонстрировало преимущество пентоксифиллина перед плацебо в отношении краткосрочной выживаемости [33]. Хотя необходимо принимать во внимание, что из исследования были исключены наиболее тяжелые больные — с ГРС, сепсисом и манифестной энцефалопатией — целесообразность применения пентоксифиллина представляется сомнительной.
Комбинация преднизолона и пентоксифиллина не выявила преимуществ по сравнению с монотерапией преднизолоном [13]. Таким образом, на сегодняшний день улучшение прогноза больных тяжелым алкогольным гепатитом, резистентных к кортикостероидам, возможно только путем выполнения срочной трансплантации печени [14].
Метаболические препараты («гепатопротекторы»)
Международные гепатологические ассоциации не рекомендуют применение лекарственных средств данной группы при АБП, что обусловлено слабой доказательной базой.
В исследовании J. Mato пероральное применение в дозе 1200 мг в сутки на протяжении двух лет сопровождалось более низкой летальностью или потребностью в трансплантации печени по сравнению с группой плацебо у больных компенсированным и субкомпенсированным алкогольным циррозом (класс, А и В по ) — 12% и 29% (p = 0.04), соответственно. Количество пациентов, прекративших и продолживших употребление алкоголя, было сопоставимо в обеих группах [35].
Результаты недавно опубликованного исследования и соавторов указывают на более низкую частоту ГРС у больных, получавших комбинацию преднизолон + по сравнению с монотерапией преднизолоном (p = 0.035). Показатели летальности в группах при этом статистически значимо не различались [28].
и соавторы представили результаты парентерального применения глицирризиновой кислоты у пациентов с алкогольным стеатогепатитом. Помимо отмеченного выше позитивного влияния на алкогольную зависимость, констатировано значимое снижение активности трансаминаз и уровня сывороточного билирубина [26].
L- ускоряет метаболизм аммиака, уменьшая проявления печеночной энцефалопатии. Показано, что препарат обладает способностью улучшать биохимические параметры у пациентов с хронической патологией печени, в том числе АБП [36]. Не исключено, что этот эффект обусловлен дезинтоксикацией обладающего универсальным цитотоксическим действием аммиака.
Неудовлетворительные результаты лечения тяжелых форм АБП служат основанием для разработки новых подходов, базирующихся на ключевых патогенетических механизмах. К находящимся на разных стадиях изучения, относятся модулирование иннатного иммунного ответа, подавление кишечной бактериальной и эндотоксиновой транслокации, блокирование апоптоза и активация фарнезоидного Х рецептора. В качестве многообещающего направления рассматривается технология индукции плюрипотентных стволовых клеток [37].
История медицины свидетельствует о том, что именно элиминация этиологического фактора определяет успех лечения большинства болезней, в том числе в эпидемиологическом ракурсе. Так, широкое внедрение в клиническую практику антигеликобактерной терапии позволило значимо снизить распространенность язвенной болезни желудка и двенадцатиперстной кишки, а противовирусных препаратов — эффективно контролировать заболеваемость гепатитом С. Казалось бы, в отношении АБП и других заболеваний решение проблемы лежит на поверхности: абстиненция ведет к выздоровлению или, по крайней мере, резкому снижению риска фатальных последствий. Однако этот постулат вызывает, по крайней мере, два вопроса: 1) что делать с больными, которые хотят, но не могут отказаться от алкоголя вследствие зависимости; 2) какой тактики ведения следует придерживаться в случае прогрессирования патологических изменений, несмотря на абстиненцию. Следовательно, весьма актуальным остается вопрос о медикаментозном лечении АБП, особенно тяжелых ее форм — гепатита и цирроза. Достижения в этой области не столь грандиозны, как в других разделах гепатологии. Многие лекарственные средства, на которые ранее возлагались надежды, основанные на результатах экспериментальных и пилотных данных, не оправдали их в рандомизированных контролированных исследованиях; показательным примером могут служить эссенциальные фосфолипиды. Тем важнее выбрать из относительно небольшого терапевтического арсенала препараты, проверенные временем и зарекомендовавшие себя с позиций доказательной медицины.
European Association for the Study of Liver. EASL clinical practical guidelines: management of alcoholic liver disease. J. Hepatol. 2012; 57: 399–420.
Mathurin P., Bataller R. Trends in the management and burden of alcoholic liver disease. J. Hepatol. 2015; 62(1S): S..
Lefkowitch of alcoholic liver disease. Clin. Liver Dis. 2005; 9: 37–53.
Lucey M., Mathurin P., Morgan hepatitis. N. Engl. J. Med. 2009; 360: 2758–2769.
DiMartini A., Dew M.A., Day N. et al. Trajectories of alcohol consumption following liver transplantation. Am. J. Transplant. 2010; 10: 2305–2312.
Stickel F., Buch S., Lau K. et al. Genetic variation in the PNPLA3 gene is associated with alcoholic liver injury in Caucasians. Hepatology. 2010; 53: 86–95.
Trépo E., Gustot T., Degré D. et al. Common polymorphism in the PNPLA3/adiponutrin gene confers higher risk of cirrhosis and liver damage in alcoholic liver disease. J. Hepatol. 2011; 55: 906–912.
Liu Y.L., Patman G.L., Leathart J.B. et al. Carriage of the PNPLA3 rs738409 C >G polymorphism confers an increased risk of fatty liver disease associated hepatocellular carcinoma. J. Hepatol. 2014; 61: 75–81.
Bataller R., North K. Brenner polymorphisms and the progression of liver fibrosis: a critical appraisal. Hepatology. 2003; 37: 493–503.
Naveau S., Giraud Borotto E. et al. Excess weight risk factor for alcoholic liver disease // Hepatology. 1997; 25: 108–111.
Poynard T., Mathurin P., Lai C.L. et al. A comparison of fibrosis progression in chronic liver diseases. J. Hepatol. 2003; 38: 257–265.
Song M., Chen T., Prough alcohol consumption causes liver injury in male mice through enhanced hepatic inflammatory response. Alcohol. Clin. Exp. Res. 2016; 40(3): 518–528.
Mathurin P., Louvet A., Duhamel A. et al. Prednisolone with vs. without pentoxifylline and survival of patients with severe alcoholic hepatitis: a randomized clinical trial. JAMA. 2013; 310: 1033–1041.
Mathurin P., Moreno C., Samuel D. et al. Early liver transplantation for severe alcoholic hepatitis // N. Engl. J. Med. 2011; 365: 1790–1800.
S., Franzmann M., Andersen I.B. et al. Longterm prognosis of fatty liver: risk of chronic liver disease and death. Gut. 2004; 53: 750–755.
Raynard B., Balian A., Fallik D. et al. Risk factors of fibrosis in liver disease. Hepatology. 2002; 35: 635–638.
Dunn W., Sanyal A.J., Brunt E.M. et al. Modest alcohol consumption is associated with decreased prevalence of steatohepatitis in patients with fatty liver disease (NAFLD) J. Hepatol. 2012; 57: 384–391.
Miller W.R, Walters S.T., Bennett effective is alcoholism treatment in the United States? J. Stud. Alcohol. 2001; 62: 211–220.
Corrao G., Bagnardi Zambon A., Torchio P. of alcohol intake in relation to risk of liver cirrhosis. Alcohol Alcohol. 1998; 33: 381–392.
Bellentani S., Saccoccio G., Costa G. et al. Drinking habits as cofactors of risk for alcohol induced liver damage. The Dionysos Study Group. Gut. 1997; 41: 845–850.
Vuittonet C.L., Halse M., Leggio L et al. Pharmacotherapy for alcoholic patients with alcoholic liver disease. Am. J. Health Syst. Pharm. 2014; 71(15): 1265–1276.
Leggio L., Kenna G.A., Ferrulli A. et al. Preliminary findings on the use of metadoxine for the treatment of alcohol dependence and alcoholic liver disease. Hum. Psychopharmacol. 2011; 26: 554–559.
Никитин И.Г, Байкова И.Е., Волынкина В.М. и др. Опыт использования глицирризиновой кислоты в лечении пациентов с алкогольной болезнью печени. Росс. журн. гастроэнтерол. гепатол. колопроктол. 2009; 19(1): 53–58.
Mendenhall C., Roselle G.A., Gartside P., Moritz T. Relationship of protein calorie malnutrition to alcoholic liver disease: A reexamination of data from two Veterans Administration Cooperative Studies. Alcoholism: Clinical and Experimental Research. 1995; 19(3): 635–641.
Tkachenko P, Maevskaya M, Pavlov A et al. Prednisolone plus S- in severe alcoholic hepatitis. Hepatol Int. 2016 Jun 23.
Diehl and alcoholic liver disease. Alcohol. 2004; 34: 81–87.
Louvet A., Naveau S., Abdelnour M. et al. The Lille model: a new tool for therapeutic strategy in patients with severe alcoholic hepatitis treated with steroids. Hepatology. 2007; 45: 1348–1354.
Gustot T., Maillart E., Bocci M. et al. Invasive aspergillosis in patients with severe alcoholic hepatitis. J. Hepatol. 2014; 60: 267–274.
Thursz M., Richardson P., Allison M.E. et al. Steroids or pentoxifylline for alcoholic hepatitis: results of the STOPAH trial. Hepatology. 2014; 60: LB1.
E., Thevenot T., Piquet M.A. al. Glucocorticoids plus in severe alcoholic hepatitis. N. Engl. J. Med. 2011; 365: 1781–1789.
Грюнграйф К., Й. Эффективность гранул L- при лечении хронических заболеваний печени. Сучасна гастроентерология. 2008; 2: 59–66.
Saberi B, Dadabhai AS, Jang YY Current Management of Alcoholic Hepatitis and Future Therapies. J Clin Transl Hepatol. 2016; 4(2): 113–122.
Рисунок. Схема стадийного течения алкогольной болезни печени (по P. Mathurin, R. Bataller, 2015, с изменениями).
Алкогольный гепатоз
При постоянном или длительном употреблении алкогольных напитков нарушается функционирование всего организма, и в частности печени. Мышечные структуры начинают накапливать жирные кислоты на клеточном уровне, что ведет к нарушению обменного процесса и дальнейшей дистрофии печени. Так развивается алкогольный гепатоз. Данное заболевание необходимо вовремя диагностировать и лечить.
Симптомы
Начало болезни может протекать практически бессимптомно и походить на признаки хронической усталости или нарушения пищеварения. Симптомами алкогольного гепатоза могут быть следующие: слабость, быстрая утомляемость, снижение веса, потеря аппетита, нарушение концентрации внимания и другие. Развитие болезни без необходимого лечения проявляется более сложной симптоматикой: вздутием живота, тошнотой, изжогой, дискомфортом и тяжестью в правом боку. В зависимости от степени поражения печени симптомы могут усиливаться и добавляться другие признаки: нарушение стула, изменение цвета кожи (на серовато-бледный), сильная тошнота с последующей рвотой, дерматологические аномалии и прочее. Вариабельность симптомов не позволяет диагностировать заболевание самостоятельно. При проявлении перечисленных признаков необходимо обратиться к лечащему врачу.
Диагностика
Для постановки правильного диагноза и выбора дальнейшего метода лечения врач анализирует информацию, полученную при разговоре с пациентом, выслушав его жалобы, и при его визуальном и физикальном осмотре. Если есть подозрения на алкогольный гепатоз, то для дополнительной диагностики могут понадобиться лабораторные (анализ крови, мочи, копрограмма) и инструментальные методы (ультразвуковое обследование, биопсия, компьютерная томография и другие).
Лечение
Лечение назначается только врачом и зависит от тяжести заболевания, возраста пациента, его физиологических особенностей и других факторов. Одними из основных шагов к выздоровлению станут отказ от употребления алкоголя, соблюдение диеты и особого режима питания. Нужно отказаться от жареных и копченых продуктов, исключить острые приправы, соленья, консервы и предпочесть отварные блюда или приготовленные на пару. Рацион должен включать 5–6 приемов пищи небольшими порциями. Выполнение предписаний врача и оптимистичный настрой помогут избавиться от заболевания и почувствовать себя здоровым, радостным человеком.
Фосфоглив® при жировом гепатозе

Механизм развития жирового гепатоза печени
В основе патогенетических механизмов жирового гепатоза лежат:
Характерной особенностью патологического состояния является повышение количества триглицеридов более чем на 10 % от общей сухой массы печени. Из-за этого при гепатозе происходит отложение жировых капель в гепатоцитах, развитие «ожирения» печеночных клеток, их последующая гибель и замещение фиброзной соединительной тканью.
Жир в клетках печени может накапливаться по нескольким причинам:
На сегодняшний день распространенность стеатоза в общей популяции достигает 40 %.
Степени гепатоза
В зависимости от количества и места накопления жира принято выделять 4 степени жирового гепатоза печени:
Причины жирового гепатоза
К основным причинам развития жирового гепатоза печени относят:
Клинические признаки гепатоза
Основные симптомы заболевания
На ранней стадии заболевания симптомы жирового гепатоза печени практически не наблюдаются. Это объясняется способностью гепатоцитов к активной регенерации. Однако по мере накопления жира клетки печени перестают справляться со своей функцией. У пациентов появляются следующие симптомы:
Диагностика
Диагностика жирового гепатоза включает в себя сбор анамнеза, оценку самочувствия и физикального статуса пациента, а также лабораторные и инструментальные методы обследования печени.
Лабораторные методы исследования:
Инструментальные диагностические методики:
Лечение жирового гепатоза печени
В связи с наличием большого разнообразия причин, обуславливающих развитие патологического процесса, лечение жирового гепатоза считается достаточно сложной задачей, требующей грамотного комплексного подхода. Обязательными условиями успешной терапии являются:
Диета
Пациентам с повышенной массой тела рекомендуется диетическое питание, направленное на нормализацию жирового и холестеринового обмена. В соответствии с принципом диеты № 5 в суточный рацион больного гепатозом должны входить:
Блюда готовятся на пару, запекаются или отвариваются и подаются только в теплом виде. Прием горячей, холодной, острой и жареной пищи запрещен. Питание должно быть дробным – 5–6 раз в день.
В список продуктов, рекомендованных при лечении гепатоза печени, входят:
Запрещенные продукты при гепатозе:
Лечение жирового гепатоза печени при помощи здоровой диеты требует строгого соблюдения принципов сбалансированного питания. Оптимальная потеря веса – не более 1 кг за неделю. В случае резкого снижения массы тела возможно развитие стеатоза, способного повлечь за собой воспаление, усиление активности фиброгенеза и увеличение скорости развития фиброза.
Медикаментозная терапия
Медикаментозное лечение жирового гепатоза печени проводится в 2 этапа.
Симптоматическое лечение гепатоза печени предусматривает использование противовоспалительных средств, пищеварительных ферментов, витаминов, препаратов антифиброзного действия и пробиотиков, нормализующих микрофлору кишечника.
Фосфоглив* при лечении жирового гепатоза
Фосфоглив* – современный гепатопротектор, нашедший широкое применение в гастроэнтерологии и гепатологии. Этот препарат патогенетического действия обладает восстанавливающими, противовоспалительными и антифиброзными свойствами и может использоваться для лечения гепатоза. В состав гепатопротектора входят два активных компонента: эссенциальные фосфолипиды и глицирризиновая кислота.
Эссенциальные фосфолипиды способствуют:
Применение Фосоглива* в комплексном лечении гепатоза способствует:
Препарат обладает благоприятным профилем безопасности и имеет доказательства клинической эффективности. Для достижения максимального действия при лечении гепатоза печени Фосфоглив* следует принимать курсами согласно инструкции по применению.
Алкогольная болезнь печени
Согласно МКБ 10-го пересмотра выделяют следующие расстройства печени:
Болезни печени объединяет различные нарушения структуры паренхимы и функционального состояния гепатоцита, вызванные систематическим употреблением спиртных напитков. Алкогольные болезни печени относятся к токсическим.
Выделяют:
Жировой гепатоз печени. Симптомы и лечение
У 30% больных жировой дистрофией печени жалоб не наблюдается. Часто у 70% больных наблюдается гепатомегалия с гладкой поверхностью. Иктеричность, увеличение селезенки обнаруживаются редко.
В биоптатах определяют до 10% жира на влажный вес биопсионного материала, гепатоциты содержат крупные жировые капли.
У 1/3 больных жировой дистрофией печени имеет место гипербилирубинемия, гиперлипидемия, снижение поглотительно-экскреторной функции, установленное на основании бромсульфалеиновой пробы, нерезкое повышение аминотрансферазной активности и гаммаглютамилтранспептидазы. Жировая дистрофия печени подтверждается данными УЗИ на основании эхосимеотики, свойственной жировому гепатозу.
Разновидностью жирового гепатоза печени при хроническом алкоголизме является синдром Циве. Кровь характеризуется выраженным нарушением липидного зеркала (гиперхолестеринемия, гипертриглицеридемия, гиперфосфолипидемия). Наблюдается гемолиз крови (как результат снижения резистентности эритроцитов на фоне дефицита витамина Е), повышение уровня билирубина.
Жировой гепатоз печени, лечение
Жировая дистрофия печени без наличия фиброза не является предцирротическим состоянием. При прекращении употребления спиртных напитков структура органа обычно восстанавливается за 4-6 недель.
При жировом гепатозе печени назначается диета с достаточным количеством белка, полиненасыщенных жирных кислот (растительные масла, рыба), препараты, содержащие силимарин (гепатопротекторы-антиоксиданты), поливитаминные драже, содержащие микроэлементы, особенно важен цинк, так как он является составляющей ферментов алкогольдегидрогеназу, супероксид-дисмутазу (антиокислительная система организма), ферментов, стимулирующих иммунную систему.
Кроме диеты для лечения жирового гепатоза печени необходимы витамины. Непременно следует назначать альфа-токоферол либо витаминными препаратами, либо увеличить потребление витамин-Е-содержащих продуктов: преимущественно нерафинированные растительные масла, желток, орехи, гречка, петрушка, проросшие семена пшеницы.
Алкогольный фиброз печени
Клинические и функциональные проявления фиброза и жирового гепатоза идентичны. Отличительной особенностью первого является повышение в крови аминокислот пролина, оксипролина, являющихся крупной составляющей коллагена.
Перивенулярный фиброз может быть остановлен отказом от алкоголя, лечением как при жировой дистрофии печени. Хронический центролобулярный склероз трансформируется в цирроз даже при полной абстиненции, однако лечение, отказ от алкоголя задерживают развитие стадии цирроза.
Алкогольный гепатит и цирроз печени
Алкогольный гепатит соответственно Международным классификациям болезней печеночного органа делят на острый и хронический. Болезнь является одним из основных вариантов, наряду с алкогольным фиброзом, трансформируется в цирроз.
Установлена зависимость недостатка антигена гистосовместимости HLA В40 с развитием хронического активного гепатита с последующим переходом в цирроз.
Эта форма гепатита (острый некроз) может развиваться на фоне жировой дистрофии печени, острых гепатитов, фиброза или цирроза. При циррозе развитие острого гепатита (некрозов) очень часто приводит к распадной (паренхиматозной) и шунтовой (портокавальной) печеночной энцефалопатии, что чаще всего заканчивается летальным исходом.
Гистологически наблюдается перивенулярное поражение гепатоцитов, баллонная дистрофия, их некроз, алкогольный гиалин (тельца Мэллори), лейкоцитарная инфильтрация, перицеллюлярный фиброз и т.д. Некроз гепатоцитов центра печеночных гексагональных долек.
Острый гепатит часто развивается у лиц молодого, среднего возраста после запоя с предшествующим длительным употреблением алкоголя. Характерно острое появление болевого, диспепсического синдромов, однако у некоторых больных заболевание может развиваться постепенно.
Наиболее частый желтушный вариант: нарастает резкая слабость, отсутствие аппетита, тошнота, рвота, желтуха, диарея, резкая потеря массы тела. Боли локализуются у правого подреберья, подложечной области. Может быть лихорадка.
При обследовании выявляется желтуха, гепатомегалия, лихорадка. Область расположения органа болезненна при пальпации, гладкая. У части больных увеличивается селезенка, появляется ладонный рубероид (эритема), кожные сосудистые звездочки, тремор рук (астериксис), что является признаком печеночной энцефалопатии, нарушение психики (заторможенность, возбуждение, галлюцинации), асцит, устойчивый к диуретикам.
Отмечаются сопутствующие инфекции: пневмония, пиелонефрит, активный туберкулез. Холестатический вариант с кожным зудом, светлым калом, темной мочой встречаются редко. Кровь характеризует выраженная гипербилирубинемия, гиперхолестеринемия, повышение активности щелочной фосфатазы, гаммаглютамилтранспептидазы, незначительное повышение AST, ALT.
Выделяют молниеносный (фульминантный) острый алкогольный гепатит, который протекает тяжело, часто с неблагоприятным прогнозом, латентный вариант с бессимптомным течением. Всегда наблюдается лейкоцитоз со сдвигом влево, резкое увеличение СОЭ.
Прогностически неблагоприятными симптомами является печеночная энцефалопатия, гепаторенальный синдром, удлинение протромбинового времени более чем на 50%, рецидивы острого гепатита на стадии сформировавшегося цирроза. Прогноз наиболее благоприятен при латентной форме острого гепатита.
Выздоровление возможно при полном отказе от алкоголя, но это не всегда гарантирует отсутствие впоследствии цирроза.
Хронический гепатит делят на персистирующий и активный легкой, средней, тяжелой степени, чаще всего представляющие собой стадии прогрессирования острого гепатита.
Хронический персистирующий гепатит гистоморфологически проявляется перицеллюлярным и субсинусоидальным фиброзом, тельцами Мэллори, баллонной дистрофией гепатоцитов. Подобная картина без прогрессирования фиброза может сохраняться 5-10 лет даже при умеренном употреблении алкоголя.
Хронический персистирующий гепатит сопровождается умеренными болями живота, вздутием, анорексией, неустойчивым стулом, отрыжкой, изжогой. Печеночный орган увеличен незначительно, уплотнен. Диффузное уплотнение, увеличение подтверждается данными УЗИ. Умеренно повышается активность гаммаглютамилтранспептидазы, трансаминаз сыворотки крови, а иногда тимоловой пробы.
Хронический активный гепатит имеет вышеописанную гистоморфологическую картину алкогольного гепатита с наличием более или менее выраженным активным фиброзом, склерозирующим гиалиновым некрозом. Воздержание от алкоголя на протяжение 3-6 мес. приводит к улучшению морфологической картины по типу хронического неалкогольного гепатита. Для хронического активного гепатита при наличии аутоиммунной деструкции паренхимы характерно прогрессирование процесса с переходом к циррозу.
Клинические проявления более яркие, чем при персистируюшем гепатите. Чаще наблюдается желтуха, спленомегалия (при переходе в цирроз орган резко может уменьшиться). Значительно повышается билирубин, гаммаглютамилтранспептидаза, иммуноглобулин А, умеренно тимоловая проба, трансаминазная активность крови.
При электронно-микроскопическом исследовании биоптатов, взятых у больных хроническим алкоголизмом, алкогольный гиалин выявляется как фибриллярный или гранулярный материал. Фибриллы гиалина короче и толще нормальных тонофиламентов. Образование телец Мэллори в гепатоцитах описано при ряде заболеваний неалкогольной этиологии: сахарном диабете, индийском детском циррозе, болезни Вильсона-Коновалова, первичном билиарном циррозе, раке печени, после операции наложения кишечного анастомоза по поводу ожирения.
Характерные ультраструктурные изменения гепатоцитов и звездчатых ретикулоэндотелиоцитов отражают токсическое воздействие этанола на организм.
Изменения гепатоцитов представлены гиперплазией, вакуолизацией элементов гладкой цитоплазматической сети, образованием гигантских митохондрий, имеющих неправильную форму. Изменения звездчатых ретикулоэпителиоцитов свидетельствуют о несостоятельности их фагоцитарной функции: цитолемма их не образует выростов, единичные лизосомы с электронно-светлым содержанием.
Постоянно встречающимися морфологическими маркерами воздействия этанола на печень являются:
Важное диагностическое значение при хронических гепатитах (алкогольных, как любой другой этиологии) имеет проведение УЗИ органов брюшной полости (печени, селезенки и других органов), а также на предмет выявления асцита и размеров воротной вены. Ультразвуковая допплерография должна выполняться для исключения или установления степени выраженности портальной гипертензии. Традиционно продолжают применять при диагностическе радионуклидную гепатоспленосцинтиграфию.
Алкогольная жировая дистрофия печени [жирная печень] (K70.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Алкогольная жировая печень (стеатоз печени), согласно общей классификации алкогольных поражений печени (Логинов А.С., Джалалов К.Д., Блок Ю.Е.), разделяется на следующие формы:
1. Без фиброза.
2. С фиброзом.
3. В сочетании с острым алкогольным гепатитом.
4. С внутрипеченочным холестазом.
5. С гиперлипемией и гемолизом (синдром Циве).
Этиология и патогенез
Патоморфология
При внешнем осмотре печень большая, желтая с жирным блеском; гепатоциты нагружены жиром, признаков воспаления или фиброза не обнаруживается. Жировая дистрофия печени диагностируется, когда содержание жира в печени превышает 10% ее влажной массы, при этом более 50% печеночных клеток содержат жировые капли, размеры которых достигают величины ядра печеночной клетки или превышают его. Жировой дистрофии часто сопутствует умеренный сидероз звездчатых ретикулоэндотелиоцитов.
Эпидемиология
Признак распространенности: Распространено
Соотношение полов(м/ж): 0.5
Возраст: преимущественно 20-60 лет.
Раса: лица белой расы имеют статистически более низкую скорость развития всех форм алкогольной болезни печени.
Пол: считается, что женщины более подвержены риску заболевания. Имеется несколько гипотез на этот счет (гормональный фон, низкое содержание алкогольдегидрогеназы в слизистой желудка, высокое содержание аутоантител к слизистой желудка у пьющих женщин), но ни одна из них не нашла подтверждения.
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Алкогольный стеатоз обычно протекает бессимптомно у амбулаторных больных.
Тщательный анамнез, особенно в отношении количества потребления алкоголя, имеет важное значение для определения роли алкоголя в этиологии ненормальных результаты тестов печени. Опрос членов семьи может выявить связанные с алкоголем проблемы в прошлом.
Американская ассоциация по изучению заболеваний печени (AASLD) в рекомендациях 2010 года акцентирует внимание на важность использования специальных опросников для выяснения анамнеза у пациентов, в отношении которых данные анамнеза, собранные обычными способами, кажутся недостоверными. Также применение опросника рекомендуется в случаях подозрительных (клинически, лабораторно, инструментально) на алкогольный стеатоз печени.
Диагностика
Критерием диагностики алкогольной жировой дистрофии печени является наличие алкогольного анамнеза и гистологическое исследование биоптата. Диагноз считается обоснованным, если не менее 50% гепатоцитов содержат крупные липидные вакуоли, оттесняющие ядро клетки к периферии цитоплазмы (см. раздел «Этиология и патогенез»). Однако на практике к биопсии прибегают довольно редко и ведущими методиками подтверждения диагноза являются методы визуализации.
1. УЗИ:
— различная эхогенность структуры паренхимы печени (при неалкологольном стеатозе, как правило, отмечаются только яркие гиперэхогенные изменения);
— для алкогольного стеатоза печени характерна сонографическая картина как очагового, так и диффузного поражения (на стадии алкогольного гепатита отмечается только диффузное поражение).
Алкогольный стеатоз печени, как и любой другой стеатоз, идентифицируется УЗИ только при наличии более 30% поражения ткани печени. Чувствительность метода около 75%.
2. Компьютерная томография, магнитно-резонансная томография являются чувствительными методами, однако не свидетельствуют в пользу именно алкогольной этиологии стеатоза.
Лабораторная диагностика
2. Возможно повышение уровня щелочной фосфатазы (около 20-40% пациентов) в диапазоне 200-300%.
3. Гипербилирубинемия (выявляется у 30-35% пациентов), связанная по-видимому с алкогольным гемолизом или сопутствующим холестазом.
Примечания
2. Изменения в определении натощак инсулина и уровня глюкозы должны насторожить врача относительно потенциального нарушения толерантности к глюкозе, которое нередко сопутствует стеатозу.
3. У большинства пациентов присутствует нерезкое снижение поглотительно-экскреторной функции печени по данным бромсульфалеиновой пробы (в настоящее время применяется редко).
Алкогольная
болезнь печени
Алкогольная болезнь печени (АБП) — это комплекс патологических изменений в печени, развитие которых вызвано хроническим употреблением алкоголя в токсических дозах.
Цирроз печени в России
АБП можно было бы назвать алкогольной жировой болезнью печени, что связано с развитием жировой дистрофии печени на первой стадии заболевания при систематическом употреблении этанола в высоких дозах. 1 Такой феномен, накопление жира в клетках печени, происходит и при неалкогольной жировой болезни печени.
Причины, факторы риска
Механизм развития АБП
Этанол в желудке и в печени окисляется до ацетальдегида, весьма реактогенного соединения, которое повреждает белки, нарушает их функции, что в свою препятствует нормальной функции клеток печени, стимулирует перекисное окисление липидов свободными радикалами.
При этом нарушается обмен жиров и отложение жировых капель в клетках печени. Токсическое действие ацетальдегида ведет также к повреждению мембран клеток и, в конечном счете, их гибели. 1
Стадии и их симптомы
Клинические проявления АБП зависят от стадии заболевания, которые перетекают из одной в другую:
При осмотре пациента с циррозом врач может обратить внимание на так называемый алкогольный габитус, или «facies alcoholica»: телеангиоэктазии, контрактура Дюпиетрена (характерно неразгибающиеся пальцы руки), атрофия мышц плечевого пояса, увеличение лимфоузлов и слюнных желез. 12 Кроме того, на данной стадии может параллельно развиваться алкогольная полинейропатия (чаще всего нарушения ощущения и движения в конечностях), воспаление поджелудочной железы (панкреатит), поражение сердца (кардиомиопатия).
Диагностика
Результаты лабораторных исследований также помогают подтвердить диагноз 8 :