Чем можно объяснить что такие белки как гемоглобин и инсулин
Чем можно объяснить что такие белки как гемоглобин и инсулин
Гемоглобин (Hb) – это сложный железосодержащий белок, который находится в эритроцитах крови и частично в плазме. Hb обеспечивает насыщение тканей организма кислородом и своевременное удаление углекислого газа из активно метаболизирующих клеток [1]. Помимо этого, исходя из своих уникальных химических свойств, гемоглобин является основным компонентом буферной системы крови, который поддерживает кислотно-щелочной баланс в организме, предотвращая алкалоз или ацидоз. Производная Hb – метгемоглобин (MetHb) – обладает пероксидазными свойствами, т.е. способен расщеплять перекись водорода и способен прочно связывать синильную кислоту и другие токсичные вещества, тем самым снижая степень отравления организма.
Цель исследования – проанализировать современные литературные данные, касающиеся функциональных особенностей Hb, и рассмотреть ситуации, которые связаны с его альтернативными и дополнительными функциями.
Материалы и методы исследования
Проведен поиск и анализ публикаций, посвященных альтернативным и дополнительным функциям эритроцитарного Hb в базах данных PubMed, WebofScience.
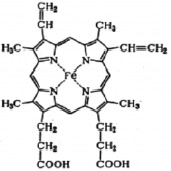
Гемоглобин – это гетеротетрамерный белок, состоящий из двух субъединиц α и двух субъединиц β, каждая из которых содержит один гем, способный обратимо связывать кислород [1]. Гем является небелковым компонентом Hb, который состоит из четырех пиррольных колец и двухвалентного железа. Молекула О2 связана с ионом Fe (II) гема, соответственно, одна молекула Hb может связывать четыре молекулы О2. Структура гема представлена на рис. 1 [2].
Рис. 1. Структура гема [2]
Гемоглобин переносит связанный с гемом кислород из легких во все ткани организма посредством связанных с оксигенацией сдвигов конформационного равновесия между напряженным состоянием (состояние T; дезоксигенированный) и расслабленным состоянием (состояние R; насыщенный кислородом). R-форма Hb обладает более высоким сродством к кислороду, чем Т-форма. Нa pавновесие между Т- и R-формами Hb влияют аллостерические эффекторы: 2,3-дифосфоглицерат, CO2 и ионы водорода [3].
В эритрoцитaх челoвекa oбнаруженo несколько фoрм Hb. Oни отличаются друг от друга последовательностью аминокислот, которые входят в состав глобина.
Выделяют физиологический (нормальный) и патологический Hb.
HbA – это «зрелый» гемоглобин, который имеется у каждого человека. При рождении его содержание составляет 80 %, а затем повышается до 95–98 %.
HBF – фетальный гемоглобин. Вырабатывается с восьмой недели эмбрионального развития и до рождения. В отличие от HbA, HBF обладает большим сродством к кислороду.
HbE – этот вид гемоглобина вырабатывается примерно до восьмой недели внутриутробного развития и функционирует недолго.
В настоящее время известно более 250 видов патологического Hb. Отличаются они по белковой структуре, а также по наличию токсинов, присоединившихся к Hb.
MetHb – метгемоглобин – содержит трехвалентный ион железа. Он формируется при действии на Hb оксидов азота и хлоратов. MetHb не способен связывать кислород, из-за этого возникает гипоксия тканей.
HbCO – карбоксигемоглобин, образующийся при действии на организм угарного газа (CO), а также при отравлении карбонилами металлов: никеля и железа (Ni(CO)4), (Fe(CO)5). HbCO постоянно находится в крови в небольшом количестве, но его концентрация может колебаться от условий и образа жизни.
HbS – гемоглобин серповидно-клеточной анемии. Серповидно-клеточная анемия – это наследственное заболевание системы крови, для которого характерно нарушение образования нормальных цепей гемоглобина. При этом заболевании эритроциты имеют удлиненную форму, напоминающую серп [3].
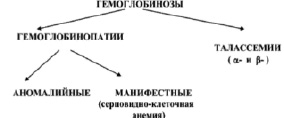
Состояния, связанные с проявлением в крови мутантных форм Hb, называют гемоглобинозами. Классификация гемоглобинозов представлена на рис. 2 [4].
Рис. 2. Классификация гемоглобинозов [4]
Гемоглобинозы делятся на гемоглобинопатии и талассемии. Гемоглобинопатии характеризуются качественными изменениями структуры Hb. Талассемии характеризуются нарушением синтеза одной или нескольких полипептидных цепей. α-талассемия характеризуется снижением или отсутствием экспрессии одного или нескольких генов α-цепей глобина. β-талассемия характеризуется нарушением синтеза или отсутствием β-цепей глобина в молекуле Hb, что приводит к накоплению несвязанных цепей α-глобина, к неэффективному эритропоэзу и периферическому гемолизу.
Реакции гемоглобина с оксидом азота и его производными. Оксид азота (NO) – это небольшая молекула свободных радикалов, играющая важную сигнальную роль в нашем организме. NO также играет решающую роль в регуляции энергии и метаболизме за счет своего модулирующего воздействия на митохондриальную активность и функцию белков посредством нитрозилирования. Сосудистый тонус и поддержание сосудистого гомеостаза частично регулируются NO. Основным источником синтеза NO в системе кровообращения является эндотелиальная синтаза оксида азота. Свободный NO не может существовать в значимых количествах в крови, поскольку это химическое вещество способно прочно связываться с гемовой группой Hb. Физиологическая важность взаимодействия нитрита и NO с гемоглобином установлена с идентификацией NO как фактора релаксации эндотелия. Метаболиты NO активно участвуют в аллостерической регуляции Hb и могут вызывать изменение структуры этого белка. Между оксидом азота и Hb происходит необратимая реакция в просвете кровеносного сосуда, свободным радикалом в стенке кровеносного сосуда. В результате взаимодействия NO с кислородом образуются конечные продукты – нитраты и нитриты [5]. Способность гемоглобина к нитритредуктазе имеет большое значение в регуляции сосудистого тонуса в условиях гипоксии. Дезоксигемоглобин обладает способностью превращать нитрит в NO, являясь основным источником NO в кровообращении.
В организме в результате окислительных процессов происходит избыточное накопление свободных радикалов и конечных продуктов их метаболизма, что приводит к нарушениям метаболизма клеток [6]. Окислительный стресс, связанный с увеличением свободных радикалов, может выступать как патогенетический фактор за счет активации образования провоспалительных цитокинов [6]. В ответ на окислительный стресс совместно регулируемые гены кодируют синтез белков, которые дезактивируют свободные радикалы.
Гемоглобиновая буферная система. Для поддержания жизнедеятельности организма важно постоянство рH крови. В этом участвуют буферные системы. Самой мощной буферной системой является гемоглобиновая. Кислую часть буфера составляет оксигенированный гемоглобин H-HbO2. Он почти в 80 раз легче отдает ионы водорода, чем восстановленный Н-Нb.
Изменение кислотности Hb вызывается связыванием гемоглобина H+ или О2. Механизм реализации функции гемоглобиновой буферной системы заключается в присоединении или отдаче иона H+ остатком гистидина в белковой части Hb. Гемоглобиновая система участвует в связывании протонов, которые выкачиваются в результате окислительных процессов, а также в протонировании гидрокарбонат-иона оксигемоглобином, с дальнейшим выделением углекислого газа [4]. Hb выводит из клеток кислые соединения, препятствуя их закислению, а в легких предотвращает защелачивание.
Связывание гемоглобина с мембраной. Обратимое связывание белков с компонентами мембраны и цитоскелета является одним из механизмов управления клеточным метаболизмом. Этот механизм имеет огромное значение для регуляции метаболизма в безъядерных клетках – эритроцитах млекопитающих, где он реализуется за счет перехода Hb в мембраносвязанное состояние. Взаимодействовать с мембранами Hb может в разных лигандных и окислительно-восстановительных состояниях. Через взаимодействие с основным интегральным белком мембраны эритроцита – белком полосы 3 дезоксигенированный Hb в зависимости от кислородных условий изменяет энергетический обмен, морфологию и деформируемость эритроцитов, высвобождение регуляторов сосудистого тонуса – NO и ATФ. Сигнальную функцию выполняют также и продукты окислительной денатурации Hb – необратимые гемихромы. Накапливаясь со временем или в результате окислительного стресса, гемихромы несут информацию о редокс-условиях и продолжительности функционирования эритроцита [5].
Методологии количественного определения гемоглобина. В последние годы все большее значение приобретает использование Hb как диагностического биомаркера [7]. Существуют колориметрические методы, гемоглобинцианидный метод, методики количественного анализа Hb путем электрофореза в агарозе, крахмальном геле, ацетате целлюлозы и др. Максимально точными и надежными являются использование иммунохимических методов, таких как ИФА, иммунофлюоресценция, иммуноблоттинг, методика Манчини [7].
Одним из важных показателей является концентрация Hb. Снижение концентрации наблюдается при анемиях. Повышение уровня Hb встречается при гемоглобинуриях [2].
Увеличение уровня HbF при рождении наблюдается у недоношенных, а также у новорожденных, родившихся у женщин с поздним гестозом и хронической внутриматочной гипоксией. Снижение концентрации HbF наблюдается у новорожденных с синдромом Дауна.
Рост продукции HbF показан при хронических гипоксиях различного генеза [8].
Метгемоглобин и карбоксигемоглобин при COVID-19. После вспышки новой коронавирусной инфекции, уделено место метгемоглобину (MetHb) и карбоксигемоглобину (COHb), поскольку у тяжелобольных пациентов часто наблюдаются повышенные концентрации данных соединений гемоглобина в крови. Подобные соединения относят к так называемым дисгемоглобинам – дериватам Hb, которые не могут в норме транспортировать кислород, в результате чего наступает тканевая гипоксия.
У пациентов после COVID-19 наблюдается пониженная концентрация Hb. В 2020 г. после проведенных исследований ученые выдвинули предположение, что инфекция взаимодействует в организме с железосодержащим белком и впоследствии разрушает его. Этот вывод был сделан на основе того, что в организмах пациентов с анемией был выявлен в большом количестве гем [8].
Синдром матового стекла, обнаруживаемый в легких на КТ – это скопление [8], атакованного вирусом и утратившего способность к переноске кислорода [8]. Ученые обнаружили, что у пациентов наблюдается низкий уровень ферритина – белка, который является «хранилищем» железа в организме. На фоне недостаточного количества ферритина развивается анемия.
Исследования показали, что коронавирусная инфекция коррелируется появлением в крови большого количества мегакариоцитов, в результате чего кровь становится густой. Эритроцитам труднее перемещаться по густой крови, в результате чего возникает гипоксия.
Ученые полагают, что причиной гибели пациентов может быть атака вируса на красный костный мозг, внутренний эндотелий и эритроциты [8].
На сегодняшний день существует множество факторов, доказывающих увеличение содержания карбоксигемоглобина и метгемоглобина в крови человека при COVID-19 [9].
Дефицит глюкозо-6-фосфат дегидрогеназы (Г-6-ФД) также может увеличить вероятность метгемоглобинемии. Недостаточность Г-6-ФД имеет серьезные патологические последствия в эритроцитах. Для лиц с дефицитом Г-6-ФД инфекция SARS-CoV-2 представляет собой дополнительный фактор риска [8]. Г-6-ФД катализирует реакцию образования восстановленного NADPH, который, в свою очередь, участвует в поддержании антиоксидантной системы защиты эритроцитов от свободных радикалов.
MetHb может образовываться как побочный продукт физиологической реакции в виде адаптивной повышенной передачи сигналов оксида азота (NO) вследствие острой анемии. Анемия может быть связана с инфекцией или системной воспалительной реакцией, называемой «анемией воспаления», как часть физиологической реакции на заболевание [9]. Согласно исследованию Bellmann-Weiler et al. [9] из 259 госпитализированных пациентов с COVID-19 24,7 % были анемичны при поступлении, причем большинство страдало воспалительной анемией (68,8 %). Во время госпитализации процент пациентов с анемией увеличился (около 68,8 % на 7-й день). Значительно более высокая смертность во время госпитализации была также обнаружена у пациентов с анемией при поступлении. Анемия связана с повышенной концентрацией NO, приводящей к вазодилатации. Она предотвращала тканевую гипоксию, но в то же время вызывала NO-основанное окисление Hb в MetHb. MetHb активирует путь NF-kB в эндотелиальных клетках, связанный с продукцией хемокинов (IL-8) и цитокинов (IL-6). Активация путей NF-kB и MAPK с последующим высвобождением хемокинов IL-8 и хемокинового моноцитарного хемоаттрактантного белка-1 (MCP-1) также наблюдалась в эндотелиальных клетках, подвергнутых воздействию MetHb [8]. Это подчеркивает, что повышение уровня MetHb в крови оказывает влияние на выработку цитокинов/хемокинов – факт, который может иметь особое значение для COVID-19, поскольку при тяжелом течении заболевания наблюдается «цитокиновый шторм». И следует иметь в виду, что гипоксия также вызывает выработку IL-8 и IL-6 [9].
Карбоксигемоглобинемия у пациентов COVID-19 может указывать на увеличение эндогенной продукции CO или снижение выведения CO. Эндогенная продукция СО обусловлена активацией гемоксигеназной ферментной системы, катализирующей распад гема и высвобождение СО в ходе реакции. Затем CO может реагировать с Hb, что приводит к образованию COHb. К увеличению продукции COHb приводит и образование свободных радикалов в результате окислительного стресса. Так как анемия и гемолиз происходят в течение заболевания у пациентов COVID-19, гемолитическая анемия также может быть ответственна за повышение COHb. Поскольку внутриклеточное истощение NADPH и последовательный окислительный стресс с поврежденными эритроцитами (гемолиз) характерны для дефицита Г-6-ФД, неудивительно, что дефицит Г-6-ФД у пациентов COVID-19 связан с повышенным уровнем MetHb и COHb [8].
При нарушении дыхания происходит снижение элиминации СО. Пациенты с COVID-19 характеризуются нарушением дыхания. Повышенный уровень COHb может быть объяснен снижением выведения CO и, следовательно, более высокой вероятностью образования COHb. Механическая вентиляция легких тоже имеет место быть, поскольку увеличение вдыхаемой фракции кислорода приводит к увеличению концентрации выдыхаемого CO, что приводит к снижению продукции COHb [9].
Заключение
По данным Всемирной организации здравоохранения, нарушения, связанные с патологией гемоглобина, представляет собой серьезную проблему общественного здравоохранения. Необходимо разрабатывать программы по скрининговым лабораторным дифференциально-диагностическим тестам, специальные биохимические, иммунологические и морфологические методы определения гемоглобина крови.
Диагностика сахарного диабета 1 и 2 типов
Сахарный диабет — это группа метаболических (обменных) заболеваний, характеризующихся гипергликемией, которая развивается вследствие абсолютного или относительного дефицита инсулина и проявляется также глюкозурией, полиурией, полидипсией, нарушениями лип
Сахарный диабет — это группа метаболических (обменных) заболеваний, характеризующихся гипергликемией, которая развивается вследствие абсолютного или относительного дефицита инсулина и проявляется также глюкозурией, полиурией, полидипсией, нарушениями липидного (гиперлипидемия, дислипидемия), белкового (диспротеинемия) и минерального (например, гипокалиемия) обменов, кроме того, провоцирует развитие осложнений. Клинические проявления болезни иногда могут быть связаны с перенесенной инфекцией, психической травмой, панкреатитом, опухолью поджелудочной железы. Нередко сахарный диабет развивается при ожирении и некоторых других эндокринных заболеваниях. Определенную роль может играть также наследственность. Сахарный диабет по медико-социальной значимости находится непосредственно после сердечных и онкологических заболеваний.
Выделяют 4 клинических типа сахарного диабета: сахарный диабет 1 типа, сахарный диабет 2 типа, другие типы (при генетических дефектах, эндокринопатиях, инфекциях, болезнях поджелудочной железы и др.) и гестационный диабет (диабет беременных). Новая классификация пока не является общепринятой и носит рекомендательный характер. Вместе с тем необходимость пересмотра старой классификации обусловлена прежде всего появлением новых данных о гетерогенности сахарного диабета, а это, в свою очередь, требует разработки особых дифференцированных подходов к диагностике и лечению заболевания. СД
1 типа — хроническое заболевание, вызванное абсолютным дефицитом инсулина, возникающим вследствие недостаточной его выработки поджелудочной железой. СД 1 типа приводит к стойкой гипергликемии и развитию осложнений. Частота выявляемости — 15:100 000 населения. Развивается преимущественно в детском и подростковом возрасте. СД
2 типа — хроническое заболевание, вызванное относительным дефицитом инсулина (снижена чувствительность рецепторов инсулинзависимых тканей к инсулину) и проявляющееся хронической гипергликемией с развитием характерных осложнений. На долю СД 2 типа приходится 80% всех случаев сахарного диабета. Частота встречаемости — 300:100 000 населения. Преобладающий возраст, как правило, старше 40 лет. Чаще диагностируется у женщин. Факторы риска — генетические и ожирение.
Скрининг на сахарный диабет
Комитет экспертов ВОЗ рекомендует проводить обследование на диабет следующих категорий граждан:
Для скрининга (как централизованного, так и децентрализованного) сахарного диабета ВОЗ рекомендует определение как уровня глюкозы, так и показателей гемоглобина А1с.
Гликозилированный гемоглобин — это гемоглобин, в котором молекула глюкозы конденсируется с β-концевым валином β-цепи молекулы гемоглобина. Гликозилированный гемоглобин имеет прямую корреляцию с уровнем глюкозы в крови и является интегрированным показателем компенсации углеводного обмена на протяжении последних предшествовавших обследованию 60–90 дней. Скорость образования HbA1c зависит от величины гипергликемии, а нормализация его уровня в крови происходит через 4–6 нед после достижения эугликемии. В связи с этим содержание HbA1c определяют в случае необходимости контроля углеводного обмена и подтверждения его компенсации у больных диабетом в течение длительного времени. По рекомендации ВОЗ (2002 г.), определение содержания гликозилированного гемоглобина в крови больных сахарным диабетом следует проводить 1 раз в квартал. Этот показатель широко используется как для скрининга населения и беременных женщин, проводящегося с целью выявления нарушений углеводного обмена, так и для контроля лечения больных сахарным диабетом.
Компания БиоХимМак предлагает оборудование и реактивы для анализа гликозилированного гемоглобина HbA1c фирм Drew Scientific(Англия) и Axis-Shield (Норвегия) — мировых лидеров, специализирующихся на клинических системах для мониторинга диабета (см. в конце данного раздела). Продукция этих компаний имеет международную стандартизацию NGSP по измерению HbA1c.
Профилактика сахарного диабета
СД 1 типа — это хроническое аутоиммунное заболевание, сопровождающееся деструкцией β-клеток островков Лангерганса, поэтому очень важен ранний и точный прогноз заболевания на предклинической (асимптоматической) стадии. Это позволит остановить клеточную деструкцию и максимально сохранить клеточную массу β-клеток.
Скрининг группы высокого риска для всех трех типов антител поможет предотвратить или снизить заболеваемость диабетом. У лиц из группы риска, имеющих антитела к двум и более антигенам, диабет развивается в течение 7–14 лет.
Для выявления лиц группы высокого риска развития сахарного диабета 1 типа необходимо провести исследование генетических, иммунологических и метаболических маркеров заболевания. При этом следует отметить, что иммунологические и гормональные показатели целесообразно исследовать в динамике — 1 раз в 6–12 мес. В случае обнаружения аутоантител к β-клетке, при нарастании их титра, снижении уровней С-пептида, необходимо до появления клинических симптомов начать проводить лечебные профилактические мероприятия.
Маркеры сахарного диабета 1 типа
HLA-типирование
Согласно современным представлениям, СД 1 типа, несмотря на острое начало, имеет длительный скрытый период. Принято выделять шесть стадий в развитии заболевания. Первая из них — стадия генетической предрасположенности характеризуется наличием или отсутствием генов, ассоциированных с сахарным диабетом 1 типа. Большое значение имеет наличие антигенов HLA, особенно II класса — DR 3, DR 4 и DQ. При этом риск развития заболевания возрастает многократно. На сегодняшний день генетическая предрасположенность к развитию сахарного диабета 1 типа рассматривается как комбинация различных аллелей нормальных генов.
Наиболее информативными генетическими маркерами сахарного диабета 1 типа являются HLA-антигены. Изучение генетических маркеров, ассоциированных с сахарным диабетом 1 типа у больных с LADA, представляется целесообразным и необходимым для проведения дифференциального диагноза между типами сахарного диабета при развитии заболевания после 30 лет. «Классические» гаплотипы, характерные для СД 1 типа, были выявлены у 37,5% больных. В то же время у 6% пациентов были обнаружены гаплотипы, считающиеся протективными. Возможно, именно этим можно объяснить более медленное прогрессирование и более мягкое клиническое течение сахарного диабета в этих случаях.
Антитела к клеткам островков Лангерганса (ICA)
Выработка специфических аутоантител к β-клеткам островков Лангерганса ведет к разрушению последних по механизму антителозависимой цитотоксичности, что, в свою очередь, влечет за собой нарушение синтеза инсулина и развитие клинических признаков СД 1 типа. Аутоиммунные механизмы разрушения клеток могут иметь наследственную природу и/или запускаться рядом внешних факторов, таких как вирусные инфекции, воздействие токсических веществ и различные формы стресса. СД 1 типа характеризуется наличием асимптоматической стадии преддиабета, которая может длиться в течение нескольких лет. Нарушение синтеза и секреции инсулина в этот период могут выявляться только с помощью теста определения толерантности к глюкозе. В большинстве случаев у этих лиц с асимптоматическим течением СД I типа выявляются аутоантитела к клеткам островков Лангерганса и/или антитела к инсулину. Описаны случаи выявления ICA за 8 и более лет до появления клинических признаков СД 1 типа. Таким образом, определение уровня ICA может использоваться для ранней диагностики и выявления предрасположенности к СД 1 типа. У пациентов с наличием ICA наблюдается прогрессивное снижение функции β-клеток, что проявляется нарушением ранней фазы секреции инсулина. При полном нарушении этой фазы секреции появляются клинические признаки СД 1 типа.
Исследования показали, что ICA определяются у 70% больных со впервые выявленным СД 1 типа — по сравнению с контрольной недиабетической популяцией, где ICA выявляются в 0,1–0,5% случаев. ICA также определяются у близких родственников больных диабетом. Эти лица составляют группу повышенного риска развития СД 1 типа. В ряде исследований было показано, что у ICA-позитивных близких родственников больных диабетом впоследствии развивается СД 1 типа. Высокая прогностическая значимость определения ICA определяется еще и тем, что у пациентов с наличием ICA, даже при отсутствии признаков диабета, в конечном счете, тоже развивается СД 1 типа. Поэтому определение ICA облегчает раннюю диагностику СД 1 типа. Было показано, что определение уровня ICA у больных с сахарным диабетом 2 типа может помочь в выявлении диабета еще до появления соответствующих клинических симптомов и определить необходимость терапии инсулином. Следовательно, у больных диабетом 2 типа при наличии ICA можно с большой вероятностью предположить развитие инсулиновой зависимости.
Антитела к инсулину
Антитела к инсулину находят у 35–40% пациентов со впервые выявленным сахарным диабетом 1 типа. Сообщалось о корреляции между появлением антител к инсулину и антител к островковым клеткам. Антитела к инсулину могут наблюдаться в стадии преддиабета и симптоматических явлений сахарного диабета 1 типа. Антиинсулиновые антитела в ряде случаев также появляются у пациентов после лечения инсулином.
Декарбоксилаза глутаминовой кислоты (GAD)
Исследования последних лет позволили выявить основной антиген, представляющий собой главную мишень для аутоантител, связанных с развитием инсулинзависимого диабета, — декарбоксилаза глутаминовой кислоты. Это мембранный фермент, осуществляющий биосинтез тормозного нейромедиатора центральной нервной системы млекопитающих — гамма-аминомасляной кислоты, был впервые найден у пациентов с генерализованными неврологическими расстройствами. Антитела к GAD — это очень информативный маркер для идентификации преддиабета, а также выявления индивидуумов с высоким риском развития СД 1 типа. В период асимптоматического развития диабета антитела к GAD могут выявляться у пациента за 7 лет до клинического проявления болезни.
По данным зарубежных авторов, частота обнаружения аутоантител у больных с «классическим» сахарным диабетом 1 типа составляет: ICA — 60–90%, IAA — 16–69%, GAD — 22–81%. В последние годы опубликованы работы, авторы которых показали, что у больных с LADA аутоантитела к GAD являются наиболее информативными. Однако, по данным ЭНЦ РФ, лишь у 53% больных с LADA были выявлены антитела к GAD, по сравнению с 70% ICA. Одно не противоречит другому и может служить подтверждением необходимости определения всех трех иммунологических маркеров для достижения более высокого уровня информативности. Определение этих маркеров позволяет в 97% случаев дифференцировать СД 1 типа от 2 типа, когда клиника сахарного диабета 1 типа маскируется под 2 тип.
Клиническая ценность серологических маркеров СД 1 типа
Наиболее информативным и надежным представляется одновременное исследование в крови 2–3 маркеров (отсутствие всех маркеров — 0%, один маркер — 20%, два маркера — 44%, три маркера — 95%).
Определение антител против клеточных компонентов β-клеток островков Лангерганса, против декарбоксилазы глутаминовой кислоты и инсулина в периферической крови важно для выявления в популяции лиц, предрасположенных к развитию заболевания, и родственников больных диабетом, имеющих генетическую предрасположенность к СД 1 типа. Недавнее международное исследование подтвердило огромную важность этого теста для диагностики аутоиммунного процесса, направленного против островковых клеток.
Диагностика и мониторинг сахарного диабета
Для постановки диагноза и мониторинга сахарного диабета используются следующие лабораторные исследования (по рекомендациям ВОЗ от 2002 г.).
Длительное время как для выявления СД, так и для контроля степени его компенсации рекомендовалось определение содержания глюкозы в крови натощак и перед каждым приемом пищи. Исследования последних лет позволили установить, что более четкая ассоциация между уровнем глюкозы в крови, наличием сосудистых осложнений диабета и степенью их прогрессирования, выявляется не с показателями гликемии натощак, а со степенью ее увеличения в период после приема пищи — постпрандиальная гипергликемия.
Необходимо подчеркнуть, что критерии компенсации сахарного диабета претерпели существенное изменение на протяжении последних лет, что можно проследить на основании данных, представленных в таблице.
Таким образом, критерии диагностики СД и его компенсации, в соответствии с последними рекомендациями ВОЗ (2002 г.), необходимо «ужесточить». Это обусловлено исследованиями последних лет (DCCT, 1993; UKPDS, 1998), которые показали, что частота, время развития поздних сосудистых осложнений СД и скорость их прогрессирования имеют прямую корреляцию со степенью компенсации СД.
Инсулин
Инсулин — гормон, вырабатываемый β-клетками островков Лангерганса поджелудочной железы и участвующий в регуляции метаболизма углеводов и поддержании постоянного уровня глюкозы в крови. Инсулин первоначально синтезируется как препрогормон с молекулярной массой 12 кDa, затем внутри клетки подвергается процессингу с образованием прогормона с молекулярной массой 9 кDa и длиною в 86 аминокислотных остатка. Этот прогормон депонируется в гранулах. Внутри этих гранул дисульфидные связи между цепями А и В инсулина и С-пептидом разрываются, и в результате образуется молекула инсулина с молекулярной массой 6 кDa и длиной в 51 аминокислотный остаток. При стимуляции из клеток освобождаются эквимолярные количества инсулина и С-пептида и небольшое количество проинсулина, а также других промежуточных веществ (
Е. Е. Петряйкина, кандидат медицинских наук
Н. С. Рытикова, кандидат биологических наук
Морозовская детская городская клиническая больница, Москва