Что образуется в красном костном мозге
Не костный и не мозг
Спинномозговая пункция, 70 тысяч евро за донорство и другие фантазии о костном мозге
Первой в мире успешной трансплантации костного мозга на днях исполнится 50 лет, но в этой сфере по-прежнему живут удивительные заблуждения. Причем даже среди тех, кто связан с темой по долгу службы. Мы решили собрать главные ошибки и рассказать, как все устроено на самом деле.
Фантазия №1. Костный мозг – это мозг. Спинной или даже головной
«Донор костного мозга, это как? Череп вскрывают, что ли?» (из вопросов медицинскому директору Национального регистра доноров костного мозга имени Васи Перевощикова Ольге Макаренко перед донорской акцией в городе Каменске-Уральском, 15.09.2018, vk.com).
На самом деле. В костном мозге нет нервных клеток, костный мозг – вообще не мозг. Это главный кроветворный орган человека. Он находится внутри тазовых костей, ребер, грудины, костей черепа, в эпифизах (расширенных концах) длинных трубчатых костей и представляет собой мягкую, пронизанную сосудами массу ярко-красного цвета с большим количеством гемопоэтических стволовых клеток. Это «клетки-заготовки», которые пока не определились со своим будущим и могут превращаться в клетки разных типов. В костном мозге из стволовых клеток образуются клетки крови – лейкоциты, эритроциты и тромбоциты, которые затем попадают в кровеносную систему через капилляры. На костный мозг приходится примерно 5% веса человека.
Фантазия №2. Костный мозг достают большим шприцем из позвоночника или других костей
«Сара: Тете Косиме нужно кое-что. Это называется костный мозг. Его возьмут из твоего бедра. И им придется использовать большой шприц.
Кира: Я не люблю шприцы.
Сара: Я знаю. Но ты заснешь. И ничего не почувствуешь.
Кира: Тетя Косима умрет, если я этого не сделаю?
Сара: Ей очень нехорошо. Поэтому, скорее всего, да.
Кира: Ну тогда… я согласна»
(из сериала «Темное дитя», 2-й сезон, 9-я серия).
На самом деле. Для пересадки костного мозга нужен не костный мозг как таковой, а гемопоэтические (кроветворные) стволовые клетки. Их можно получать не только из костей, но и из крови, и чаще используется как раз второй способ. Донору дают специальные препараты, которые выгоняют гемопоэтические стволовые клетки из костного мозга в кровь. Процедура их забора устроена так: кровь берут из вены на одной руке, выделяют из нее гемопоэтические стволовые клетки и возвращают обратно через вену на другой руке. Процедура длится несколько часов, наркоз не требуется. А первый способ предполагает общую анестезию: из тазовых костей с помощью нескольких пункций берут до 5% костного мозга донора – это примерно литр смеси костного мозга и крови. Как правило, способ выбирает сам донор.
Фантазия №3. Донора костного мозга подбирают по группе крови
«Мне 42, группа крови 2+ Срочно буду донором костного мозга, недорого» (объявление на сайте deskmed.ru).
На самом деле. Совместимость костного мозга двух неродственников – большая редкость, в среднем – 1 на 10 тыс. Ткани донора и реципиента должны быть как можно более (в идеале – полностью) совместимы, иначе на чужеродный белок в организме может возникнуть иммунная реакция. Требования к совместимости тканей различны. В случае костного мозга сложность в том, что может возникнуть не только иммунная реакция реципиента на донорский костный мозг, но и обратная реакция – «трансплантат против хозяина». Пересаженный костный мозг может воспринять организм реципиента как чужеродный и начать с ним бороться. А вот группа крови у людей с тканевой совместимостью может быть разная.
Лучшие доноры костного мозга – родные братья и сестры. Для них вероятность совместимости – 25%. Во всех остальных случаях доноров подбирают по регистрам – гигантским базам данных о потенциальных донорах. Это люди, которые выразили готовность стать донорами костного мозга и прошли так называемое типирование – сдали кровь для определения своей тканевой совместимости.
Фантазия №4. Участник регистра обычно становится донором, иногда даже несколько раз
«Сегодня еще нет понятия «Почетный донор» для доноров костного мозга. Мы готовим объективное обоснование, что нужно принять такое решение и, конечно, повышать сумму компенсации подоходного налога» (глава ФМБА Владимир Уйба, из интервью «Известиям», 8 июня 2017 года).
На самом деле. Звание почетного донора ассоциируется с многократным донорством. Но даже однократное донорство костного мозга – удел немногих участников регистра. По статистике ВОЗ, ежегодно в мире проводится более 50 тыс. трансплантаций костного мозга, при этом в части операций используются доноры-родственники. Международный регистр насчитывает примерно 30 млн человек. Так что шанс участника регистра в течение года стать реальным донором – менее 1/600. В России донором стал каждый 300-й участник регистра. Бывают случаи, что подходящий реципиент наконец найден, но участник регистра вступил в него так давно, что уже забыл о своем решении и не готов к донорству.
Фантазия №5. На своем костном мозге можно неплохо заработать
На самом деле. Если речь не идет о родственной трансплантации, донора можно найти только через регистры. Ни один из существующих регистров не предусматривает вознаграждения донорам. Получение подходящего костного мозга в европейских базах, от поиска до доставки, обходится примерно в €18 тыс., в российской – примерно втрое дешевле. Но это медицинские и логистические расходы, донор не получает из этих денег ни копейки.
Корреспондент Русфонда позвонил по телефону, указанному в приведенном выше объявлении, и предложил продать свой костный мозг. Оператор спросил про группу крови (см. фантазию №3), сообщил, что она «очень хорошая» и вполне подходит, после чего предложил приехать на Сухаревскую площадь, 3 (это адрес НИИ имени Склифосовского) для сдачи анализов с последующим донорством костного мозга и получением денег. После вопроса о вероятности гистосовместимости оператор вежливо сообщил, что не будет продолжать разговор. Обычно с «донора» просто пытаются получить деньги за предварительные анализы, и на этом история заканчивается.
Фантазия №6. В России нет регистра костного мозга, потому что еще не приняли закон о нем
«Сейчас учет доноров и реципиентов осуществляется пятью медицинскими организациями с разными подходами. Есть все основания Минздраву России проанализировать сведения, включенные в данные регистры, и создать единую базу. Но хочу подчеркнуть, что создание такой базы невозможно без внесения изменений в действующую статью 147 ФЗ» (Татьяна Голикова, вице-премьер, на заседании Совета при правительстве РФ по вопросам попечительства в социальной сфере, 14 сентября 2018 года).
На самом деле. Отдельные регистры костного мозга создаются в России с конца 1970-х годов. Сейчас существует полтора десятка таких региональных регистров. В 2013 году Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова и Русфонд заключили договор о сотрудничестве для создания единого регистра доноров костного мозга. Он был создан в подведомственном университету НИИ детской онкологии, гематологии и трансплантологии имени Р.М. Горбачевой. Было разработано программное обеспечение для объединения баз данных. В следующие несколько лет в базу вошли уже существовавшие в России регистры. Сейчас в ней больше 85 тыс. потенциальных доноров. В 2015 году регистр был назван именем Васи Перевощикова – мальчика, которому так и не успели найти донора. Сейчас Русфонд работает над регистром без участия НИИ Горбачевой. В 2017 году Минюст зарегистрировал Национальный регистр доноров костного мозга имени Васи Перевощикова (БФ «РДКМ», регистрационный номер 1177700013853).
В начале сентября в Казани заработала новая NGS-лаборатория, специализирующаяся на первичном типировании добровольцев. Ее мощность – 25 тыс. доноров в год (для сравнения: в 2017 году страна протипировала всего 15 тыс. добровольцев). На типирование одного потенциального донора российские регистры тратят сейчас минимум 14 тыс. руб., Русфонд снизил стоимость реагентов в казанской лаборатории до 7 тыс. руб. Активацию донора из Национального регистра (подтверждение совместимости, полное обследование, подготовку к донации, командировку, страховку и забор костного мозга) будет оплачивать Русфонд.
Население России генетически очень разнообразно, у нас очень много малых народов (например, на Северном Кавказе), много смешанных браков. Для многих жителей России найти донора в международном регистре просто невозможно, потому стране так необходим Нацрегистр.
Фантазия №7. В России с трансплантацией костного мозга все неплохо
«Мы сделали существенный скачок в объемах и в качествах пересадки костного мозга. Только у детей мы сделали за прошлый год 500, а всего 1,5 тыс. операций. Если считать расчетно, сколько нам всего нужно, – нам нужно еще плюс 40%, примерно так. На данный момент в РФ имеются все необходимые механизмы и мощности для того, чтобы это сделать, несмотря на высокую стоимость таких операций Сейчас мы все равно всем делаем, но просто люди ждут» (Вероника Скворцова, министр здравоохранения РФ, 16 июля 2018 года).
На самом деле. Рассчитать потребности в трансплантации костного мозга пока не представляется реальным: оценки специалистов могут различаться на порядок. По данным NCBI (National Center for Biological Information), в США ежегодно производятся примерно 20 тыс. трансплантаций костного мозга. Если экстраполировать эти данные на Россию, получится, что у нас должны ежегодно производиться примерно 9 тыс. пересадок.
Фантазия №8. Регистр должно создавать государство, а управлять им может только врач
«В Германии, на которую обычно ссылаются как на образец, учредители регистров – это государство в лице федеральной или местной власти, а во главе стоят известные медики. Потому что логистика донорства знакома только им. Регистры доноров должны существовать только совместно с трансплантационными центрами» (Борис Афанасьев, директор НИИ Детской гематологии, онкологии и трансплантологии имени Р.М. Горбачевой, из интервью Русфонду, сентябрь 2018 года).
На самом деле. Крупнейший в Германии Немецкий регистр доноров костного мозга (DKMS) основан в 1991 году Петером Харфом после смерти его жены от лейкемии. Петер Харф – экономист по образованию, параллельно с работой над регистром он руководил косметической компанией Coty. Его дочь Катарина, тоже работавшая в сфере бизнеса, – создательница американского отделения фонда. Сейчас в DKMS больше 8 млн потенциальных доноров. Национальный регистр Германии, объединяющий данные всех донорских центров, создан Красным Крестом земли Баден-Вюртемберг – это общественная организация.
Старейший в Германии Регистр Штефана Морша (названный именем юноши, который болел раком крови, ему сделали трансплантацию, но он умер после операции) создали в 1986 году родители Штефана – Эмиль и Хилтруд. Эмиль до сих пор возглавляет эту организацию, а оперативным управлением в фонде занимается сестра Штефана Сюзанна.
Фантазия №9. Регистры доноров всегда развиваются очень медленно
«В какие сроки вы планируете создать регистр? – Наш единственный план – работать в этом направлении. Но сказать, что это будет через два или три года, мы пока не можем. Зарубежные страны шли к своим регистрам десятки лет. Мы начали эту работу всего пять лет назад» (глава ФМБА Владимир Уйба, из интервью «Известиям» 8 июня 2017 года).
На самом деле. По мировым масштабам наполнение регистров костного мозга пока идет в России чрезвычайно медленно. Например, немецкий DKMS за первый год своего существования сумел привлечь 68 тыс. потенциальных доноров. Сейчас DKMS работает на территории нескольких стран, но в те годы он ограничивался Германией.
Донорство костного мозга не имеет границ: в прошлом году больше 300 трансплантаций было произведено в России с использованием зарубежного донорского материала. Логика всемирного сотрудничества в этой сфере предполагает, что страны не только пользуются международной базой, но и способствуют ее пополнению.
Фото: Justyna Miszkiewicz/Welcomeimages
Происхождение стволовых кроветворных клеток в эмбриональном развитии
В организме взрослых млекопитающих кроветворение происходит главным образом в костном мозге. На протяжении всей жизни в нем поддерживаются стволовые кроветворные клетки (СКК), образующие все типы форменных элементов крови. В эмбриональном развитии кроветворение происходит в нескольких анатомических образованиях – желточном мешке, аорто-гонадо-мезонефральной области, плаценте и печени. Однако до сих пор не вполне ясно, где именно в ходе развития эмбриона впервые появляются клетки-предшественники, дающие начало СКК зрелого костного мозга. В обзоре рассмотрены современные представления об особенностях кроветворных клеток, образующихся в желточном мешке, аорто-гонадо-мезонефральной области и плаценте, и их вкладе в заселение печени зародыша, а впоследствии и костного мозга взрослого организма.
Костный мозг – основной орган кроветворения у взрослых млекопитающих, в котором на протяжении всей жизни воспроизводятся стволовые кроветворные клетки (СКК) и образуются зрелые клетки крови. СКК взрослого организма способны давать все типы форменных элементов крови (нейтрофилы, базофилы, эозинофилы, моноциты, лимфоциты, эритроциты, тромбоциты). Кроме того, после деления СКК воспроизводят самих себя, т.е. самоподдерживаются. Благодаря этому они обеспечивают кроветворение неопределенно долгое время. Основным функциональным критерием наличия в ткани СКК является способность к восстановлению кроветворения как после естественной гибели клеток, так и в ходе патологических процессов или действия повреждающих агентов. Полный набор этих свойств появляется у СКК только после рождения, в результате созревания их предшественников, так называемых пре-стволовых кроветворных клеток (пре-СКК), которые возникают в раннем развитии задолго до формирования костного мозга. Хотя процесс образования кроветворной системы изучается более 100 лет, остается не ясным вопрос, где впервые возникают клетки, дающие начало СКК, существующим во взрослом организме.
В печени зародыша собственные предшественники кроветворных клеток не образуются. Кроветворение в ней начинается и поддерживается только за счет миграции клеток, приходящих из желточного мешка, АГМ и плаценты. В печени СКК не только самоподдерживаются и размножаются, но и впервые в эмбриогенезе образуют все типы кроветворных клеток красного и белого рядов. Таким образом, печень является основным кроветворным органом развивающегося плода и обеспечивает его потребность как в стволовых, так и в зрелых клетках крови, что становится особенно важным на тех стадиях развития, когда желточный мешок уже прекращает выполнять кроветворную функцию. В конце внутриутробного периода печень переключается на выполнение специфических функций, свойственных ей во взрослой жизни, а кроветворная активность ней угасает. СКК при этом покидают печень и перемещаются в костный мозг, где к тому моменту уже складываются условия для их существования и самообновления. Попав в костный мозг, СКК прекращают интенсивно делиться и переходят в состояние покоя.
Ведущая роль в смене мест, где в ходе индивидуального развития происходит кроветворение, принадлежит микроокружению. В желточном мешке, АГМ, плаценте и печени оно неодинаково, и это обуславливает различия в поведении кроветворных клеток в этих органах. Так, под влиянием микроокружения плаценты СКК активно размножаются, а микроокружение печени благоприятствует не только их делению, но и дифференцировке. Ключевую роль в формировании микроокружения, или ниши для СКК, играют мезенхимные стромальные клетки (МСК). В ходе развития эмбриона МСК появляются в местах кроветворной активности, по-видимому, подготавливая «ложе» для кроветворных клеток, причем обе системы – мезенхимная и кроветворная – развиваются скоординировано. В индивидуальном развитии МСК претерпевают не только количественные, но и функциональные изменения, что отражает процесс созревания кроветворной ниши. Именно качественные изменения качества кроветворного микроокружения, происходящее параллельно с изменениями СКК, могут иметь определяющее влияние на приобретение последними дефинитивных свойств, присущих клеткам взрослого организма.
Таким образом, эмбриональное кроветворение осуществляется во многих анатомических образованиях, обеспечивающих на протяжении пренатального периода разные этапы формирования и созревания кроветворных клеток. Кроветворные функции этих образований частично перекрываются, но каждое из них имеет и уникальные особенности: желточный мешок служит первым местом продукции функционально активных клеток крови (примитивных эритроцитов), в АГМ закладываются de novo предшественники дефинитивных СКК, плацента обеспечивает размножение СКК, а печень – их поддержание и дифференцировку в множественных направлениях. Существование нескольких мест для кроветворения способствует, с одной стороны, быстрому образованию первых дифференцированных клеток крови, необходимых эмбриону для выживания и роста, а с другой – продукции множества СКК, которые потребуется организму в дальнейшем, уже после рождения. Однажды возникнув, СКК собираются в печени зародыша для размножения и дифференцировки, после чего заселяют костный мозг. На этом пути они попадают в различные ниши и подвергаются различным воздействиям, способствующим их размножению и функциональному созреванию, в результате чего приобретают свойства СКК взрослого организма.
Хотя эмбриональное развитие кроветворной системы изучается уже много лет, многие вопросы, связанные с происхождением клеток крови в эмбриогенезе, до сих пор остаются без ответа. Дальнейшее изучение клеточных и молекулярных механизмов формирования СКК в индивидуальном развитии имеет несомненную значимость не только для понимания фундаментальных аспектов функционирования кроветворной системы, но и для совершенствования методов лечения гематологических заболеваний.
«. Сообразно с моими силами и моим разумением» — донорство костного мозга — вклад в здоровое будущее
«. Сообразно с моими силами и моим разумением» — донорство костного мозга — вклад в здоровое будущее
Авторы
Редакторы
Статья на конкурс «Био/Мол/Текст»: Представленная статья посвящена трансплантации костного мозга. В результате проведенного опроса (около 150 респондентов) мы выявили среднюю осведомленность по данному вопросу и решили осветить тонкости процесса, разобрать биологические механизмы, лежащие в его основе, и продемонстрировать некоторые современные тенденции.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Что собой представляет костный мозг?
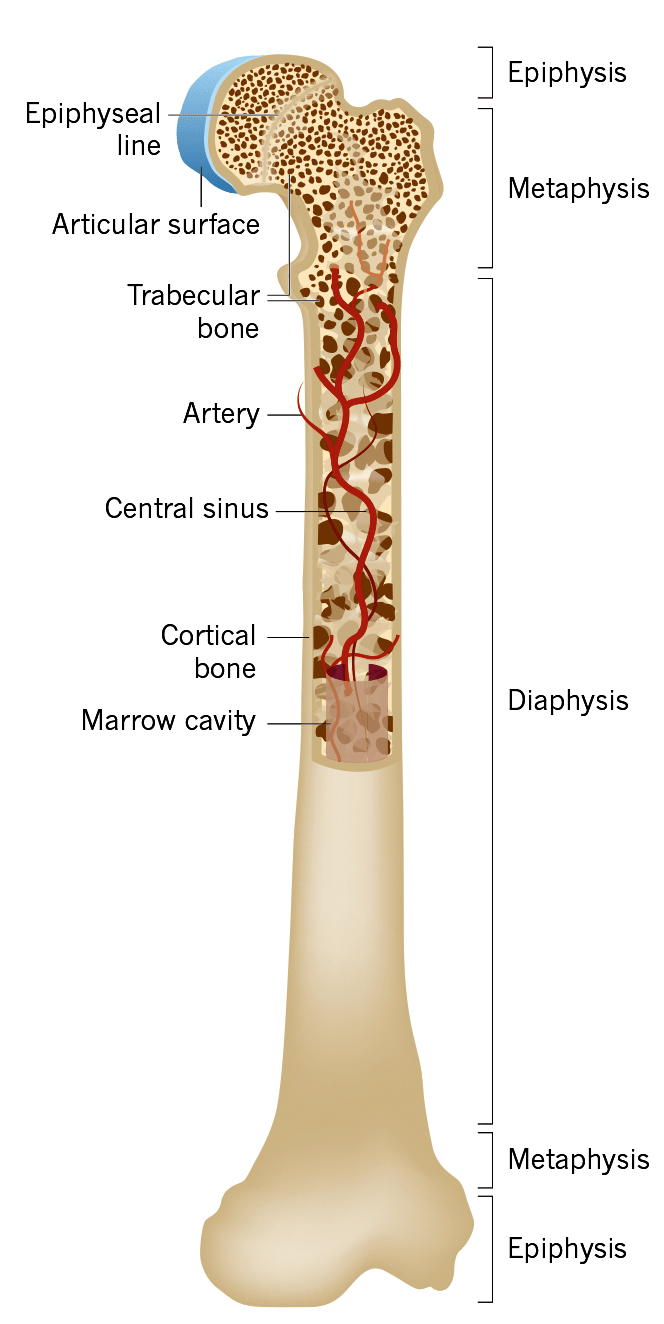
Рисунок 1. Общая анатомия кости
Сочетание слов «костный» и «мозг» может сбивать с толку и навевать стереотипные образы. Под мозгом мы привыкли представлять «рыхлую массу» в форме грецкого ореха, располагающуюся в голове. Костный мозг интуитивно можем путать со спинным, ошибочно предполагая, что он располагается в позвоночном столбе.
На самом же деле, костный мозг (КМ) — это гемо- и лимфопоэтический орган, располагающийся в полостях губчатой части и костномозговых каналах костей (рис. 1).
Выделяют две разновидности КМ — красный, цвет которого обусловлен обилием крови и гемопоэтичеких клеток, и желтый, окраска которого связана с наличием большого количества жировых клеток (адипоцитов), замещающих большинство кроветворных клеток [1].
Первоначально у человека имеется только красная разновидность, которая по мере взросления частично переходит в желтую.
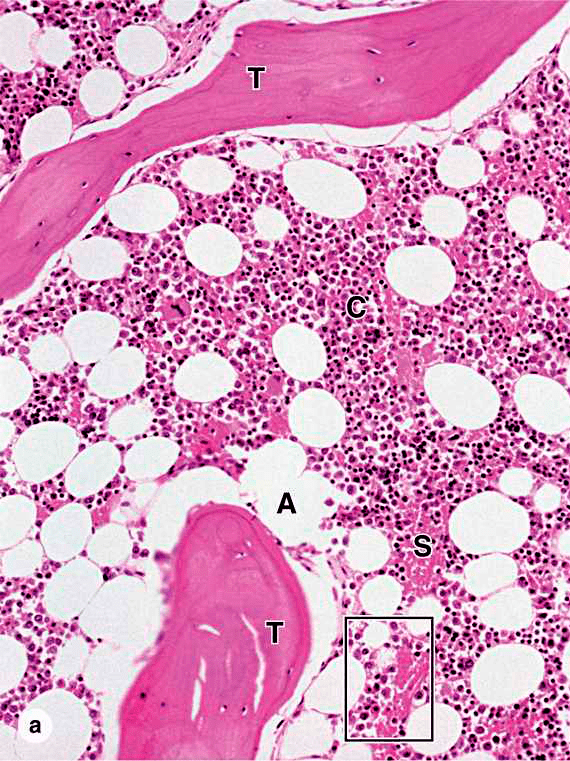
Красный костный мозг (рис. 2) состоит из ретикулярной стромы соединительной ткани, кровяных тяжей или островков клеток и синусоидальных капилляров. Строма представлена фибробластическими (стромальными = ретикулярными = адвентициальными) клетками, макрофагами и тонкими ретикулярными волокнами, состоящими из коллагена I типа, протеогликанов, фибронектинов и ламинина. Желтый костный мозг представляет собой подобную структуру, отличающуюся большим числом адипоцитов и меньшим количеством сосудов, гемопоэтических клеток [2].
Рисунок 2. Гистологический срез красного костного мозга. Т — трабекулы губчатой кости; А — адипоциты; S — синусоиды, заполненные кровью; C — кроветворные тяжи.
Какие функции выполняет кровеносная система?
Стабильное кровообращение необходимо каждому организму. Кровь выполняет множество разнообразных функций:
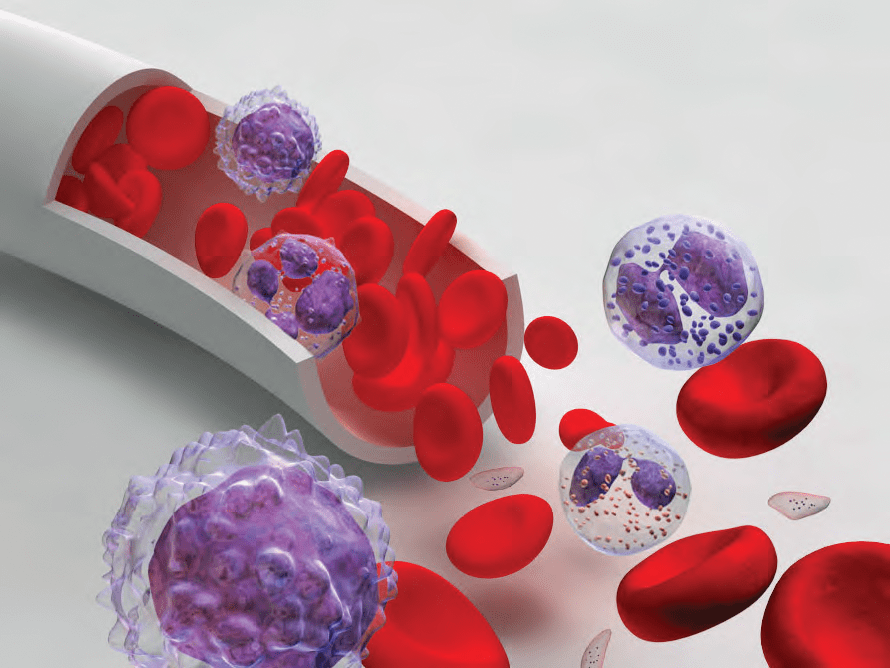
Столь большое разнообразие функций кровь может выполнять благодаря необычности своего гистологического строения: (1) форменные элементы (эритроциты, лейкоциты и тромбоциты) и (2) плазма (рис. 3). Источником форменных элементов является костный мозг. Бóльшая часть пула клеток формируется красным костным мозгом, остальная — желтым. [4].
Рисунок 3. Схема кровеносного сосуда с форменными элементами
Почему люди нуждаются в костном мозге?
Костный мозг является одним из центральных органов как кровеносной, так и иммунной систем [5]. Как отмечалось ранее, в нем находятся гемопоэтических стволовые клетки, способные дифференцироваться в различные клетки крови, например, в эритроциты, макрофаги или Т-лимфоциты.
Возникновение патологий этого органа приводит к снижению эффективности его деятельности, что ведет к ухудшению работоспособности иммунной и кровеносной систем. Организм человека становится более уязвимым. Возникает потребность в трансплантации донорского материала.
Нарушение целостности костного мозга может, произойти, например, при лечении онкозаболеваний. Вследствие применения химио- и лучевой терапии уничтожаются раковые, но вместе с ними и другие активно делящиеся клетки организма, в том числе, компоненты костного мозга. Организм теряет возможность производить форменные элементы крови.
Без трансплантации костного мозга подобное лечение нередко может принести больше вреда, нежели пользы, поскольку в итоге приводит к серьезным нарушениям в работе всего организма. В трансплантации нуждаются люди, больные лейкозом, апластической анемией, злокачественными лимфомами, аутоиммунными заболеваниями и пр.
Информированность о трансплантации костного мозга
Мы провели опрос группы потенциальных доноров (141 человека) из разных городов России (Санкт-Петербург, Москва, Орел, Казань и др.). Опросник состоял из 17 вопросов, 7 из которых были построены по методу семантического потенциала Ч. Осгуда.
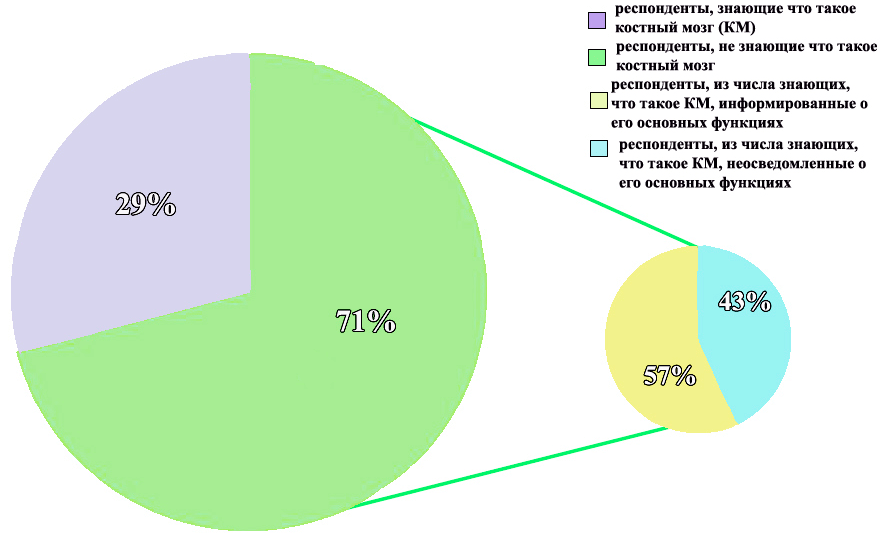
В результате проведения опроса была установлена средняя осведомленность граждан по вопросу устройства костного мозга и его функций: более половины опрошенных (71%, то есть 100 человек) дали верное определение костному мозгу, из них наиболее полно и верно перечислили его функции 43% респондентов (рис. 4).
Рисунок 4. Диаграмма анализа информированности о костном мозге и его функциях
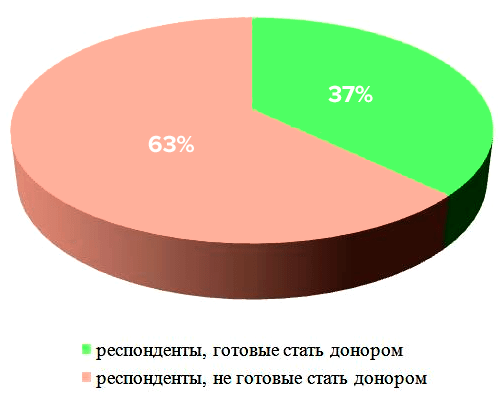
Большинство опрошенных (95,3%) знают о наличии донорства костного мозга в разной степени (от информированности о самом факте подобной операции, до сведений о многих деталях процесса). Люди осведомлены о проблеме благодаря СМИ (43,4% опрошенных), социальным сетям (50,4%) и близкому кругу (друзьям, родственникам) — 24%. Меньше половины респондентов задумывалось о том, что, став донором, смогли бы спасти жизнь (48,3%). Больше половины опрошенных (62,4%) (рис. 5) не стали бы совершать донацию костного мозга и не знают о наличии регистра доноров (65,4%). Респонденты в большинстве случаев не согласились бы сдавать костный мозг в связи со страхом получить болевые ощущения (47%) и необратимые травматичные изменения собственного здоровья (56,7%).
Рисунок 5. Диаграмма анализа количества потенциальных доноров костного мозга
Трансплантация
Трансплантация КМ состоит из четырех этапов:
Трансплантация гемопоэтических клеток костного мозга бывает двух видов: аутологичная и аллогенная.
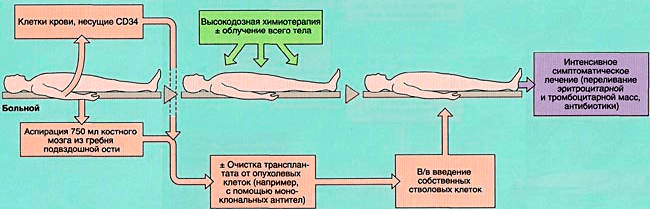
При аутологичной пересадке (рис. 6а) используются собственные стволовые клетки пациента. До жесткой химиотерапии отбираются и замораживаются клетки костного мозга. Далее, после проведения процедуры, они вводятся обратно в организм.
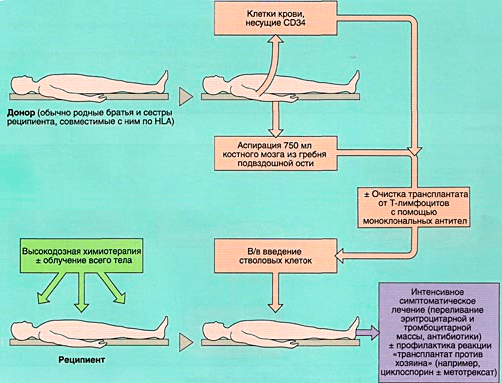
Аллогенная трансплантация (рис. 6б) представляет собой пересадку гемопоэтической ткани от здорового подходящего донора. Выделяют три вида подобной трансплантации (в зависимости от источника материала): совместимого родственного, совместимого неродственного и не полностью совместимого родственного происхождения.
Рисунок 6а. Схема аутологичной трансплантации костного мозга
Рисунок 6б. Схема аллогенной трансплантации костного мозга
Выделение нескольких типов обусловлено различием главного комплекса гистосовместимости (МНС) у разных людей и разной вероятностью возникновения осложнений при трансплантации.
Прежде чем обсудить непосредственно аллогенную трансплантацию, разберемся в том, что же такое МНС, откуда он берется и зачем нужен.
Главный комплекс гистосовместимости (МНС) — это несколько групп генов, кодирующих специфический мембранный белок — лейкоцитарный антиген человека (HLA), который осуществляет презентацию антигенов. Благодаря этому процессу происходит распознавание чужеродных антигенов и формирование адаптивного иммунного ответа. Основа последнего заключается в активации В-лимфоцитов, ответственных за формирование антител, и Т-лимфоцитов с макрофагами, обеспечивающих клеточный иммунитет (физическое удаление инородного агента). Поскольку комплекс гистосовместимости является тонкой структурой и направлен на защиту собственного организма, то у разных людей данный фактор может быть различен, следовательно, при смешивании биологических тканей, будь то кровь или костный мозг, есть шанс возникновения реакции «трансплантат против хозяина» (РТПХ). Проявление такой реакции может привести к полному неприживлению материала (иммунный ответ реципиента на клетки донора). Во избежание возникновения РТПХ до пересадки у донора и рецепиента определяют степень гистосовместимости путем HLA-типирования. По тому, насколько высока совместимость, и выделяют типы аллогенной трансплантации:
Как происходит процедура типирования и донации стволовых клеток?
Для типирования и определения HLA-генотипа у потенциального донора берут образец крови до 10 мл [9]. Проводят лабораторные исследования и вносят полученную информацию в общероссийскую базу — Национальный регистр доноров.
Если потенциальный донор подходит больному, начинается процесс изъятия стволовых клеток. Его возможно осуществить двумя путями: шприцом из тазовой кости, или с помощью препаратов, которые способствуют выходу недифференцированных стволовых клеток в кровь. В первом случае, донора госпитализируют в больницу и под общим наркозом производят забор. В тазовой кости делают несколько маленьких разрезов, через которые специальными иглами извлекают около литра жидкого костного мозга (такой объем составляет не более 5% от общего количества и компенсируется организмом в течение двух недель).
Побочные эффекты для донора при данном способе забора могут быть следующими: болевые ощущения в тазовых костях, снижение уровня гемоглобина, тошнота, сонливость, слабость (последствия наркоза).
Во втором случае донор проходит подготовительный период (около пяти дней). В течение этого времени человеку подкожно вводится препарат (рекомбинантные факторы роста = гранулоцит-колониестимулирующий фактор = гранулоцит-макрофаг-колониестимулирующий фактор) для стимуляции пролиферации и мобилизации стволовых клеток. На пятый день донору проводят процедуру афереза (получение отдельных компонентов костного мозга путем центрифугирования) длительностью 3–5 часов. Кровь забирается из вены, проходит клеточный сепаратор (установку с несколькими камерами и системой подвода/вывода жидкости и клеточной культуры, предназначенную для разделения пула на группы по размеру, удельному весу и другим характеристикам) и возвращается донору. После прохождения через аппарат, из крови выделяют небольшое количество стволовых клеток. Процедура повторяется несколько раз для отбора необходимого количества материала. Суммарно через аппарат может проходить до 15 литров крови, из которых в сепараторе остается до 200 мл (остальное отправляется обратно донору).
Побочные эффекты для донора могут быть различны: ломота в костях, связанная с активным делением клеток костного мозга; обострение аутоиммунных заболеваний (например, артрита, красной волчанки).
Риски, связанные с серьезными последствиями для организма донора в обоих случая минимален, однако при применении перфузионного катетера есть шанс возникновения кровотечения, появления абсцесса или иной местной инфекции [6]. Как правило, спустя 2–3 недели все неприятные ощущения и последствия донации проходят.
В мировой практике существует регламент, по которому донор и реципиент не должны знать друг о друге. Максимум предоставляемой информации — возраст и пол. Знакомство может произойти лишь спустя два года после трансплантации. Донорам также не сообщают: помог ли их костный мозг вылечить больного. Это не тайна, а вынужденная анонимность. Регламент соблюдается в целях предосторожности и в силу психологических и этических причин.
История от реального донора костного мозга
«Я заключила некую сделку с небесами», — говорит Алла Багирянц, которая стала реальным донором костного мозга. В 2015 году маме девушки поставили диагноз: множественная миелома (рак плазматических клеток крови). Это подвигло девушку изучить данную тему. Так она узнала, что при этом типе заболеваний может понадобиться пересадка костного мозга. Лечение миеломы проходило с помощью трансплантации аутологичных стволовых клеток. Это помогло матери Аллы, теперь она в ремиссии. Болезнь близкого человека послужила толчком, и девушка вступила в регистр доноров костного мозга в Центре гематологии.
В 2019 году Алла узнала, что есть совпадение со сторонним реципиентом и необходимо приехать в клинику для расширенного типирования. Следовало провести дополнительные анализы, чтобы удостовериться, что ни одно заболевание не осталось незамеченным. Пересаживать стволовые клетки от не совсем здорового человека может быть опасно для реципиента, ведь на момент трансплантации иммунитет пациента полностью подавлен.
«Когда наступил непосредственный момент донации, — говорит Алла, — меня проконсультировали о двух способах извлечения стволовых клеток: из тазобедренной кости и из периферической крови. Я выбрала второй вариант, доверясь врачам. Мне сделали укол лейкостима. Он стимулирует выход гемопоэтических клеток в кровь. Затем в обе руки вставили катетеры. Из одной забирали кровь, которая проходила через центрифугу, в которой сепарировались гемопоэтические клетки. А во вторую возвращали оставшуюся кровь, не содержащую стволовых клеток. По прошествии некоторого времени после начала донации у меня стали неметь конечности и лицо, но я быстро сообщила медсестрам, и они сделали мне укол, который помог. Весь процесс занял около четырех часов. После процедуры я чувствовала себя хорошо, единственной проблемой была небольшая ломота в костях. Стволовые клетки сдавала в два захода, так как с первого раза не получилось взять нужное количество. Вся донация не страшнее, чем обычная сдача крови».
Расширение базы регистра позволит быстрее находить «генетического близнеца» нуждающемуся, тем самым увеличивая его шанс на выздоровление.
Что происходит при трансплантации с больным?
Перед тем как приступить к введению гемопоэтических клеток, врачи проводят процедуру кондиционирования (химиотерапию или лучевую терапию). Это делается с целью уничтожения раковых клеток (если лечение касается онкозаболеваний) или подавления иммунной системы, чтобы увеличить шанс приживления донорских клеток. Такой процесс имеет свои негативные последствия: тошнота и рвота, выпадение волос, кровотечения, сердечная и почечная недостаточности.
Затем наступает следующий этап. После того как врачи сделали пункцию (прокол стенки сосуда, полости или какого-либо органа с лечебной или диагностической целью) у донора, начинается непосредственное переливание реципиенту. Стволовые клетки попадают в организм больного и начинают свою работу. Донорские клетки с течением времени компенсируют недостаток клеток костного мозга реципиента, налаживая кроветворение и иммунную систему. Процесс приживления обычно требует нескольких недель, после чего показатели крови начинают нормализовываться.
Риск развития патологических реакций существует на всех стадиях адаптации организма после трансплантации. Реакция может начаться в течение первых месяцев после пересадки или развиться куда позже. Это происходит вследствие того, что донорские клетки подвергаются иммунному ответу организма реципиента.
Лечение спинного мозга с применением костного
Центральная нервная система имеет ограниченные способности к восстановлению, на которые негативно влияют различные факторы, в том числе связанные с повреждениями спинного мозга. Нарушения нервных структур и воспалительные процессы в них могут привести к инвалидности.
Однако исследования в области восстановления нейронов ЦНС дали почву для развития регенеративных методов лечения. Одним из многообещающих направлений в исследовании является метод введения стволовых клеток костного мозга совместно с плазмой крови, обогащенной тромбоцитами. Такой метод стимулирует регенерацию нейронов, поддерживая рост аксонов. Предполагалось, что данный вид лечения, с использованием концентрата клеток костного мозга, предпочтительнее из-за низкой способности на иммунный ответ и их большой распространенности.
На базе института Cedar Stem Cell Institute (штат Огайо, США) проводились процедуры ввода PRP (плазмы крови, обогащенной тромбоцитами) совместно с BMAC (концентратом стволовых клеток костного мозга) пациентам, имеющим повреждения в спинном мозге. Целью исследования было оценить изменения в состоянии пациентов, имеющих любой тип SCI (повреждение спинного мозга), а также отследить изменения индекса инвалидности ODI (показателя инвалидности, где более высокие значения эквивалентны более высокой инвалидности: от 0% до 100%).
Первый этап — выделение PRP и BMAC
Для получения PRP у пациентов отбирают по 60 мл периферической крови, добавляют 10 мл антикоагулянта цитратдекстрозы и центрифугируют полученную смесь с последующим концентрированием. В результате этого в среднем получается 7–8 мл плазмы, обогащенной тромбоцитами.
Получения BMAC проводят с помощью иглы для биопсии, которая через кожу и подкожные ткани вводится в правый гребень подвздошной кости. При помощи медленной аспирации отбирается 2 шприца по 25 мл, в которые добавляется по 1000 ед\мл гепарина. Полученную смесь фильтруют и центрифугируют в течение 10 минут, получая в итоге 17 мл BMAC.
После отбора PRP и BMAC смешивают в соотношении 1:2. Последним этапом данного метода является введение полученного препарата пациенту.
В эксперименте принимали участие семь человек с различными повреждениями спинного мозга, средний возраст пациентов составил 43,7 ± 2,33 года. После получения травмы пациенты перенесли минимум два вмешательства (физиотерапию и хирургическое вмешательство), а в период от 2,4 месяцев до 6,2 лет после травмы получили лечение смесью PRP и BMAC.
Показатели ODI отслеживали с помощью опроса по категориям: интенсивность боли, уход за собой, подъем, ходьба, положения сидя и стоя, сон, сексуальная жизнь, социальная жизнь и путешествия. Пациенты должны были оценить свое состояние от 0 (нет дискомфорта из-за травмы) до 5 (максимальный дискомфорт) в каждой категории. Все оценки складывались и делились на 50, чтобы получить процент функциональной инвалидности.
У 6 из 7 пациентов на момент начала эксперимента имелась значительная функциональная инвалидность. Один пациент после процедуры прекратил свои наблюдения, а динамика остальных пяти была отображена в исследовании. У двух пациентов наблюдались изменения от «тяжелой инвалидности» до «минимальной инвалидности», они вернули способность выполнять все бытовые дела самостоятельно. Показатели третьего пациента улучшились на 40% за год, а у четвертого улучшилось состояние на 28% за два месяца наблюдения.
Побочные эффекты наблюдались у одного из семи подопечных. Он не мог получать внутривенное введение препарата. Пациент сообщил о головной боли и трудностях, связанных с памятью.
Данный метод лечения помогает избежать дополнительного травмирования, которое возникает при введении инъекций в пораженный участок спинного мозга. Он безопасен и эффективен для восстановления после травм. У пациентов наблюдается положительная динамика и минимальное количество побочных эффектов. Потенциал такого лечения велик, и оно претендует занять передовое место при борьбе с повреждениями спинного мозга.
Как сегодня ищут донора костного мозга?
Мировая практика показала, что данные о донорах, протипированных по HLA, лучше хранить в виде единой информационной базы. Регистр Всемирной ассоциации доноров костного мозга содержит данные 37 млн добровольцев из 55 стран.
Формирование РДКМ (регистр доноров костного мозга) в России только начинает набирать обороты. Например, Русфонд совместно с Первым Санкт-Петербургским государственным медицинским университетом им. академика Павлова создал базу доноров костного мозга. Регистр был назван в честь Васи Перевощикова — больного, умершего от лейкоза в девять лет из-за отсутствия донора. Сегодня в регистре числится 40 258 потенциальных доноров. Однако регистра, объединяющего все города России, — нет, что усложняет поиск донора по всей стране. База разрознена по городам и учреждениям, поэтому шанс встретить генетически подходящего донора составляет 1:10 000.
Обращение к зарубежным регистрам возможно не всегда, поскольку процедура донации от иностранного гражданина может стоить порядка 20–50 тысяч долларов. Помимо этого, из-за многовариантности генотипов (связанной, например, с многонациональностью России) поиски донора могут закончиться провалом, т.к. не будет обнаружен подходящий по HLA-типу человека.
Вследствие этого в 20–40% случаев поиск в европейских регистрах заканчивается неудачей.
«В России нет обобщенной базы доноров костного мозга, — комментирует Виктор Андронов, заслуженный донор России, основатель движения “Энергия жизни”. — Они сообщаются между собой, обмениваясь данными, но дружат не все. Проблема заключается в том, что у нас до сих пор отсутствует законодательная база — нет закона о донорстве костного мозга. Организация Русфонд создала большую базу доноров, которая сейчас является самой перспективной в стране.
Помимо отсутствия общероссийского регистра проблемой является недостаточная информированность людей. Многие путают костный со спинным мозгом, считают, что процедура является болезненной, а иногда и вовсе не знают о донорстве.
В идеале, в регистре должен быть каждый. Нам стоило бы жить под лозунгом: “Все помогают всем”. В условиях коронавируса это крайне важно, т.к. нам с иностранными донорами очень сложно в этот период.
Количество доноров в регистре — вопрос национальной безопасности и индекса человеческой отзывчивости».
Создание единого регистра является решением проблем с трансплантацией, поскольку это снизит затраты на поиск и активацию донора, что увеличит шансы на жизнь нуждающихся в пересадке.
Людей спасет отзывчивость и причастность к общему делу. Донорство способно объединять против общей проблемы, связанной с серьезными заболеваниями. Трансплантация костного мозга — шанс на жизнь.