Что означает очаговое образование
Очаги в легких на КТ — что это?
ЧТО ТАКОЕ ОЧАГ В ЛЕГОЧНОЙ ТКАНИ?
Легочный очаг — это ограниченный участок снижения прозрачности легочной ткани (затемнение, уплотнение) небольших размеров, обнаруживаемый с помощью рентгенрафии или компьютерной томографии (КТ) легких, не сочетающийся с патологией лимфатических узлов или спадением части легкого — ателектазом. По западной терминологии, термином «узел» или «очаг» об означается затемнение размером менее 3 см; если диаметр участка больше 3 см, используется термин «объемное образование». Российская школа рентгенологии традиционно называет «очагом» участок диаметром до 10-12 мм.
Если рентгенография или компьютерная томография (КТ) выявляет один подобный участок, речь идет о одиночном (или солитарном) очаге; при обнаружении нескольких участках — о единичных очагах. При множественных очагах, захватывающих в той или иной степени всю легочную ткань, говорят о диссеминированом заболевании, или диссеминации очагов.
Сделать КТ легких в Санкт-Петербурге
В этой статье речь пойдет об одиночных очагах, их рентгенологических проявлениях, и врачебных действиях при их обнаружении. Существуют целый ряд заболеваний самой разной природы, которые могут проявляться очагом на рентгенограммах или компьютерных томограммах.
Одиночные или единичные очаги в легких наиболее часто встречаются при следующих заболеваниях:
Обнаружение одиночного узла на рентгенограмме органов грудной клетки ставит сложную задачу, с которой сталкиваются многие врачи: дифференциально-диагностический ряд при подобных изменениях может быть длинным, однако главной задачей является определить, является ли характера поражения доброкачественным или злокачественным. Решение этого вопроса является ключевым при определении дальнейшей тактики лечения и обследования. В спорных и неясных случаях для точного определения доброкачественности или злокачественности очагового образования рекомендуется Второе мнение — пересмотр КТ или рентгенографии легких в профильном учреждении опытным специалистом.
МЕТОДЫ ДИАГНОСТИКИ ОЧАГОВ В ЛЕГКИХ
Первичным методом исследования обычно является рентгенография органов грудной клетки. При ней большая часть солитарных легочных очагов обнаруживаются случайно. В некоторых исследованиях изучалось использование низкодозовой КТ органов грудной клетки в качестве инструмента скрининга рака легкого; так, применение КТ приводит к обнаружению более мелких узлов, которым необходимо дать оценку. По мере увеличения доступности, важную роль в диагностике солитарных легочных очагов будут также играть ПЭТ и ОФЭКТ.
Критериями доброкачественности выявленного очага являются возраст пациента менее 35 лет, отсутствие иных факторов риска, стабильность узла на протяжении более чем 2 года по данным рентгенографии, либо внешние признаки доброкачественности, обнаруживаемые на рентгенограммах. Вероятность злокачественности изменений у этих пациентов низкая, им необходимо периодическое выполнение рентгенограмм органов грудной клетки или КТ каждые 3–4 месяца в течение первого года, и каждые 4–6 месяцев на протяжении второго года.
ОГРАНИЧЕНИЯ И ОШИБКИ МЕТОДОВ ДИАГНОСТИКИ
Рентгенография грудной клетки характеризуется лучшим разрешением по сравнению с КТ при определении степени выраженности обызвествления и его размеров. В то же время, визуализация некоторых легочных узлов может быть осложнена из-за наложений других органов и тканей.
Применение КТ ограничено дороговизной этого исследования и необходимостью внутривенного контрастирования, риском развития побочных реакций после его введения. КТ не такой доступный метод исследования, как рентгенография; кроме того, компьютерный томограф, в отличие от рентгеновских аппаратов, не может быть переносным. ПЭТ и ОФЭКТ гораздо дороже по сравнению с КТ и МРТ, а доступность этих методов диагностики может быть различной.
Необходимо избегать ошибок интерпретации. Так, за опухолевый узел в легким можно ошибочно принять тени сосков, опухоли в мягких тканях грудной стенки, костные структуры, плевральные наложения, а также округлый ателектаз или участок воспалительной инфильтрации. Для снижения риска ошибки полезно заручиться вторым мнением.
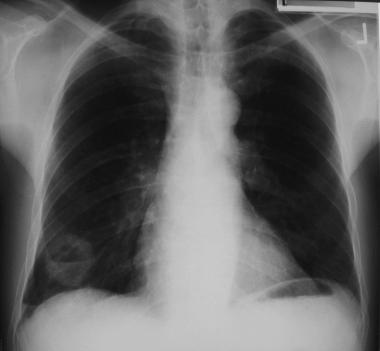
Часто солитарные легочные узлы впервые обнаруживаются на рентгенограммах органов грудной клетки и являются случайной находкой. Первым вопросом, на который необходимо ответить, располагается ли обнаруженный очаг в легком или находится вне его. С целью уточнения локализации изменений выполняется рентгенография в боковой проекции, рентгеноскопия, КТ. Обычно узлы становится различимыми на рентгенограммах, когда достигают размера 8–10 мм. Иногда могут обнаруживаться узлы размером 5 мм. На рентгенограммах можно определить размер очага, темпы его роста, характер краев, наличие обызвествлений – изменения, которые могут помочь оценить выявленный узел как доброкачественный или злокачественный.
Периферическое образование правого легкого с наличием полости (абсцесс). Рентгенограмма в прямой проекции.
Размер узла
Узлы, имеющие размер больше 3 см, более вероятно, отражают злокачественные изменения, в то время как узлы меньше 2 см, скорее всего, являются доброкачественными. Однако размер узла сам по себе имеет ограниченное значение. У некоторых пациентов мелкие узлы могут иметь злокачественную природу, а крупные – отражать доброкачественные изменения.
Темп роста узла
Время удвоения объема бронхогенного рака обычно составляет 20–400 дней; временной промежуток, необходимый для удвоения объема, составляющий 20–30 дней и меньше, характерен для инфекций, инфаркта легкого, лимфомы и быстро растущих метастазов. Если время удвоения объема больше 400 дней, это свидетельствует о доброкачественности изменений, за исключением карциноидной опухоли низкой степени злокачественности. Отсутствие изменений размеров узла на протяжении более чем 2 лет с большой степенью вероятности говорит о доброкачественном процессе. Тем не менее, определить размер очага без ошибки невозможно. На рентгенограмме грудной клетки оценить увеличение размера узла на 3 мм может быть сложно; проведение измерений на рентгенограммах после цифровой обработки позволяет более точно определить размер очага.
Контуры очага
Узлы доброкачественного характера обычно имеют четко очерченные, ровные контуры. Злокачественные узлы характеризуются типичными неправильными, мультицентрическими, спикулообразными (по типу «лучистого венца») краями. При этом наиболее значимым признаком, позволяющим предположить злокачественность изменений, является лучистость краев; крайне редко злокачественные опухоли имеют ровные края.
Кальцинированный очаг в легком
Отложения солей кальция, обызвествления больше типичны для доброкачественных очаговых образований, однако при КТ они также обнаруживаются приблизительно в 10% злокачественных узлов. При доброкачественных процессах обычно обнаруживаются пять типичных типов обызвествления: диффузный, центральный, ламинарный, концентрический и в виде «попкорна». Обызвествления в виде «попкорна» являются характерными для гамартом, точечные или эксцентрично расположенные кальцинаты наблюдаются преимущественно в злокачественных узлах. Более точно обнаружить и оценить обызвествления можно при помощи КТ.
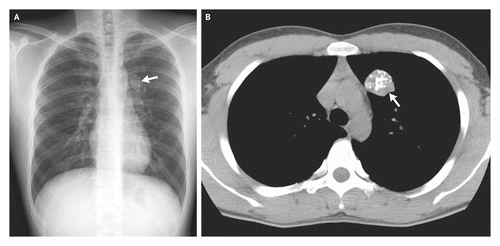
Доброкачественные образования в легких встречаются относительно редко, однако в типичных случаях КТ позволяет четко отличить их от злокачественной опухоли. Объемное образование левого легкого — гамартома. Кальцинация в виде «попкорна».
ОЧАГИ В ЛЕГКИХ НА КТ — ЧТО ЭТО?
Очаговые образования в легких на КТ выявляются лучше, чем на обзорной рентгенографии. На КТ можно различить очаговые изменения размером 3–4 мм, также лучше визуализируются специфические морфологические признаки (характерные, например, для округлого ателектаза или артерио-венозной мальформации). Кроме того, КТ позволяет лучше оценить те области, которые обычно плохо различимы на рентгенограммах: верхушки легких, прикорневые зоны, а также реберно-диафргамальные синусы. Также на КТ может быть обнаружен множественный характер очагового поражения; КТ может применяться для стадирования опухоли; помимо этого, под контролем КТ осуществляется игольная биопсия.
Сделать КТ легких в Санкт-Петербурге
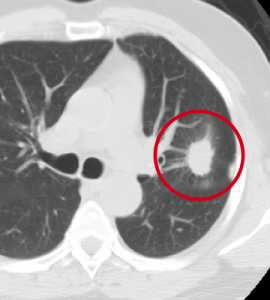
Периферическое образование левого легкого. Типичные КТ-признаки периферического рака: округлая форма, неровные лучистые контуры.
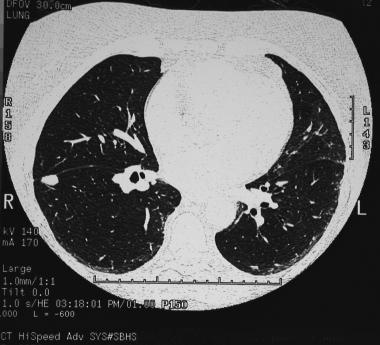
Субплевральные очаги в легких — что это? Компьютерная томография демонстрирует узловое образование, прилежащее к междолевой плевре. Признаки подобных очагов не являются специфичными и требуют дополнительного обследования. Биопсия подтвердила грибковую инфекцию.
Рентгеновская плотность очага на КТ
С помощью компьютерной томографии может быть выполнено измерения определенного показателя — коэффициент ослабления, или рентгеновской плотности очага. Результаты измерения (КТ-денситометрии) выводятся в единицах шкалы Хаунсфилда (Ед. Х, или HU). Ниже приведены несколько примеров коэффициентов ослабления:
Кровь: от 40 до 60 ЕХ
Некальцинированный узел: от 60 до 160 ЕХ
Кальцинированный узел: больше 200 ЕХ
При использовании КТ-денситометрии появляется возможность обнаружения скрытых кальцинатов, которые можно не заметить визуально даже на тонких КТ-срезах высокого разрешения. Кроме того, измерение плотности помогает обнаружить жировую ткань внутри узла, что является признаком его доброкачественности, особенно в случаях гамартомы.
КТ с контрастным усилением
Злокачественные узлы обычно более богаты сосудами, чем доброкачественные. Оценка контрастного усиления узла производится путем измерения его плотности до и после введения контраста с интервалом 5 минут. Повышение плотности менее чем на 15 Ед. Х позволяет предположить доброкачественную природу узла, в то время как контрастное усиление на 20 Ед. Х и больше характерно для злокачественных поражений (чувствительность 98%, специфичность 73%).
Симптом питающего сосуда
Симптом питающего сосуда характерен для внутрилегочных узлов сосудистой этиологии, например, гематогенных легочных метастазов или септических эмболов.
Толщина стенки полостного образования
Полость может обнаруживаться и в злокачественных, и в доброкачественных узлах. Наличие полости с тонкой стенкой (1 мм и меньше) является признаком, указывающим на доброкачественную природу изменений, в то время как наличие толстой стенки не позволяет сделать вывод о доброкачественности или злокачественности образования.
МАГНИТНО-РЕЗОНАНСНАЯ ТОМОГРАФИЯ (МРТ) ЛЕГКИХ
При стадировании рака легкого МРТ позволяет добиться лучшей визуализации поражений плевры, диафрагмы и грудной стенки по сравнению с КТ. В то же время МРТ менее применима в оценке легочной паренхимы (особенно для выявления и характеристики легочных очаговых изменений) из-за меньшего пространственного разрешения. Поскольку МРТ является более дорогим и менее доступным методом исследования, этот способ диагностики используют в качестве резервного для оценки опухолей, которые затруднительно оценить посредством КТ (например, опухоль Панкоста).
УЗИ нечасто применяется в оценке солитарных легочных очагов; этот метод имеет ограниченное значение и используется для контроля при выполнении чрезкожной биопсии более крупных узлов, расположенных в периферических отделах.
РАДИОНУКЛИДНАЯ ДИАГНОСТИКА ОЧАГОВЫХ ИЗМЕНЕНИЙ ЛЕГКИХ
Использование методов ядерной медицины (сцинтиграфия, ОФЭКТ, ПЭТ) в оценке солитарных внутрилегочных узлов изучалось при помощи научных исследований. Так, использование ПЭТ и ОФЭКТ было одобрено в США для оценки внутрилегочных узлов.
Клетки злокачественного новообразования характеризуются большей метаболической активностью по сравнению с неопухолевыми клетками, вследствие чего уровень накопления глюкозы в них выше. При ПЭТ органов грудной клетки используется соединение радиоактивного нуклида фтора с массовым числом 18 и аналога глюкозы ( F 18-фтордезоксиглюкоза, ФДГ). Увеличение накопления ФДГ обнаруживается в большинстве злокачественных опухолей, и этот момент является основополагающим в дифференциальной диагностике доброкачественных и злокачественных легочных узлов.
Накопление ФДГ может быть оценено количественно с использованием стандартизированного коэффициента накопления, использующегося с целью приведения к единому значению показателей, зависящих от веса пациента и количества введенного радиоизотопа, что позволяет сравнить накопление радиофармпрепарата в различных очагах поражения у разных пациентов. Значение стандартизированного коэффициента накопления, превышающее 2,5, используется в качестве «маркера» злокачественности. Еще одним преимуществом ПЭТ с ФДГ является лучшее обнаружение метастазов в средостении, что позволяет более оптимально стадировать рак легкого.
ОФЭКТ
Степень достоверности ПЭТ и ОФЭКТ легких
При использовании мета-анализа, усредненная чувствительность и специфичность при обнаружении злокачественных изменений в в фокальных легочных очагах любого размера составила 96% и 73,5% соответственно. В случае легочных узлов чувствительность и специфичность составила 93,9% и 85,8% соответственно.
Ошибки при ПЭТ-КТ легких
При ПЭТ с ФДГ ложноположительные результаты могут быть обусловлены метаболически активными узлами иной природы, например, инфекционными гранулемами или воспалительными очагами. Кроме того, опухоли, характеризующиеся низкой метаболической активностью, например, карциноидная опухоль и бронхиолоальвеолярный рак, могут никак себя не обнаруживать. При высоких сывороточных концентрациях глюкозы она конкурирует в клетках с ФДГ, в результате чего накопление радиоизотопа снижается.
Василий Вишняков, врач-радиолог
При написании статьи использованы следующие материалы:
Что означает очаговое образование
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Впервые выявленные очаговые образования легких малого размера (до 2 см в диаметре). Динамическое наблюдение или операция?
Журнал: Хирургия. Журнал им. Н.И. Пирогова. 2016;(10): 57-60
Павлов Ю. В., Рыбин В. К. Впервые выявленные очаговые образования легких малого размера (до 2 см в диаметре). Динамическое наблюдение или операция?. Хирургия. Журнал им. Н.И. Пирогова. 2016;(10):57-60.
Pavlov Iu V, Rybin V K. First time revealed small formations of lungs (under 2 cm in diameter). Dynamic follow-up or surgery?. Khirurgiya. 2016;(10):57-60.
https://doi.org/10.17116/hirurgia20161057-60
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Факультетская хирургическая клиника им. Н.Н. Бурденко Московской медицинской академии им. И.М. Сеченова
Одиночный очаг в легких (ООЛ) определяют как локальный участок уплотнения легочной ткани округлой или близкой к ней формы диаметром до 3 см [15]. Это международное определение отличается от традиционного отечественного представления о легочных очагах, источником которого является фтизиатрическая практика (в классификации туберкулеза легких размер очагов не превышает 1 см, а уплотнения большего размера определяются как инфильтраты, туберкуломы и другие виды изменений) [14, 15].
Патологические образования легких малого размера (до 2 см) в большинстве случаев выявляются при проведении компьютерной томографии грудной клетки, выполняемой по различным причинам [10, 11, 14, 16-18].
Между тем по результатам одного КТ-исследования часто трудно провести дифференциальную диагностику, требуются повторные исследования в динамике. При воспалительном процессе очаги исчезают через 1-2 мес. В случае атипичной железистой гиперплазии очаги не изменяются в течение нескольких лет. При аденокарциноме можно заметить увеличение размера и/или усиление плотности, а также сосудистую конвергенцию [11, 12].
Обнаруженные при таком обследовании очаговые образования в легочной ткани нередко остаются без внимания специалистов, что порой влечет за собой неутешительные результаты лечения этой категории больных.
По мнению С.В. Миллер и соавт. [8], диагностическая торакотомия является завершающим методом комплексного обследования больных с округлыми образованиями легких небольшого размера и обеспечивает действительно раннюю диагностику и своевременное хирургическое лечение. Следовательно, радикальное хирургическое вмешательство, предпринятое при округлом образовании в легком, генез которого неясен, является методом, позволяющим провести морфологическую верификацию ранней стадии злокачественной опухоли и выполнить органосохраняющую операцию.
Другие авторы считают, что в настоящее время не существует единого подхода к определению характера очаговых образований легких. Очевидно, что при высоком риске злокачественной опухоли оптимальный подход заключается в возможно более ранней морфологической верификации диагноза. В случае низкого риска злокачественного процесса более рационально проводить динамическое наблюдение [11].
Результатом этих действий может быть выделение группы пациентов с очевидно доброкачественным процессом, о чем свидетельствуют отсутствие динамики роста очага на протяжении 2 и более лет, наличие «доброкачественных» обызвествлений, включений жира (гамартома) или жидкости (киста) в очаге по данным КТ. В такой ситуации необходимо только наблюдение. Сюда же относятся случаи артериовенозных мальформаций и других сосудистых изменений, а также воспалительные процессы в легких (округлый туберкулезный инфильтрат, туберкулома, мицетома и др.), требующие специфического лечения [5, 9, 13].
Ежегодно в России раком легкого заболевают свыше 63 тыс. человек, в том числе свыше 53 тыс. мужчин. У более 20 тыс. пациентов (34,2%) рак легкого выявляется в IV стадии, поэтому задача обнаружения злокачественных опухолей легких на ранних стадиях их развития чрезвычайно актуальна [2, 7, 8].
Угрожающим фактором при диагностике опухолей легких малого диаметра является их бессимптомность. Отсутствие жалоб, скудная клиническая картина заболевания, сложности с профилактикой и первичным выявлением очагов делают проблему образований легких до 2 см в диаметре актуальной для научных изысканий и практически значимой для сохранения здоровья и нередко жизни пациентов.
Материал и методы
У всех больных при рентгенологическом исследовании, включая компьютерную томографию, были впервые выявлены очаговые образования в легких размером от 0,5 до 2 см. Всем пациентам были выполнены операции удаления участков легочной ткани с опухолью из различных доступов: 44 видеоторакоскопические резекции легкого, 43 миниторакотомии с видеосопровождением, 23 миниторакотомии. Окончательный диагноз формулировали после планового гистологического исследования удаленного патологического образования легкого. Летальных исходов не было.



Результаты и обсуждение

Во 2-й группе у 13 пациентов был выявлен рак легкого. Доброкачественные опухоли (гамартомы) легкого имелись у 18 больных, у 7 пациентов была диагностирована туберкулома. Таким образом, в этой группе частота злокачественных и доброкачественных опухолей вместе с туберкуломами составила 88,4%.
Таким образом, диагностический алгоритм исследований у больных с впервые выявленными периферическими образованиями легких определяют данные мультиспиральной компьютерной томографии. При малом размере образований (от 0,5 до 2 см) показано их удаление без морфологического подтверждения диагноза до операции. Оптимальный оперативный доступ для хирургического лечения пациентов с опухолями легких малого размера следует выбирать в зависимости от диаметра и количества патологических образований. При единичной опухоли легкого размером менее 0,5 см, впервые выявленной при компьютерной томографии, наиболее целесообразной тактикой будет динамическое наблюдение больного и проведение контрольной компьютерной томографии через 3, 6, 12 мес.
Очаговые образования печени
Выделяют следующие основные группы очаговых поражений печени:
1. Непаразитарные кисты печени:
2. Паразитарные кисты печени:
3. Доброкачественные опухоли печени:
4. Злокачественные опухоли печени:
5. Послеоперационные и посттравматические кисты печени:
Непаразитарные кисты печени
Непаразитарные кисты печени — это разнообразные формы, объединяемые по одному общему признаку — образованию в печени полости (или полостей), заполненных жидкостью. Развиваются кисты из зачатков желчных ходов и превращаются в полости, выстланные изнутри эпителием, который продуцирует жидкость. Встречаются у 5-6% населения. При этом заболевание встречается в 3-5 раз чаще у женщин и проявляет себя в возрасте от 40 до 55 лет. Выявляются, как правило, случайно при ультразвуковом исследовании или компьютерной томографии.
Одиночная киста печени представляет собой образование в печени округлой формы.
Множественные кисты характеризуются поражением не более 30% ткани печени, с преимущественным расположением в одной, реже в обеих долях с сохранением ткани печени между ними.
Ложные кисты печени развиваются после травматического повреждения печени, их стенка состоит из фиброзно-изменённой ткани печени. Ложные кисты печени могут также образовываться после лечения абсцесса печени, удаления эхинококковой кисты (эхинококкэктомии). Содержимое кист печени представляет собой светлую прозрачную или бурую прозрачную жидкость с примесью крови или желчи. Они чаще встречаются в левой доле печени.
Для поликистоза печени характерно кистозное замещение не менее 60% ткани печени с обязательным расположением кист в обеих долях печени и отсутствием ткани печени между стенками кист.
Главной особенностью непаразитарных кист печени является их преимущественно бессимптомное течение. Проявления болезни (боли в правом подрёберье и других отделах живота) отмечаются редко и связаны с растяжением капсулы печени или брюшной стенки, а также со сдавлением близлежащих органов и желчных протоков.
Определяющими в постановке диагноза являются инструментальные методы исследования. Традиционно, обнаружение у больных очаговых поражений печени является случайной находкой при такой, казалось бы, обыденной процедуре, как ультразвуковое исследование органов брюшной полости, либо на КТ или МРТ.
При динамическом наблюдении пациентов с кистами печени отмечено, что кисты имеют тенденцию к постоянному росту. По мере роста кисты вохрастает опасность возникновения осложнений (кровотечение, кровоизлияние, разрыв кисты).
Всё это определяет необходимость наблюдать больных с непаразитарными кистами печени сразу после их выявления, даже при небольших размерах.
Паразитарные кисты печени
Среди паразитарных кист выделяют эхинококковые и альвеококковые.
Эхинококкоз относят к одному из наиболее тяжёлых паразитарных заболеваний организма человека. Заболевание развивается при внедрении и росте в различных органах личинки ленточного глиста — эхинококка Echinococcus granulosus. Первичным хозяином его являются собаки, волки, шакалы, лисы и др. О географической распространённости заболевания может говорить тот факт, что оно не выявлено только в Антарктиде. Заболеваемость эхинококкозом печени у населения данного региона составляет 1,2 — 1,4 на 100000 населения.
Основной проблемой выявления эхинококкоза остаётся факт длительного бессимптомного течения. Молодое население, страдающее данной патологией, редко обращается к врачу. При сборе анамнеза трудно выявить факт контакта с больным животным в течение последних 5 лет. Нередко пациенты указывают на контакты подобного рода более 10 лет назад, либо вспомнить о них не могут вообще. Размеры кист для пациента при их обнаружении являются неожиданностью, кисты вмещают от 1,5 до 6 л жидкости.
Алвеококкоз печени возникает при паразитировании цестоды Echinococcus multilocularis в личиночной стадии. Эти два указанных вида эхинококка резко отличаются между собой как в морфологическом, биологическом, экологическом, так и в патогенетическом отношении. Поражение Echinococcus multilocularis для европейской части России не характерно.
Современные УЗИ-аппараты, обладающие высокой разрешающей способностью, цветным контрастированием и возможностью трёхмерной реконструкции изображения, позволяют специалистам выявить точное расположение кисты печени.
При небольших кистах более информативна магнитно-резонансная томография МРТ (в режиме жёсткой гидрографии), позволяющая выявить описанные выше характеристики паразитарной кисты или компьютерная томография (КТ) на томографах последнего поколения.
Иммунологические методы в диагностике эхинококкоза имеют большое, едва ли не решающее значение. Наиболее информативным является иммунно-ферментный анализ (РИФА, ELIZA). Реакция практически не имеет противопоказаний и применима для выявления эхинококкозов и рецидивов заболевания посредством их неоднократного проведения. При одновременном использовании нескольких иммунологических тестов диагностическая эффективность их составляет более 80%.
Наиболее распространённым методом лечения больных эхинококкозом до сих пор являются традиционные хирургические вмешательства. Чаще всего применяют различные виды эхинококкэктомий (удаления кист) с последующим проведением длительного противорецидивного медикаментозного лечения.
Доброкачественные опухоли печени
Доброкачественные опухоли печени представляют собой малосимптомные образования, происходят как из эпителиальной ткани (гепатоцеллюлярная аденома и др.), так и из стромальных (узелковая гиперплазия печени) и сосудистых элементов (гемангиома и др.).
Аденома печени — редкая доброкачественная опухоль.
Первый тип чаще встречается у женщин детородного возраста, второй — у мужчин. Встречается в виде одного или нескольких узлов, отграниченых от ткани печени, имеет капсулу (оболочку) диаметром от 1 до 20 см. При обнаружении аденомы в печени показано оперативное лечение, т.к. при её энергичном росте возможен разрыв опухоли с повреждением сосудов и кровотечением.
Гемангиома печени — доброкачественная опухоль, происходит преимущественно из венозных элементов печени, обычно находят случайно при УЗИ или КТ. Возможные осложнения: сдавление желчных протоков, сосудов, разрыв с обильным кровотечением, злокачественное перерождение. Необходимо отличать от метастазов, аденомы, лимфангиомы, нодулярной гиперплазии. Лечение строго в специализированных стационарах.
Нодулярная гиперплазия — редкое опухолеподобное поражение нецирротической печени; представлена множеством узлов диаметром 0,1-4,0 см, изменения печени минимальны, размеры обычно в пределах нормы. Необходимо отличать от цирроза, метастазов печени. Для диагностики применяют компьютерную томографию (КТ) с контрастным усилением или магнитно-резонансную томографию (МРТ).
Учитывая, отсутствие абсолютно точных и однозначно свидетельствующих в пользу доброкачественной опухоли признаков и лабораторных маркеров, по мнению большинства специалистов, необходим последовательный, поэтапный диагностический подход.
Послеоперационные и посттравматические кисты печени
Абсцесс печени — отграниченное гнойно-деструктивное поражение печени, возникающее в результате заноса инфекции с током крови, лимфы, с желчью или контактным путём. Чаще располагается в правой доле печени, под капсулой, обычно округлой формы и проявляется дискомфортом, болями в правом подрёберье и верхней части живота.
Причиной возникновения абсцессов является обычно внутрибрюшная инфекция.
Болеют преимущественно люди среднего и пожилого возраста. Заболевание одинаково часто поражает и мужчин, и женщин. Клинические проявления достаточно неспецифичны и включают лихорадку, озноб, боли в правом подрёберье, недомогание и похудание. В 30% случаев лихорадка может отсутствовать. Жалобы на боли в животе предъявляют только 45% пациентов. У многих пациентов преобладают клинические признаки основного заболевания — аппендицита, дивертикулита или поражения желчных протоков.
Самый распространённый источник инфекции (35% случаев) при абсцессах печени — заболевания желчных путей. Как правило, это холангит или острый холецистит. У 10-20% пациентов с абсцессами печени, обусловленными заболеваниями желчных путей, выявляются злокачественные опухоли поджелудочной железы, общего желчного протока и ампулы фатерова соска. К развитию абсцессов печени могут также привести хирургические или эндоскопические вмешательства на желчных протоках. Иногда абсцессы печени образуются вследствие паразитарной инвазии желчных путей (круглыми червями или трематодами), что вызывает инфицирование желчи.
Второй по частоте источник инфекции при абсцессах печени — внутрибрюшные инфекции, когда бактерии попадают в печень по воротной вене. В 30% случаев к образованию абсцессов печени приводят дивертикулит, болезнь Крона, неспецифический язвенный колит и перфорация кишки. Примерно у 15% больных абсцессы печени обусловлены прямым проникновением бактерий из близко расположенного очага инфекции, как это происходит, например, при поддиафрагмальном абсцессе или при эмпиеме желчного пузыря. Возможен также перенос бактерий в печень с артериальной кровью из отдалённых очагов инфекции (при эндокардите или тяжёлых заболеваниях зубов).
Ультразвуковое исследование (УЗИ) печени всегда проводится больным с лихорадкой и изменённым анализом крови. Однако, компьютерная томография (КТ) является более информативным методом исследования для выявления деструктивных изменений в печени. У 50-80% пациентов с абсцессами печени определяются изменения на обзорных рентгенограммах грудной клетки.
С диагностической и лечебной целями необходимо проведение пункционной тонкоигольной аспирационной биопсии (ПТАБ) под контролем УЗИ, что позволяет установить микробную флору, установить чрескожный чреспечёночный дренаж с целью проведения лечебной санации полости абсцесса, а также подобрать антибиотик, наиболее чувствительный к данному виду микрофлоры.
Малоинвазивное хирургическое лечение абсцессов печени включает в себя пункцию и дренирование его полости.
Гематомы и отграниченные скопления жидкости — (травматическое, послеоперационное) скопление крови или жидкости, излившейся при повреждении сосудов в любой паренхиматозный орган или в анатомическую полость.
Диагностируется при помощи УЗИ, КТ, МРТ. Отмечаются следующие изменения (стадии развития): в раннем периоде определяется жидкость, содержащая образование (сгустки); далее сгустки превращаются в сформированные массы, появляются перегородки различной толщины, стенки становятся более плотными, толстыми; при дальнейшем нарастании фиброзных процессов и кальцинации происходит постепенное рассасывание гематомы; при сохранении жидкого компонента — формирование псевдокисты.
При установлении диагноза тактика как при абсцессах печени.
Важным диагностическим этапом является дифференцирование доброкачественного и злокачественного процесса.
Злокачественные опухоли печени
Необходимо отметить, что характер злокачественного роста опухоли можно поставить только при гистологическом исследовании препарата. Т.е., необходимо получить для исследования часть образования. Это возможно сделать только во время лапароскопии, когда визуальному осмотру становиться доступной вся брюшная полость. «Слепое» пунктирование печени под контролем только ультразвука считаем необоснованно опасным из-за низкой информативности и возможности развития осложнений.
К большому сожалению, обнаружение очагов в печени очень часто становится возможным лишь на поздних стадиях заболевания, когда выполнить хирургическое вмешательство уже невозможно. Этому способствует не только «скрытый» и быстрый рост опухоли, низкая онконастороженность врачей в поликлиниках, поздние обращения пациентов за медицинской помощью, но и характер самих образований в печени.
Необходимо отметить ещё раз, что при проведении стандартного УЗИ выявить очаг не так просто из-за его одинаковой со здоровой печенью проницаемости для ультразвуковых волн. КТ, МРТ могут дать четкое заключение в 85-92% случаев по статистике. К великому сожалению не существует на сегодня стопроцентных диагностических методов исследований. Любое сомнение решается в пользу операции.
Отличным дополнением к УЗИ является функция эластографии и эластометрии, а также оценка кровотока в стенке или капсуле образования, что является чрезвычайно важным для дальнейшей тактики ведения пациента.
Очаговые поражения печени встречаются достаточно часто,диагностируются на поздних сроках, поэтому настоятельно рекомендуем: при первом же обнаружении объемного образования печени, обращаться в специализированные медицинские учреждения, где вам окажут профессиональную медицинскую помощь.
Процесс комплексного обследования такого больного включает в себя несколько последовательных этапов.