Что предпочтительнее для возмещения глобулярного объема при геморрагическом шоке
Геморрагический шок: признаки и клинические симптомы, первая помощь, лечение
Симптомы развития болезни
Диагностировать ГШ можно по разным клиническим проявлениям. Общими признаками такого патологического состояния являются:
Ставить диагноз, основываясь только на субъективных ощущениях пациента, крайне опасно, так как клиника геморрагического шока будет зависеть от степени тяжести состояния.
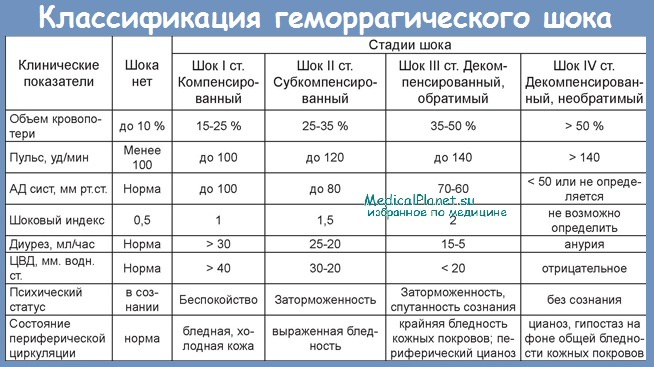
При классификации стадий ГШ главным образом берется во внимание объем кровопотери и гемодинамические нарушения, которые вызываются в организме. Каждая стадия заболевания будет иметь свои признаки:
Стадии геморрагического шока и классификация острой кровопотери — это сопоставимые понятия.
Неотложная помощь
В первую очередь, на до-госпитальном этапе, необходимо провести доступные манипуляции по временной остановке кровотечения любыми подручными материалами. После чего необходимо связаться с реанимационной бригадой или доставить больного в стационар самостоятельно.
Далее, оказание первой неотложной помощи при геморрагическом шоке должно проводиться по правилу «3-х катетеров», которое включает в себя 3 стадии:
После чего, последовательно проводится необходимая диагностика и интенсивная терапия, по следующему алгоритму:
Клиническая картина
Для геморрагического шока характерны следующие симптомы и признаки:
В целом, клиника проявлений геморрагического шока у человека зависит не только от скорости кровопотери, но и от уровня индивидуальных компенсаторных механизмов, которые напрямую зависят от возраста, конституционного сложения, сопутствующих усугубляющих факторов, например, заболеваний сердца и лёгких.
Тяжелее других острые кровотечения переносят дети и люди преклонных лет, беременные с гестозом, а также люди, страдающие ожирением или со сниженным иммунитетом.
Синдром диссеминированного внутрисосудистого свертывания крови
Самым опасным осложнением гиповолемического шока является синдром диссеминированного внутрисосудистого свертывания или ДВС-синдром. Он проявляется нарушением макроциркуляции, в результате которого останавливается микроциркуляция, что ведет к отмиранию жизненно важных органов. Первыми страдают сердце, легкие и головной мозг. Затем атрофируются мягкие ткани и появляется ишемия. ДВС-синдром — состояние, когда при контакте с кислородом кровь начинает свертываться еще в сосудах. Из-за этого образуются тромбы, которые и нарушают процесс циркуляции.
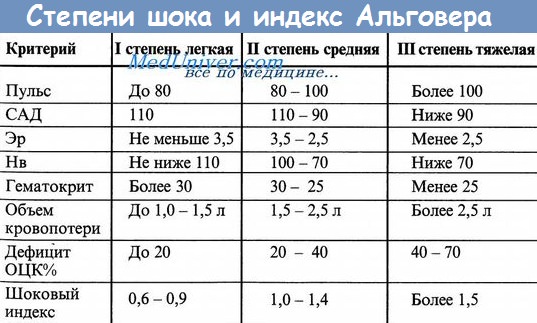
Определение величины кровопотери
Уточнить масштабы ухудшения состояния пациента и величину потери крови допустимо двумя способами.
Что предпочтительнее для возмещения глобулярного объема при геморрагическом шоке
Эффективность лечения острой кровопотери и геморрагического шока зависит от своевременности, качества и объема восполнения ОЦК, коррекции нарушений гомеостаза.
Алгоритм интенсивной терапии массивной кровопотери и геморрагического шока.
1. При наружном кровотечении осуществляют временную его остановку путем наложения жгута, зажима на кровоточащий сосуд, придавливанием (пальцами, кулаком, давящей повязкой).
2. Проводят ингаляцию кислорода через интраназальные катетеры, лицевую маску, по показаниям выполняют интубацию трахеи и ИВЛ.
3. Оценивают состояние больного: определяют артериальное давление, ЧСС, частоту дыхания, Sp02, уровень сознания, характер травмы, на основе которой можно ориентировочно определить объем кровопотери.
4. Обеспечивают надежный доступ к сосудистому руслу и измерению ЦВД, что достигается катетеризацией центральной вены (подключичной или наружной яремной, одной или обоих бедренных вен). При быстрой (одномоментной) массивной кровопотере (более 40% ОЦК) для внутриартериального нагнетания инфузионно-трансфузионных сред катетеризируют бедренную артерию.
В зависимости от объема острой кровопотери выделяют 4 типа реакции организма:
I тип. Дефицит ОЦК не более 15% устраняется приспособительными реакциями организма и значительно не отражается на общем функциональном состоянии организма. Клинически отмечается чувство жажды, тахикардия в покое, ортостатаческая тахикардия (превышение частоты сердечных сокращений стоя над частотой сердечных сокращений лежа не менее, чем на 20 ударов в минуту). Внутривенной инфузии для восполнения кровопотери в подавляющем большинстве случаев не требуется.
3 тип. Дефицит ОЦК составляет 25-40%. Состояние больного в ответ на кровопотерю расценивается как средней тяжести или тяжелое. При острой кровопотере может наблюдаться легкое или средней степени психомоторное возбуждение. Бледность кожных покровов и видимых слизистых выражена. Одышка до 24-28 дыханий в минуту. Тахикардия 120 ударов в минуту и более. Экстрасистолия. Артериальная гипотензия в положении лежа. Олигурия.
Восполнение кровопотери и проведение лекарственной терапии в ближайшие 15-30 минут после кровопотери позволяет не допустить или быстро купировать развитие симптомокомплекса геморрагического шока.
4 тип, так называемая массивная кровопотеря, составляющая более 40-50% ОЦК. Состояние больного расценивается как крайне тяжелое. Острая кровопотеря в таком объеме, как правило, сопровождается оглушенностью, заторможенностью, спутанностью сознания. Дыхание частое (более 28 в мин.), поверхностное, возможно его угнетение. Систолическое артериальное давление снижается до 70 мм рт.ст. и ниже. Тахикардия 120 ударов в минуту и более.
Геморрагический шок
Используйте навигацию по текущей странице
Геморрагический шок (ГШ) — это критическое состояние организма, связанное с острой кровопотерей, в результате чего возникает кризис макро-и микроциркуляции, синдром полиорганной и полисистемной недостаточности. С патофизиологической точки зрения — это кризис микроциркуляции, его неспособность обеспечить адекватный тканевой обмен, удовлетворить потребность тканей в кислороде, энергетических продуктах, удалить токсичные продукты обмена.
Организм здорового человека кровопотерю до 20% ОЦК (примерно 1000 мл) может восстановить за счет аутогемодилюции и перераспределению крови в сосудистом русле. При кровопотере более 20-25% эти механизмы могут ликвидировать дефицит ОЦК. При массивной кровопотере стойкая вазоконстрикция остается ведущей «защитной» реакцией организма, в связи с чем поддерживается нормальный или близкий к нему артериальное давление, осуществляется кровоснабжение мозга и сердца (централизация кровообращения), но за счет ослабления кровотока в мышцах внутренних органов, в том числе в почках, легких, печени.
Долговременная устойчивая вазоконстрикция, как защитная реакция организма сначала, в течение некоторого времени поддерживает в определенных пределах артериальное давление, в дальнейшем, при прогрессировании шока и при отсутствии адекватной терапии, способствует последовательному развитию тяжелых нарушений микроциркуляции, формированию «шоковых» органов и развитию острой почечной недостаточности и других патологических состояний.
Тяжесть и скорость нарушений при ГШ зависит от длительности артериальной гипотонии, восходящего состояния органов и систем. При восходящей гиповолемии кратковременная гипоксия в родах ведет к шоку, так как является пусковым механизмом нарушения гемостаза.
Клиника геморрагического шока
Геморрагический шок проявляется слабостью, головокружением, тошнотой, сухостью во рту, потемнением в глазах, при увеличении кровопотери — потерей сознания. В связи с компенсаторным перераспределением крови ее количество уменьшается в мышцах, коже проявляется бледностью кожных покровов с серым оттенком конечности холодные, влажные. Уменьшение почечного кровотока проявляется снижением диуреза, в последующем с нарушением микроциркуляции в почках, с развитием ишемии, гипоксии, некроза канальцев. При увеличении объема кровопотери нарастают симптомы дыхательной недостаточности: одышка, нарушение ритма дыхания, возбуждение, периферийное цианоз.
Выделяют четыре степени тяжести геморрагического шока:
Лечение геморрагического шока
Устранение причины кровотечения — главный момент лечения геморрагического шока. Выбор метода остановки кровотечения зависит от ее причины. При лечении большое значение имеет скорость компенсации кровопотери и своевременное хирургическое лечение. При II степени тяжести геморрагический шок является абсолютным показанием к оперативной остановке кровотечения.
Инфузионная терапия при геморрагическом шоке должна проводиться в 2-3 вены: при АД в пределах 40-50 мм рт.ст. объемная скорость инфузии должна быть 300 мл / мин при АД 70-80 мм рт.ст. — 150-200 мл / мин при стабилизации АД до 100-110 мм рт.ст. инфузия проводится капельно под контролем АД и почасового диуреза.
Соотношение коллоидов и кристаллоидов должно быть 2:1. В инфузионную терапию включаются: реополиглюкин, волекам, эритромасса, нативная или свежезамороженная плазма (5-6 флаконов), альбумин, раствор Рингера-Локка, глюкоза, панангин, преднизолон, коргликон, для коррекции метаболического ацидоза — 4% раствор гидрокарбоната натрия, трисамин. При гипотензивном синдроме — введение дофамина или допамина. Объем инфузии должен превышать предполагаемую кровопотерю на 60-80%, одновременно проводится гемотрансфузия в объеме не более 75% кровопотери при ее одномоментном замещении, затем отсроченная гемотрансфузия в меньших дозах.
Для ликвидации вазоспазма после устранения кровотечения и ликвидации дефицита ОЦК применяют ганглиоблокаторы с препаратами, которые улучшают реологические свойства крови (реополиглюкин, трентал, компламин, курантил). Необходимо применять глюкокортикоиды в больших дозах (30-50мг/кг гидрокортизона или 10-30мг/кг преднизолона), мочегонные средства, искусственную вентиляцию легких.
Для лечения ДВС-синдрома при ГШ применяют свежезамороженную плазму, ингибиторы протеаз — контрикал (трасилол) по 60-80000 ОД, гордокс по 500-600000 ОД. Дицинон, этамзилат, андроксон снижают ломкость капилляров, усиливают функциональную активность тромбоцитов. Применяют сердечные гликозиды, иммунокорректоры, витамины, по показаниям — антибактериальную терапию, анаболики (неробол, ретаболил), эссенциале.
Летальность при геморрагическом шоке зависит от времени устранения кровотечения, объема кровопотери и проведения мероприятий интенсивной терапии. В настоящее время она составляет около 15% от всех случаев.
Большое значение после интенсивной терапии имеет реабилитационная терапия, лечебная гимнастика.
Что предпочтительнее для возмещения глобулярного объема при геморрагическом шоке
Советы по тактике при геморрагическом шоке от кровотечения
1. Что такое геморрагический шок?
Это уменьшение объема циркулирующей крови в результате кровопотери. Быстрая остановка кровотечения и гемотрансфузия способствуют снижению летальности, которая все равно остается очень высокой.
2. Что такое необратимый геморрагический шок?
В 1940 году Уиггерс (C.J. Wiggers) продемонстрировал, что геморрагический шок вызывает такие изменения в организме, которые не устраняются простым возмещением кровопотери. Восемьдесят процентов животных, у которых был вызван тяжелый геморрагический шок, погибли в течение 24 часов, несмотря на реинфузию им выпущенной крови.
«Необратимый шок» обусловлен продолжающейся потерей плазмы в результате ее утечки из сосудистого русла между эндотелиальными клетками и развитием изотонического отека скелетных мышц. Уиггерс доказал, что эти потери можно компенсировать дополнительной инфузией солевых изотопических растворов.
3. Какова классификация геморрагического шока?
Первый класс кровопотери: объем циркулирующей крови (ОЦК) снижается на 15%; клинические симптомы кровопотери практически отсутствуют; иногда наблюдается тахикардия.
Второй класс кровопотери: ОЦК снижается на 15-30% (750-1500 мл у больного весом 70 кг); развивается тахикардия, тахипноэ, снижается систолическое давление.
Третий класс кровопотери: ОЦК снижается на 30-40% (приблизительно 2000 мл для взрослых); развивается тахикардия, тахипноэ, угнетение сознания, гипотензия, уменьшается количество мочи.
Четвертый класс кровопотери: ОЦК уменьшается более чем па 40%, что сразу представляет опасность для жизни; развивается резкая тахикардия, значительное снижение систолического давления вплоть до исчезновения пульса на периферических артериях, прекращается фильтрация мочи почками, кожные покровы становятся холодными и бледными.
4. Чему равен в норме ОЦК?
В норме ОЦК составляет 7% веса тела взрослых, что приблизительно составляет 70 мл/кг. У детей ОЦК составляет 9% веса тела или 90 мл/кг.
5. Какие механизмы ведут к гипотензии?
Около 70% ОЦК приходится на венозную систему и обеспечивает преднагрузку сердцу. Уменьшение объема венозной крови приводит к снижению наполнения сердца. Согласно закону Старлинга, чем больше растягивается сердечная мышца, тем выше сократительная способность сердца. С другой стороны, снижение наполнения сердца приводит к ослаблению сокращения, уменьшению ударного объема и сердечного выброса.
Кроме того, стойкий геморрагический шок ведет к деполяризации мембран в скелетных мышцах, что способствует перемещению воды из внеклеточного пространства внутрь клетки. Это перемещение вызывает дальнейшее снижение ОЦК.
6. Как организм компенсирует снижение ОЦК?
Резкое снижение давления в крупных сосудах приводит к возбуждению симпатической нервной системы и освобождению эндогенных катехоламинов. Эта реакция в сочетании с угнетением вагусного центра в стволе мозга (рефлекс Марея (Marey)) вызывает вазоконстрикцию, тахикардию, повышение силы сердечных сокращений.
Сосуды по-разному воспринимают стимулы к вазоконстрикции (принципы демократии при этом не учитываются); самую высокую способность к вазокопстрикции проявляют кожные, брыжеечные и почечные сосуды. Снижение почечного кровотока ведет к освобождению ренина, который способствует превращению ангиотензина-1 в ангиотензин-2.
Ангиотензин-2 является потенциальным вазоконстриктором и также стимулирует освобождение альдостерона и антидиуретического гормона гипофиза. При этом усиливается реабсорбция натрия и воды в почечных канальцах, что, в свою очередь, увеличивает объем циркулирующей жидкости.
7. Меняется ли с возрастом способность к компенсации снижения ОЦК?
8. Как реагируют клетки на геморрагический шок?
При неадекватном кровоснабжении и оксигенации клетки неспособны осуществлять нормальный аэробный метаболизм, что приводит к образованию молочной кислоты и развитию метаболического ацидоза. Снижается образование аденозин-трифосфата (АТФ), и клетка не может поддерживать поляризованность мембраны.
Первым тому свидетельством становится набухание эндоплазматического ретикулума, затем повреждаются митохондрий, выбрасываются лизосомальпые ферменты и внутрь клетки поступают натрий и вода. Депонирование воды в клетках увеличивает дефицит межклеточной жидкости и объема циркулирующей в сосудах крови.
9. Каковы клинические симптомы геморрагического шока?
Частый пульс и низкое систолическое давление. При инвазивном мониторинге выявляется снижение диуреза, центрального венозного давления, давления заклинивания в легочных капиллярах, сердечного выброса и насыщения кислородом смешанной крови.
10. Можно ли исключить геморрагический шок, если гематокрит в норме?
Нет. Концентрация эритроцитов снижается только после инфузии экзогенной жидкости или после перемещения интерстициальной жидкости в кровяное русло. Если не проводить инфузионную терапию, то второе обычно происходит через 24 часа после развития шока.
11. Чем геморрагический шок отличается от других видов шока?
Кардиогенный констриктивный шок (в результате тампонады сердца или напряженного пневмоторакса) характеризуется повышением центрального венозного давления и уравниванием давлений в правых и левых отделах сердца. Нейрогенный шок напоминает геморрагический, поскольку в основе его лежит снижение объема циркулирующей жидкости за счет депонирования крови в венах и снижения тонуса артерий ниже уровня повреждения спинного мозга.
Септический шок может развиться у травматологических больных, которые обратились за медицинской помощью с опозданием. Первыми симптомами септического шока являются лихорадка, теплые розовые кожные покровы и повышенный сердечный выброс.
12. Что такое тахикардия?
Тахикардией считается количество сердечных сокращений >160 ударов в минуту у детей первых дух лет жизни, > 140 ударов в минуту у детей дошкольного возраста и > 100 ударов в минуту у взрослых. Будьте внимательны, больной может принимать препараты, урежающие сердечный ритм (например, b-блокаторы).
13. Где может “потеряться” кровь при кровопотере?
В отличие от явной потери крови при наружных повреждениях, кровь может скапливаться в брюшной и грудной полостях, забрюшинном пространстве (после перелома костей таза) и бедрах. Эта скрытая потеря крови может перевести геморрагический шок в необратимую стадию и привести к летальному исходу.
14. Каковы первостепенные лечебные мероприятия при геморрагическом шоке?
Остановить кровотечение и восполнить объем циркулирующей жидкости. В первую очередь нужно поставить широкопросветный периферический внутривенный катетер (14G или 16G). Закон Пуазейля гласит, что сопротивление жидкости пропорционально четвертой степени радиуса просвета катетера. Если периферическую вену катетеризировать не удается, нужно катетеризировать центральную вену (бедренную, подключичную или внутреннюю яремную). У детей хорошо себя зарекомендовали внутрикостные катетеры, введенные в большеберцовую кость.
15. В каком количестве и какой тип жидкости нужно назначить в первую очередь?
Взрослым нужно быстро перелить 1-2 литра подогретого Рингер-лактата. Маленьким детям инфузию проводят из расчета 20 мл/кг веса.
16. Нужно ли применять коллоидные растворы для лечения геморрагического шока?
Споры относительно преимуществ кристаллоидных и коллоидных растворов (растворы альбумина или декстранов) при лечении геморрагического шока продолжаются. Мета-анализ многочисленных проспективных клинических исследований указывает па снижение летальности у травматологических больных при восстановлении объема циркулирующей жидкости кристаллоидными растворами в отличие от коллоидных растворов.
Как ни странно, эти исследования не выявили между реанимацией кристаллоидными либо коллоидными растворами никаких различий во влиянии на развитие отека легких, необходимость гемотрансфузии или продолжительность госпитализации.
17. В каких случаях необходимо сразу провести гемотрансфузию?
В критических ситуациях проводится трансфузия эритроцитарной массы первой группы резус-отрицателыюй без перекрестного совмещения (резус-ноложительную кровь можно использовать у мужчин, которым ранее гемотрапсфузии не проводились; женщинам всегда переливают резус-отрицательиую кровь во избежание сенсибилизации, которая может осложнить будущие беременности).
18. Каковы физиологические осложнения гемотрансфузии?
Наиболее распространенным осложнением является гипотермия, вызванная переливанием холодной крови. Эта проблема может быть устранена, если контейнер крови поместить в быстросогревающую систему. Замещение кровопотери только эритроцитарной массой и кристаллоидными растворами может привести к разбавлению факторов свертывания. В этих случаях необходимо дополнительное переливание свежезамороженной плазмы.
При переливании донорской крови, содержащей цитрат, требуется дополнительное введение кальция (после трансфузии каждых четырех доз крови вводят 250 мг глюконата кальция). Существуют доказательства того, что долго хранящаяся кровь содержит продукты распада жиров, которые способствуют развитию воспаления с повреждением тканей и последующей полиорганной недостаточностью. Медиатором процесса являются нейтрофилы.
Кроме того, во время гемотрапсфузии существует риск заражения гепатитами В и С, ВИЧ-инфекцией и вирусом Т-клеточной лимфомы человека.
19. Существует ли альтернатива переливанию донорской крови?
С экономической точки зрения достаточно выгодна аутотрансфузия крови, полученной при эвакуации гемоторакса через торакостомический дренаж. Кровь собирают, фильтруют, смешивают с антикоагулянтами (цитратом) и возвращают больному. Иногда используются аппараты для сбора крови во время операции и последующей ее реинфузии. Однако количество крови, пригодной к реинфузии, ограничено.
В настоящее время нельзя купить настоящий заменитель крови, однако несколько таких препаратов находятся на стадии апробации Управления по контролю за качеством пищевых продуктов и лекарственных средств (FDA). Эти кровезаменители содержат различные виды очищенного гемоглобина (без эритроцитов), молекулы которого химически связаны, что задерживает его выделение с мочой. Действие кровезаменителей напоминает нативный гемоглобин, но период их полувыведения достаточно короткий.
Кровезаменители не нужно совмещать с кровью больного; они не содержат инфекционных возбудителей и гораздо дольше могут храниться при комнатной температуре.
20. Почему геморрагический шок вызывает нарушение функции внутренних органов?
Тяжелый геморрагический шок запускает мощную воспалительную реакцию, которую иногда не удается остановить даже соответствующими реанимационными мероприятиями. Во время вьетнамской войны раненым оказывалась своевременная медицинская помощь. Тем не менее у лиц, перенесших геморрагический шок, позднее развивалась легочная недостаточность или респираторный дистресс-синдром взрослых (РДСВ).
Больных с РДСВ можно перевести па искусственную вентиляцию легких, но в дальнейшем они погибнут от сочетанной недостаточности печени, почек, сердца и костного мозга (т.е. тяжелой нолиоргапной недостаточности). Полиорганная недостаточность остается ведущей причиной поздней посттравматической летальности. Помимо нарушения синтеза АТФ, при шоке освобождаются фактор активации тромбоцитов, интерлейкин-8 и метаболиты арахидоновой кислоты, которые способствуют адгезии нейтрофилов к эндотелиальным клеткам и освобождению цитотоксичных медиаторов.
Происходит повреждение внутренних органов. Мезентериальное кровяное русло является очагом синтеза нровоспалительных веществ (кишечник — двигатель полиорганной недостаточности). Помимо непосредственной активации нейтрофилов, в мезентериальных сосудах происходит освобождение нровоспалительных веществ в лимфатическую систему, что также способствует активации нейтрофилов и повреждению легких.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Чурсин В.В. Трансфузионная терапия при острой массивной кровопотере (методические рекомендации)
Информация
Список сокращений
Введение
Тактика интенсивной терапии при острой массивной кровопотере
Всё это верно при единственном условии – достаточный газообмен в лёгких. Это, в свою очередь, при корректной ИВЛ и отсутствии органических поражений лёгких, будет зависеть только от перфузии лёгких.
Таким образом, всё зацикливается на достаточной перфузии в малом и большом кругах кровообращения. От чего же зависит перфузия? Основных фактора два: производительность сердца и сосудистый тонус.
Механизм компенсации острой кровопотери общеизвестен: при уменьшении ОЦК происходит, в первую очередь, уменьшение ёмкости венозной системы (1 этап), что поддерживает преднагрузку на достаточном уровне. Далее, при увеличении концентрации катехоламинов, спазмируются артериолы (2 этап) и развивается централизация кровообращения (3 этап), характеризующаяся генерализованным спазмом сосудов, за исключением сосудов мозга и лёгких, а также коронарных артерий.
Если в этот момент не помочь организму, то защитная реакция переходит в патологическую. Причин тому несколько: резко повышается нагрузка на миокард вследствие увеличения постнагрузки, развивается ишемия в органах и тканях, принесённых в жертву ради спасения мозга, нарушается гуморальная регуляция из-за метаболической интоксикации и выброса биологически активных веществ из повреждённых и ишемизированных тканей и т.д. В итоге, организм, спасая одно, губит всё.
Коагулопатии
Гемостатики
Этамзилат (Дицинон). Препарат увеличивает образование в стенках капилляров мукополисахаридов большой молекулярной массы и повышает устойчивость капилляров, нормализует их проницаемость при патологических процессах, улучшает микроциркуляцию. снижает время кровотечения. Стимулирует физиологические механизмы свертывающей системы крови, уменьшая время кровотечения и увеличивая чиcло тромбоцитов, их активность и период жизни в кровяном русле. Его действие проявляется в значительном статистическом уменьшении времени кровотечения, а также в умеренном увеличении числа тромбоцитов. Оказывает гемостатическое действие, которое обусловлено активацией формирования тромбопластина в месте повреждения мелких сосудов.
Препарат стимулирует образование фактора свертывания крови III, нормализует адгезию тромбоцитов. Препарат не влияет на протромбиновое время, не обладает гиперкоагуляционными свойствами и не способствует образованию тромбов.
Транексамовая кислота относится к синтетическим ингибиторам фибринолиза и, вследствие своего структурного сходства с лизином, способна по конкурентному типу блокировать процесс активации плазминогена, предупреждая лизис тромба в зоне повреждения сосуда. Следовательно, этот препарат, как и другие ингибиторы фибринолиза теоретически целесообразно использовать для остановки кровотечения, связанного с первичной системной или местной активацией фибринолиза.
На практике, однако, выполнение этого правила представляет серьезную проблему, поскольку предполагает необходимость лабораторно и визуально подтвердить показания к назначению препарата и исключить другие возможные причины кровотечения. Более того, при диссеминированном сосудистом свертывании крови или в случае массивного кровотечения, вызвавшего системное повышение гемостатического потенциала в комплексе с гиповолемией и гиподинамией кровообращения, целенаправленное стремление блокировать фибринолиз может оказаться опасным, а введение ингибиторов – усилить нарушения микроциркуляции и ишемию внутренних органов, повысить риск артериальных и венозных тромбозов. Такая точка зрения хорошо известна. Она основана на современных представлениях о механизмах тромбообразования и фибринолиза, и, в целом, является ответом на вопрос о том, почему, несмотря на явный гемостатический эффект введения ингибиторов фибринолиза, во многих клинических ситуациях использование этих препаратов в плановой хирургии остается довольном редким явлением.
Другой целью систематического обзора, выполненного ассоциацией Кохрана было сравнительное изучение эффективности трех наиболее широко используемых в мировой клинической практике ингибиторов фибринолиза: апротинина, эпсилон-аминокапроновой кислоты и транексамовой кислоты. В сравнительных исследованиях этих препаратов некоторые преимущества были отмечены у апротинина, однако статистически значимыми они оказались только для определенной группы кардиохирургических больных с высоким риском. В остальных областях хирургии достоверных отличий по эффективности ТСК и апротинина не выявлено, при этом, однако установлено, что по антифибринолитической активности транексамовая кислота значительно превосходит эпсилон-аминокапроновую кислоту.
Таким образом, учитывая отличия в стоимости препаратов, по показателю «цена – эффект» использование ТСК во многих клинических ситуациях может быть наиболее перспективным. Например, это может касаться операции тотального протезирования коленного сустава – вмешательства, при котором целесообразность применения ТСК можно считать наиболее обоснованным.