Чем лечить инфекционный мононуклеоз у взрослого
Мононуклеоз: мифы и реальность
Распространённые мифы о мононуклеозе.
Статью подготовила Елена Колганова- врач-педиатр клиники DocDeti.
Мононуклеоз является вирусным заболеванием, возбудителем которого выступает вирус Эпштейна-Барр (ВЭБ).
1. Поражённые белым налётом миндалины, как при ангине.
2. Увеличенные печень и селезенка
3. Увеличенные лимфоузлы на шее, в некоторых случаях до такой степени, что могут мешать голове поворачиваться.
4. Аденоиды-затрудненное носовое дыхание, храп.
Ряд неспецифических симптомов интоксикации при мононуклеозе:
В большинстве случаев течение данного заболевания не сопровождается симптомами, а у детей к 5-ти летнему возрасту, в 50% случаев, уже имеются антитела к ВЭБ.
Если говорить о взрослом населении, то в 90-95% случаев, в организме имеются защитные титры антител против мононуклеоза, т.к они перенесли эту инфекцию в раннем возрасте.
Для борьбы с симптомами инфекционного мононуклеоза педиатром может быть назначен антибиотик амоксисциллин/ампициллин. У детей, которые получают данные препараты, в 85% случаях наблюдается появление сыпи на теле, которая сопровождается пятнами и зудом. Такая сыпь может задержаться на длительное время (до трех месяцев).
Даже после полного выздоровления, на протяжении пары месяцев ВЭБ может проявляться в слюне. На протяжении всей жизни, без всяких симптомов и клинических изменений, ВЭБ может выделяться у человека. Это и вызывает передачу вируса.
Если в слюне у здорового человека обнаружили ВЭБ, то никаких лечебных действий проводить не нужно!
1. В случае, если был перенесён мононуклеоз, то про отпуск на море можно забыть.
2. Раньше встречалось мнение, что ВЭБ под влиянием УФ-лучей принимает онкогенную активность и увеличивает возможные риски развития онкозаболеваний крови-лейкозов. Но такая связь не подтверждена в ходе современных клинических исследований. Отмечается возможная причастность ВЭБ к развитию лимфомы Беркетта, назофарингеальной карциномы и определённых видов рака желудка. Но это самостоятельные заболевания, а не проявление мононуклеоза. Развиться они могут у людей, имеющих к этому предрасположенность и сопутствующую тяжелую патологию: СПИД, малярию, первичные иммунодефициты. Лимфома Беркетта распространена в странах Африки, а назофарингеальная карцинома – в Китае.
4. Ещё одно распространённое заблуждение заключается в том, что нужно избегать посещения детских коллективов и противопоказана вакцинация в течении 6-12 месяцев. Эти советы не нашли подтверждения в ходе международных исследований, а значит не имеют обоснования. Перенесенный мононуклеоз не является противопоказанием к прививкам, а находиться в детских коллективах можно сразу, после улучшения самочувствия у ребёнка.
5. Большим заблуждением считается хронический мононуклеоз, которым ребёнок страдает несколько лет и излечить его можно только сложной схемой приёма иммуномодуляторов. Инфекционный мононуклеоз является острой инфекцией, продолжительность которой 3-4 недели. После перенесенного заболевания, на протяжении 3-4 месяцев может наблюдаться состояние, которое похоже на хроническую усталость (вялость, бледность, сонливость, отсутствие интереса к играм, апатия). Лечить это состояние не нужно, его нужно просто пережить.
Инфекционный мононуклеоз: симптомы и лечение у детей и взрослых
Мононуклеоз (иногда его называют моноцитарной ангиной или доброкачественным лимфобластозом) – инфекционное вирусное заболевание. Передается воздушно-капельным, а также бытовым путем. Мононуклеозом чаще болеют дети и подростки. После сорока лет болезнь встречается редко, поскольку взрослые люди имеют иммунитет, который образуется на всю жизнь.
Дети раннего возраста переносят недуг легче, чем подростки и взрослые. Чаще всего болеют мононуклеозом в возрасте 14-17 лет. Инкубационный период составляет от 1 до 6,5 недель. Заболевание обычно протекает с высокой температурой и поражением лимфатических узлов, часто страдают печень и селезенка.
Патология опасна своими осложнениями. При отсутствии правильного лечения она может стать хронической.
Возбудитель
Возбудитель – вирус Эпштейна-Барра. Он принадлежит к семейству Herpesviridae, то есть является одним из вирусов герпеса. Отличается тем, что вызывает не гибель клеток, а их усиленный рост. Способен к размножению в B-лимфоцитах.
Симптомы инфекционного мононуклеоза
Для мононуклеоза характерны такие симптомы:
Диагностика
При подозрении на наличие инфекции врач всегда делает анализ крови и по результатам ставит точный диагноз.
При поражении B-лимфоцитов организм начинает вырабатывать специфические клетки очень характерного вида, называемые мононуклеарами. Они и дали название этой болезни. При патологии в крови должны обнаруживаться антитела к вирусу Эпштейна-Барра. Чтобы исключить стрептококковую ангину, может понадобиться анализ мазков из горла.
Течение заболевания
При правильном лечении острая фаза болезни длится одну-две недели, затем наступает выздоровление.
Однако иногда патология приобретает хроническую форму и длится годами. Обычно это наблюдается во взрослом возрасте. При хроническом течении недуга больной постоянно испытывает слабость, боль в горле и суставах. Из-за сниженного иммунитета пациент регулярно страдает от простудных заболеваний.
Осложнения
Как правило, прогноз благоприятный, но иногда могут встречаться следующие осложнения, характерные для острой и хронической формы:
Лечение
Специфического лечения не существует. Антибактериальную терапию назначают только в том случае, если на фоне вирусной инфекции развиваются какие-либо бактериальные поражения. Противопоказаны «Оксациллин» и «Ампициллин» из-за высокой частоты развития аллергических реакций.
Функциональное состояние печени при инфекционном мононуклеозе у взрослых
Инфекционный мононуклеоз — широко распространенное инфекционное заболевание. Для инфекционного мононуклеоза характерна выраженная полиорганность процесса, растянутый лихорадочный период, вариабельность клинической картины, несоответствие симптомов течени
Инфекционный мононуклеоз — широко распространенное инфекционное заболевание. Для инфекционного мононуклеоза характерна выраженная полиорганность процесса, растянутый лихорадочный период, вариабельность клинической картины, несоответствие симптомов течения болезни выраженности биохимических изменений
Инфекционный мононуклеоз — широко распространенное инфекционное заболевание. Особенностью патогенеза инфекционного мононуклеоза (ИМ) является клинический полиморфизм и поражение иммунной системы, при котором стимулируется синтез иммуноглобулинов, что может провоцировать появление злокачественных лимфопролиферативных заболеваний [6; 7; 9; 10; 11].
 |
| Рисунок 1. Функциональное состояние печени определяется с помощью биохимического анализатора ЭББОТ VP (США) |
Как правило, отмечается выраженная полиорганность процесса, при которой поражение ротоглотки встречается довольно часто и, по данным одних авторов, носит вирусный характер, по мнению других — бактериальный [5] или смешанный вирусно-бактериальный [4; 12;].
При лечении антибиотиками (в частности, ампициллином) нередко наблюдаются аллергические осложнения. Еще одной особенностью ИМ является растянутый во времени лихорадочный период, по-видимому обусловленный ангинозным процессом.
Обнаружение характерных принципов поражения органов, в частности печени, крайне важно для выявления типичных биохимических сдвигов и понимания особенностей патогенеза с целью коррекции проводимой терапии. Под нашим наблюдением находилось 26 больных ИМ средней степени тяжести, поступивших в клинику на 10 — 15-й день болезни. У всех больных заболевание характеризовалось подострым постепенным началом —субфебрильной температурой в течение 5—7 суток, умеренными болями в горле при глотании, болями в области шеи за счет увеличения лимфатических узлов, а также постепенным нарастанием признаков интоксикации.
На момент поступления в стационар интоксикация отмечалась у всех больных, лимфоаденопатия — в 95% случаев, причем увеличивались в большей степени лимфатические узлы шейной группы, ангина выявлялась в 85% случаев, гепатомегалия — в 80%, тогда как желтуха наблюдалась только в 25% случаев, а спленомегалия — в 20% случаев.
В 55% случаев после применения ампициллина заболевание осложнялось появлением сыпи токсико-аллергического характера.
Инфекционный мононуклеоз диагностировался на основании клинической картины заболевания (наличия лихорадки и симптомов интоксикации, полилимфаденопатии, ангины, гепатоспленомегалии), эпидемиологического анамнеза, а также по характерным лабораторным данным:
а) в периферической крови наблюдался лимфоцитоз, выявлялись атипичные мононуклеары с широкой светлой базофильной протоплазмой;
б) при серологическом исследовании крови реакция Хофф-Бауэра была положительной в 100% случаев.
Анализ биохимических данных показал (см. таблицу), что у больных рассматриваемой группы изменены основные биохимические параметры, преимущественно связанные с ферментами печени. Во всех случаях отмечается повышение уровня активности АЛТ и ЩФ, реже АСТ и ГГТ. Отмечается повышение тимолового показателя, что свидетельствует о выраженных диспротеинемических сдвигах, вероятно связанных с появлением в крови дополнительных белковых фракций [2].
Характеристика основных биохимических параметров у больных инфекционным мононуклеозом средней тяжести
Наблюдается изменение уровней билирубина и мочевины в крови. Детальный биохимический анализ позволил выявить, что инфекционный мононуклеоз характеризуется цитолизом в печени со значительным повышением АЛТ в среднем до 414 МЕ/л и повышением АСТ в среднем до 260 МЕ/л, а также выраженным снижением коэффициента де Ритиса до 0,73 при норме больше 1. Все это свидетельствует об энзимологических признаках поражения печени. Значительный разброс коэффициента де Ритиса (от 0,2 до 3,19) свидетельствует не только о признаках поражения печени, но и о вероятном поражении сердца у некоторых больных. Более тщательный анализ этого коэффициента позволил выделить биохимически два типа цитолиза. У 15 больных из рассмотренной группы коэффициент де Ритиса оказался меньше 1, а у остальных — больше 1, что, безусловно, свидетельствует о разнокачественности цитолиза: в первом случае, с преобладанием АСТ, доминирует «сердечный» тип цитолиза, а во втором отмечается «печеночный».
Превышение активности АСТ над АЛТ в пределах нормальных значений обычно характерно для здоровых людей. Однако повышение АСТ с одновременным ростом отношения АСТ/АЛТ (коэффициент де Ритиса больше 2) свидетельствует о поражении сердца, это же отношение с коэффициентом де Ритиса, меньшим 1, говорит о поражении печени. Высокие уровни ферментемии при всех видах вирусного гепатита характеризуются низким коэффициентом де Ритиса (за исключением дельта-гепатита) и являются прогностически неблагоприятным признаком течения болезни.
При клиническом наблюдении за больными ИМ не отмечалось признаков поражения сердечно-сосудистой системы, однако при электрокардиографическом исследовании у 38% больных выявлялись признаки поражения сердца, заключавшиеся в изменении конечной части желудочкового комплекса.
Нами было установлено, что основную группу составили 18 больных, у которых значения АЛТ доходили до 200 МЕ/л, а то время как повышение АСТ до этого уровня отмечалось у 25 больных. Таким образом, эти данные указывают как на сочетание поражения органов (печень, сердце), так и на скорее диффузное, чем локальное поражение печени.
Встречались отдельные больные с гигантскими значениями ферментемии по АСТ и АЛТ.
Уровень активности ЩФ, в среднем равный 380 МЕ/л (разброс значений от 80 до 780), указывает на несколько возможных источников (костная ткань, кишечник, печень, лимфатическая система) ее происхождения или на высокую активность процесса в одном из них. Уровень активности ГГТ, относящейся к мембранным структурам, как и ЩФ, равный в среднем 75 МЕ/л (от 2 до 380), указывает на заинтересованность мембранных структур различных клеток, однако соотношение ЩФ/ГГТ характеризуется выраженным превалированием первого фермента над вторым (в среднем 18,1).
Сумма активности ЩФ+ГГТ преобладает над суммой АСТ+АЛТ. Это, во-первых, отличает ИМ от вирусного гепатита и, во-вторых, показывает, что «холестатическая пара» явно доминирует над «цитолитической» в основном за счет гигантских значений ЩФ (у 16 больных ЩФ выше 400 МЕ/л), в связи с чем коэффициент ЩФ/ГГТ имеет значительную вариабельность, но с обязательным превышением ЩФ над ГГТ в среднем до 18.
Повышенное СОЭ указывает на признаки грубого повреждения форменных элементов крови (это подтверждается спленомегалией, появлением билирубина в моче, а также случаями желтухи), что увеличивает функциональную нагрузку на печень, связанную с детоксикацией продуктов разрушения гемоглобина. Все это происходит на фоне диспротеинемии и сопровождается одновременным снижением уровня общего белка в среднем до 63,4 г/л — вероятно, за счет подавления белок-синтетической функции, что подтверждается и снижением уровня мочевины.
Нормальный уровень билирубина указывает на эффективную детоксицирующую функцию печени, несмотря на то, что потемнение мочи свидетельствует об усилении распада эритроцитов. Высокий уровень общей ЛДГ можно считать дополнительным признаком компенсируемого распада эритроцитов, в которых она богато представлена [1; 3].
Высокие значения ЩФ и ГГТ вряд ли могут быть результатом холестаза, поскольку уровень ЩФ слишком высок, а уровень ГГТ не соответствует уровню ЩФ. Все это происходит на фоне функциональной диспротеинемии, подтверждаемой умеренным повышением тимолового показателя до 33 (от 2 до 68 ед.).
Повышенный в среднем до 570 мг% уровень b-ЛП указывает на изменения в обмене липидов при данной инфекции или является результатом гепариновой недостаточности, вызванной тромбогеморрагическими расстройствами, так как гепарин является активатором липолиза в липопротеидах и его потребление значительно возрастает при гемореологических нарушениях. Однако все вышеперечисленные причины вряд ли объясняют столь высокие уровни ЩФ. Нам кажется более вероятным считать ее происхождение из бурно разрастающейся лимфоидной ткани, строма которой богато представлена ЩФ.
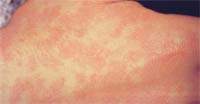 |
| Рисунок 2. Сыпь при инфекционном мононуклеозе |
Анализ биохимических данных выявил во всех рассмотренных случаях поражение печени с гигантскими уровнями АЛТ, которые клинически не всегда сочетались с биохимическими нарушениями. Клинические признаки поражения печени у этих больных проявлялись в гепатомегалии, субиктеричности склер, в ряде случаев анорексии. Динамика показателей и их уровни указывают на явно выраженный цитолитический компонент. Повышение ЩФ и ГГТ, традиционно рассматриваемое как признак холестаза, не сочетается (за единичными исключениями) с повышением билирубина, а значительное превышение ЩФ над ГГТ ставит вопрос о дополнительном источнике ее появления (кости, кишечник, лимфоидная ткань). Аналогичная патология у детей протекает с понижением уровня ЩФ даже при обязательной для их возраста ферментемии, по данным М. А. Гаспарян [4]. Вполне допустимо предположение, что в определенный момент заболевания происходит компенсаторное торможение функционирования костной ткани, что проявляется в обратном (по сравнению со взрослыми) феномене. Низкие по отношению к ЩФ значения ГГТ, возможно, указывают на подавление детоксицирующей системы печени в патогенезе данной инфекции. Так, более детальный анализ показал сохранение нормальных значений ГГТ в 30% общего числа наблюдений, что как раз и указывает не на поражение, а на заинтересованность детоксицирующей системы организма [5], к которой она и относится.
Хотя анализ биохимических данных и выявляет несоответствие между лабораторными и клиническими показателями (компенсированный вариант цитолиза), но значительная вариативность биохимических изменений в общем соответствует клиническому, иммунологическому и гуморально-клеточному полиморфизму ИМ.
Таким образом, анализ биохимических данных у больных инфекционным мононуклеозом выявил следующее: во-первых, характерную для ИМ картину энзимологических сдвигов – преобладание мембранно-холестатической пары над цитолитической за счет преимущественного повышения ЩФ; во-вторых, несоответствие клинического течения болезни выраженности биохимических изменений. И, главное — повышение уровня ЩФ указывает на необходимость выявления источника ее происхождения, а не соответствующий ей уровень ГГТ свидетельствует о заинтересованности детоксицирующей системы организма, к которой она относится.
Литература
Данная страница не существует!
Услуги инфекционной клиники
Диагностика, профилактика и лечение
Фиброэластометрия и УЗ-диагностика молочных желез, щитовидной железы, мошонки, брюшной полости
Биохимия. Анализ крови: общий, клинический. Анализы на витамины, микроэлементы и электролиты. Анализ на ВИЧ-инфекцию, вирусные гепатиты, бактерии, грибки и паразиты
Максимально точное определение выраженности фиброза печени неинвазивным методом при помощи аппарата FibroScan 502 TOUCH
Гинеколог в H-Сlinic решает широчайший спектр задач в области женского здоровья. Это специалист, которому вы можете полностью доверять
Дерматовенерология в H-Сlinic — это самые современные и эффективные алгоритмы диагностики и лечения заболеваний, передающихся половым путем, грибковых и вирусных поражений, а также удаление доброкачественных невусов, бородавок, кондилом и папиллом
Возможности вакцинопрофилактики гораздо шире Национального календаря прививок. H-Clinic предлагает разработку плана вакцинации и современные высококачественные вакцины в наличии
Терапевт в H-Сlinic эффективно решает задачи по лечению заболеваний, которые зачастую могут становиться большой проблемой при наличии хронического инфекционного заболевания
Врач-кардиолог H-Сlinic проведет комплексную диагностику сердечно-сосудистой системы и при необходимости назначит эффективное терапию. Сердечно-сосудистые проблемы при инфекционных заболеваниях, требуют специфичных подходов, которые мы в состоянии обеспечить
Наша цель — новое качество вашей жизни. Мы используем современные диагностические алгоритмы и строго следуем наиболее эффективным протоколам лечения.
Общая терапия, Инфекционные заболевания, Гастроэнтерология, Дерматовенерология, Гинекология, Вакцинация, УЗИ и фиброэластометрия, Кардиология, Неврология
Биохимия, Общий/клинический анализ крови, Витамины и микроэлементы/электролиты крови, ВИЧ-инфекция, Вирусные гепатиты, Другие инфекции, бактерии, грибки и паразиты, Комплексы и пакеты анализов со скидкой
В наличии и под заказ качественные бюджетные решения и препараты лидеров рынка лечения инфекционных болезней. Аптека H-Clinic готова гибко реагировать на запросы наших клиентов. Мы поможем с оперативным поиском препаратов, которые обычно отсутствуют в сетях.
Инфекционный мононуклеоз
Инфекционный мононуклеоз – острое проявление вирусного заболевания, клинически затрагивающее ротовую область, глотку, селезенку, печень и лимфоузлы. Провокатор его возникновения – герпесвирус Эпштейна-Барра, встречающийся как у взрослых, так и среди детей.
Распространенность недуга не зависит от времени года или пола человека. Впрочем, исследователи выявили некоторую закономерность: у подростков, проходящих пубертатный период, болезнь определяется чаще.
Основные причины
Причина инфекционного мононуклеоза одна – вирус Эпштейна-Барра. Им можно заразиться после контакта с заболевшим человеком. Так как частицы вируса сохраняются в слюне носителя, то основной способ передачи его – воздушно-капельный.
Поймать вирус можно, воспользовавшись одними предметами обихода с зараженным носителем. Часто передача происходит половым путем, а также через поцелуи, невымытые руки, посуду и т.д.
В некоторых случаях вирус передается в момент переливания крови, а также от матери к малышу в период вынашивания.
Наиболее подвержены болезни люди с ослабленным иммунитетом, острой нехваткой полноценного сна и рационального питания.
Симптоматика недуга
Симптомы инфекционного мононуклеоза проявляются не сразу: инкубационный период может колебаться в промежутке от 5 до 45 дней. В некоторых случаях заболевший может отмечать у себя следующие первичные признаки:
Постепенно проявления увеличивают свою интенсивность, к ним добавляются такие симптомы:
Спустя время заболевший замечает:
Если обратиться к врачу, то тот может обратить внимание на увеличение размеров селезенки и печени и симптомы фолликулярной, катаральной или язвенно-некротической ангины. К ним относятся увеличение миндалин, желтоватый налет на стенках глотки, возможна легкая кровоточивость.
Инфекционный мононуклеоз у детей по своим проявлениям схож с данным недугом у взрослых, отличаясь лишь повышенной скоростью развития.
После того, как печень и селезенка увеличиваются, они сразу дают сигнал об этом пожелтением глазных склер и кожи, а также более темным цветом мочи заболевшего. Могут наблюдаться кожные высыпания, сопровождающиеся легким зудом.
Возможные осложнения
Инфекционный мононуклеоз у взрослых и тем более детей игнорировать нельзя, так как он чреват осложнениями:
Диагностика недуга
В крови обнаруживаются атипичные мононуклеары. К слову, именно из-за них пациенту рекомендуется три раза с определенными промежутками времени проходить серологическое обследование, так как эти вещества характерны и для ВИЧ-инфекции.
Дополнительно сдается ПЦР для определения вируса Эпштейна-Барра и его активности в организме пациента. Могут быть дополнительно найдены М-иммуноглобулины.
При инфекционном мононуклеозе с характерными признаками ангины рекомендуется дополнительно осмотр отоларинголога.
Лечение заболевания
В зависимости от особенности протекания лечение инфекционного мононуклеоза может проходить в условиях стационара или дома. Больному полагается соблюдение постельного режима, а в некоторых случаях – еще и специальной диеты.
Комплекс лечения направлен на снятие интоксикации организма, симптомов, приведение его в стабильное состояние. Наряду с этим назначается витаминная терапия (качественное питание, витаминные комплексы по возрасту).
Тяжелые случаи инфекционного мононуклеоза с явно выраженными некротизирующими процессами требуют участия антибиотиков. В случае если имеет место разрыв селезенки, то в экстренном порядке осуществляется ее полное удаление.
Профилактические меры
Если заболевание проходит без серьезных осложнений и под наблюдением врача, прогноз благоприятный. После выздоровления в течение года рекомендуется несколько раз сдавать общий анализ крови и анализ на определение активности вируса Эпштейна-Барра.
К другим мерам профилактики инфекционного мононуклеоза относятся:
Ответы на распространенные вопросы
Как не заболеть инфекционным мононуклеозом?
К сожалению, полностью оградить себя от этого заболевания невозможно. Однако можно предпринять профилактические меры, чтобы снизить риск осложнений. В период простудных заболеваний желательно избегать мест большого скопления людей.
Какие могут быть последствия этой болезни?
Последствия инфекционного мононуклеоза – это осложнения, с которыми сталкивается ослабленный организм или тот, который не получил должного лечения. К ним относятся дополнительная бактериальная инфекция, менингоэнцефалит, гепатит. В большинстве основное последствие заболевания – падением иммунитета.
Инфекционный мононуклеоз: чем лечить?
Лечение подбирается врачом в индивидуальном порядке. Важно снять симптомы и токсическую нагрузку на организм. При наличии бактериальной инфекции – использовать антибиотики.
Не нашли ответа на свой вопрос?
Наши специалисты готовы проконсультировать вас по телефону:
Новые подходы к терапии инфекционного мононуклеоза

Инфекционный мононуклеоз — вирусное, широко распространенное заболевание, для которого характерна системность поражения с вовлечением в патологический процесс лимфоидных органов и тканей, сердечно-сосудистой, иммунной, систем, костного мозга, печени, селе
Infectious mononucleosis is a viral, widely-spread disease characterized by systemacy of the lesion, with involvement of lymphoid organs and tissues, cardiovascular and immune systems, marrow, liver, spleen and other organs in the pathological process. Comparative study of clinical and laboratory indices in the acute period of infectious mononucleosis was conducted, including treatment with human recombinant interferon alpha-2b, along with highly active antioxidants — C and E vitamins.
Герпесвирусные инфекции широко распространены среди детей и взрослых. По данным Всемирной организации здравоохранения (ВОЗ) до 90% взрослого и детского населения планеты инфицировано герпесвирусами, причем у 50% из них отмечают манифестное, рецидивирующее течение вызываемых ими заболеваний. Инфекционный мононуклеоз является наиболее характерным типичным клиническим проявлением герпесвирусных инфекций [1]. Инфекционный мононуклеоз (ИМ) — вирусное, широко распространенное заболевание, для которого характерна системность поражения с вовлечением в патологический процесс лимфоидных органов и тканей, сердечно-сосудистой, иммунной систем, костного мозга, печени, селезенки и других органов [2, 3]. В мире инфекционным мононуклеозом ежегодно заболевают от 16 до 800 лиц на 100 тыс. населения. В России ежегодно регистрируют 40–80 случаев ИМ на 100 тыс. населения [1, 2, 4]. Установлена роль вируса Эпштейна–Барр в развитии злокачественных новообразований, аутоиммунных, неврологических заболеваний и синдрома хронической усталости. Показано, что после перенесенной инфекции новое поколение В-клеток содержит несколько генокопий вируса Эпштейна–Барр в латентной форме, в результате чего вирус может длительно персистировать в организме, вызывая иммунодефицитное состояние и повышая риск развития онкогематологических заболеваний [5–7]. В последние годы доказана гепатотропность герпетических вирусов, которые могут вызывать различные поражения печени — от бессимптомного гепатита до гепатоцеллюлярной карциномы [2].
В связи с этим назначение интерферона α-2b человеческого рекомбинантного в комплексе с высокоактивными антиоксидантами витаминами Е и С (препарата Виферон®), обладающего иммуномодулирующими, противовирусными, антипролиферативными свойствами, подавляющего репликацию РНК- и ДНК-содержащих вирусов, могло бы способствовать более быстрому клиническому выздоровлению, оказать положительное влияние на лабораторные показатели и тем самым предотвратить хроническое течение.
Целью данного исследования явилось сравнительное изучение клинико-лабораторных показателей в острый период ИМ при лечении препаратом Виферон®.
В задачи иследования входило:
1) оценить эффективность использования симптоматической и патогенетической терапии у пациентов с ИМ;
2) оценить эффективность применения препарата Виферон® у пациентов с ИМ на фоне симптоматической и патогенетической терапии;
3) исследовать сравнительную эффективность лечения препаратом Виферон® с базисной стандартной терапией у пациентов с ИМ.
Материал и методы исследования
Проведено открытое проспективное рандомизированное контролируемое исследование в группах больных с острым ИМ. В исследование были включены 40 пациентов, больных острым ИМ средней степени тяжести, проходивших стационарное лечение в Воронежской областной клинической инфекционной больнице. Основная группа (1-я группа) — 20 пациентов, наряду с базисной терапией получала препарат рекомбинантного интерферона α-2b в комплексе с высокоактивными антиоксидантами витаминами Е и С Виферон®, и группа сравнения (2-я группа) — 20 пациентов, которым проводили только базисную стандартную терапию. Критерии включения пациентов были: лечение в стационаре, верифицированный диагноз ИМ, возраст старше 18 лет, поступавших в клинику на 1–5 день от начала заболевания и не получавших в домашних условиях препаратов интерферона и иммуномодуляторов, наличие информированного согласия на участие в исследовании.
Лечение пациентов в группах на всех этапах исследования осуществляли согласно стандартным режимам лечения (на основании основных положений Федеральных клинических рекомендаций по диагностике и лечению инфекционного мононуклеоза, 2013), включающего базисную стандартную терапию (дезинтоксикационная, десенсибилизирующая и антибактериальная терапия).
Набор больных в группы осуществляли методом пар, рандомизация проводилась с помощью генератора случайных чисел, больные в группах были сопоставимы по полу и возрасту.
Литература
* ФГБОУ ВО ВГМУ им. Н. Н. Бурденко Минздрава России, Воронеж
** БУЗ ВО ВОКИБ, Воронеж
*** ФГБУ НИЦЭМ им. Н. Ф. Гамалеи Минздрава России, Москва
Новые подходы к терапии инфекционного мононуклеоза/ Ю. Г. Притулина, В. В. Кунина, А. А. Монастырский, Т. Н. Малюткина, В. В. Малиновская, А. Н. Шувалов
Для цитирования: Лечащий врач № 9/2019; Номера страниц в выпуске: 57-59
Теги: герпесвирусные инфекции, иммунодефицитные состояния, интерферон
Современные подходы к лечению Эпштейна–Барр-вирусной инфекции у взрослых
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ).
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ). Практикующие врачи в своей повседневной практике чаще сталкиваются с клинически манифестными формами первичной Эпштейна–Барр-вирусной инфекции (ЭБВИ) в виде острой, как правило, не верифицированной респираторной инфекцией (более 40% случаев) или инфекционным мононуклеозом (около 18% всех заболеваний) [1, 2]. В большинстве случаев эти заболевания протекают доброкачественно и заканчиваются выздоровлением, но с пожизненной персистенцией ВЭБ в организме переболевшего [1, 3–5].
Однако в 10–25% случаев первичное инфицирование ВЭБ, протекающее бессимптомно, и острая ЭБВИ могут иметь неблагоприятные последствия [6–9] с формированием лимфопролиферативных и онкологических заболеваний, синдрома хронической усталости, ВЭБ-ассоциированного гемофагоцитарного синдрома и др. [7, 9, 11–14].
До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ВЭБ. Перед врачом, к которому обращается пациент с острой ЭБВИ, всегда встает вопрос: что предпринять в каждом конкретном случае, чтобы максимально снизить риск развития хронической ЭБВИ и ВЭБ-ассоциированных патологических состояний Этот вопрос не праздный, и ответить на него действительно очень трудно, т. к. до сих пор нет четкой патогенетически обоснованной схемы лечения больных, а имеющиеся рекомендации часто противоречат друг другу.
По мнению многих исследователей, лечение ЭБВИ-мононуклеоза (ЭБВИМ) не требует назначения специфической терапии [15–17]. Лечение больных, как правило, проводится в амбулаторных условиях, изоляция пациента не требуется. Показаниями к госпитализации следует считать длительную лихорадку, выраженный синдром тонзиллита и/или синдром ангины, полилимфаденопатию, желтуху, анемию, обструкцию дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, гематологических, со стороны сердечно-сосудистой и дыхательной системы, синдром Рейе).
При легком и среднетяжелом течении ЭБВ ИМ больным целесообразно рекомендовать палатный или общий режим с возвращением к обычной деятельности на адекватном для каждого конкретного больного физическом и энергетическом уровне. Проведенное многоцентровое исследование показало, что необоснованно рекомендуемый строгий постельный режим удлиняет период выздоровления и сопровождается длительным астеническим синдромом, требующим нередко медикаментозного лечения [18].
При легком течении ЭБВ ИМ лечение больных ограничивается поддерживающей терапией, включающей адекватную гидратацию, полоскание ротоглотки раствором антисептиков (с добавлением 2% раствора лидокаина (ксилокаина) при выраженном дискомфорте в глотке), нестероидные противовоспалительные препараты, такие как парацетамол (Ацетаминофен, Тайленол). По мнению ряда авторов назначение блокаторов Н2 рецепторов, витаминов, гепатопротекторов и местная обработка миндалин различными антисептиками являются малоэффективными и необоснованными способами лечения [19, 20]. Из экзотических методов лечения следует упомянуть рекомендуемое Ф. Г. Боковым и соавт. (2006) применение мегадоз бифидобактерий при лечении больных острым мононуклеозом [21].
Мнения о целесообразности назначения антибактериальных препаратов при лечении ЭБВИМ весьма противоречивы. По мнению Gershburg E. (2005) тонзиллит при ИМ часто асептический и назначение антибактериальной терапии не оправдано. Также нет смысла в применении антибактериальных средств при катаральной ангине [4]. Показанием для назначения антибактериальных препаратов является присоединение вторичной бактериальной инфекции (развитие у больного лакунарной или некротической ангины, таких осложнений, как пневмония, плеврит и др.), о чем свидетельствуют сохраняющиеся более трех суток выраженные воспалительные изменения показателей крови и фебрильная лихорадка. Выбор препарата зависит от чувствительности микрофлоры на миндалинах больного к антибиотикам и возможных побочных реакций со стороны органов и систем.
Противопоказаны препараты из группы аминопенициллинов (ампициллин, амоксициллин (Флемоксин Солютаб, Хиконцил), амоксициллин с клавуланатом (Амоксиклав, Моксиклав, Аугментин)) из-за возможности развития аллергической реакции в виде экзантемы. Появление сыпи на аминопенициллины не является IgE-зависимой реакцией, поэтому применение блокаторов Н1 гистаминовых рецепторов не имеет ни профилактического, ни лечебного эффекта [19].
По мнению ряда авторов до настоящего времени сохраняется эмпирический подход к назначению глюкокортикостероидов больным с ЭБВИ [23]. Глюкокортикостероиды (преднизолон, преднизон (Делтазон, Метикортен, Оразон, Ликвид Пред), Солу Кортеф (гидрокортизон), дексаметазон) рекомендуются больным с тяжелым течением ЭБВИМ, с обструкцией дыхательных путей, неврологическими и гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [4, 24]. Суточная доза преднизолона составляет 60–80 мг в течение 3–5 дней (реже 7 дней) с последующей быстрой отменой препарата. Одинаковой точки зрения на назначение этим больным глюкокортикостероидов при развитии миокардита, перикардита и поражениях ЦНС нет.
При тяжелом течении ЭБВИМ показана внутривенная дезинтоксикационная терапия, при разрыве селезенки — хирургическое лечение.
Наиболее дискуссионным остается вопрос о назначении противовирусной терапии больным с ЭБВИ. В настоящее время известен большой перечень препаратов, являющихся ингибиторами ВЭБ репликации в культуре клеток [4, 25–27].
По данным E. Gershburg, J. S. Pagano (2005) все современные «кандидаты» для лечения ЭБВИ могут быть разделены на две группы:
I. Подавляющие активность ДНК-полимеразы ВЭБ:
II. Различные соединения, не ингибирующие вирусной ДНК-полимеразы (механизм изучается): марибавир, бета-L-5 урацил йододиоксолан, индолокарбазол.
Однако проведенный метаанализ пяти рандомизированных контролируемых испытаний с участием 339 больных ЭБВИМ, принимавших ацикловир (Зовиракс), показал неэффективность препарата [28, 29].
Одна из возможных причин кроется в цикле развития ВЭБ, в котором ДНК вируса имеет линейную либо циркулярную (эписома) структуру и размножается в ядре клетки хозяина. Активная репликация вируса происходит при продуктивной (литической) стадии инфекционного процесса (ДНК ВЭБ линейной формы). При острой ЭБВИ и активации хронической ЭБВИ происходит цитолитический цикл развития вируса, при котором он запускает экспрессию собственных ранних антигенов и активирует некоторые гены клеток макроорганизма, продукты которых участвуют в репликации ВЭБ. При латентной ЭБВИ ДНК вируса имеет вид эписомы (круговой суперспиральный геном), находящейся в ядре. Циркулярный геном ДНК ВЭБ характерен для CD21+ лимфоцитов, в которых даже при первичном инфицировании вирусом практически не наблюдается литической стадии инфекционного процесса, а ДНК воспроизводится в виде эписомы синхронно с клеточным делением инфицированных клеток. Гибель пораженных ВЭБ В лимфоцитов связана не с опосредованным вирусом цитолизом, а с действием цитотоксических лимфоцитов [4].
При назначении противовирусных препаратов при ЭБВИ врач должен помнить, что их клиническая эффективность зависит от правильной трактовки клинических проявлений болезни, стадии инфекционного процесса и цикла развития вируса на этой стадии. Однако не менее важным является и тот факт, что большинство симптомов ЭБВИ связаны не с прямым цитопатическим действием вируса в инфицированных тканях, а с опосредованным иммунопатологическим ответом ВЭБ-инфицированных В лимфоцитов, циркулирующих в крови и находящихся в клетках пораженных органов. Именно поэтому аналоги нуклеозидов (ацикловир, ганцикловир и др.) и ингибиторы полимеразы (Фоскарнет), подавляющие репликацию ВЭБ и уменьшающие содержание вируса в слюне (но не санирующие ее полностью [4], не оказывают клинического эффекта на тяжесть и продолжительность симптомов ЭБВИМ.
Показаниями для лечения ЭБВИМ противовирусными препаратами являются: тяжелое, осложненное течение болезни, необходимость профилактики ВЭБ-ассоциированной В-клеточной лимфопролиферации у иммунокомпрометированных пациентов, ВЭБ-ассоциированная лейкоплакия. Bannett N. J., Domachowske J. (2010) рекомендуют применять ацикловир (Зовиракс) внутрь в дозе 800 мг внутрь 5 раз в сутки в течение 10 дней (или 10 мг/кг каждые 8 часов в течение 7–10 дней). При поражениях нервной системы предпочтителен внутривенный способ введения препарата в дозе 30 мг/кг/сут 3 раза в сутки в течение 7–10 дней.
По мнению E. Gershburg, J. S. Pagano (2005), если под действием каких-либо факторов (например, иммуномодуляторов, при ВЭБ-ассоциированных злокачественных опухолях — применение лучевой терапии, гемцитабина, доксорубицина, аргинина бутирата и др.) удается перевести ДНК ВЭБ из эписомы в активную репликативную форму, т. е. активировать литический цикл вируса, то в этом случае можно ожидать клинический эффект от противовирусной терапии.
В комплексной терапии рекомендуется внутривенное введение иммуноглобулинов (Гаммар-П, Полигам, Сандоглобулин, Альфаглобин и др.) 400 мг/кг/сут, № 4–5.
В последние годы все чаще для лечения ЭБВИ стали применять рекомбинантные альфа-интерфероны (Интрон А, Роферон-А, Реаферон-ЕС) по 1 млн ME в/м в течение 5–7 дней или через день; при хронической активной ЭБВИ — 3 млн ME в/м 3 раза в неделю, курс 12–36 недель.
В качестве индуктора интерферона при тяжелом течении ЭБВИ рекомендуется использовать Циклоферон по 250 мг (12,5% 2,0 мл) в/м, 1 раз в сутки, № 10 (первые двое суток ежедневно, затем через день) или по схеме: 250 мг/сут, в/м на 1-й, 2-й, 4-й, 6-й, 8-й, 11-й, 14-й, 17-й, 20-й, 23-й, 26-й и 29-й день в сочетании с этиотропной терапией. Перорально Циклоферон назначается по 0,6 г/сут, курсовая доза (6–12 г, т. е. 20–40 таблеток).
Медикаментозная коррекция астенического синдрома при хронической ЭБВИ включает назначение адаптогенов, высоких доз витаминов группы В, ноотропных препаратов, антидепрессантов, психостимуляторов, препаратов с прохолинергическим механизмом действия и корректоров клеточного метаболизма [30–32].
Залогом успешного лечения больного с ЭБВИ являются комплексная терапия и строго индивидуальная тактика ведения как в стационаре, так и во время диспансерного наблюдения.
Литература
Коварный инфекционный мононуклеоз: разберемся, чем он опасен и как его обнаружить
Сейчас все чаще можно услышать сложное и несколько пугающее название болезни — инфекционный мононуклеоз (ИМ). Но даже если это название для вас ново, вероятность, что вы или ваш ребенок уже столкнулись с его возбудителем, достаточно велика. При том, что распространенность этой болезни весьма широка, она не всегда диагностируется правильно. Это связано с тем, что проявляться мононуклеоз может по-разному — как у детей, так и у взрослых. Он способен умело маскироваться и имеет тенденцию к хронитизации. Неудивительно, что мононуклеоз считается крайне коварным явлением.
Давайте разберемся с его причинами, симптомами и, что особенно важно, с его диагностикой!
Что вызывает мононуклеоз?
Самая частая причина болезни — вирус Эпштейна — Барр (ВЭБ) — одна из разновидностей (4-й тип) человеческого вируса герпеса. Иногда сходные симптомы может давать другая разновидность герпеса — цитомегаловирус (ЦМВ). Главный путь передачи данного ВЭБ — через капельки слюны. Поэтому мононуклеоз называют еще «болезнью поцелуев». По данным ВОЗ, вирусом Эпштейна — Барр заражено не менее 95 % населения мира. Именно этот вирус является причиной многих ошибок и трудностей в диагностике.
Мононуклеоз у детей: симптомы и течение
Чаще всего первые проявления инфекционного мононуклеоза возникают у детей раннего возраста и впоследствии у подростков в пубертатном периоде. В любом случае для детского возраста характерно острое начало инфекции.
Какие симптомы в этом случае можно заметить?
В целом острая фаза инфекционного мононуклеоза длится около двух-трех недель. Как и другие разновидности герпес-вирусов, вирус Эпштейна — Барр склонен к сохранению в организме в латентном состоянии на всю жизнь.
Проявления инфекционного мононуклеоза у взрослых
Особенность инфекционного мононуклеоза у взрослых — «смазанные» симптомы, что объясняет частые ошибки в диагностики. При переходе в хроническую форму болезнь протекает с периодическими обострениями. Если на первом месте среди симптомов оказываются, например, постоянные ангины и бронхиты, то есть шанс ежегодно получать диагноз ОРВИ, так и не выяснив истинную причину своих проблем.
Каковы проявления инфекционного мононуклеоза у взрослых?
Чем хуже обстоят дела с иммунитетом, тем чаще и мощнее будут рецидивы инфекции.
Скрытые опасности вируса Эпштейна — Барр
Ученые выявили тесную связь вируса Эпштейна — Барр с развитием некоторых видов новообразований (назофарингеальной карциономы) и болезней крови (лимфомы Бёркитта). Своевременное лечение обострений инфекционного мононуклеоза может снизить риск подобных осложнений.
Зачем нужна проверка на вирус Эпштейна — Барр?
Частые ангины, признаки ухудшения работы печени и другие перечисленные выше проявления встречаются при многих заболеваниях, что вызывает трудности в постановке диагноза на основе клинических проявлений. Возможности современных лабораторных исследований позволяют быстро прояснить ситуацию и сделать дифференциальную диагностику намного проще и точней.
Заболевания, под которые может маскироваться инфекция, вызванная вирусом Эпштейна — Барр:
Лабораторные тесты — это единственный и надежный способ обеспечить такую реализацию диагностики инфекционного мононуклеоза, результат который будет точным и информативным.
Лабораторная диагностика инфекционного мононуклеоза
Существует три главных критерия для лабораторного подтверждения диагноза:
Первые два пункта оцениваются с помощью развернутого общего анализа крови с лейкоцитарной формулой. Такой анализ позволяет установить процентное соотношение разных видов белых кровяных телец, выявить мононуклеары — измененные на фоне активности вируса Эпштейна — Барр белые кровяные клетки.
Серологический тест включает определение иммуноглобулинов класса М и G к нескольким видам вирусных антигенов (в том числе к капсидному, раннему и ядерному антигену) и позволяет сделать вывод о давности заражения, переходе инфекции в хроническую форму и ее реактивации (новом обострении).
Существует еще один метод диагностики инфекционного мононуклеоза, вызванного вирусом Эпштейна — Барр, — метод полимеразной циклической реакции (ПЦР). Данный метод молекулярной биологии, основанный на выявлении ДНК возбудителей инфекции, является сегодня одним из самых точных и чувствительных методов диагностики инфекционных заболеваний. ПЦР позволяет определять не только наличие инфекции, признаки ее реактивации, но вирусную нагрузку, то есть количественное присутствие вирусной ДНК в крови. Применение метода ПЦР в настоящее время можно считать лучшим вариантом для выявления первичной инфекции ВЭБ у детей раннего возраста, а также у лиц с иммунодефицитными состояниями, когда серодиагностика малоэффективна.
Диагностика инфекционного мононуклеоза в LAB4U
В LAB4U можно пройти все виды исследований, необходимые для точной диагностики инфекционного мононуклеоза как у взрослых, так и у детей. Оптимальным для этого является специализированный диагностический комплекс анализов «Инфекционный мононуклеоз», который включает:
Комплекс успешно используется для контроля эффективности лечения заболевания. Все анализы, входящие в комплекс, можно сдать по отдельности — если, по мнению вашего лечащего врача, это необходимо. Также в LAB4U можно пройти и диагностику наличия вируса Эпштейн — Барр методом ПЦР. Как сказано выше, ПЦР-диагностика особенно эффективна для детей младшего возраста при первичном выявлении данной инфекции. Для взрослых пациентов, у которых течение инфекционного мононуклеоза сопровождается нарушением работы печени, в LAB4U предусмотрен комплекс анализов «Печеночные пробы», содержащий все необходимые компоненты для объективной оценки состояния этого органа.
Для первичной диагностики вируса Эпштейна — Барр у детей раннего возраста (до 3-х лет) применяется метод ПЦР-диагностики. Это исследование и ряд других, которые могут потребоваться при комплексном обследовании при наличии инфекционного мононуклеоза, можно всегда найти в каталоге онлайн-лаборатории LAB4U.
Инфекционный мононуклеоз: симптомы и лечение
4.00 (Проголосовало: 4)
Инфекционный мононуклеоз — это острое инфекционное заболевание, протекающее с высокой температурой, воспалением миндалин, увеличением лимфатических узлов, печени, селезёнки, и специфическим изменением в картине крови (появление в анализе мононуклеаров). Вызвано заболевание вирусом Эпштейна-Барра, который относится к семейству герпесвирусов.
Источником инфекции становится больной человек или носитель инфекции. Обычно мононуклеоз лечит врач-инфекционист, но очень часто такие пациенты впервые появляются именно у врача оториноларинголога, с жалобами на температуру и боль в горле.
Инфекционный мононуклеоз встречается повсеместно. Им болеют лица всех возрастных групп, но чаще это лица от 14 до 18 лет, реже дети раннего возраста и взрослые старше 40 лет.
Симптомы мононуклеоза
С первых дней заболевания увеличиваются печень и селезенка, иногда отмечаются боли в животе. Реже у больных возникает желтушность кожи и склер, сыпь.
Часто, на фоне приема антибиотиков пенициллинового ряда, по какой-то причине назначенных врачом, у больных появляется аллергическая сыпь.
Заболевание продолжается от 2-х до 4-х недель, иногда дольше. Постепенно исчезают лихорадка и налеты на миндалинах, нормализуется картина крови, размеры лимфатических узлов, селезенки и печени. Температура может держаться до 2-х недель, в отдельных случаях до месяца.
Диагностика инфекционного мононуклеоза
Диагностируется инфекционный мононуклеоз на основании нескольких анализов:
Иногда проводится диагностика для определения ВИЧ-инфекции, которая может проявляется как мононуклеоз.
Лечение мононуклеоза
Больных с лёгким и среднетяжёлым течением болезни лечат на дому. При более тяжелом течении необходимо стационарное лечение. Необходимость постельного режима определяется выраженностью интоксикации.
Лечение мононуклеоза симптоматическое. Используются противовирусные, жаропонижающие, противовоспалительные препараты. На стадии выздоровления средства для повышения иммунитета. Местно применяют антисептические средства, обезболивающие спреи для обеззараживания и облегчения состояния пациента. Допускается использование растворов для полоскания зева. Если нет аллергии на продукты пчеловодства, применяют мед. Это средство укрепляет иммунитет, смягчает горло и борется с бактериями.
Пациентам назначают специальную диету, которую необходимо соблюдать в течение полугода. Не разрешается ничего жирного, копченого, сладкого, горох, фасоль.
После выздоровления необходимо наблюдение инфекционистом на протяжении 6 месяцев. Перенесенное заболевание оставляет после себя стойкий иммунитет.
В условиях «ЛОР клиники №1» высококвалифицированные специалисты оториноларингологи проведут полный осмотр лор-органов с помощью эндоскопической техники. Назначат адекватное лечение, проведут диагностические мероприятия для постановки верного диагноза и при необходимости направят к другим профильным специалистам.








