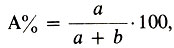Что означает децимолярный раствор
Что означает децимолярный раствор
Концентрация растворов
Концентрацией раствора называется количество (масса или объем) растворенного вещества, содержащееся в определенном количестве (массе или объеме) раствора или растворителя. Ее выражают различными способами. В химии наиболее часто применяются следующие способы:
2. Молярная концентрация, или молярность, выражается числом молей растворенного вещества, содержащихся в 1 л раствора. Раствор, в 1 л которого содержится один моль растворенного вещества, называется молярным. Если в 1 л раствора содержится 0,1 моль вещества, то он называется децимолярным, 0,01 моль-сантимолярным, 0,001 моль-миллимолярным. Размерность молярной концентрации-моль/л.
4. Нормальная концентрация, или нормальность, выражается числом эквивалентов вещества, содержащихся в 1 л раствора. Раствор, в 1 л которого содержится один эквивалент (экв) растворенного вещества, называется нормальным. Если в 1 л раствора содержится 0,1 экв вещества, то он называется децинормальным, 0,01 экв-сантинормальным, 0,001 экв-миллинормальным. Нормальность обычно обозначается буквой н. (иногда N).
Нормальный раствор готовится аналогично молярному.
Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Познание
Автор: Филиппова Наталья Викторовна
Должность: преподаватель химии
Учебное заведение: ГБПОУ «Соликамский технологический колледж»
Населённый пункт: г.Соликамск Пермский край
Наименование материала: МЕТОДИЧЕСКАЯ РАЗРАБОТКА
Тема: РАСТВОРЫ.СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ
Раздел: среднее образование
Министерство образования и науки Пермского края
Государственное бюджетное профессиональное образовательное учреждение
«Соликамский технологический колледж»
для выполнения контрольной работы
для студентов специальности
250405 Технология комплексной переработки древесины
Способы выражения концентрации растворов.
– это гомогенная система, состоящая из двух или более
компонентов, содержание которых можно изменять в
определенных пределах без нарушения однородности.
показывает, сколько вещества растворено в данном
растворе или растворители.
Концентрации вещества можно выразить:
показывает сколько единиц массы вещества растворено в 100 единицах
массы раствора (количество грамм растворенного вещества в 100 граммах
Нахождение массы растворенного вещества:
1. Приготовить 5% раствор поваренной соли.
Это значит, что в 100 грамм этого раствора содержится 5 грамм
поваренной соли и 95 грамм воды.
2.Какова массовая доля соли в растворе, если в 200 г воды растворили 50 г
1.Какие массы поваренной соли и воды надо взять для приготовления 500 г
раствора с массовой долей соли в нем 4%.
2.В 100 г воды растворили 31,6 г нитрата калия. Рассчитайте массовую долю
растворенного вещества в растворе этой соли.
приготовления 600 г сиропа с массовой долей сахара в нем 10%.
сульфата меди содержится
40 г сульфата меди.
Вычислите массовую долю сульфата меди в растворе.
6.Нитрат калия массой 10 г растворили в 80 г воды. Определите процентную
концентрацию полученного раствора.
7.Для получения в лаборатории водорода применяют цинк и раствор серной
кислоты приготовленный из 1 объёма кислоты с плотностью ρ= 1,84 г/см
объёмов воды. Какова С% этого раствора кислоты?
(плотность раствора 1,04
9.Определите массу азотной кислоты в объеме 2 л с массовой долей 10 % и
плотностью = 1,05 г/см
растворенного в 1000 мл раствора (1 л) (выражается числом молей в одном
1 М одномолярный раствор = 1 моль/л
2 М двумолярный раствор =2 моль/л
0,1 М децимолярный раствор
0,2 М двудецимолярный раствор
0,01 М сантимолярный раствор
0,001 М милимолярный раствор
Нахождение массы растворенного вещества:
1. Приготовить децимолярный раствор сульфата натрия.
Отвешиваем 14,2 г сульфата натрия, высыпаем в мерную колбу и доливаем
2.Приготовить 600 мл 2 М раствора карбоната натрия.
Отвесить 127,2 г соли, высыпать в
мерную колбу и долить воды до
приготовления 250 мл 0,1 М раствора.
молярную концентрацию если раствор с плотностью 1,25 гр/см
3.Вычислите молярность раствора, приготовленного в мерной колбе на 500
приготовленном в мерной колбе на 500 мл из 11,25 г кристаллогидрата CuSO
6.Какая масса сульфата бария ВаSO
получится при сливании 200 мл 0,5 М
раствора сульфата алюминия Al
и 150 мл 2 М раствора хлорида бария
выражается числом эквивалентов растворенного вещества в 1 л раствора.
Нахождение массы растворенного вещества:
– реальная или условная частица вещества, которая
химически равноценна одному иону водорода (для обменных реакций) или
одному электрону (для окислительно – восстановительных реакций).
Фактически это частица, обладающая одной единицей валентности или
оперирующая одним электроном.
Эквиваленты сложных веществ находятся:
1.Приготовить 400 мл сантинормального раствора сульфата натрия.
)=142 г/моль преобразуем формулу
2. Определить нормальную концентрацию раствора содержащего 30 г
хлорида алюминия в 500 мл раствора.
1.Сколько грамм азотной кислоты содержится в 2 л ее 0,1 Н раствора?
2.Сколько граммов ортофосфорной кислоты нужно для приготовления 10 мл
кристаллогидрата хлорида бария ВаСl
4.Для нейтрализации 25 мл раствора серной кислоты потребовалось 40 мл 0,1
Н раствора гидроксида натрия. Определите С
5.Какую реакцию имеет раствор, полученный при смешивании 100 мл 0,1Н
раствора серной кислоты с 50 мл 0,5 н раствора гидроксида калия? Сколько
грамм образуется сульфата калия?
– выражается числом молей
растворенного вещества в 1000 г растворителя
сколько грамм растворенного вещества содержится в 1 мл
Переход от процентной концентрации к молярной концентрации:
Переход от процентной концентрации к нормальной концентрации:
Переход от молярной концентрации к процентной концентрации:
Переход от нормальной концентрации к процентной концентрации:
плотность раствора равна 1,373 г/см
2.Определить С% двунормального
раствора серной кислоты с плотностью
3.Масса 66,8 г серной кислоты плотностью = 1,25 г/см
растворили в 133,2 г
воды. Определите С%, С
требуется для приготовления 50 мл 2 н раствора?
5. Найдите молярную концентрацию вещества Na
плотностью 1,11 г/мл.
6.2 л хлора при (н.у.) растворены в 5 л воды. Определите процентную и
молярную концентрации полученного раствора, если объем раствора принять
равным объему воды.
7.Определить С% двунормального раствора серной кислоты (ρ=1,063 г/см
серной кислоты (ρ=1,44 г/см
Способы вычисления при приготовлении разбавленных растворов из
Для получения суперфосфата применяют 65%-ный раствор серной кислоты.
Сколько 92%-ного раствора серной кислоты и воды потребуется для
приготовления 1 т этого раствора?
из формулы выражает
приготовления 1 л 10 % раствора (ρ=1,049 г/см
2.Какие объёмы 95% раствора серной кислоты (ρ=1835 г/л) и воды нужно для
приготовления 1 л 25% раствора (ρ=1180 г/л).
приготовления 500г 15%-ного раствора этой кислоты?
4.Какие объемы 30% ортофосфорной кислоты (ρ=1,18 г/см
для приготовления 100 л 8% раствора (ρ=1,04 г/см
5.Сколько 22 н раствора плавиковой кислоты (ρ=1123 г/л) и 10 н раствора
плавиковой кислоты (ρ=1036 г/л) потребуется
Способы вычисления при смешивании растворов.
Метод «креста», диагональная схема, правило смешивания, «Андреевский
Используется для решения задач для двух компонентов смеси при условии, что
свойство компонентов поддаются аддитивному сложению.
А- m, масса, объем или количество первого компонента;
В- m, масса, объем или количество второго компонента;
— свойство первого компонента;
— свойство второго компонента;
Свойства: плотность твердого вещества, относительная плотность,
относительно атомная масса, относительно молекулярная масса, молярная
масса, концентрации (С%, С
отношение компонентов обратно пропорционально разности величин свойств
(концентраций) компонентов и смеси
Правило смешения не применимо к расчету объемов растворов, концентрация
которых выражается через отношение к объему (кроме слабо разбавленных)
В каком отношении должны быть взяты объемы 0,5 н раствора и 0,1 раствора,
чтобы получить 0,2 н раствор?
Составляем диагональную схему:
60% раствора с 250 т 96% раствора.
2.Сколько грамм воды и 87% раствора серной кислоты необходимо взять для
приготовления 600 г 55% раствора?
3.Сколько граммов 8% и 75% растворов необходимо взять для приготовления
400 г 42 % раствора?
4.Уксусная эссенция – 80% раствор уксусной кислоты (СН
граммов этой эссенции и воды необходимо взять для приготовления 200 мл 3
% раствора уксуса применяемого как приправа к пище? Плотность эссенции
можно принять равной 1 г/см
5.Сколько грамм нужно взять 20% и 32,1 % растворов соляной кислоты,
чтобы приготовить 242 г 26,7% раствора соляной кислоты?
получить 4% раствор?
7.Сколько воды надо испарить из 800 г 10% раствора, чтобы получить 25%
8.Для нейтрализации щелочи, попавшей в глаза, применяется 2% раствор
борной кислоты. Сколько граммов насыщенного раствора, содержащего 4,7%
этой кислоты понадобится для приготовления 0,5 л 2 % раствора?
Расчет массы воды, которая прибавляется к раствору для разбавления
С – получившаяся концентрация,
Преобразованная формула нахождения концентрации
Расчет концентрации раствора при добавлении к раствору вещества.
К 327,5 г 50% – ного раствора вещества добавили 140 г воды. Массовая доля
вещества в конечном растворе равна?
Ответ получившаяся концентрация 35
Р.S. можно формулу преобразовать
2.В 200 г 2%-ного раствора поваренной соли растворили 20 г хлорида натрия.
Какова массовая доля хлорида натрия в полученном растворе?
3.К 450 г 15 %-ного раствора гидроксида кальция добавили 60 г того же
вещества. Массовая доля в конечном растворе равна?
4.Какую массу воды надо добавить к 200 г 70%-ного раствора уксусной
кислоты, чтобы получить 9%-ный раствор?
5.К 300 г 10%-ного раствора
сахарозы добавили 150 мл воды. Какова
массовая доля сахарозы в полученном растворе?
6.Какую массу гидроксида калия надо добавить к 400 г 5%-ного раствора
КОН, чтобы довести массовую долю до 40%?
7.Какую массу оксида серы (VI) надо добавить к 400 г 20%-ного раствора
серной кислоты, чтобы повысить ее массовую долю до 30%?
раствора добавили 100 л воды. Какова С
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Раствор серной кислоты плотностью 1,335 г/см
имеет концентрацию 577 г/л.
Вычислить молярность раствора.
Раствор хлорида калия плотностью 1,131 г/см
содержит 245,7 г соли на 1000 г воды.
Вычислить моляльность раствора.
Вычислите молярность и мольную концентрацию эквивалента 20%-го раствора
хлорида кальция плотностью 1,178 г/см
Сколько граммов вещества содержится в 75 см
0,3Н раствора серной кислоты?
5. В результате установки титра раствора KMnO
получены данные (г/см
Обработать данные методом математической статистики
6. Перечислить основные правила работы в химической лаборатории.
7. Определение плотности с помощью пикнометров, ареометров и гидростатическим
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Определить моляльность 30%-го раствора нафталина (С
) в ацетоне. Плотность
Определить мольные доли компонентов в растворе тригидроксибензола в воде, если
концентрация раствора 80 %, плотность 1,208 г/см
Чему равна мольная концентрация эквивалента 30%-го раствора гидроксида натрия
плотностью 1,328 г/см
Сколько граммов вещества содержится в 50 см
0,2Н раствора соляной кислоты?
При определении мольной концентрации эквивалента NaOH получены данные
Обработать данные методом математической статистики.
Назначение и классификация химической посуды, правила обращения с химической
посудой, хранения, сушка, правила мытья химической посуды, механические и
химические методы очистки химической посуды;
азеотропный, денситометрический, химический.
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Плотность раствора 1,252 г/см
Вычислить мольную концентрацию эквивалента 91%-го раствора серной кислоты.
Плотность раствора 1,825 г/см
Имеется 3 л 10%-го раствора азотной кислоты плотностью 1,054 г/см
молярную концентрацию раствора.
Сколько граммов вещества содержится в 31 см
0,16Н раствора гидроксида калия?
В результате определения зольности бумаги (%):
Обработать данные методом математической статистики.
6. Отбор проб твердых веществ, жидкостей и газов
7. Косвенные методы определения влажности – психрометрический, гигрометрический,
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Определить моляльность 91%-го раствора серной кислоты. Плотность раствора 1,825
Вычислить мольные доли спирта и воды в 96% растворе этанола.
азотной кислоты плотностью 1,12 г/см
Какова молярная концентрация раствора, содержащего 0,32 г гидроксида натрия в 40
5.В результате определения содержания серебра в сплаве получены данные (%)
Обработать данные методом математической статистики.
6. Взвешивание. Технические и аналитические весы. Правила взвешивания
7. Вязкость жидкостей. Вискозиметры. Определение кинетической, динамической и
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Вычислить моляльность 10%-го раствора серной кислоты.
Рассчитать мольные доли воды и спирта в 40% растворе этанола.
Вычислите молярность, моляльность и мольную концентрацию эквивалента 16%- го
раствора хлорида аммония плотностью 1,149 г/см
На нейтрализацию 1 л раствора, содержащего 1,4 г гидроксида калия, требуется 50
раствора серной кислоты. Вычислите мольную концентрацию эквивалента раствора
При определении мольной концентрации эквивалента раствора серной кислоты
получены данные (моль/дм
Обработать данные методом математической статистики.
6.Устройства для нагревания, сушки, прокаливания и охлаждения.
7.Методы определения температуры плавления – в капилляре, на нагреваемой
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Вычислить моляльность 47%-го раствора этанола. Плотность раствора 0,9204 г/см
Вычислить мольные доли гидроксида натрия и воды в 40% растворе щелочи.
Какой объем 20,01%-го раствора соляной кислоты плотностью 1,1 г/ см
Сколько граммов вещества содержалось в 35 см
0,4 Н раствора гидроксида натрия?
Чему равен титр раствора гидроксида натрия?
При определении содержания железа в руде получены данные (%):
Обработать данные методом математической статист
6.Вакуумная техника. Измерение и регулирование давления.
7.Хроматография на бумаге и в тонком слое – применение, оборудование, технология и
методика выполнения анализа.
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Раствор серной кислоты имеет концентрацию 577 г/л. Вычислить содержание серной
кислоты в массовых долях. Плотность раствора 1,335 г/см
Определить мольные доли спирта и воды в 60% растворе этанола.
10%-го раствора азотной кислоты плотностью 1,065 г/ см
массу вещества, содержащуюся в данном объеме раствора.
Какой объем соляной кислоты с массовой долей 20% и плотностью 1,1 г/ см
200 вещества? Какова мольная концентрация эквивалента этого раствора?
При определении влажности древесины получены данные (%):
Обработать данные методом математической статистики.
Устройства для нагревания, сушки, прокаливания и охлаждения
7.Методы определения температуры кипения – по Сиволобову, по ГОСТ 18995-73,
по учебной практике
Выполнение работ по профессии
«Лаборант химического анализа»
Определить мольные доли компонентов в 12% растворе нафталина (С
Прививка от полиомиелита
Огромное спасибо замечательному доктору гинекологу Виктории Викторовне за отличный, очень грамотный, очень профессиональный и очень душевный прием. Я получила рекомендации по лечению и профилактике.
Рекомендую всем женщинам посетить этого замечательного доктора.
Полиомиелит – высококонтагиозное вирусное заболевание, которое приводит к параличу рук, ног и дыхания, а также может стать причиной смерти. Возбудители полиомиелита проникают на слизистую рта преимущественно через загрязненную воду. Возможно также заражение воздушно-капельным путем.
Плохие гигиенические условия благоприятствуют передаче. Инкубационный период составляет от 3 до 35 дней. После того как человек переболеет, у него вырабатывается пожизненный иммунитет (защита от инфекции) к одному вирусному типу (но есть полиовирусы типа 1, 2 и 3). Только вакцинация полностью защищает от инфекций всех трех типов. Сделать прививку от полиомиелита можно в клинике «РебенОК» по лучшим ценам в Москве.
Чем опасен полиомиелит?
Большая часть инфекций (>95%) протекает без симптомов, но при этом образуются антитела. Если есть признаки болезни, существуют различные картины болезни:
· Абортивный полиомиелит: воспаление желудочно-кишечного тракта (гастроэнтерит), лихорадка, тошнота, боль в горле, боли в мышцах и головные боли без участия центральной нервной системы.
· Непаралитический полиомиелит (асептический менингит): воспаление мозговой оболочки без паралича.
· Паралитический полиомиелит (1 из 200 инфекций) с типичными симптомами паралича: при этом самостоятельное дыхание может стать невозможным, может потребоваться пожизненное использование искусственной вентиляции легких. Паралич также может привести к смерти.
Еще через десятилетия после заражения может возникнуть постполиотический синдром. Лечения полиомиелита не существует. Предусмотрено только назначение симптоматической терапии для устранения дискомфорта.
Виды вакцин
Доступны различные вакцины, которые врач вводит с помощью шприца в нескольких разовых дозах. Вакцинация от полиомиелита для младенцев часто сочетается с другими вакцинами. Комбинированная прививка распределяется по четырем разовым дозам: первую получают младенцы в возрасте 3 месяцев, последнюю – на втором году жизни.
Виды вакцин от полиомиелита:
· Прививка ОПВ (оральная полиомиелитная вакцина). Выпускается в форме капель и содержит ослабленные формы двух типов вирусов. Пассивный иммунитет вырабатывается в кишечнике.
· Прививка ИПВ (инактивированная вакцина). Имеет вид однородной суспензии, выпускается в одноразовых шприцах по 0,5 мл. В составе находятся «мертвые» вирусы трех типов.
ОПВ дешевле. Препарат производится в России и имеет хорошие отзывы. Инактивированная вакцина от полиомиелита является импортным продуктом. Препараты имеют определенные отличия, имеют свои побочные реакции и положительные стороны.
В клинике «РебенОК» используется несколько препаратов. Названия вакцины от полиомиелита:
· «Пентаксим». Предназначен для детей с трехмесячного возраста. Национальный график прививок подразумевает проведение трех уколов с промежутком в полтора месяца и дальнейшей ревакцинацией через год. Вторая ревакцинация (пятое введение препарата) проводится ОПВ или ИПВ.
· «Бивак Полио». Живая прививка от полиомиелита, которая состоит из трех доз ослабленной оральной вакцины и двух доз инактивированного препарата. Проводится на первом году жизни. Ревакцинация от полиомиелита осуществляется через год после получения первой дозы.
· «Инфарикс Гекса». Комбинированный препарат, который не имеет жестких требований к подготовке. Вакцина действует против полиомиелита, столбняка, дифтерии, коклюша, гемофильной инфекции, гепатита В.
· «Полимилекс». Монопрепарат, который широко используется для профилактики полиомиелита. Вводится под кожу или внутримышечно. Препарат является «мертвым», поэтому не может стать причиной развития болезни.
Выбор препарата остается за врачом. Многие специалисты предпочитают использовать комбинированные вакцины. Если у ребенка имеются противопоказания, тогда назначаются монопрепараты.
Противопоказания
Как и все прививки, вакцинация от полиомиелита не проводится в период острого инфекционного заболевания или обострения хронической патологии. То же самое относится и к серьезным аллергическим реакциям на вакцинацию против полиомиелита или любого из его компонентов.
Плюсы и минусы
Вакцинация от полиомиелита обычно проводится в младенческом возрасте в рамках базовой иммунизации вместе с пятью другими стандартными прививками. Полиомиелит является серьезным инфекционным заболеванием, которое в стадии развития приводит к инвалидности в случае поражения серого вещества спинного мозга. Преимущества вакцинации от полиомиелита:
· позволяет избежать заражения и предотвратить инвалидность, деформации скелета и паралич;
· у привитого вырабатывается иммунитет от заболевания, поэтому даже при заражении ребенок перенесет болезнь гораздо легче;
· побочные реакции после вакцинации в преимущественном большинстве отсутствуют.
Многие считают, что вакцина имеет недостатки, которые выражены развитием болезни полиомиелит. Но вероятность такого исхода составляет не более 1 случая на 2,7 млн. человек.
Прививка не опасна для жизни и здоровья ребенка. Цель – защита от заражения в будущем путем создания барьера от инфекции. Наиболее безвредной является инактивная вакцина.
Побочные реакции
Комбинированная вакцина против полиомиелита, часто используемая у младенцев, обычно хорошо переносится. В месте инъекции может возникнуть покраснение или болезненный отек. Возможны также аллергические реакции.
Поскольку иммунная система реагирует на вакцину, это может временно вызвать различные недомогания. К ним относятся, например:
· головные боли и ломота;
· лихорадка и усталость;
· раздражительность и озноб.
Эти реакции вакцинации обычно проходят самостоятельно через 1-3 дня.
Возможные осложнения
Прививка от полиомиелита может иметь серьезные последствия для детей. Среди опасных последствий после вакцинации живой прививкой следует выделить вакциноассоциированный полиомиелит. Среди серьезных последствий также следует выделить аллергические реакции в виде зуда, сыпи и отека.
Бывает ли повышенная температура после прививки?
После введения вакцины от полиомиелита детям может повыситься температура тела. Такая реакция считается нормальной и указывает на то, что в организме начали вырабатываться антитела, необходимые для борьбы с вирусом. Небольшое повышение температуры тела наблюдается у 1-4% пациентов. Температура может повыситься до 37,5-38,6 градусов. Если показатели превышают умеренный уровень, тогда следует принять жаропонижающее средство.
Сколько прививок делают от полиомиелита?
В российском национальном календаре прививок предусмотрен следующий график вакцинации от полиомиелита:
· на 1-м году жизни – в 3,4,5 и 6 месяцев;
· на 2-м году жизни – в 18 и 20 месяцев;
· в 14-летнем возрасте – однократно.
В соответствии с календарем РФ, первые две прививки проводятся ИПВ, третья – ОПВ. Курс вакцинации подразумевает использование только инактивированных вакцин. При введении двух доз ОПВ удается обеспечить высокую местную защиту в кишечнике. При дальнейшем использовании живых вакцин снижается риск развития вакциноассоциированного полиомиелита.
Советы родителям
Если у ребенка часто возникают аллергические реакции или же он является аллергиком, то вакцинация возможна только в период ремиссии. Перед введением вакцины нет необходимости в использовании каких-то медикаментозных средств.
Если после вакцинации у ребенка возникают следующие симптомы, следует обратиться к врачу:
· появление признаков ОРЗ (насморк, кашель и пр.);
· дисфункции желудочно-кишечного тракта;
· одышка, снижение мышечного тонуса конечностей.
Речь идет о признаках вакциноассоциированного полиомиелита, которые могут появиться через 4-30 дней после введения ОПВ. Визит к педиатру необходим при нарушении сердечного ритма, появлении крапивницы и сильных головных болей.
После вакцинации рекомендуется отказаться от посещения людных мест. Ребенку нужно давать пить больше очищенной воды, а также исключить из рациона аллергенные продукты.
Предостережение для непривитых
Заявленная цель Всемирной организации здравоохранения (ВОЗ) – искоренить полиомиелит, и Россия также привержена этой цели. Тем не менее, полиомиелит по-прежнему встречается в Пакистане, Афганистане или Нигерии и также может быть перенесен туристами на территорию Российской Федерации. Поэтому вакцинация против полиомиелита по-прежнему рекомендуется, важна и необходима.
Каждый должен быть вакцинирован против полиомиелита, в идеале уже в младенчестве. Люди, которые не были привиты в детстве, или чей статус вакцинации неизвестен, должны наверстать вакцинацию от полиомиелита.
Заключение
В клинике «РебенОК» используется живая и инактивированная вакцина от полиомиелита. Предлагаем лучшие препараты, которые имеют массу положительных отзывов и документы, подтверждающие высокое качество и безопасность. У нас работают специалисты, имеющие большой практический опыт. Перед вакцинацией от полиомиелита ребенок осматривается на наличие противопоказаний, что минимизирует вероятность развития осложнений.